实验室将回收废旧三元锂离子电池经过放电、拆解、分离集流体等操作获得正极活性物质(主要成分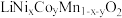 )从材料中回收锰、钴、镍的工艺流程如下:
)从材料中回收锰、钴、镍的工艺流程如下:
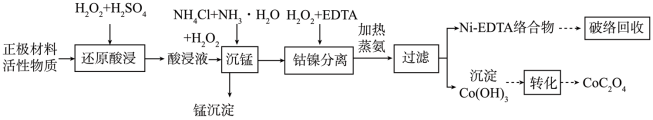
已知:①“酸浸液”中的金属离子主要有Li+、Mn2+、Co2+、Ni2+;
②“沉锰”滤液中钴、镍分别以 、
、 形式存在。
形式存在。
回答下列问题:
(1)废旧电池获得正极材料前,需将其浸入 溶液中使电池短路放电,此时溶液温度升高,该过程中能量的主要转化方式为:
溶液中使电池短路放电,此时溶液温度升高,该过程中能量的主要转化方式为:_______ 。
(2)①已知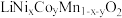 中Ni、Co、Mn化合价相同,则它们的化合价为
中Ni、Co、Mn化合价相同,则它们的化合价为_______ 。
②“酸浸”时若用一定浓度的盐酸替代双氧水和硫酸,缺点是_______ 。
(3)“沉锰”所得锰沉淀主要成分为 、
、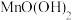 、
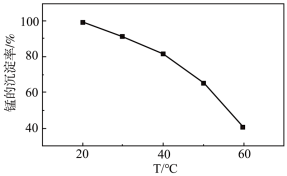
、 。反应温度对锰的沉淀率影响下图所示。
。反应温度对锰的沉淀率影响下图所示。
①“沉锰”生成 的离子方程式:
的离子方程式:_______ 。
②控制过氧化氢添加量,当反应温度升高,锰的沉淀率降低的可能原因:_______ 。
③锰沉淀最好用_______ (填字母)洗涤,洗涤液回收到“钴镍分离”使用以提高回收率。
A.蒸馏水 B. 溶液 C.氨水 D.稀硫酸
溶液 C.氨水 D.稀硫酸
(4)“钴镍分离”过程中添加适量 加热蒸氨得到
加热蒸氨得到 沉淀的离子方程式
沉淀的离子方程式_______ 。
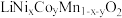 )从材料中回收锰、钴、镍的工艺流程如下:
)从材料中回收锰、钴、镍的工艺流程如下:
已知:①“酸浸液”中的金属离子主要有Li+、Mn2+、Co2+、Ni2+;
②“沉锰”滤液中钴、镍分别以
 、
、 形式存在。
形式存在。回答下列问题:
(1)废旧电池获得正极材料前,需将其浸入
 溶液中使电池短路放电,此时溶液温度升高,该过程中能量的主要转化方式为:
溶液中使电池短路放电,此时溶液温度升高,该过程中能量的主要转化方式为:(2)①已知
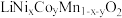 中Ni、Co、Mn化合价相同,则它们的化合价为
中Ni、Co、Mn化合价相同,则它们的化合价为②“酸浸”时若用一定浓度的盐酸替代双氧水和硫酸,缺点是
(3)“沉锰”所得锰沉淀主要成分为
 、
、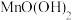 、
、 。反应温度对锰的沉淀率影响下图所示。
。反应温度对锰的沉淀率影响下图所示。
①“沉锰”生成
 的离子方程式:
的离子方程式:②控制过氧化氢添加量,当反应温度升高,锰的沉淀率降低的可能原因:
③锰沉淀最好用
A.蒸馏水 B.
 溶液 C.氨水 D.稀硫酸
溶液 C.氨水 D.稀硫酸(4)“钴镍分离”过程中添加适量
 加热蒸氨得到
加热蒸氨得到 沉淀的离子方程式
沉淀的离子方程式
更新时间:2022-09-14 10:33:11
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铱(77Ir)和锇(76Os)属于铂族金属,与金、银合称贵重金属,可以用于电气、精密仪表、催化剂等领域。铱锇矿的主要成分有Ir、Os、Ir2O3、OsO2,还含有CuO和SiO2等杂质,从铱锇矿中提取铱和锇的流程如下:
回答下列问题:
(1)“酸溶I”的目的是___________ ;酸溶I后溶渣的主要成分除Ir、Os外,还有___________ (填化学式)。
(2)“氧化挥发”是将溶渣置于300~800℃的管式炉内,通入空气氧化。再用NaOH溶液吸收OsO4生成Na2OsO4,该反应的离子方程式为___________ 。
(3)“沉锇”时,NH4Cl与Na2OsO4发生反应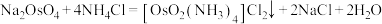 ,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是
,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是___________ 。
(4)“碱熔”时,“残渣I”中的Ir与Na2O2反应生成IrO2·nNa2O和O2,该反应的化学方程式为___________ 。
(5)“沉铜”过程中,当通入H2S达到饱和时测得溶液的pH=1,此时溶液中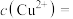
___________ mol/L。[已知:25℃,H2S溶于水形成饱和溶液时, ;H2S的电离常数
;H2S的电离常数 ,
, ;
;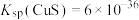 ]
]
(6)化合物 IrO2的四方晶格结构如图所示,其棱边夹角均为90°。已知IrO2晶体密度为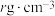 ,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为
,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为___________ (用代数式表示)g/mol。
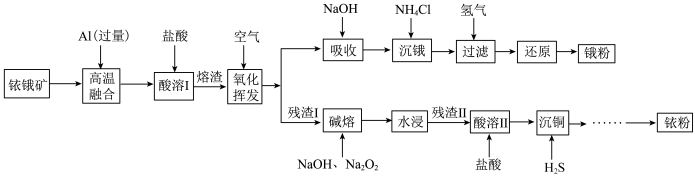
回答下列问题:
(1)“酸溶I”的目的是
(2)“氧化挥发”是将溶渣置于300~800℃的管式炉内,通入空气氧化。再用NaOH溶液吸收OsO4生成Na2OsO4,该反应的离子方程式为
(3)“沉锇”时,NH4Cl与Na2OsO4发生反应
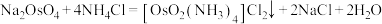 ,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是
,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是(4)“碱熔”时,“残渣I”中的Ir与Na2O2反应生成IrO2·nNa2O和O2,该反应的化学方程式为
(5)“沉铜”过程中,当通入H2S达到饱和时测得溶液的pH=1,此时溶液中
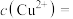
 ;H2S的电离常数
;H2S的电离常数 ,
, ;
;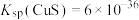 ]
](6)化合物 IrO2的四方晶格结构如图所示,其棱边夹角均为90°。已知IrO2晶体密度为
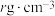 ,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为
,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为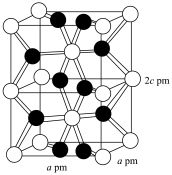
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】纳米铁可用于制作高密度磁性材料。以铁屑(含少量 杂质)为原料制备纳米铁粉流程如下:
杂质)为原料制备纳米铁粉流程如下: 是一种二元酸
是一种二元酸
(1)“酸溶”过程中可以加快反应速率和提高浸出率的方法有_______ 。(写出两种)。
(2)写出“酸溶”时氧化还原反应的离子方程式:_______ 、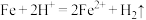 。
。
(3) 固体经灼烧后得到红棕色固体和
固体经灼烧后得到红棕色固体和 混合气体,若产物中
混合气体,若产物中 ,则“灼烧”过程中发生反应的化学方程式为
,则“灼烧”过程中发生反应的化学方程式为_______ 。
(4)取少量产品分散于水中,_______ (填操作步骤),可验证所得铁粉直径是否为纳米级
(5)纳米铁粉可用于处理含氧酸性废水中的 ,反应原理如图所示。
,反应原理如图所示。 的去除,原因是
的去除,原因是_______ 。
②该过程中体现了纳米铁粉的_______ 性(填“氧化”或“还原”)。
 杂质)为原料制备纳米铁粉流程如下:
杂质)为原料制备纳米铁粉流程如下:
 是一种二元酸
是一种二元酸(1)“酸溶”过程中可以加快反应速率和提高浸出率的方法有
(2)写出“酸溶”时氧化还原反应的离子方程式:
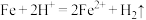 。
。(3)
 固体经灼烧后得到红棕色固体和
固体经灼烧后得到红棕色固体和 混合气体,若产物中
混合气体,若产物中 ,则“灼烧”过程中发生反应的化学方程式为
,则“灼烧”过程中发生反应的化学方程式为(4)取少量产品分散于水中,
(5)纳米铁粉可用于处理含氧酸性废水中的
 ,反应原理如图所示。
,反应原理如图所示。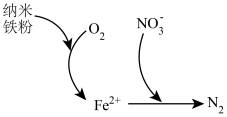
 的去除,原因是
的去除,原因是②该过程中体现了纳米铁粉的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室用粗锌(含少量铜、硫化亚铁)和稀硫酸反应制备氢气,并用氢气还原硫酸锂制备硫化锂的装置如下:

已知硫化锂易潮解,在加热条件下易被空气中的氧气氧化。回答下列问题:
(1)利用装置B还可制备的常见气体有___________ (填化学式,举两例)。
(2)按气流从左至右,装置的连接顺序是c→___________ (填小写字母,装置可重复利用)。
(3)实验过程中,应先打开K一段时间后,再点燃酒精灯,原因是___________ 。
(4)若装置A中只有两种产物生成,该反应的化学方程式___________ 。
(5)采用装置E对装置B中混合物进行分离,再将滤液进行蒸发浓缩、降温结晶可得到副产物皓矾( )晶体。对装置B中混合物进行分离时采用装置E,目的是
)晶体。对装置B中混合物进行分离时采用装置E,目的是___________ 。
(6)测定产品纯度的方法:取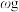 产品,加入足量
产品,加入足量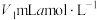 稀硫酸,充分反应后,煮沸溶液,冷却后滴加酚酞溶液作指示剂。用
稀硫酸,充分反应后,煮沸溶液,冷却后滴加酚酞溶液作指示剂。用 标准溶液滴定,消耗NaOH标准溶液
标准溶液滴定,消耗NaOH标准溶液 。产品中
。产品中 的纯度表达式为
的纯度表达式为___________ 。
(7)下列操作会导致测得产品中 的纯度偏低的是___________(填标号)。
的纯度偏低的是___________(填标号)。

已知硫化锂易潮解,在加热条件下易被空气中的氧气氧化。回答下列问题:
(1)利用装置B还可制备的常见气体有
(2)按气流从左至右,装置的连接顺序是c→
(3)实验过程中,应先打开K一段时间后,再点燃酒精灯,原因是
(4)若装置A中只有两种产物生成,该反应的化学方程式
(5)采用装置E对装置B中混合物进行分离,再将滤液进行蒸发浓缩、降温结晶可得到副产物皓矾(
 )晶体。对装置B中混合物进行分离时采用装置E,目的是
)晶体。对装置B中混合物进行分离时采用装置E,目的是(6)测定产品纯度的方法:取
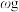 产品,加入足量
产品,加入足量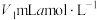 稀硫酸,充分反应后,煮沸溶液,冷却后滴加酚酞溶液作指示剂。用
稀硫酸,充分反应后,煮沸溶液,冷却后滴加酚酞溶液作指示剂。用 标准溶液滴定,消耗NaOH标准溶液
标准溶液滴定,消耗NaOH标准溶液 。产品中
。产品中 的纯度表达式为
的纯度表达式为(7)下列操作会导致测得产品中
 的纯度偏低的是___________(填标号)。
的纯度偏低的是___________(填标号)。| A.产品加入足量稀硫酸,充分反应后,溶液未煮沸 |
| B.量取稀硫酸的滴定管未润洗 |
| C.配制NaOH标准溶液时仰视刻度线 |
| D.滴定终点时发现滴定管尖嘴有气泡 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】以菱锰矿(主要成分为MnCO3,还含有Fe3O4、FeO、MgCO3等杂质)为原料制备MnSO4的工艺流程如下图:
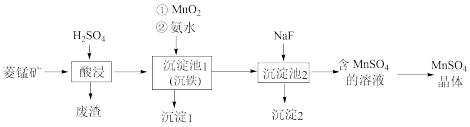
已知:常温下,Ksp(MnS)=1×10-11.金属离子生成氢氧化物沉淀的pH如下表:
(1)酸浸时选择H2SO4而不是HCl的原因可能是___________ 和___________ ,沉淀池1中,加入MnO2时发生反应的离子方程式为___________ 。
(2)该工艺流程中废渣和沉淀1、2均需用水洗涤,并将洗涤液返回酸浸工序,目的是___________ 。
(3)沉淀2的化学式是___________ ,不能用NaOH代替NaF,其原因是___________ 。
(4)含MnSO4溶液中还含有___________ 杂质(填离子符号),利用KMnO4溶液与Mn2+反应生成黑色沉淀的现象可以检验Mn2+,发生反应的离子方程式为___________ 。
(5)电解MnSO4溶液可进一步获得二氧化锰,电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降。欲使溶液中c(Mn2+)≤1.0×10-5 mol·L-1,则应保持溶液中c(S2-)≥___________ mol·L-1。

已知:常温下,Ksp(MnS)=1×10-11.金属离子生成氢氧化物沉淀的pH如下表:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀 | 1.5 | 6.3 | 7.6 | 9.6 |
| 完全沉淀 | 2.8 | 8.3 | 10.2 | 11.6. |
(2)该工艺流程中废渣和沉淀1、2均需用水洗涤,并将洗涤液返回酸浸工序,目的是
(3)沉淀2的化学式是
(4)含MnSO4溶液中还含有
(5)电解MnSO4溶液可进一步获得二氧化锰,电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降。欲使溶液中c(Mn2+)≤1.0×10-5 mol·L-1,则应保持溶液中c(S2-)≥
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学小组在查阅文献及实验探究的基础上,深刻地认识了卤素的性质。
I.F2与C12的相似性。1971年N.H.Studier和E.H.Appelman从冰(-40℃)的氟化作用中首次发现F2、C12与水的反应相似。
(1)写出氟气与水发生上述反应的化学方程式_____________________________________ 。
II.次氯酸钠和氯酸钾的制备。按图装配仪器并检查装置的气密性。

第一步:在锥形瓶内放约3g MnO2粉末,安全漏斗深入试管底部;
第二步:在管6中放4mL 6mol·L-1KOH溶液(放热水浴中),管7中放4mL 2mol· L-1NaOH溶液(放冰水浴中)。打开控制夹3,关闭控制夹4;
第三步:由漏斗加入15mL 9mol·L-1HCl溶液,缓慢加热,控制氯气均匀产生。热水浴温度控制在323K~328K;
第四步:一段时间后,停止加热,……
(2)锥形瓶中用小试管的优点为_________________________________________________ 。
(3)停止加热后的操作是____________________________________ ,再将管6和管7拆下。
(4)查阅文献资料知道,将NaClO溶液加热,NaClO分解可生成NaClO3,据此推断若将KC1O3加热至673K,其分解的化学方程式为_____________________________________ 。
Ⅲ.C1-、Br-、I-的混合液中C1-的鉴定
已知:Ksp(AgC1)=1.8×10-10 Ksp(AgBr)=5.4×10-13 Ksp(AgI)=8.5×10-17
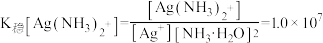
第一步:取2-3滴C1-、Br-、I-的混合液,加1滴6mol·L-1HNO3溶液酸化,滴加0.1mol·L-1AgNO3溶液至沉淀完全,加热2min,离心分离,弃去溶液:
第二步:在沉淀中加入5~10滴2mol·L-1NH3·H2O溶液,剧烈搅拌,并温热1min,离心沉降,移清液于另一支试管中。
(5)已知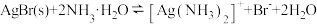 ,设平衡时[Ag(NH3)2]+浓度为0.1mol·L-1,则溶解AgBr沉淀所需氨水的最低浓度约为
,设平衡时[Ag(NH3)2]+浓度为0.1mol·L-1,则溶解AgBr沉淀所需氨水的最低浓度约为_______ mol·L-1( )。
)。
(6)根据上述计算,可推知清液中溶质主要成分的化学式为_________________________ 。
第三步:清液用6mol·L-1HNO3酸化,
(7)现象是_______________________________________________ ,证实C1-存在。反应的离子方程式为__________________________________________________ 。
I.F2与C12的相似性。1971年N.H.Studier和E.H.Appelman从冰(-40℃)的氟化作用中首次发现F2、C12与水的反应相似。
(1)写出氟气与水发生上述反应的化学方程式
II.次氯酸钠和氯酸钾的制备。按图装配仪器并检查装置的气密性。

第一步:在锥形瓶内放约3g MnO2粉末,安全漏斗深入试管底部;
第二步:在管6中放4mL 6mol·L-1KOH溶液(放热水浴中),管7中放4mL 2mol· L-1NaOH溶液(放冰水浴中)。打开控制夹3,关闭控制夹4;
第三步:由漏斗加入15mL 9mol·L-1HCl溶液,缓慢加热,控制氯气均匀产生。热水浴温度控制在323K~328K;
第四步:一段时间后,停止加热,……
(2)锥形瓶中用小试管的优点为
(3)停止加热后的操作是
(4)查阅文献资料知道,将NaClO溶液加热,NaClO分解可生成NaClO3,据此推断若将KC1O3加热至673K,其分解的化学方程式为
Ⅲ.C1-、Br-、I-的混合液中C1-的鉴定
已知:Ksp(AgC1)=1.8×10-10 Ksp(AgBr)=5.4×10-13 Ksp(AgI)=8.5×10-17
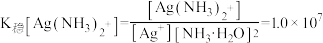
第一步:取2-3滴C1-、Br-、I-的混合液,加1滴6mol·L-1HNO3溶液酸化,滴加0.1mol·L-1AgNO3溶液至沉淀完全,加热2min,离心分离,弃去溶液:
第二步:在沉淀中加入5~10滴2mol·L-1NH3·H2O溶液,剧烈搅拌,并温热1min,离心沉降,移清液于另一支试管中。
(5)已知
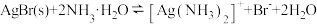 ,设平衡时[Ag(NH3)2]+浓度为0.1mol·L-1,则溶解AgBr沉淀所需氨水的最低浓度约为
,设平衡时[Ag(NH3)2]+浓度为0.1mol·L-1,则溶解AgBr沉淀所需氨水的最低浓度约为 )。
)。(6)根据上述计算,可推知清液中溶质主要成分的化学式为
第三步:清液用6mol·L-1HNO3酸化,
(7)现象是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】下表是几种弱电解质的电离平衡常数K、难溶电解质的溶度积Ksp(25℃)。
回答下列问题:
(1)室温下相同浓度的①CH3COONa②Na2CO3③NaH2PO4④Na2HPO4四种溶液,它们的pH由大到小的顺序为_______ (填编号)。
(2)向Na2HPO4溶液中通入少量CO2反应的离子方程式为____ 。
(3)25℃时,向10mL0.01mol·L-1CH3COOH溶液中滴加VmL0.01mol·L-1氨水,下列说法错误的是___ 。
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c( )>c(CH3COO-)>c(H+)>c(OH-)
)>c(CH3COO-)>c(H+)>c(OH-)
C.V=5时,2c(NH3·H2O)+2c( )=c(CH3COO-)+c(CH3COOH)
)=c(CH3COO-)+c(CH3COOH)
D.V=10时,混合液中水的电离程度大于10mL0.01mol·L-1醋酸溶液中水的电离程度
(4)升高温度可增大AgBr的溶解度,不同温度下AgBr在溶液中的沉淀溶解平衡曲线如图所示。回答下列问题:
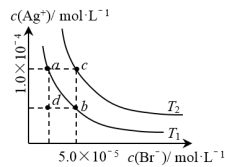
①T1_______ T2(填“>”“=”或“<”);
②T1温度时,对于AgBr的沉淀溶解平衡体系,下列说法正确的是_______ ;
A.加入NaBr可使溶液由b点变为a点
B.升温可使溶液由b点变为d点
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点
D.T1曲线上方区域(不含曲线)任意一点对应的溶液中,均有AgBr沉淀
③用饱和NaCl溶液处理少量AgBr沉淀,使其中的Br-全部转化到溶液中。该沉淀转化反应的平衡常数K=_______ 。
| 电解质 | 平衡方程式 | K | Ksp |
| CH3COOH | CH3COOH⇌CH3COO-+H+ | 1.76×10-5 | |
| H2CO3 | H2CO3⇌H++  ⇌H++ ⇌H++ | K1=4.31×10-7 K2=5.61×10-11 | |
| H3PO4 | H3PO4⇌H++  ⇌H++ ⇌H++  ⇌H++ ⇌H++ | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 | |
| NH3·H2O | NH3·H2O⇌ +OH- +OH- | 1.76×10-5 | |
| AgBr | AgBr⇌Ag++Br- | 5.4×10-13 | |
| AgCl | AgCl⇌Ag++Cl- | 1.8×10-10 |
回答下列问题:
(1)室温下相同浓度的①CH3COONa②Na2CO3③NaH2PO4④Na2HPO4四种溶液,它们的pH由大到小的顺序为
(2)向Na2HPO4溶液中通入少量CO2反应的离子方程式为
(3)25℃时,向10mL0.01mol·L-1CH3COOH溶液中滴加VmL0.01mol·L-1氨水,下列说法错误的是
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(
 )>c(CH3COO-)>c(H+)>c(OH-)
)>c(CH3COO-)>c(H+)>c(OH-)C.V=5时,2c(NH3·H2O)+2c(
 )=c(CH3COO-)+c(CH3COOH)
)=c(CH3COO-)+c(CH3COOH)D.V=10时,混合液中水的电离程度大于10mL0.01mol·L-1醋酸溶液中水的电离程度
(4)升高温度可增大AgBr的溶解度,不同温度下AgBr在溶液中的沉淀溶解平衡曲线如图所示。回答下列问题:

①T1
②T1温度时,对于AgBr的沉淀溶解平衡体系,下列说法正确的是
A.加入NaBr可使溶液由b点变为a点
B.升温可使溶液由b点变为d点
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点
D.T1曲线上方区域(不含曲线)任意一点对应的溶液中,均有AgBr沉淀
③用饱和NaCl溶液处理少量AgBr沉淀,使其中的Br-全部转化到溶液中。该沉淀转化反应的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫酸镍是一种重要的化工中间体,是镍行业研究的热点。一种以石油化工中的废镍催化剂(主要成分为NiCO3和SiO2,还含有少量Fe2O3、Cr2O3)为原料制备硫酸镍的工业流程如图:

已知:Ⅰ.NiS、Ni(OH)2、Cr(OH)3均难溶于水,Cr(OH)3是两性氢氧化物;
Ⅱ.Fe(OH)3不溶于NH4Cl-氨水的混合液,Ni(OH)2溶于NH4Cl-氨水的混合液生成[Ni(NH3)6]2+。
请回答下列问题:
(1)“酸溶”时应先将废镍催化剂粉碎,再与20%硫酸在100℃下反应2h,该操作的目的为____ 。
(2)“滤渣Ⅰ”的主要成分为___ (填化学式),该物质在工业上的用途为___ (任写一种)。
(3)“一次碱析”时,加入的NaOH溶液需过量,含铬微粒发生反应的离子方程式为__ 。
(4)“氨解”的目的为___ 。“净化”时通入H2S的目的是___ 。
(5)“氧化”时发生反应的离子方程式为___ 。
(6)“系列操作”具体是指____ 、过滤、洗涤、干燥。若所得NiSO4·7H2O晶体不纯,应继续进行的提纯操作名称为____ 。

已知:Ⅰ.NiS、Ni(OH)2、Cr(OH)3均难溶于水,Cr(OH)3是两性氢氧化物;
Ⅱ.Fe(OH)3不溶于NH4Cl-氨水的混合液,Ni(OH)2溶于NH4Cl-氨水的混合液生成[Ni(NH3)6]2+。
请回答下列问题:
(1)“酸溶”时应先将废镍催化剂粉碎,再与20%硫酸在100℃下反应2h,该操作的目的为
(2)“滤渣Ⅰ”的主要成分为
(3)“一次碱析”时,加入的NaOH溶液需过量,含铬微粒发生反应的离子方程式为
(4)“氨解”的目的为
(5)“氧化”时发生反应的离子方程式为
(6)“系列操作”具体是指
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硝酸铜是一种重要的化工原料,可由工业含铜废料制备,含铜废料的主要成分为Cu、CuS、CuSO4等,制备流程如图所示:
(1)“焙烧”时,CuS与空气中的O2反应生成CuO和SO2,该反应的化学方程式为_______ ,提高“焙烧”效率的方法为_______ 。(任写一种)
(2)“过滤”所得滤液中溶质的主要成分为_______ 。
(3)①“淘洗”所用时溶液A可以是_______ 。(填标号)。
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.㳖硫酸
②如何证明“淘洗”已完全_______ 。
(4)“反应”阶段所用的试剂是20%的HNO3溶液和10%的H2O2溶液,反应过程中无红棕色气体生成。
①理论上反应所消耗的H2O2和HNO3的物质的量之比为_______ 。
②若不加10%的H2O2溶液,只用20%的HNO3溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为_______ 。
(5)某工厂用m1kg上述工业含铜废料(含铜元素80%)制备Cu(NO3)2•3H2O,最终得到产品m2kg,产率为_______ 。(分数化为最简)
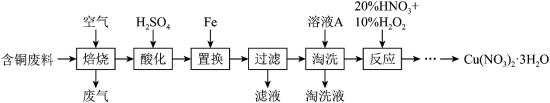
(1)“焙烧”时,CuS与空气中的O2反应生成CuO和SO2,该反应的化学方程式为
(2)“过滤”所得滤液中溶质的主要成分为
(3)①“淘洗”所用时溶液A可以是
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.㳖硫酸
②如何证明“淘洗”已完全
(4)“反应”阶段所用的试剂是20%的HNO3溶液和10%的H2O2溶液,反应过程中无红棕色气体生成。
①理论上反应所消耗的H2O2和HNO3的物质的量之比为
②若不加10%的H2O2溶液,只用20%的HNO3溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
(5)某工厂用m1kg上述工业含铜废料(含铜元素80%)制备Cu(NO3)2•3H2O,最终得到产品m2kg,产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。
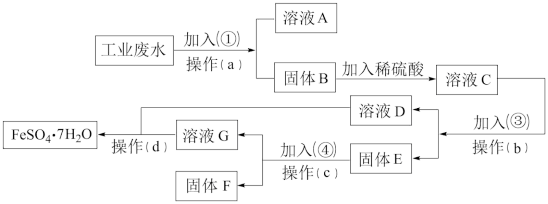
(1)若加入的试剂①为NaOH,加入试剂①的目的________________ 。
(2)加入试剂③所发生的离子反应方程式为________________ 。
(3)写出E和加入试剂④所发生的离子反应方程式为________________ 。
(4)从溶液D和溶液G中得到FeSO4· 7H2O晶体的操作为________________ 、洗涤、干燥。
(5)工业上常用溶液G制得净水剂 Na2FeO4,流程如下
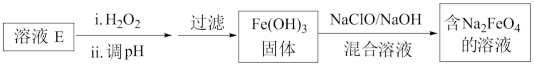
请写出由Fe(OH)3制取为Na2FeO4的离子方程式________________ 。(已知NaClO还原为 NaCl)

(1)若加入的试剂①为NaOH,加入试剂①的目的
(2)加入试剂③所发生的离子反应方程式为
(3)写出E和加入试剂④所发生的离子反应方程式为
(4)从溶液D和溶液G中得到FeSO4· 7H2O晶体的操作为
(5)工业上常用溶液G制得净水剂 Na2FeO4,流程如下

请写出由Fe(OH)3制取为Na2FeO4的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为__________________ ;得到滤渣1的主要成分为______ (写化学式)。
(2)第②步加H2O2的作用是______________________ (用离子方程式表示);使用H2O2的优点是____________ ;调溶液pH的目的是使____________ 生成沉淀。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是______________ 。

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
(2)第②步加H2O2的作用是
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、FeO、CoO等)为原料制备
、FeO、CoO等)为原料制备 的工艺流程如图。
的工艺流程如图。

资料:金属离子沉淀的pH
(1)进入酸浸池之前先要对矿石进行粉碎,目的是___________ 。
(2)酸浸后所得溶液的金属阳离子包括 、
、 、
、___________ 。
(3)沉淀池1中,先加 氧化后再加氨水。写出加
氧化后再加氨水。写出加 时发生反应的离子方程式:
时发生反应的离子方程式:___________ 。
(4)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是___________ 。
(5)如图为 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为蒸发结晶,
晶体”的操作为蒸发结晶,___________ 洗涤,干燥。

(6)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
ⅰ.称取ag废渣,加酸将锰元素全部溶出成 ,过滤,将滤液定容于
,过滤,将滤液定容于 容量瓶中;
容量瓶中;
ⅱ.取 溶液于锥形瓶中,加入少量催化剂和过量
溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分反应后,煮沸溶液使过量的
溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。
ⅲ.加入指示剂,用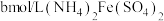 溶液滴定。滴定至终点时消耗
溶液滴定。滴定至终点时消耗 溶液的体积为
溶液的体积为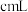 ,
, 重新变成
重新变成 .
.
①补全步骤ⅱ中反应的离子方程式:___________ 。

②废渣中锰元素的质量分数为___________ 。
 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、FeO、CoO等)为原料制备
、FeO、CoO等)为原料制备 的工艺流程如图。
的工艺流程如图。
资料:金属离子沉淀的pH
金属离子 |
|
|
|
|
开始沉淀 | 1.5 | 6.3 | 7.4 | 7.6 |
完全沉淀 | 2.8 | 8.3 | 9.4 | 10.2 |
(2)酸浸后所得溶液的金属阳离子包括
 、
、 、
、(3)沉淀池1中,先加
 氧化后再加氨水。写出加
氧化后再加氨水。写出加 时发生反应的离子方程式:
时发生反应的离子方程式:(4)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是
(5)如图为
 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为蒸发结晶,
晶体”的操作为蒸发结晶,
(6)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
ⅰ.称取ag废渣,加酸将锰元素全部溶出成
 ,过滤,将滤液定容于
,过滤,将滤液定容于 容量瓶中;
容量瓶中;ⅱ.取
 溶液于锥形瓶中,加入少量催化剂和过量
溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分反应后,煮沸溶液使过量的
溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。ⅲ.加入指示剂,用
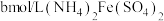 溶液滴定。滴定至终点时消耗
溶液滴定。滴定至终点时消耗 溶液的体积为
溶液的体积为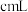 ,
, 重新变成
重新变成 .
.①补全步骤ⅱ中反应的离子方程式:

②废渣中锰元素的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸铁铵[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。
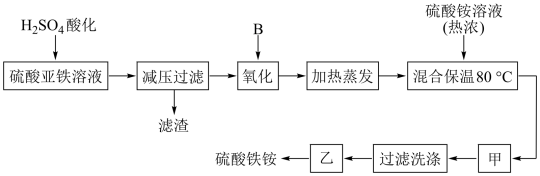
请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是_________ ,滤渣A的主要成分是________ 。
(2)下列物质中最适合的氧化剂B是______ (填字母);反应的离子方程式___________ 。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲名称分别是:甲______________ ,乙为常温晾干。
(4)上述流程中,氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,所加试剂为__ (写化学式),能否用酸性的KMnO4溶液?_________ 填“能”或“否”)理由是:_______ 。(可用语言或方程式说明)
(5)称取14.00 g样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba(NO3)2溶液,恰好完全反应。则该硫酸铁铵的化学式为______________________ 。

请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是
(2)下列物质中最适合的氧化剂B是
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲名称分别是:甲
(4)上述流程中,氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,所加试剂为
(5)称取14.00 g样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba(NO3)2溶液,恰好完全反应。则该硫酸铁铵的化学式为
您最近一年使用:0次





