从古至今,铁及其化合物在人类生产生活中的作用发生了巨大改变。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是___________ (填字母序号)。
a. b.
b. c.
c. d.
d.
基态 原子的价电子的运动状态有
原子的价电子的运动状态有___________ 种。
若将该成分溶于足量的稀硫酸中,再滴加 溶液,溶液变红,继续滴加双氧水至过量,溶液红色褪去,同时有气泡产生。
溶液,溶液变红,继续滴加双氧水至过量,溶液红色褪去,同时有气泡产生。
猜想一:气泡可能是 的反应产物
的反应产物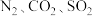 或
或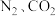 ;
;
猜想二:气泡还可能是___________ ,理由是___________ 。(用化学方程式表示)
(2)硫酸渣的主要化学成分为: 约45%,
约45%, 约40%,
约40%, 约10%,
约10%, 约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
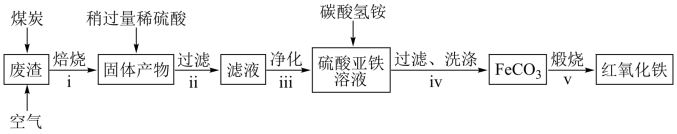
回答下列问题:
①在步骤i中产生的有毒气体可能有___________ 。
②步骤iv中,生成 的离子方程式是
的离子方程式是___________ 。
(3)古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是___________ 。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是
a.
 b.
b. c.
c. d.
d.
基态
 原子的价电子的运动状态有
原子的价电子的运动状态有若将该成分溶于足量的稀硫酸中,再滴加
 溶液,溶液变红,继续滴加双氧水至过量,溶液红色褪去,同时有气泡产生。
溶液,溶液变红,继续滴加双氧水至过量,溶液红色褪去,同时有气泡产生。猜想一:气泡可能是
 的反应产物
的反应产物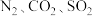 或
或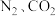 ;
;猜想二:气泡还可能是
(2)硫酸渣的主要化学成分为:
 约45%,
约45%, 约40%,
约40%, 约10%,
约10%, 约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
回答下列问题:
①在步骤i中产生的有毒气体可能有
②步骤iv中,生成
 的离子方程式是
的离子方程式是(3)古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是
更新时间:2022/09/30 22:28:03
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
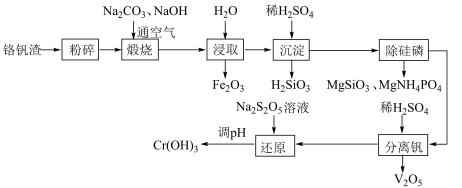
【推荐1】铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、硅磷等的化合物,从铬钒渣中分离提取铬和钒的-种流程如图所示: 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。
回答下列问题:
(1)“煅烧”前粉碎铬钒渣的目的是_______ 。
(2)基态Cr原子的价层电子轨道表示式为_______ 。
(3)“沉淀”“还原”步骤中稀硫酸能否换成稀盐酸?_______ (填“能”或“否”),写出可能的原因:_______ 。
(4)“除硅磷”步骤中,使硅、磷分别以 和
和 的形式沉淀,为达到该目的使用的试剂除
的形式沉淀,为达到该目的使用的试剂除 外还需要另外一种,写出该试剂的化学式:
外还需要另外一种,写出该试剂的化学式:_______ 。
(5)“还原”步骤中,若用 还原
还原 ,会生成较稳定的蓝色的过氧化铬(
,会生成较稳定的蓝色的过氧化铬( ,Cr为
,Cr为 价),分析
价),分析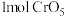 分子中存在过氧键的数目为
分子中存在过氧键的数目为_______  (
( 表示阿伏加德罗常数的值),生成
表示阿伏加德罗常数的值),生成 的离子反应方程式为
的离子反应方程式为_______ 。
(6)若取10吨铬钒渣进行上述流程,V元素在整个流程中利用率为95%,最终生成 1.8吨,则该铬钒渣中V元素的质量分数为
1.8吨,则该铬钒渣中V元素的质量分数为_______ %(保留三位有效数字)。
 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。回答下列问题:
(1)“煅烧”前粉碎铬钒渣的目的是
(2)基态Cr原子的价层电子轨道表示式为
(3)“沉淀”“还原”步骤中稀硫酸能否换成稀盐酸?
(4)“除硅磷”步骤中,使硅、磷分别以
 和
和 的形式沉淀,为达到该目的使用的试剂除
的形式沉淀,为达到该目的使用的试剂除 外还需要另外一种,写出该试剂的化学式:
外还需要另外一种,写出该试剂的化学式:(5)“还原”步骤中,若用
 还原
还原 ,会生成较稳定的蓝色的过氧化铬(
,会生成较稳定的蓝色的过氧化铬( ,Cr为
,Cr为 价),分析
价),分析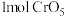 分子中存在过氧键的数目为
分子中存在过氧键的数目为 (
( 表示阿伏加德罗常数的值),生成
表示阿伏加德罗常数的值),生成 的离子反应方程式为
的离子反应方程式为(6)若取10吨铬钒渣进行上述流程,V元素在整个流程中利用率为95%,最终生成
 1.8吨,则该铬钒渣中V元素的质量分数为
1.8吨,则该铬钒渣中V元素的质量分数为
您最近一年使用:0次
【推荐2】下表为元素周期表的一部分,其中的编号代表对应的不同元素。
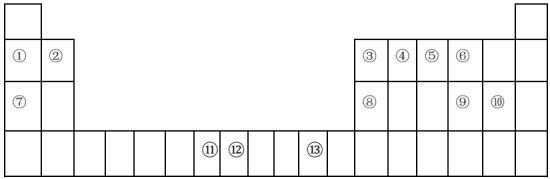
回答下列问题(涉及到元素序号用化学用语作答):
(1)写出基态⑥原子的电子排布式______
(2)基态③原子中电子占据最高能级的符号是______ ,该能级的电子云轮廓图为______ 形。基态⑦原子共有______ 种不同运动状态的电子。
(3)表中属于ds区的元素是______ 。
(4)写出⑧的氧化物与NaOH溶液反应的离子方程式______ 。
(5)从原子结构角度解释非金属性⑩>⑨的原因______ 。
(6)元素⑪(设为字母A)和元素⑫(设为字母B)的部分电离能数据(用 ,
, ,
, 表示)
表示)
如表:
比较两元素的 ,
, 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,请解释原因
再失去一个电子难,请解释原因______ 。

回答下列问题(涉及到元素序号用化学用语作答):
(1)写出基态⑥原子的电子排布式
(2)基态③原子中电子占据最高能级的符号是
(3)表中属于ds区的元素是
(4)写出⑧的氧化物与NaOH溶液反应的离子方程式
(5)从原子结构角度解释非金属性⑩>⑨的原因
(6)元素⑪(设为字母A)和元素⑫(设为字母B)的部分电离能数据(用
 ,
, ,
, 表示)
表示)如表:
元素 | A | B | |
电离能/( |
| 717 | 759 |
| 1509 | 1561 | |
| 3248 | 257 | |
 ,
, 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,请解释原因
再失去一个电子难,请解释原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】利用分类和氧化还原反应的知识能实现物质的转化。
(1)请从下列试剂中选择最合适的完成指定转化(试剂可以重复选择)。
试剂: 溶液、氨水、
溶液、氨水、 溶液、
溶液、 溶液、
溶液、 溶液、稀盐酸、AlCl3溶液
溶液、稀盐酸、AlCl3溶液
① 溶液→
溶液→ 溶液的离子方程式:
溶液的离子方程式:___________ 。
② 溶液
溶液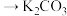 溶液的化学方程式:
溶液的化学方程式:___________ 。
③NH3→ 的离子方程式:
的离子方程式:___________ 。
④Na2CO3溶液与稀盐酸反应的离子方程式:___________ 。
⑤AlCl3溶液与氨水反应的离子方程式:___________ 。
(2)生物浸出法可有效回收含硫矿石中的有色金属,酸性条件下,某生物浸出法主要物质转化如图。___________ 。
②步骤Ⅱ发生反应的离子方程式为___________ 。
(1)请从下列试剂中选择最合适的完成指定转化(试剂可以重复选择)。
试剂:
 溶液、氨水、
溶液、氨水、 溶液、
溶液、 溶液、
溶液、 溶液、稀盐酸、AlCl3溶液
溶液、稀盐酸、AlCl3溶液①
 溶液→
溶液→ 溶液的离子方程式:
溶液的离子方程式:②
 溶液
溶液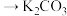 溶液的化学方程式:
溶液的化学方程式:③NH3→
 的离子方程式:
的离子方程式:④Na2CO3溶液与稀盐酸反应的离子方程式:
⑤AlCl3溶液与氨水反应的离子方程式:
(2)生物浸出法可有效回收含硫矿石中的有色金属,酸性条件下,某生物浸出法主要物质转化如图。

②步骤Ⅱ发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】某兴趣小组对物质X(仅含2种常见元素)进行如下探究分析
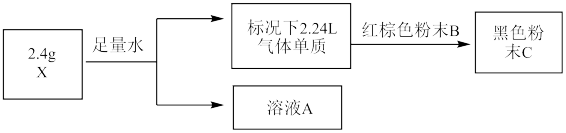
已知:溶液A的焰色试验为黄色,且A溶液恰好被含0.1molHCl的盐酸中和;红棕色粉末B是某铁矿石的主要成分。
请回答以下问题:
(1)X中所含的金属元素是_______ (填元素符号),X的化学式为_______ 。
(2)写出X与水反应的化学方程式_______ 。
(3)X在一定条件下是否可以和红棕色粉末B反应_______ (填“是”或“否”),理由:_______ 。
(4)黑色粉末C溶于盐酸后加入足量溶液A并露置于空气中,发现开始生成白色沉淀,最后沉淀变为红褐色,写出白色沉淀变为红褐色这一过程的化学方程式:_______ 。
(5)已知黑色粉末C中肯定含有一种金属单质,为了验证黑色粉末C是否为纯净物,该小组同学设计了如下实验方案,其中可行的是_______

已知:溶液A的焰色试验为黄色,且A溶液恰好被含0.1molHCl的盐酸中和;红棕色粉末B是某铁矿石的主要成分。
请回答以下问题:
(1)X中所含的金属元素是
(2)写出X与水反应的化学方程式
(3)X在一定条件下是否可以和红棕色粉末B反应
(4)黑色粉末C溶于盐酸后加入足量溶液A并露置于空气中,发现开始生成白色沉淀,最后沉淀变为红褐色,写出白色沉淀变为红褐色这一过程的化学方程式:
(5)已知黑色粉末C中肯定含有一种金属单质,为了验证黑色粉末C是否为纯净物,该小组同学设计了如下实验方案,其中可行的是_______
| A.取少量粉末加足量盐酸,观察是否产生气泡 |
| B.取少量粉末加盐酸溶解后,再加入KSCN溶液,观察是否有颜色的变化 |
| C.准确称取一定质量的粉末,在CO气氛中加热至质量恒重,对比加热前后质量变化进行分析 |
D.取少量粉末加足量 溶液充分反应后过滤,取滤渣洗净后加入足量盐酸充分搅拌后过滤再取滤液,向该滤液中加入KSCN溶液和氯水,观察颜色变化 溶液充分反应后过滤,取滤渣洗净后加入足量盐酸充分搅拌后过滤再取滤液,向该滤液中加入KSCN溶液和氯水,观察颜色变化 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A为常见的金属单质,根据如图所示的关系,请回答下列问题。
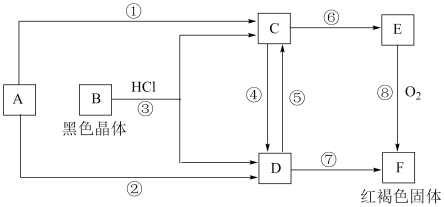
(1)写出下列物质的化学式A:___________ 、B:___________ 、D:___________ 、F:___________ 。
(2)写出反应③的离子方程式:___________ 。
(3)写出反应⑧的化学方程式:___________ 。
(4)若由D→C加入的为铁粉,写出反应⑤的离子方程式:___________ 。
(5)检验D中金属阳离子操作方法是___________ 。

(1)写出下列物质的化学式A:
(2)写出反应③的离子方程式:
(3)写出反应⑧的化学方程式:
(4)若由D→C加入的为铁粉,写出反应⑤的离子方程式:
(5)检验D中金属阳离子操作方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】取m1g某常见粉末(由M、Z两种元素组成)进行如下实验。将该粉末和足量碳粉充分混合,平铺在反应管a中,b瓶中盛足量澄清石灰水。按图连接仪器并检查好气密性。
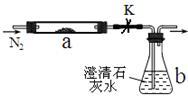
实验开始时,先进行操作G,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。经一系列测定,确定反应完全后,停止加热,继续通氮气,直到反应管冷却。此时,管中的熔融物凝固成银白色金属M,再进行分离、提纯、称量,得到m2g纯金属M,且m1=1.38m2。根据以上叙述回答问题:
(1)该粉末的化学式是_____________ ;操作G是______________________ 。
(2)停止加热前是否需要先关闭止水夹K?_________ ;原因:_____________ 。
(3)反应管a中产生金属单质的化学方程式为:__________________________ 。
(4)本实验的尾气是否需处理?_______ ;如需处理,请回答如何处理;如不需处理,请说明理由。_______________________________________________ 。
(5)在题目“一系列测定”中,当连续_____________ 时,则可确定反应管中反应已完全。
(6)某同学做该实验时,b瓶最终得到了澄清溶液,他向该溶液中加入了某物质,溶液又出现了浑浊。请书写出现浑浊的离子方程式:___________________________ 。

实验开始时,先进行操作G,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。经一系列测定,确定反应完全后,停止加热,继续通氮气,直到反应管冷却。此时,管中的熔融物凝固成银白色金属M,再进行分离、提纯、称量,得到m2g纯金属M,且m1=1.38m2。根据以上叙述回答问题:
(1)该粉末的化学式是
(2)停止加热前是否需要先关闭止水夹K?
(3)反应管a中产生金属单质的化学方程式为:
(4)本实验的尾气是否需处理?
(5)在题目“一系列测定”中,当连续
(6)某同学做该实验时,b瓶最终得到了澄清溶液,他向该溶液中加入了某物质,溶液又出现了浑浊。请书写出现浑浊的离子方程式:
您最近一年使用:0次
【推荐1】A、B、C、D、E是元素周期表中前四周期的元素,其原子序数依次增大,A为元素周期表中原子半径最小的元素,B的基态原子中占有电子的3个能级上的电子数均相等,D与B同族,C与B同周期,且C的所有p轨道上的电子数与所有s轨道上的电子数相等,E的次外层电子数是其最外层电子的7倍。
回答下列问题:
(1)B、C、D三种元素的电负性由小到大的顺序为___________ ;(用元素符号表示),D元素基态原子价层电子排布式为______________________ ;
(2)A、C形成的三原子分子中,C原子的杂化方式为___________ ;
(3)C、D形成的化合物的晶体类型为___________ ;
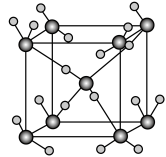
(4)金属Mg与A、E形成的化合物是目前人类已发现的体积储氢密度最高的储氢材料之一,其晶胞结构如图所示,其中黑球代表E,灰球代表Mg,白球代表A,其中白球除在棱上、面上以外,在晶胞内部还有6个。试写出该化合物的化学式:______________________ 。
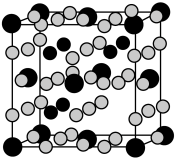
(5)B、C、E能形成如图所示三角双锥构型的配合物分子,三种元素的原子分别用大白球、小白球和黑球代表。
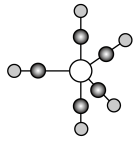
该配合物形成配位键时提供空轨道的原子是___________ (填元素符号),该配合物中大白球代表的元素的化合价为___________ 。
①在水溶液中,水以多种微粒的形式与其他化合物形成水合物。试画出如下微粒的结构图式。H5O2+:______________________
②如图为冰的一种骨架形式,依此为单位向空间延伸该冰中的每个水分子有___________ 个氢键;如果不考虑晶体和键的类型,哪一物质的空间连接方式与这种冰的连接类似______________________
回答下列问题:
(1)B、C、D三种元素的电负性由小到大的顺序为
(2)A、C形成的三原子分子中,C原子的杂化方式为
(3)C、D形成的化合物的晶体类型为
(4)金属Mg与A、E形成的化合物是目前人类已发现的体积储氢密度最高的储氢材料之一,其晶胞结构如图所示,其中黑球代表E,灰球代表Mg,白球代表A,其中白球除在棱上、面上以外,在晶胞内部还有6个。试写出该化合物的化学式:

(5)B、C、E能形成如图所示三角双锥构型的配合物分子,三种元素的原子分别用大白球、小白球和黑球代表。

该配合物形成配位键时提供空轨道的原子是
①在水溶液中,水以多种微粒的形式与其他化合物形成水合物。试画出如下微粒的结构图式。H5O2+:
②如图为冰的一种骨架形式,依此为单位向空间延伸该冰中的每个水分子有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】现有A、B、C、D、E五种元素,他们性质如下:
请回答如下问题:
(1)E原子有___________ 个未成对电子,二价E离子的电子排布式为___________ 。
(2)A2D分子中D原子的杂化类型是___________ ,D的氧化物DO3分子空间构型为___________ 。
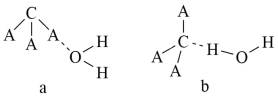
(3)CA3极易溶于水,其原因主要是___________ ,试判断CA3溶于水后,形成CA3·H2O的合理结构:___________ (填“a”或“b”),推理依据是___________ (用相关方程式表示)。
(4)在ESO4溶液中滴入过量氨水,E2+形成深蓝色配合物的离子方程式为:___________ 。
(5)ZnD的晶胞结构如图1所示,在ZnD晶胞中,D2-的配位数为___________ 。

(6)E与金形成的金属互化物结构如图2所示,其晶胞边长为a nm,该金属互化物的密度为___________ (用含a、NA的代数式表示)g·cm-3。

| A | 周期表中原子半径最小的元素 |
| B | 电负性最大的元素 |
| C | C的2p轨道中有三个未成对的单电子 |
| D | 原子核外电子数是B与C核外电子数之和 |
| E | E能形成红色(或砖红色) E2O和黑色的EO两种氧化物 |
(1)E原子有
(2)A2D分子中D原子的杂化类型是
(3)CA3极易溶于水,其原因主要是

(4)在ESO4溶液中滴入过量氨水,E2+形成深蓝色配合物的离子方程式为:
(5)ZnD的晶胞结构如图1所示,在ZnD晶胞中,D2-的配位数为

(6)E与金形成的金属互化物结构如图2所示,其晶胞边长为a nm,该金属互化物的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氟及其化合物用途非常广泛,自然界中氟多以化合态形式存在,形成的化合物有:N2F2、HBF4、 等。回答下列问题:
等。回答下列问题:
(1)氟元素基态原子最高能级电子的电子云形状为___________ ,下列为氟原子激发态的电子排布式的是___________ (填序号)。
A.1s22s22p43s1 B.1s22s22p6 C.1s22s22p5 D.1s22s12p6
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为___________ 。
②N2F2结构式为___________ ,其分子中 键与
键与 键的数目之比为
键的数目之比为___________ 。
(3)氟硼酸(HBF4,属于强酸)可由HF和BF3化合生成,常用于替代浓硫酸作铅蓄电池的电解质溶液,从化学键形成角度分析HF与BF3能化合的原因___________ 。
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物 ,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,
,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比, 的导电性
的导电性___________ (填“增强”或“减弱”), 中C-C键的键长比石墨中C-C键的
中C-C键的键长比石墨中C-C键的___________ (填“长”或“短”)。___________ ,设NA为阿伏加德罗常数的值则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
 等。回答下列问题:
等。回答下列问题:(1)氟元素基态原子最高能级电子的电子云形状为
A.1s22s22p43s1 B.1s22s22p6 C.1s22s22p5 D.1s22s12p6
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为
②N2F2结构式为
 键与
键与 键的数目之比为
键的数目之比为(3)氟硼酸(HBF4,属于强酸)可由HF和BF3化合生成,常用于替代浓硫酸作铅蓄电池的电解质溶液,从化学键形成角度分析HF与BF3能化合的原因
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物
 ,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,
,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比, 的导电性
的导电性 中C-C键的键长比石墨中C-C键的
中C-C键的键长比石墨中C-C键的
 (列出计算式)。
(列出计算式)。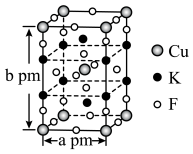
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】 (熔点
(熔点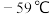 ,沸点11℃)是一种高效消毒灭菌剂,可有效灭活新冠病毒,极易溶于水,在碱性环境中发生反应:
,沸点11℃)是一种高效消毒灭菌剂,可有效灭活新冠病毒,极易溶于水,在碱性环境中发生反应: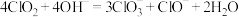 ;稳定性较差,易分解,体积分数大于10%时可能爆炸,常用
;稳定性较差,易分解,体积分数大于10%时可能爆炸,常用 和
和 混合溶液吸收转化为
混合溶液吸收转化为 保存。现利用如下装置及试剂制备
保存。现利用如下装置及试剂制备 。
。

请回答下列问题:
(1)已知75%浓硫酸密度是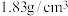 ,其物质的量浓度约为
,其物质的量浓度约为___________  。用98%浓硫酸配制该浓度的溶液
。用98%浓硫酸配制该浓度的溶液 ,除量筒、烧杯、玻璃棒之外还需要的仪器有:
,除量筒、烧杯、玻璃棒之外还需要的仪器有:___________ 。
(2)装置B生成 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为___________ 。实验过程中持续通入 的作用是
的作用是___________ 。
(3)装置C需采用冰水浴的可能原因是___________ (任写一点)。
(4)装置C中 和
和 与
与 反应制取
反应制取 的离子方程式为
的离子方程式为___________ ;加入 过量导致的后果是
过量导致的后果是___________ 。
 (熔点
(熔点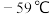 ,沸点11℃)是一种高效消毒灭菌剂,可有效灭活新冠病毒,极易溶于水,在碱性环境中发生反应:
,沸点11℃)是一种高效消毒灭菌剂,可有效灭活新冠病毒,极易溶于水,在碱性环境中发生反应: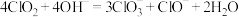 ;稳定性较差,易分解,体积分数大于10%时可能爆炸,常用
;稳定性较差,易分解,体积分数大于10%时可能爆炸,常用 和
和 混合溶液吸收转化为
混合溶液吸收转化为 保存。现利用如下装置及试剂制备
保存。现利用如下装置及试剂制备 。
。
请回答下列问题:
(1)已知75%浓硫酸密度是
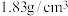 ,其物质的量浓度约为
,其物质的量浓度约为 。用98%浓硫酸配制该浓度的溶液
。用98%浓硫酸配制该浓度的溶液 ,除量筒、烧杯、玻璃棒之外还需要的仪器有:
,除量筒、烧杯、玻璃棒之外还需要的仪器有:(2)装置B生成
 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为 的作用是
的作用是(3)装置C需采用冰水浴的可能原因是
(4)装置C中
 和
和 与
与 反应制取
反应制取 的离子方程式为
的离子方程式为 过量导致的后果是
过量导致的后果是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】化学是一门以实验为基础的学科,化学所得的丰硕成果,是与实验的重要作用分不开,气体的制备就是重要的一类实验
Ⅰ、氨气的制备

(1)氨气的发生装置选择上图中的_____ 装置(填字母),实验室制备氨气反应的化学方程式为:_____ 。C装置的名称是_____ 。
(2)请从上述装置中选择必要的装置完成制备干燥纯净的氨气的实验,其装置接口连接顺序为_____ (填小写字母)。
Ⅱ、氯气的制备

(3)盛浓盐酸的仪器名称是_____ ,装 的玻璃仪器名称是
的玻璃仪器名称是_____ 。
(4)气体发生装置中发生反应的化学方程式为_____ ,检验氯气是否收集满的方法是:_____ 。
(5)上述装置中饱和食盐水的作用是_____ 。
Ⅲ、二氧化硫的制备
(6)实验室制 的方法是往
的方法是往 粉末中滴加浓
粉末中滴加浓 ,请写出其化学方程式:
,请写出其化学方程式:_____ 。
Ⅰ、氨气的制备

(1)氨气的发生装置选择上图中的
(2)请从上述装置中选择必要的装置完成制备干燥纯净的氨气的实验,其装置接口连接顺序为
Ⅱ、氯气的制备

(3)盛浓盐酸的仪器名称是
 的玻璃仪器名称是
的玻璃仪器名称是(4)气体发生装置中发生反应的化学方程式为
(5)上述装置中饱和食盐水的作用是
Ⅲ、二氧化硫的制备
(6)实验室制
 的方法是往
的方法是往 粉末中滴加浓
粉末中滴加浓 ,请写出其化学方程式:
,请写出其化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】对羟基苯甲酸酯是一类高效低毒的新一代消毒杀菌防腐剂,它的抗菌能力比苯甲酸和山梨酸及其盐类强。利用如图装置制备并提纯对羟基苯甲酸乙酯,相关有机物的物理性质如表所示。

实验步骤:
①在装置A中加入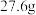 对羟基苯甲酸、
对羟基苯甲酸、 乙醇和
乙醇和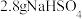 (作催化剂),放入磁力搅拌子,开动搅拌器,在
(作催化剂),放入磁力搅拌子,开动搅拌器,在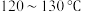 下反应
下反应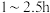 ;
;
②反应结束后,将反应后液体转移至装置D中,用图2装置进行水蒸气蒸馏,蒸馏余液倒入干净的烧杯内,冷却析晶,用质量分数为 的碳酸氢钠溶液洗涤晶体至洗涤液
的碳酸氢钠溶液洗涤晶体至洗涤液 为7.5~8.0,用图3装置抽滤,用蒸馏水冲洗滤饼,干燥,得到白色固体产品对羟基苯甲酸乙酯。
为7.5~8.0,用图3装置抽滤,用蒸馏水冲洗滤饼,干燥,得到白色固体产品对羟基苯甲酸乙酯。
请回答下列问题:
(1)仪器B的名称为___________ 。
(2)写出制备对羟基苯甲酸乙酯的化学方程式:___________ ,在此实验中,一般加入的乙醇稍微过量,原因是___________ 。
(3)图2中,加热装置C产生水蒸气,该装置中玻璃管的作用为___________ ,用水蒸气蒸馏可除去的物质是___________ 。
(4)用碳酸氢钠溶液洗涤晶体是为了除去杂质___________ ,检验晶体是否洗涤干净的操作为___________ 。
(5)经干燥后,得到对羟基苯甲酸乙酯约 ,则对羟基苯甲酸乙酯的产率为
,则对羟基苯甲酸乙酯的产率为___________ (保留三位有效数字)。
| 物质 | 相对分子质量 | 密度/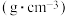 | 熔点/ | 沸点/ | 常温下状态 | 溶解性 |
| 对羟基苯甲酸 | 138 | 1.46 | 214~216 | 336 | 固态 | 微溶于水,易溶于热水和乙醇、乙醚等 |
| 乙醇 | 46 | 0.79 | 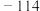 | 78 | 液态 | 与水混溶,可混溶于乙醚等 |
| 对羟基苯甲酸乙酯 | 166 | 1.08 | 116~118 | 固态 | 微溶于水,易溶于乙醇等 |

实验步骤:
①在装置A中加入
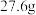 对羟基苯甲酸、
对羟基苯甲酸、 乙醇和
乙醇和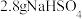 (作催化剂),放入磁力搅拌子,开动搅拌器,在
(作催化剂),放入磁力搅拌子,开动搅拌器,在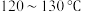 下反应
下反应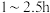 ;
;②反应结束后,将反应后液体转移至装置D中,用图2装置进行水蒸气蒸馏,蒸馏余液倒入干净的烧杯内,冷却析晶,用质量分数为
 的碳酸氢钠溶液洗涤晶体至洗涤液
的碳酸氢钠溶液洗涤晶体至洗涤液 为7.5~8.0,用图3装置抽滤,用蒸馏水冲洗滤饼,干燥,得到白色固体产品对羟基苯甲酸乙酯。
为7.5~8.0,用图3装置抽滤,用蒸馏水冲洗滤饼,干燥,得到白色固体产品对羟基苯甲酸乙酯。请回答下列问题:
(1)仪器B的名称为
(2)写出制备对羟基苯甲酸乙酯的化学方程式:
(3)图2中,加热装置C产生水蒸气,该装置中玻璃管的作用为
(4)用碳酸氢钠溶液洗涤晶体是为了除去杂质
(5)经干燥后,得到对羟基苯甲酸乙酯约
 ,则对羟基苯甲酸乙酯的产率为
,则对羟基苯甲酸乙酯的产率为
您最近一年使用:0次

 )
)

