全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。
Ⅰ.氮氧化物的研究
(1)一定条件下,将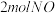 与
与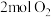 置于恒容密闭容器中发生反应:
置于恒容密闭容器中发生反应: ,下列状态能说明该反应达到化学平衡的是_______(填字母编号)。
,下列状态能说明该反应达到化学平衡的是_______(填字母编号)。
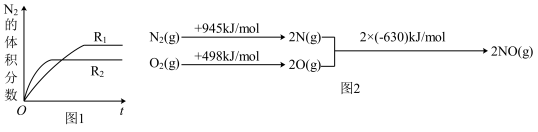
(2)已知反应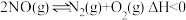 ,在不同条件时
,在不同条件时 的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线
的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线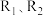 表示的是
表示的是_______ (填字旺序号)。
A.压强B.温度C.催化剂
根据图2中的能量变化数据,计算反应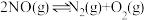 的
的
_______ 。
Ⅱ.碳氧化物研究
(3)图3甲为恒温恒容装置,乙为恒温恒压装置。已知CO和 在一定条件下可以合成甲醇:
在一定条件下可以合成甲醇: 。
。
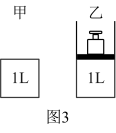
相同温度下,将 和
和 分别通入体积为1L的图3甲、乙装置中,一段时间后均达到平衡,此时CO的转化率:甲
分别通入体积为1L的图3甲、乙装置中,一段时间后均达到平衡,此时CO的转化率:甲_______ 乙(填“<”、“>”或“=”);若再向乙容器中通入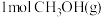 ,重新达到平衡后,
,重新达到平衡后, 在体系中的百分含量
在体系中的百分含量_______ (填“变大”或“变小”或“不变”)。
Ⅰ.氮氧化物的研究
(1)一定条件下,将
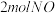 与
与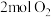 置于恒容密闭容器中发生反应:
置于恒容密闭容器中发生反应: ,下列状态能说明该反应达到化学平衡的是_______(填字母编号)。
,下列状态能说明该反应达到化学平衡的是_______(填字母编号)。| A.混合气体的密度保持不变 | B.NO的转化率保持不变 |
C.NO和 的物质的量之比保持不变 的物质的量之比保持不变 | D. 的消耗速率和 的消耗速率和 的消耗速率相等 的消耗速率相等 |
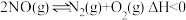 ,在不同条件时
,在不同条件时 的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线
的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线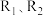 表示的是
表示的是A.压强B.温度C.催化剂
根据图2中的能量变化数据,计算反应
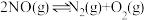 的
的

Ⅱ.碳氧化物研究
(3)图3甲为恒温恒容装置,乙为恒温恒压装置。已知CO和
 在一定条件下可以合成甲醇:
在一定条件下可以合成甲醇: 。
。
相同温度下,将
 和
和 分别通入体积为1L的图3甲、乙装置中,一段时间后均达到平衡,此时CO的转化率:甲
分别通入体积为1L的图3甲、乙装置中,一段时间后均达到平衡,此时CO的转化率:甲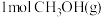 ,重新达到平衡后,
,重新达到平衡后, 在体系中的百分含量
在体系中的百分含量
更新时间:2022-11-04 11:36:56
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】钨有“光明使者”的美誉,在自然界中主要以钨(+6价)酸盐的形式存在,黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成(Fe、Mn)WO4,钨酸(B)酸性很弱,难溶于水,黑钨矿传统冶炼工艺的第一阶段是碱熔法,第二阶段则是用还原剂还原出金属钨。化合物A、B、C含有同一元素。请回答下列问题:
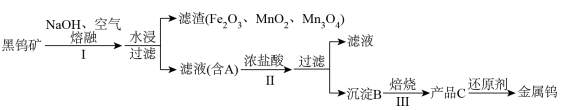
(1)为提高水浸速率,采取的措施为___________________ (写两种)。
(2)用还原剂还原出金属钨。
①碳和氢气均可还原化合物C得钨,用氢气比用碳更具有优点,其理由是___________ 。
②如果用金属铝与化合物C反应,还原出1mol钨至少需要铝的质量为___________ 。
(3)利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g) WI2(g) △H<0。
WI2(g) △H<0。
①一定温度下,向某恒容密闭容器中加入2molI2(g)和足量W(s)达平衡后,I2(g)的转化率为20%,则平衡时c[I2(g)]∶c[WI2(g)]=___________ ;相同条件下,若开始加入I2(g)的物质的量变为原来2倍,则下列数值是原来2倍的有___________ (填标号)。
A.平衡常数 B.达到平衡的时间
C.I2(g)的物质的量浓度 D.平衡时WI2(g)的体积分数
②工业上利用上述反应原理提纯金属钨的示意图如右:

反应在真空石英管中进行,先在温度为T1端放入不纯W粉末和少量I2(g),一段时间后,在温度为T2的一端得到纯净的晶体,则温度T1___________ T2(填:“>”、“<”或“=”)。
(4)写出黑钨矿中FeWO4在步骤Ⅰ中反应的化学方程式__________________________ 。

(1)为提高水浸速率,采取的措施为
(2)用还原剂还原出金属钨。
①碳和氢气均可还原化合物C得钨,用氢气比用碳更具有优点,其理由是
②如果用金属铝与化合物C反应,还原出1mol钨至少需要铝的质量为
(3)利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)
 WI2(g) △H<0。
WI2(g) △H<0。①一定温度下,向某恒容密闭容器中加入2molI2(g)和足量W(s)达平衡后,I2(g)的转化率为20%,则平衡时c[I2(g)]∶c[WI2(g)]=
A.平衡常数 B.达到平衡的时间
C.I2(g)的物质的量浓度 D.平衡时WI2(g)的体积分数
②工业上利用上述反应原理提纯金属钨的示意图如右:

反应在真空石英管中进行,先在温度为T1端放入不纯W粉末和少量I2(g),一段时间后,在温度为T2的一端得到纯净的晶体,则温度T1
(4)写出黑钨矿中FeWO4在步骤Ⅰ中反应的化学方程式
您最近一年使用:0次
【推荐2】镍钛钯废靶材含钛55%、镍25%、钯18%和杂质铝2%。从镍钛钯废靶材回收有关金属的工艺流程如下:
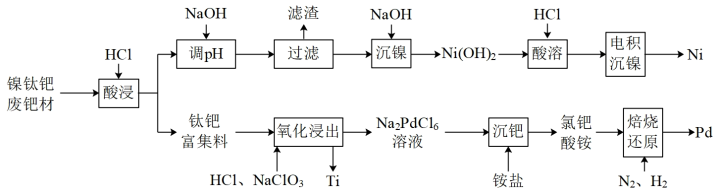
已知:Ⅰ.常温下,钛与钯均不溶于盐酸。
Ⅱ. 在溶液中存在配位平衡:
在溶液中存在配位平衡: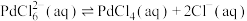

回答下列问题:
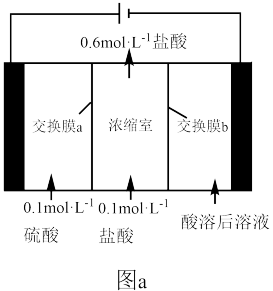
(1)“酸溶”所得溶液,经电积可得单质镍,电积沉镍装置如图a所示。电积装置中,交换膜b应为___________ 离子交换膜(填“阳”或“阴”)。电解时浓缩室溶液体积保持不变,当浓缩室得到 的盐酸时,阴极得到Ni的质量小于
的盐酸时,阴极得到Ni的质量小于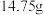 ,其原因为
,其原因为_________ 。
(2)“氧化浸出”时,钯(Pd)被氧化生成配位离子 的离子方程式为
的离子方程式为___________ 。
(3)”沉钯”时,温度保持在55~65℃,温度不易过高,其原因除防止铵盐分解外,还有_____ 。
(4)氯钯酸铵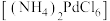 在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在
在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在___________ 操作中循环使用(填操作单元名称)。
(5)钯镍合金在较低温度下形成一种超结构有序相,其立方晶胞结构如图所示,晶胞参数为 ,结构中有两种八面体空隙,一种完全由镍原子构成(
,结构中有两种八面体空隙,一种完全由镍原子构成(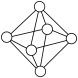 ),另一种由钯原子和镍原子共同构成(
),另一种由钯原子和镍原子共同构成(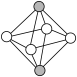 )。
)。
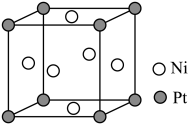
①该晶体的化学式为___________ 。
②两种八面体空隙中心的最近距离为___________ 。

已知:Ⅰ.常温下,钛与钯均不溶于盐酸。
Ⅱ.
 在溶液中存在配位平衡:
在溶液中存在配位平衡: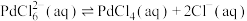

回答下列问题:
(1)“酸溶”所得溶液,经电积可得单质镍,电积沉镍装置如图a所示。电积装置中,交换膜b应为
 的盐酸时,阴极得到Ni的质量小于
的盐酸时,阴极得到Ni的质量小于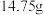 ,其原因为
,其原因为
(2)“氧化浸出”时,钯(Pd)被氧化生成配位离子
 的离子方程式为
的离子方程式为(3)”沉钯”时,温度保持在55~65℃,温度不易过高,其原因除防止铵盐分解外,还有
(4)氯钯酸铵
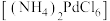 在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在
在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在(5)钯镍合金在较低温度下形成一种超结构有序相,其立方晶胞结构如图所示,晶胞参数为
 ,结构中有两种八面体空隙,一种完全由镍原子构成(
,结构中有两种八面体空隙,一种完全由镍原子构成( ),另一种由钯原子和镍原子共同构成(
),另一种由钯原子和镍原子共同构成( )。
)。
①该晶体的化学式为
②两种八面体空隙中心的最近距离为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】研究反应机理以及化学平衡的原理,是揭示化学反应的规律和获得调控化学反应的理论依据。
I.一定条件下,在容积为5L的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达平衡后,降低温度,A的体积分数减小。
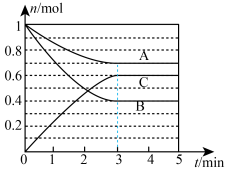
(1)该反应的化学方程式为___________ 。
(2)在一定温度下的容积不变的密闭容器中发生该反应。下列叙述中,不能说明反应达到化学平衡状态的是___________。
(3)该反应的反应速率v随时间t的关系如图所示。
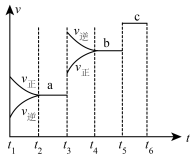
①根据上图判断,在t3时刻改变的外界条件是___________ 。
②根据上图判断a、b、c对应的平衡状态中,C的体积分数最大的是___________ 状态。
Ⅱ.在1L密闭容器中发生反应: ,其化学平衡常数K与温度T的关系如下表:
,其化学平衡常数K与温度T的关系如下表:
回答下列问题:
(4)该反应的平衡常数表达式为K=________ ;该反应的△H________ 0(填“>”或“<”)。
(5)下列措施既可以提高反应速率,又可以提高H2的平衡转化率的是___________。
(6)830℃时,将2molCO2和2molH2投入上述容器中开始反应,达到平衡时CO2的转化率为___________ 。
(7)800℃时,某时刻测得c(CO2)=0.5mol·L-1、c(H2)=1.5mol·L-1、c(CO)=0.5mol·L-1、c(H2O)=0.5mol·L-1,此时,v(正)___________ v(逆)(填“>”“<”或“=”)。
I.一定条件下,在容积为5L的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达平衡后,降低温度,A的体积分数减小。

(1)该反应的化学方程式为
(2)在一定温度下的容积不变的密闭容器中发生该反应。下列叙述中,不能说明反应达到化学平衡状态的是___________。
| A.A的消耗速率与C的生成速率比为1:2 |
| B.容器内压强不再变化 |
| C.混合气体平均摩尔质量不再改变 |
| D.混合气体密度不再改变 |
(3)该反应的反应速率v随时间t的关系如图所示。

①根据上图判断,在t3时刻改变的外界条件是
②根据上图判断a、b、c对应的平衡状态中,C的体积分数最大的是
Ⅱ.在1L密闭容器中发生反应:
 ,其化学平衡常数K与温度T的关系如下表:
,其化学平衡常数K与温度T的关系如下表:| T(℃) | 650 | 700 | 800 | 830 | 1000 |
| K | 0.5 | 0.6 | 0.9 | 1.0 | 1.7 |
(4)该反应的平衡常数表达式为K=
(5)下列措施既可以提高反应速率,又可以提高H2的平衡转化率的是___________。
| A.选择适当的催化剂 | B.增大压强 |
| C.及时分离出H2O(g) | D.升高温度 |
(6)830℃时,将2molCO2和2molH2投入上述容器中开始反应,达到平衡时CO2的转化率为
(7)800℃时,某时刻测得c(CO2)=0.5mol·L-1、c(H2)=1.5mol·L-1、c(CO)=0.5mol·L-1、c(H2O)=0.5mol·L-1,此时,v(正)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】丙烯是应用广泛的化工原料,工业上两种利用丙烷制备丙烯的反应如下:
I.丙烷直接脱氢: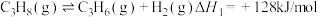
II.氧化丙烷脱氢: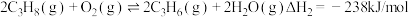
回答下列问题:
(1)反应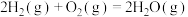 ∆H=
∆H=___________ kJ∙mol-1。
(2)一定条件下,向1L实验容器中充入1mol气态C3H8发生反应Ⅰ。其中主要副反应为:III.丙烷裂解: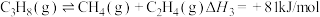 。下图为测得不同温度下C3H6的平衡产率:
。下图为测得不同温度下C3H6的平衡产率:
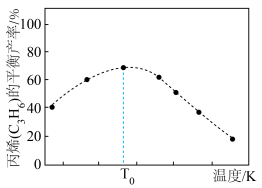
温度高于T0,C3H6的平衡产率随温度升高而减小的原因是___________ 。
(3)运用丙烷直接脱氢法,在相同温度和催化剂条件下,体积均为0.5L的恒容密闭容器中只发生反应I,测得反应的有关数据如下:
①容器a达到平衡时C3H8(g)的平衡浓度为c(C3H8)=___________ ,平衡常数为___________ 。
②容器b经过5分钟达到平衡,则用C3H8(g)表示化学反应速率v(C3H8)=___________ ,反应吸收热量Q为___________ kJ。
③容器c达到平衡时,反应对外___________ (填吸收或放出)热量。
I.丙烷直接脱氢:
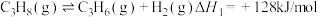
II.氧化丙烷脱氢:
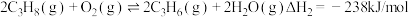
回答下列问题:
(1)反应
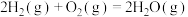 ∆H=
∆H=(2)一定条件下,向1L实验容器中充入1mol气态C3H8发生反应Ⅰ。其中主要副反应为:III.丙烷裂解:
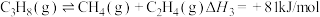 。下图为测得不同温度下C3H6的平衡产率:
。下图为测得不同温度下C3H6的平衡产率:
温度高于T0,C3H6的平衡产率随温度升高而减小的原因是
(3)运用丙烷直接脱氢法,在相同温度和催化剂条件下,体积均为0.5L的恒容密闭容器中只发生反应I,测得反应的有关数据如下:
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系的能量变化 | ||
| C3H8(g) | C3H6(g) | H2(g) | ||
| a | 0 | 1 | 1 | 放热32kJ |
| b | 1 | 0 | 0 | 吸热QkJ |
| c | 0.2 | 0.8 | 0.8 | ∆Hc |
②容器b经过5分钟达到平衡,则用C3H8(g)表示化学反应速率v(C3H8)=
③容器c达到平衡时,反应对外
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】氯乙烯是用途广泛的石油化工产品,工业上常利用乙烯氧氯化法生产:

已知:ⅰ.
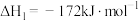
ⅱ.
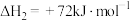
ⅲ.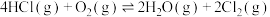
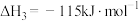
回答下列问题:
(1)
___________  。
。
(2)已知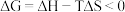 ,反应可自发进行。若
,反应可自发进行。若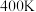 时反应ⅱ中
时反应ⅱ中 ,此时反应ⅱ
,此时反应ⅱ___________ (“能”或“不能”)自发进行。
(3)为提高反应ⅱ中氯乙烯的平衡产率,可采取的措施有___________ 。
a.加入合适的催化剂 b.升高温度 c.增大压强 d.及时氧化
(4)向 密闭容器中初始投入
密闭容器中初始投入 、
、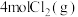 和
和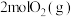 发生乙烯氧氯化反应,不同温度下测得反应在平衡时
发生乙烯氧氯化反应,不同温度下测得反应在平衡时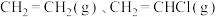 、
、 三种组分的体积分数随温度的变化如图1所示。
三种组分的体积分数随温度的变化如图1所示。___________ 和___________ 的体积分数随温度的变化。
②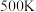 时反应进行到
时反应进行到 达到平衡,
达到平衡, 内用
内用 的浓度变化表示的
的浓度变化表示的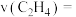
___________ ,该反应的平衡常数
___________ 。
(5) 时,控制进料浓度
时,控制进料浓度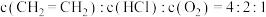 。容器中发生反应
。容器中发生反应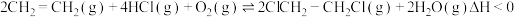 ,不同温度对
,不同温度对 的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过
的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过 转化为
转化为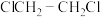 的转化率大小来体现)
的转化率大小来体现)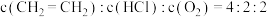 ,所得
,所得 的平衡转化率曲线应在点M的
的平衡转化率曲线应在点M的___________ (填“上”或“下”)方。
②因受现有工业设备限制,需保持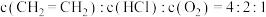 不变,在235℃、
不变,在235℃、 下,若要进一步增大
下,若要进一步增大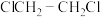 的选择性,可选择从
的选择性,可选择从___________ 方向进一步展开研究。

已知:ⅰ.

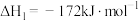
ⅱ.

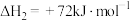
ⅲ.
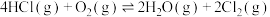
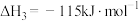
回答下列问题:
(1)

 。
。(2)已知
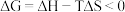 ,反应可自发进行。若
,反应可自发进行。若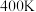 时反应ⅱ中
时反应ⅱ中 ,此时反应ⅱ
,此时反应ⅱ(3)为提高反应ⅱ中氯乙烯的平衡产率,可采取的措施有
a.加入合适的催化剂 b.升高温度 c.增大压强 d.及时氧化

(4)向
 密闭容器中初始投入
密闭容器中初始投入 、
、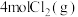 和
和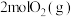 发生乙烯氧氯化反应,不同温度下测得反应在平衡时
发生乙烯氧氯化反应,不同温度下测得反应在平衡时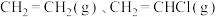 、
、 三种组分的体积分数随温度的变化如图1所示。
三种组分的体积分数随温度的变化如图1所示。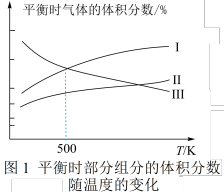
②
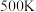 时反应进行到
时反应进行到 达到平衡,
达到平衡, 内用
内用 的浓度变化表示的
的浓度变化表示的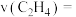

(5)
 时,控制进料浓度
时,控制进料浓度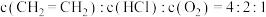 。容器中发生反应
。容器中发生反应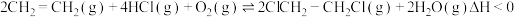 ,不同温度对
,不同温度对 的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过
的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过 转化为
转化为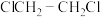 的转化率大小来体现)
的转化率大小来体现)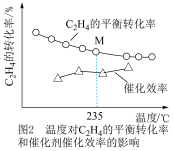
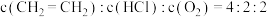 ,所得
,所得 的平衡转化率曲线应在点M的
的平衡转化率曲线应在点M的②因受现有工业设备限制,需保持
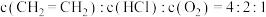 不变,在235℃、
不变,在235℃、 下,若要进一步增大
下,若要进一步增大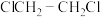 的选择性,可选择从
的选择性,可选择从
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】NO的处理与减排是烟气污染物控制的重点和难点,相关研究引起了国内外的广泛关注。
(1)理论上可采用加热使NO分解的方法处理: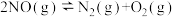 ,反应的部分数据如下表:
,反应的部分数据如下表:
通过计算得出高于7089℃时反应无法自发进行,试判断b____ 0(填“<”、“>”或“=”);反应的平衡常数表达式为____ ;实际反应时发现加热至600℃时NO仍没有明显分解,试解释原因___ 。
(2)科学家发现活性炭表面的有机结构可以被强氧化剂氧化成酚羟基、羧基(均可表示为C—OH,其电离平衡可表示为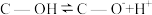 ),这些官能团可以使活性炭表面活性化,有利于NO的吸附。不同氧化剂的预氧化与吸附原理可表示为(未配平):
),这些官能团可以使活性炭表面活性化,有利于NO的吸附。不同氧化剂的预氧化与吸附原理可表示为(未配平):
预氧化: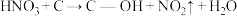
预氧化:
预氧化:
吸附: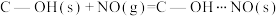
NO吸附实验分别在25℃和55℃下进行,将一定比例的 与NO混合气体在10 MPa恒压下,以相同速率持续通入到等量的、不同预氧化试剂处理的活性炭中(图象中“原始-C”表示未经处理的活性炭),获得两个温度下“NO捕获率-通气时间”的变化图:
与NO混合气体在10 MPa恒压下,以相同速率持续通入到等量的、不同预氧化试剂处理的活性炭中(图象中“原始-C”表示未经处理的活性炭),获得两个温度下“NO捕获率-通气时间”的变化图:
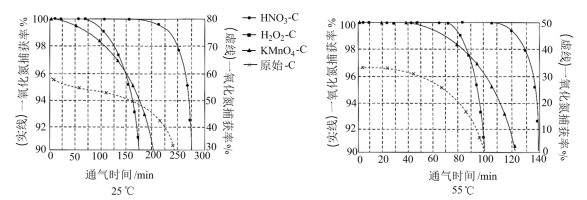
已知:NO捕获率=
请回答:
①下列描述正确的是_______
A.25℃下原始-C在通气约175分钟后吸附效果超过了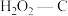
B.若其他条件不变,增大混合气体中 物质的量分数,吸附平衡会逆向移动
物质的量分数,吸附平衡会逆向移动
C.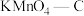 在实验中吸附效果不佳,可能是活性炭表面孔隙被堵塞
在实验中吸附效果不佳,可能是活性炭表面孔隙被堵塞
D.由图象可知升温有利于吸附平衡正向移动,故吸附过程的
②其他条件不变,55℃下增大烟气中水蒸气含量后,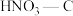 的NO捕获率会迅速降低,通气1小时后为40%,70 min后吸附到达平衡。请在对应图象中用虚线画出通气1小时后至吸附平衡为止NO捕获率的变化曲线
的NO捕获率会迅速降低,通气1小时后为40%,70 min后吸附到达平衡。请在对应图象中用虚线画出通气1小时后至吸附平衡为止NO捕获率的变化曲线____________ 。
③相比其他预氧化试剂处理的活性炭,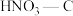 吸附效果更佳,有研究者认为可能是
吸附效果更佳,有研究者认为可能是 引入了
引入了 ,增强了活性炭的表面活性。试利用勒夏特列原理予以解释
,增强了活性炭的表面活性。试利用勒夏特列原理予以解释_______ 。
(1)理论上可采用加热使NO分解的方法处理:
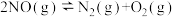 ,反应的部分数据如下表:
,反应的部分数据如下表:项目 |
|
| 正反应活化能 | 逆反应活化能 |
数据/ | a | b | 728 | 910 |
通过计算得出高于7089℃时反应无法自发进行,试判断b
(2)科学家发现活性炭表面的有机结构可以被强氧化剂氧化成酚羟基、羧基(均可表示为C—OH,其电离平衡可表示为
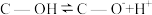 ),这些官能团可以使活性炭表面活性化,有利于NO的吸附。不同氧化剂的预氧化与吸附原理可表示为(未配平):
),这些官能团可以使活性炭表面活性化,有利于NO的吸附。不同氧化剂的预氧化与吸附原理可表示为(未配平):预氧化:
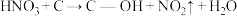
预氧化:

预氧化:

吸附:
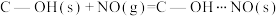
NO吸附实验分别在25℃和55℃下进行,将一定比例的
 与NO混合气体在10 MPa恒压下,以相同速率持续通入到等量的、不同预氧化试剂处理的活性炭中(图象中“原始-C”表示未经处理的活性炭),获得两个温度下“NO捕获率-通气时间”的变化图:
与NO混合气体在10 MPa恒压下,以相同速率持续通入到等量的、不同预氧化试剂处理的活性炭中(图象中“原始-C”表示未经处理的活性炭),获得两个温度下“NO捕获率-通气时间”的变化图:
已知:NO捕获率=

请回答:
①下列描述正确的是
A.25℃下原始-C在通气约175分钟后吸附效果超过了
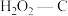
B.若其他条件不变,增大混合气体中
 物质的量分数,吸附平衡会逆向移动
物质的量分数,吸附平衡会逆向移动C.
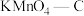 在实验中吸附效果不佳,可能是活性炭表面孔隙被堵塞
在实验中吸附效果不佳,可能是活性炭表面孔隙被堵塞D.由图象可知升温有利于吸附平衡正向移动,故吸附过程的

②其他条件不变,55℃下增大烟气中水蒸气含量后,
 的NO捕获率会迅速降低,通气1小时后为40%,70 min后吸附到达平衡。请在对应图象中用虚线画出通气1小时后至吸附平衡为止NO捕获率的变化曲线
的NO捕获率会迅速降低,通气1小时后为40%,70 min后吸附到达平衡。请在对应图象中用虚线画出通气1小时后至吸附平衡为止NO捕获率的变化曲线③相比其他预氧化试剂处理的活性炭,
 吸附效果更佳,有研究者认为可能是
吸附效果更佳,有研究者认为可能是 引入了
引入了 ,增强了活性炭的表面活性。试利用勒夏特列原理予以解释
,增强了活性炭的表面活性。试利用勒夏特列原理予以解释
您最近一年使用:0次
【推荐1】氨气广泛应用于化工、轻工、化肥、制药、合成纤维等领域,合成氨工业极大地影响了人类的发展历程。
(1)工业上用氨和二氧化碳为原料,在一定条件下合成尿素CO(NH2)2,已知:
①2NH3(g)+CO2(g)=NH2COONH4(s) ΔH = -159.5kJ/mol
②NH2COONH4(s)=CO(NH2)2(s)+H2O(g) ΔH = +116.5kJ/mol
③H2O(l)=H2O(g) ΔH = +44.0kJ/mol
写出氨气与二氧化碳生成尿素和液态水的热化学反应方程式__________ 。
(2)已知反应N2(g)+3H2(g)⇌2NH3(g) ΔH <0,一定温度下,将N2和H2以物质的量之比为1∶1充入盛有催化剂的密闭容器,下列图象t时刻一定处于平衡状态的是______ 。
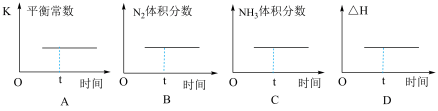
(3)200℃时,将N2(g)和H2(g)以物质的量之比为1∶3充入恒压容器中,容器内起始压强为P0,达到平衡时N2的转化率为50%,则该反应的平衡常数KP=___________ (用含有P0的式子表示。KP为分压平衡常数,气体分压=气体总压强×该气体的体积分数)
(4)某温度下,将一定量的NH3充入盛有催化剂的恒容容器中,一段时间达到平衡后,升高温度,当再次达到平衡时,N2的分压增大,原因是_________ 。
(5)我国科学家利用密度泛函理论筛选出合成氨的优良催化剂——担载单原子钼的缺陷硼氮单层材料,反应历程如图:
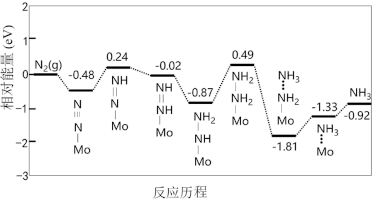
该反应历程中需要吸收能量的最大能垒(活化能)E=__________ eV。
(6)中科院大连化物所应用混合导体透氧膜制备氨合成气和液体燃料合成气,工作原理如图所示,请写出膜Ⅰ侧H2O发生的电极反应方程式:_________ 。

(7)25℃时,将2a mol/L的稀氨水与a mol/L的盐酸等体积混合后,试比较下列关系的大小(填“<”“>”或“=”):c(NH ) + c(H+)
) + c(H+)____ c(NH3∙H2O) + c(OH-) (NH3∙H2O的Kb=1.8×10-5)
(1)工业上用氨和二氧化碳为原料,在一定条件下合成尿素CO(NH2)2,已知:
①2NH3(g)+CO2(g)=NH2COONH4(s) ΔH = -159.5kJ/mol
②NH2COONH4(s)=CO(NH2)2(s)+H2O(g) ΔH = +116.5kJ/mol
③H2O(l)=H2O(g) ΔH = +44.0kJ/mol
写出氨气与二氧化碳生成尿素和液态水的热化学反应方程式
(2)已知反应N2(g)+3H2(g)⇌2NH3(g) ΔH <0,一定温度下,将N2和H2以物质的量之比为1∶1充入盛有催化剂的密闭容器,下列图象t时刻一定处于平衡状态的是

(3)200℃时,将N2(g)和H2(g)以物质的量之比为1∶3充入恒压容器中,容器内起始压强为P0,达到平衡时N2的转化率为50%,则该反应的平衡常数KP=
(4)某温度下,将一定量的NH3充入盛有催化剂的恒容容器中,一段时间达到平衡后,升高温度,当再次达到平衡时,N2的分压增大,原因是
(5)我国科学家利用密度泛函理论筛选出合成氨的优良催化剂——担载单原子钼的缺陷硼氮单层材料,反应历程如图:

该反应历程中需要吸收能量的最大能垒(活化能)E=
(6)中科院大连化物所应用混合导体透氧膜制备氨合成气和液体燃料合成气,工作原理如图所示,请写出膜Ⅰ侧H2O发生的电极反应方程式:

(7)25℃时,将2a mol/L的稀氨水与a mol/L的盐酸等体积混合后,试比较下列关系的大小(填“<”“>”或“=”):c(NH
 ) + c(H+)
) + c(H+)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】合成氨反应N2(g)+3H2(g) 2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。
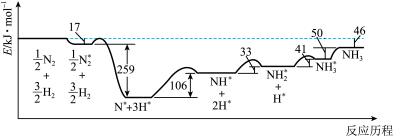
该历程中反应速率最慢的步骤的方程式为________ 。
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入 =3的混合气体,体系中各气体的含量与时间变化关系如图所示:
=3的混合气体,体系中各气体的含量与时间变化关系如图所示:

①以下叙述不能 说明该条件下反应达到平衡状态的是_________ (填字母)。
a.氨气的体积分数保持不变
b.容器中 保持不变
保持不变
c.气体平均相对分子质量保持不变
d.气体密度保持不变
e.3v(H2)=v(N2)
②反应20min时达到平衡,则0~20min内v(H2)=________ MPa•min-1,该反应的Kp=_______ MPa-2(保留小数点后两位)。(Kp为以分压表示的平衡常数)
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中_________ 点(填“d”“e”“f”或“g”)。
(3)氨化脱硝过程发生反应4NO(g)+4NH3(g)+O2(g)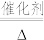 4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因_________ 。
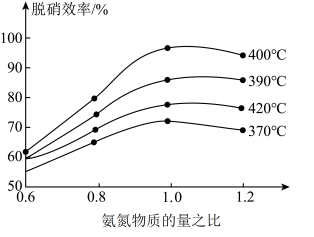
(4)25℃用甲酸吸收氨气可得到HCOONH4溶液。已知:25℃时甲酸的Ka=1.75×10-5,NH3•H2O的Kb=2×10-5。则反应NH3•H2O+HCOOH HCOO-+NH
HCOO-+NH +H2O的平衡常数K=
+H2O的平衡常数K=________ 。
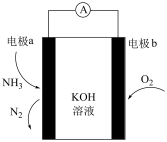
(5)化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图NH3如图。电极a上的电极反应式为:________ 。
 2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。

该历程中反应速率最慢的步骤的方程式为
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入
 =3的混合气体,体系中各气体的含量与时间变化关系如图所示:
=3的混合气体,体系中各气体的含量与时间变化关系如图所示:
①以下叙述
a.氨气的体积分数保持不变
b.容器中
 保持不变
保持不变c.气体平均相对分子质量保持不变
d.气体密度保持不变
e.3v(H2)=v(N2)
②反应20min时达到平衡,则0~20min内v(H2)=
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中
(3)氨化脱硝过程发生反应4NO(g)+4NH3(g)+O2(g)
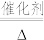 4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
(4)25℃用甲酸吸收氨气可得到HCOONH4溶液。已知:25℃时甲酸的Ka=1.75×10-5,NH3•H2O的Kb=2×10-5。则反应NH3•H2O+HCOOH
 HCOO-+NH
HCOO-+NH +H2O的平衡常数K=
+H2O的平衡常数K=(5)化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图NH3如图。电极a上的电极反应式为:

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.煤是重要的化工原料,利用煤的气化、液化可制取甲醇等有机物,其中发生的反应有:
①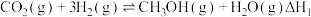
②
相关物质的化学键键能数据如下:
(1)试计算该反应
___________ 。
Ⅱ.“绿水青山,就是金山银山”,环境问题已被受全球广泛关注。氮的氧化物是大气主要污染物之一,环境保护的重要任务之一就是减少氮的氧化物等污染物在大气中的排放。
查有关资料可知:的反应历程分两步:
第一步: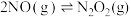 (快)
(快) 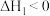 ;
;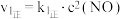 ;
;
第二步: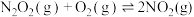 (慢)
(慢) 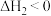 ;
;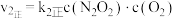 ;
;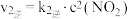
(2)一定条件下,当反应 达到平衡状态时:
达到平衡状态时:
①可用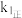 、
、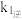 、
、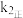 、
、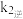 表示该反应的平衡常数,其表达式为
表示该反应的平衡常数,其表达式为
___________ ;
②已知:上述反应的平衡常数的对数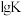 随温度的变化如图所示,在温度为
随温度的变化如图所示,在温度为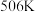 时此反应在A点达到平衡。若升高温度,B、C、D、E四点中能正确表示该反应的
时此反应在A点达到平衡。若升高温度,B、C、D、E四点中能正确表示该反应的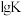 与T的关系的点为
与T的关系的点为___________ 。

(3) 是一种新型硝化剂,人们对它的性质和制备广泛关注。已知:在
是一种新型硝化剂,人们对它的性质和制备广泛关注。已知:在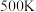 时可发生分解:
时可发生分解: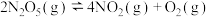 。此温度下,测得恒容密闭容器中
。此温度下,测得恒容密闭容器中 浓度随时间的变化如下表:
浓度随时间的变化如下表:
①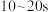 内,用
内,用 来表示的平均化学反应速率为
来表示的平均化学反应速率为___________ ;
②在此温度下,于恒容密闭容器中充入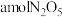 进行此反应,能说明该反应已达到化学平衡状态的是
进行此反应,能说明该反应已达到化学平衡状态的是___________ (填字母)
a.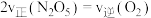
b. 和
和 的浓度之比保持不变
的浓度之比保持不变
c.在绝热容器中,反应的平衡常数不再变化
d.容器内气体的平均相对分子质量为45,且保持不变
(4)将一定量的 加入到恒温恒压的密闭容器中(温度
加入到恒温恒压的密闭容器中(温度 、压强
、压强 )。在反应
)。在反应 中,正反应速率
中,正反应速率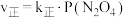 ,逆反应速率
,逆反应速率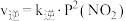 ,其中
,其中 、
、 为速率常数,p为分压(分压=总压×物质的量分数),若该条件下
为速率常数,p为分压(分压=总压×物质的量分数),若该条件下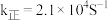 ,当
,当 的
的 分解时,
分解时,
___________ 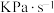 。
。
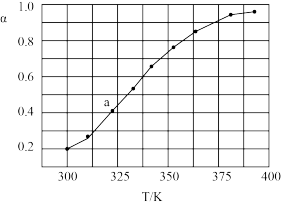
(5)将一定量 加入恒容密闭容器中,发生反应
加入恒容密闭容器中,发生反应 。测得在不同温度下,
。测得在不同温度下, 的物质的量分数
的物质的量分数 如图所示。已知
如图所示。已知 的起始压强
的起始压强 为
为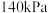 ,试计算图中a点对应温度下以平衡分压来表示的平衡常数
,试计算图中a点对应温度下以平衡分压来表示的平衡常数
___________ 。
①
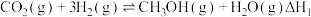
②

相关物质的化学键键能数据如下:
| 化学键 |  |  |  |  |  |
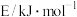 | 703 | 355 | 465 | 516 | 583 |
(1)试计算该反应

Ⅱ.“绿水青山,就是金山银山”,环境问题已被受全球广泛关注。氮的氧化物是大气主要污染物之一,环境保护的重要任务之一就是减少氮的氧化物等污染物在大气中的排放。
查有关资料可知:的反应历程分两步:
第一步:
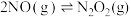 (快)
(快) 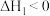 ;
;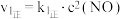 ;
;
第二步:
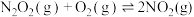 (慢)
(慢) 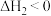 ;
;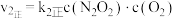 ;
;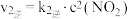
(2)一定条件下,当反应
 达到平衡状态时:
达到平衡状态时:①可用
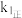 、
、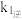 、
、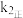 、
、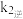 表示该反应的平衡常数,其表达式为
表示该反应的平衡常数,其表达式为
②已知:上述反应的平衡常数的对数
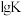 随温度的变化如图所示,在温度为
随温度的变化如图所示,在温度为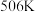 时此反应在A点达到平衡。若升高温度,B、C、D、E四点中能正确表示该反应的
时此反应在A点达到平衡。若升高温度,B、C、D、E四点中能正确表示该反应的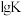 与T的关系的点为
与T的关系的点为
(3)
 是一种新型硝化剂,人们对它的性质和制备广泛关注。已知:在
是一种新型硝化剂,人们对它的性质和制备广泛关注。已知:在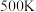 时可发生分解:
时可发生分解: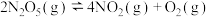 。此温度下,测得恒容密闭容器中
。此温度下,测得恒容密闭容器中 浓度随时间的变化如下表:
浓度随时间的变化如下表: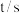 | 0 | 10 | 20 |
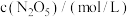 | 2.5 | 1.5 | 1.3 |
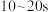 内,用
内,用 来表示的平均化学反应速率为
来表示的平均化学反应速率为②在此温度下,于恒容密闭容器中充入
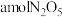 进行此反应,能说明该反应已达到化学平衡状态的是
进行此反应,能说明该反应已达到化学平衡状态的是a.
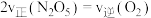
b.
 和
和 的浓度之比保持不变
的浓度之比保持不变c.在绝热容器中,反应的平衡常数不再变化
d.容器内气体的平均相对分子质量为45,且保持不变
(4)将一定量的
 加入到恒温恒压的密闭容器中(温度
加入到恒温恒压的密闭容器中(温度 、压强
、压强 )。在反应
)。在反应 中,正反应速率
中,正反应速率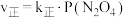 ,逆反应速率
,逆反应速率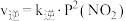 ,其中
,其中 、
、 为速率常数,p为分压(分压=总压×物质的量分数),若该条件下
为速率常数,p为分压(分压=总压×物质的量分数),若该条件下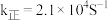 ,当
,当 的
的 分解时,
分解时,
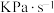 。
。(5)将一定量
 加入恒容密闭容器中,发生反应
加入恒容密闭容器中,发生反应 。测得在不同温度下,
。测得在不同温度下, 的物质的量分数
的物质的量分数 如图所示。已知
如图所示。已知 的起始压强
的起始压强 为
为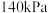 ,试计算图中a点对应温度下以平衡分压来表示的平衡常数
,试计算图中a点对应温度下以平衡分压来表示的平衡常数

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】掺杂硒的纳米氧化亚铜催化剂可用于工业合成甲醇,其反应为
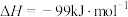 ,回答下列问题:
,回答下列问题:
(1)按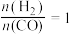 投料,将
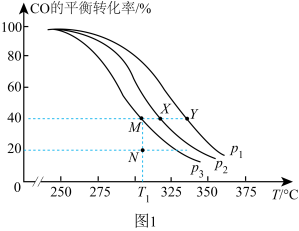
投料,将 与CO充入一密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的变化关系如图1所示。
与CO充入一密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的变化关系如图1所示。
已知: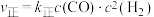 ,
,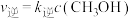 ,其中
,其中 、
、 为速率常数。
为速率常数。
①根据影响化学反应速率的因素,推测下列对速率常数的大小没有影响的是_______ (填标号)。
A.温度 B.活化能 C.反应物浓度 D.催化剂
②压强 、
、 、
、 由小到大的顺序是
由小到大的顺序是_______ 。
③ ℃、压强为
℃、压强为 时,若密闭容器体积为VL,向其中充入
时,若密闭容器体积为VL,向其中充入 和3molCO发生反应,5min后反应达到平衡,则0~5min内,
和3molCO发生反应,5min后反应达到平衡,则0~5min内,
_____  。若N点对应的压强为
。若N点对应的压强为 ,则反应处于该点时
,则反应处于该点时
_____ (填“>”“<”或“=”) 。X、Y、M三点对应的平衡常数从大到小的顺序是
。X、Y、M三点对应的平衡常数从大到小的顺序是_____ 。
(2)向10L恒容密闭容器中充入2molCO和 发生反应,若体系起始时和平衡时温度均为325℃,体系总压强
发生反应,若体系起始时和平衡时温度均为325℃,体系总压强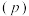 与时间
与时间 的关系如图2中曲线I所示,曲线II为只改变某一条件的变化曲线。
的关系如图2中曲线I所示,曲线II为只改变某一条件的变化曲线。
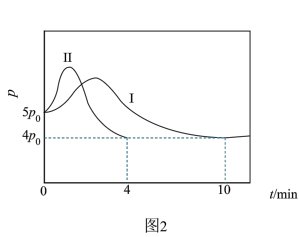
①曲线II所对应的反应改变的条件可能为_______ 。
②体系总压强先增大后减小的原因为_______ 。
③该条件下 的平衡转化率为
的平衡转化率为_______ %(结果保留1位小数)。

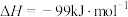 ,回答下列问题:
,回答下列问题:(1)按
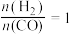 投料,将
投料,将 与CO充入一密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的变化关系如图1所示。
与CO充入一密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的变化关系如图1所示。
已知:
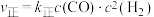 ,
,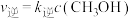 ,其中
,其中 、
、 为速率常数。
为速率常数。①根据影响化学反应速率的因素,推测下列对速率常数的大小没有影响的是
A.温度 B.活化能 C.反应物浓度 D.催化剂
②压强
 、
、 、
、 由小到大的顺序是
由小到大的顺序是③
 ℃、压强为
℃、压强为 时,若密闭容器体积为VL,向其中充入
时,若密闭容器体积为VL,向其中充入 和3molCO发生反应,5min后反应达到平衡,则0~5min内,
和3molCO发生反应,5min后反应达到平衡,则0~5min内,
 。若N点对应的压强为
。若N点对应的压强为 ,则反应处于该点时
,则反应处于该点时
 。X、Y、M三点对应的平衡常数从大到小的顺序是
。X、Y、M三点对应的平衡常数从大到小的顺序是(2)向10L恒容密闭容器中充入2molCO和
 发生反应,若体系起始时和平衡时温度均为325℃,体系总压强
发生反应,若体系起始时和平衡时温度均为325℃,体系总压强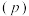 与时间
与时间 的关系如图2中曲线I所示,曲线II为只改变某一条件的变化曲线。
的关系如图2中曲线I所示,曲线II为只改变某一条件的变化曲线。
①曲线II所对应的反应改变的条件可能为
②体系总压强先增大后减小的原因为
③该条件下
 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】合成氨工业和硫酸工业在国民经济中占有重要地位。
(1)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO其反应为:[Cu(NH3)2]++CO+NH3 [Cu(NH3)3CO]+ △H<0。吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用。铜氨液再生适宜的生产条件是
[Cu(NH3)3CO]+ △H<0。吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用。铜氨液再生适宜的生产条件是_______ 。
(2)将等物质的量的H2和N2通入绝热恒容密闭容器中发生反应N2(g)+3H2(g) 2NH3(g) △H<0,下列选项表明反应一定已达平衡状态的是_______(填标号,下同)。
2NH3(g) △H<0,下列选项表明反应一定已达平衡状态的是_______(填标号,下同)。
接触法制硫酸的关键反应为SO2的催化氧化,二氧化硫在V2O5作用下的催化氧化是工业上生产硫酸的主要反应。SO2的催化氧化热化学方程式为:2SO2(g)+O2(g) 2SO3(g) △H=akJ·mol-1其催化机理分为三步:
2SO3(g) △H=akJ·mol-1其催化机理分为三步:
第1步:SO2(g)+V2O5(s) SO3(g)+V2O4(s) △H=bkJ·mol-1
SO3(g)+V2O4(s) △H=bkJ·mol-1
第2步:V2O4(s)+O2(g)+2SO2(g) 2VOSO4(s) △H=ckJ·mol-1
2VOSO4(s) △H=ckJ·mol-1
第3步:_______。
(3)第3步热化学方程式_______ (△H的值用a、b、c的代数式表示)。
(4)T℃时,将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。3min时反应达到平衡,此时测得O2还剩余0.1mol。则达平衡时SO2的转化率为_______ ;从反应开始至达到平衡,用SO3表示反应速率为_______ 。
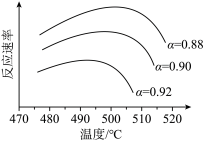
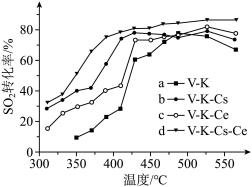
(5)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是_______。
(6)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是_______ (填标号)。
(7)设O2的平衡分压为p,SO2的平衡转化率为α,用含p和α的代数式表示上述催化氧化反应的Kp=_______ (用平衡分压代替平衡浓度计算)。
(1)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO其反应为:[Cu(NH3)2]++CO+NH3
 [Cu(NH3)3CO]+ △H<0。吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用。铜氨液再生适宜的生产条件是
[Cu(NH3)3CO]+ △H<0。吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用。铜氨液再生适宜的生产条件是(2)将等物质的量的H2和N2通入绝热恒容密闭容器中发生反应N2(g)+3H2(g)
 2NH3(g) △H<0,下列选项表明反应一定已达平衡状态的是_______(填标号,下同)。
2NH3(g) △H<0,下列选项表明反应一定已达平衡状态的是_______(填标号,下同)。| A.容器内的压强不再变化 |
| B.相同时间内,断开H-H键的数目和生成N-H键的数目相等 |
| C.容器内气体的浓度c(N2):c(H2):c(NH3)=1:3:2 |
| D.N2的体积分数不再发生变化 |
接触法制硫酸的关键反应为SO2的催化氧化,二氧化硫在V2O5作用下的催化氧化是工业上生产硫酸的主要反应。SO2的催化氧化热化学方程式为:2SO2(g)+O2(g)
 2SO3(g) △H=akJ·mol-1其催化机理分为三步:
2SO3(g) △H=akJ·mol-1其催化机理分为三步:第1步:SO2(g)+V2O5(s)
 SO3(g)+V2O4(s) △H=bkJ·mol-1
SO3(g)+V2O4(s) △H=bkJ·mol-1第2步:V2O4(s)+O2(g)+2SO2(g)
 2VOSO4(s) △H=ckJ·mol-1
2VOSO4(s) △H=ckJ·mol-1第3步:_______。
(3)第3步热化学方程式
(4)T℃时,将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。3min时反应达到平衡,此时测得O2还剩余0.1mol。则达平衡时SO2的转化率为
(5)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是_______。

| A.温度越高,反应速率越大 |
| B.可根据不同α下的最大速率,选择最佳生产温度 |
| C.α=0.88的曲线代表平衡转化率 |
| D.α越大,反应速率最大值对应温度越低 |
(6)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是

(7)设O2的平衡分压为p,SO2的平衡转化率为α,用含p和α的代数式表示上述催化氧化反应的Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】研究氮、碳及其化合物的资源化利用具有重要的意义。
(1)过渡金属催化还原氮气合成氨具有巨大前景。催化过程一般有吸附—解离—反应—脱附等过程,图示为N2和H2在固体催化剂表面合成氨反应路径的势能面图(部分数据略),其中“*”表示被催化剂吸附。
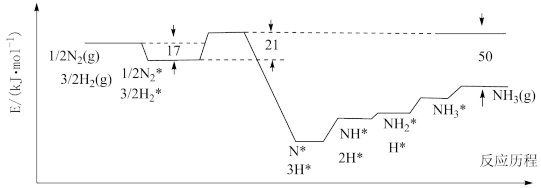
氨气的脱附是过程_____ (填“吸热”或“放热”),合成氨的热化学方程式为_____ 。
(2)若将2.0molN2和6.0molH2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2温度下n(H2)的变化,曲线B表示T1温度下n(NH3)的变化,T2温度下反应到a点恰好达到平衡。
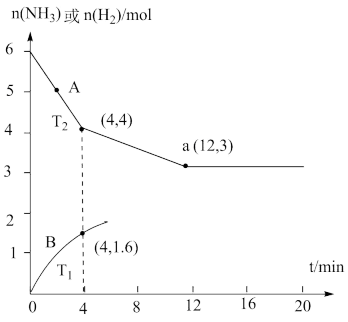
①T2温度下,从开始到12min用NH3浓度变化表示的平均反应速率V(NH3)=_____ mol•L-1•min-1,达平衡时N2的转化率为_____ 。
②温度T1_____ T2(填“>”“<”或“=”下同)。T1温度下恰好平衡时,曲线B上的点为b(m,n),则m_____ 12,n_____ 2。
(3)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
①C(s)+H2O(g) CO(g)+H2(g) △H1=+131.3kJ•mol-1 K1
CO(g)+H2(g) △H1=+131.3kJ•mol-1 K1
②C(s)+2H2O(g) CO2(g)+2H2(g) △H2=+90.3kJ•mol-1 K2
CO2(g)+2H2(g) △H2=+90.3kJ•mol-1 K2
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.0kJ•mol-1 K3
CO2(g)+H2(g) △H3=-41.0kJ•mol-1 K3
三个反应的平衡常数随温度变化的关系如图所示,则表示K1、K2、K3的曲线分别是c、_____ 、_____ 。

(4)CO2在Cu—ZnO催化下,同时发生如下反应①、②,是解决温室效应和能源短缺的重要手段。
①CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1<0
CH3OH(g)+H2O(g) △H1<0
②CO2(g)+H2(g) CO(g)+H2O(g) △H2>0
CO(g)+H2O(g) △H2>0
在容积不变的密闭容器中,保持温度不变,充入一定量的CO2和H2,起始及达平衡时,容器内各气体的物质的量及总压强如表所示:
若容器内反应①、②均达到平衡时,P0=1.4p,反应①的平衡常数Kp=_____ (Kpa)-2。(用含P的式子表示,各气体的分压=总压强×气体物质的量分数,如P(CO2)=P总×nCO2%)
(1)过渡金属催化还原氮气合成氨具有巨大前景。催化过程一般有吸附—解离—反应—脱附等过程,图示为N2和H2在固体催化剂表面合成氨反应路径的势能面图(部分数据略),其中“*”表示被催化剂吸附。

氨气的脱附是过程
(2)若将2.0molN2和6.0molH2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2温度下n(H2)的变化,曲线B表示T1温度下n(NH3)的变化,T2温度下反应到a点恰好达到平衡。

①T2温度下,从开始到12min用NH3浓度变化表示的平均反应速率V(NH3)=
②温度T1
(3)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
①C(s)+H2O(g)
 CO(g)+H2(g) △H1=+131.3kJ•mol-1 K1
CO(g)+H2(g) △H1=+131.3kJ•mol-1 K1②C(s)+2H2O(g)
 CO2(g)+2H2(g) △H2=+90.3kJ•mol-1 K2
CO2(g)+2H2(g) △H2=+90.3kJ•mol-1 K2③CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-41.0kJ•mol-1 K3
CO2(g)+H2(g) △H3=-41.0kJ•mol-1 K3三个反应的平衡常数随温度变化的关系如图所示,则表示K1、K2、K3的曲线分别是c、

(4)CO2在Cu—ZnO催化下,同时发生如下反应①、②,是解决温室效应和能源短缺的重要手段。
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1<0
CH3OH(g)+H2O(g) △H1<0②CO2(g)+H2(g)
 CO(g)+H2O(g) △H2>0
CO(g)+H2O(g) △H2>0在容积不变的密闭容器中,保持温度不变,充入一定量的CO2和H2,起始及达平衡时,容器内各气体的物质的量及总压强如表所示:
| CO2 | H2 | CH3OH | CO | H2O | 总压/KPa | |
| 起始/mol | 0.5 | 0.9 | 0 | 0 | 0 | P0 |
| 平衡/mol | n | 0.3 | p |
您最近一年使用:0次






