回答下列问题:
(1)写出下列物质的电离方程式:H2SO4_______ 、NH3·H2O_______ 、H2S_______ 、NaHCO3_______ 。
(2)现有①CH3COOH、②HCl两种溶液,选择填空:
A.①>② B.①<② C.①=②
①当它们的物质的量浓度相同时,其pH的关系为_______ 。
②当它们的物质的量浓度、体积相同时,消耗NaOH的物质的量的关系为_______ 。
③当它们的pH相同、体积相同时,分别加入足量锌,相同状况下产生气体的体积关系为_______ 。
(3)已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是_______。
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是_______。
(1)写出下列物质的电离方程式:H2SO4
(2)现有①CH3COOH、②HCl两种溶液,选择填空:
A.①>② B.①<② C.①=②
①当它们的物质的量浓度相同时,其pH的关系为
②当它们的物质的量浓度、体积相同时,消耗NaOH的物质的量的关系为
③当它们的pH相同、体积相同时,分别加入足量锌,相同状况下产生气体的体积关系为
(3)已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH
 CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是_______。
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是_______。| A.加少量烧碱固体 | B.降低温度 | C.加少量醋酸钠固体 | D.加水 |
更新时间:2022-10-22 18:03:01
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】某二元酸(H2A)在水中的电离方程式是:H2A=H++HA- ,HA- H++A2-。已知0.1mol·L-1 的NaHA溶液中c(H+)=0.01 mol·L-1 . 则0.1mol·L-1 H2A溶液中氢离子的物质的量浓度应
H++A2-。已知0.1mol·L-1 的NaHA溶液中c(H+)=0.01 mol·L-1 . 则0.1mol·L-1 H2A溶液中氢离子的物质的量浓度应_________ 0.11 mol·L-1 (填“<”,“>”或“=”), 理由是:_______________ 。
 H++A2-。已知0.1mol·L-1 的NaHA溶液中c(H+)=0.01 mol·L-1 . 则0.1mol·L-1 H2A溶液中氢离子的物质的量浓度应
H++A2-。已知0.1mol·L-1 的NaHA溶液中c(H+)=0.01 mol·L-1 . 则0.1mol·L-1 H2A溶液中氢离子的物质的量浓度应
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请回答下列问题:
(1)某浓度的氨水中存在平衡:NH3·H2O NH
NH +OH-。若增大NH
+OH-。若增大NH 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。
a.加入NH4Cl固体 b.适当升高温度 c.通入NH3 d.加入少量浓盐酸
(2)常温下,c(H+)相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
①加适量醋酸钠晶体后,醋酸溶液中c(H+)___________ (填“增大”、“减小”或“不变”,下同),盐酸中c(H+)___________ 。
②加水稀释10倍后,醋酸溶液中的c(H+)___________ (填“>”、“=”或“<”)盐酸中的c(H+)。
③加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸___________ (填“>”“=”或“<”)盐酸。
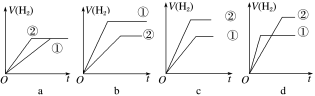
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是___________ (填字母)。(①表示盐酸,②表示醋酸)
(3)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是___________ (填字母)。
a.电离程度增大 b.溶液中离子浓度都增大 c.Ka(乙酸)不变 d.溶液中醋酸分子减少
(1)某浓度的氨水中存在平衡:NH3·H2O
 NH
NH +OH-。若增大NH
+OH-。若增大NH 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是a.加入NH4Cl固体 b.适当升高温度 c.通入NH3 d.加入少量浓盐酸
(2)常温下,c(H+)相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
①加适量醋酸钠晶体后,醋酸溶液中c(H+)
②加水稀释10倍后,醋酸溶液中的c(H+)
③加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

(3)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是
a.电离程度增大 b.溶液中离子浓度都增大 c.Ka(乙酸)不变 d.溶液中醋酸分子减少
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)将等体积等物质的量浓度的盐酸和氨水混合后,呈___________ 性,溶液中c( )与c(Cl-)的大小关系是
)与c(Cl-)的大小关系是___________ ;
(2)常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈___________ 性,溶液中c( )与c(Cl-)的大小关系是
)与c(Cl-)的大小关系是___________ ;
(3)将物质的量浓度相同的盐酸与氨水混合后,溶液中c( )与c(Cl-)浓度相等,则混合溶液呈
)与c(Cl-)浓度相等,则混合溶液呈___________ 性,盐酸与氨水体积大小关系是___________ ;
(4)常温下,将m mol/L的盐酸和n mol/L氨水等体积混合后,溶液的pH=7,m与n的大小关系是___________ ,则盐酸中c(H+)与氨水中c(OH-)的大小关系是___________ 。
 )与c(Cl-)的大小关系是
)与c(Cl-)的大小关系是(2)常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈
 )与c(Cl-)的大小关系是
)与c(Cl-)的大小关系是(3)将物质的量浓度相同的盐酸与氨水混合后,溶液中c(
 )与c(Cl-)浓度相等,则混合溶液呈
)与c(Cl-)浓度相等,则混合溶液呈(4)常温下,将m mol/L的盐酸和n mol/L氨水等体积混合后,溶液的pH=7,m与n的大小关系是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】常温下,有c(H+)相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
(1)加适量醋酸钠晶体后,醋酸溶液中c(H+)_______ (填“增大”“减小”或“不变”,下同),盐酸中c(H+)______ 。
(2)加水稀释10倍后,醋酸溶液中的c(H+)______ (填“>”“=”或“<”)盐酸中的c(H+)。
(3)加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸_______ (填“>”“=”或“<”)盐酸。
(4)使温度都升高20℃,溶液中c(H+):醋酸________ (填“>”“=”或“<”)盐酸。
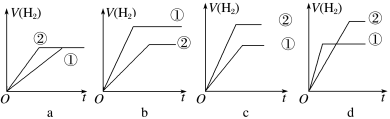
(5)分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)
(1)加适量醋酸钠晶体后,醋酸溶液中c(H+)
(2)加水稀释10倍后,醋酸溶液中的c(H+)
(3)加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸
(4)使温度都升高20℃,溶液中c(H+):醋酸
(5)分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH⇌CH3COO-+H+;ΔH>0
(1)25℃时,浓度均为0.1mol/L的盐酸和醋酸溶液,下列说法正确的是______ (填序号)
①两溶液的pH相同
②两溶液的导电能力相同
③由水电离出的c(OH-)相同
④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
(2)25℃时,向pH均为1的盐酸和醋酸溶液中分别加水,随加水量的增多,两溶液pH的变化如图所示,则符合盐酸pH变化的曲线是______ ;

(3)25℃时,向体积为Va mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va______ Vb(填“>”、“<”或“=”),请写出此时电荷守恒关系式:______ ;
(1)25℃时,浓度均为0.1mol/L的盐酸和醋酸溶液,下列说法正确的是
①两溶液的pH相同
②两溶液的导电能力相同
③由水电离出的c(OH-)相同
④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
(2)25℃时,向pH均为1的盐酸和醋酸溶液中分别加水,随加水量的增多,两溶液pH的变化如图所示,则符合盐酸pH变化的曲线是

(3)25℃时,向体积为Va mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】人类食用醋的历史已有10000多年,有关醋的文字记载也至少有3000年,醋和食盐一样属于最古老的调味品。
Ⅰ.某兴趣小组为确定 是弱电解质并分析其中的变化,设计如下实验方案。
是弱电解质并分析其中的变化,设计如下实验方案。
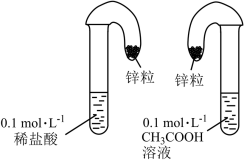
方案一:如图所示,取纯度、质量、大小相同的锌粒于两只相同气球中,同时将锌粒分别加入盛有10mL 溶液和稀盐酸的试管中,充分反应。
溶液和稀盐酸的试管中,充分反应。
方案二:用pH计测定浓度为0.1 的
的 溶液的pH。
溶液的pH。
方案三:配制pH=3的 溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
回答下列问题:
(1)方案一中,说明 是弱电解质的实验现象是
是弱电解质的实验现象是___________ (填字母)。
a.两个试管上方的气球同时鼓起,且体积一样大
b.装有盐酸的试管上方的气球鼓起慢
c.装有 的试管上方的气球鼓起慢
的试管上方的气球鼓起慢
d.装有 的试管上方的气球鼓起体积小
的试管上方的气球鼓起体积小
(2)方案二中,测得0.1 的
的 溶液的pH
溶液的pH___________ 1(填“>”“<”或“=”)。
(3)方案三中,所得醋酸溶液与pH=5的盐酸溶液,比较c(CH3COO-)___________ c(Cl-)(填“>”“<”或“=”)。
Ⅱ.完成下列问题
(4)根据 在溶液中的电离平衡移动的原理分析,为使
在溶液中的电离平衡移动的原理分析,为使 的电离程度和
的电离程度和 都减小,
都减小,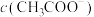 增加,可向0.1
增加,可向0.1 的
的 溶液中,选择加入的试剂是
溶液中,选择加入的试剂是___________ (填化学式)。
(5)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是___________ (填选项字母,下同)。
A.c(H+) B.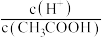 C.c(H+)∙c(OH-) D.
C.c(H+)∙c(OH-) D. E.
E.
若该溶液升高温度,上述5种表达式的数据一定增大的是___________ 。
(6)25℃时,将amolL-1的醋酸溶液与bmolL-1氢氧化钠溶液等体积混合,反应后溶液恰好显中性,则溶液中c(Na+)___________ c(CH3COO-)(填写“>”、“=”或“<”)。
Ⅰ.某兴趣小组为确定
 是弱电解质并分析其中的变化,设计如下实验方案。
是弱电解质并分析其中的变化,设计如下实验方案。方案一:如图所示,取纯度、质量、大小相同的锌粒于两只相同气球中,同时将锌粒分别加入盛有10mL
 溶液和稀盐酸的试管中,充分反应。
溶液和稀盐酸的试管中,充分反应。
方案二:用pH计测定浓度为0.1
 的
的 溶液的pH。
溶液的pH。方案三:配制pH=3的
 溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
溶液250mL,取5mL稀释至500mL,再用pH计测其pH。回答下列问题:
(1)方案一中,说明
 是弱电解质的实验现象是
是弱电解质的实验现象是a.两个试管上方的气球同时鼓起,且体积一样大
b.装有盐酸的试管上方的气球鼓起慢
c.装有
 的试管上方的气球鼓起慢
的试管上方的气球鼓起慢d.装有
 的试管上方的气球鼓起体积小
的试管上方的气球鼓起体积小(2)方案二中,测得0.1
 的
的 溶液的pH
溶液的pH(3)方案三中,所得醋酸溶液与pH=5的盐酸溶液,比较c(CH3COO-)
Ⅱ.完成下列问题
(4)根据
 在溶液中的电离平衡移动的原理分析,为使
在溶液中的电离平衡移动的原理分析,为使 的电离程度和
的电离程度和 都减小,
都减小,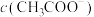 增加,可向0.1
增加,可向0.1 的
的 溶液中,选择加入的试剂是
溶液中,选择加入的试剂是(5)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+) B.
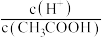 C.c(H+)∙c(OH-) D.
C.c(H+)∙c(OH-) D. E.
E.
若该溶液升高温度,上述5种表达式的数据一定增大的是
(6)25℃时,将amolL-1的醋酸溶液与bmolL-1氢氧化钠溶液等体积混合,反应后溶液恰好显中性,则溶液中c(Na+)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】25℃时部分弱电解质的电离常数如下表:
(1)①25℃时,pH相等的HCN、 、
、 物质的量浓度从大到小的顺序是
物质的量浓度从大到小的顺序是_______ 。
②下列反应方程式正确的是_______ 。
A.少量的 通入到NaClO溶液中:
通入到NaClO溶液中: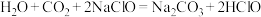
B.往 溶液中滴加少量
溶液中滴加少量 :
:
C.往 溶液中滴加过量HCN:
溶液中滴加过量HCN: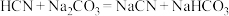
D.往 溶液中滴加HClO:
溶液中滴加HClO:
(2)25℃时,氨水与 的混合溶液
的混合溶液 ,该溶液中
,该溶液中 :
:
___________ 。
(3)请设计实验证明, 溶液中存在
溶液中存在 的电离平衡:
的电离平衡:_______ 。
| 物质 | HCN |  | HClO |  |  |
| 电离常数 | 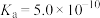 |  |  |   |  |
 、
、 物质的量浓度从大到小的顺序是
物质的量浓度从大到小的顺序是②下列反应方程式正确的是
A.少量的
 通入到NaClO溶液中:
通入到NaClO溶液中: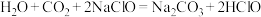
B.往
 溶液中滴加少量
溶液中滴加少量 :
:
C.往
 溶液中滴加过量HCN:
溶液中滴加过量HCN: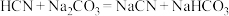
D.往
 溶液中滴加HClO:
溶液中滴加HClO:
(2)25℃时,氨水与
 的混合溶液
的混合溶液 ,该溶液中
,该溶液中 :
:
(3)请设计实验证明,
 溶液中存在
溶液中存在 的电离平衡:
的电离平衡:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某酸HA是一元弱酸,25℃时的电离平衡常数Ka=4.0×10-8。
(1)写出该酸的电离方程式____ ,其电离平衡常数表达式Ka=____ 。
(2)25℃时,向1mol•L-1HA溶液中加入1mol•L-1盐酸,会____ (“抑制”或“促进”)HA的电离,c(H+)____ (填“增大”、“减小”或“不变”),电离平衡常数Ka____ (填“增大”、“减小”或“不变”)。
(3)常温条件下,某浓度的盐酸溶液的pH=3,则其中c(H+)=____ mol/L,c(OH-)=____ mol/L。
(4)常温下等体积混合0.1mol/L的盐酸和0.06mol/L的Ba(OH)2溶液后,溶液pH=____ 。
(1)写出该酸的电离方程式
(2)25℃时,向1mol•L-1HA溶液中加入1mol•L-1盐酸,会
(3)常温条件下,某浓度的盐酸溶液的pH=3,则其中c(H+)=
(4)常温下等体积混合0.1mol/L的盐酸和0.06mol/L的Ba(OH)2溶液后,溶液pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】25℃时10mL0.10mol/L醋酸中存在电离平衡:CH3COOH CH3COO-+H+
CH3COO-+H+
(1)加入少量冰醋酸,醋酸电离程度___________ (填“增大”、“减小”、“不变”,下同)
(2)加入少量0.5mol/L盐酸,上述平衡向___________ 移动,c(H+)___________
(3)加入一定量蒸馏水,上述平衡向___________ 移动,n(H+)___________
(4)加入少量的Na2CO3固体,醋酸电离程度___________
 CH3COO-+H+
CH3COO-+H+(1)加入少量冰醋酸,醋酸电离程度
(2)加入少量0.5mol/L盐酸,上述平衡向
(3)加入一定量蒸馏水,上述平衡向
(4)加入少量的Na2CO3固体,醋酸电离程度
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答:
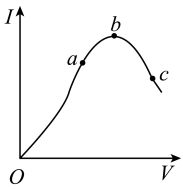
(1)“O”点处冰醋酸的导电能力为0的原因是_______________________ ;
(2)在a、b、c三点处,溶液中c(H+)由小到大的顺序为________ (用字母表示);
(3)在a、b、c三点处,电离程度最大的是________ (用字母表示);
(4)若使c点处的溶液中c(CH3COO-)增大,c(H+)减小,可采取的措施有①_____________ ;②______________ ;③____________ 。

(1)“O”点处冰醋酸的导电能力为0的原因是
(2)在a、b、c三点处,溶液中c(H+)由小到大的顺序为
(3)在a、b、c三点处,电离程度最大的是
(4)若使c点处的溶液中c(CH3COO-)增大,c(H+)减小,可采取的措施有①
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)内因:___________________ 。
(2)外因:①浓度:_________________________
②温度:________________________________________
③酸碱度
(3)酸式盐溶液的酸碱性:强酸酸式盐显__________ ,原因是_____________________________ 。多元弱酸酸式盐溶液的酸碱性取决于_____________________________________ ,例如NaHCO3溶液显碱性,原因是_________________ ,_______________________________ (离子方程式和文字说明);
NaHSO3溶液显酸性的原因是________________ ,_____________________ (离子方程式和文字说明)。
(4)用↑、↓、→、←表示,填表:CH3COONa溶液改变下列条件,填写变化情况:CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-_______________
(2)外因:①浓度:
②温度:
③酸碱度
(3)酸式盐溶液的酸碱性:强酸酸式盐显
NaHSO3溶液显酸性的原因是
(4)用↑、↓、→、←表示,填表:CH3COONa溶液改变下列条件,填写变化情况:CH3COO-+H2O
 CH3COOH+OH-
CH3COOH+OH-| 改变条件 | 平衡移动 | c(CH3COO-) | c(OH-) | 水解 |
| 加入CH3COONa | ||||
| 通入HCl | ||||
| 升温 | ||||
| 加水 | ||||
| 加NaOH | ||||
| 加HAc | ||||
| 加NH4Cl |
您最近一年使用:0次



