在密闭容器中进行如下反应: ,达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况。
,达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况。
(1)增加C的含量,平衡____________ ,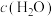
___________ .
(2)保持反应容器体积和温度不变,通入 ,平衡
,平衡____________ ,
____________ .
(3)在一定温度下,缩小反应容器体积,平衡向____________ 方向移动,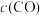
___________ , 的转化率
的转化率
______________ 。
(4)保持反应容器体积不变,升高温度,平衡向_________ 方向移动,
___________ .
(5)保持反应容器体积和温度不变,再通入 ,平衡向
,平衡向__________ 方向移动, 的转化率
的转化率
_________ ,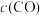
___________ 。
 ,达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况。
,达平衡后,改变下列条件,用“正反应”“逆反应”或“不移动”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断物质的量变情况。(1)增加C的含量,平衡
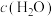
(2)保持反应容器体积和温度不变,通入
 ,平衡
,平衡
(3)在一定温度下,缩小反应容器体积,平衡向
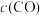
 的转化率
的转化率
(4)保持反应容器体积不变,升高温度,平衡向

(5)保持反应容器体积和温度不变,再通入
 ,平衡向
,平衡向 的转化率
的转化率
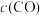
更新时间:2022-12-03 09:53:24
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在恒温恒容的容器中发生反应N2+3H2 2NH3,当反应达到平衡后,判断改变下列措施化学平衡移动的方向(填“正向移动”“逆向移动”或“不移动”)。
2NH3,当反应达到平衡后,判断改变下列措施化学平衡移动的方向(填“正向移动”“逆向移动”或“不移动”)。
(1)向容器中充氮气:_____ 。
(2)向容器中充氢气:_____ 。
(3)向容器中充氨气:_____ 。
(4)向容器中充氦气:_____ 。
(5)向容器中充入氯化氢气体:_____ 。
 2NH3,当反应达到平衡后,判断改变下列措施化学平衡移动的方向(填“正向移动”“逆向移动”或“不移动”)。
2NH3,当反应达到平衡后,判断改变下列措施化学平衡移动的方向(填“正向移动”“逆向移动”或“不移动”)。(1)向容器中充氮气:
(2)向容器中充氢气:
(3)向容器中充氨气:
(4)向容器中充氦气:
(5)向容器中充入氯化氢气体:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为________ 。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
_______CuSO4+_______PH3+_______H2O=_______Cu3P↓+_______H3PO4+_______H2SO4_______
(3)工业制备PH3的流程如图所示。

①白磷和烧碱溶液反应的化学方程式为:_________________ 。
②若起始时有1 mol P4参加反应,则整个工业流程中共生成________ mol PH3。
II. 、
、 、
、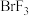 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是__________ 。
(2)溴化碘( )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为_______ ;
(3)已知某些离子的还原性强弱顺序为 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_________ ;
(1)AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
_______CuSO4+_______PH3+_______H2O=_______Cu3P↓+_______H3PO4+_______H2SO4
(3)工业制备PH3的流程如图所示。

①白磷和烧碱溶液反应的化学方程式为:
②若起始时有1 mol P4参加反应,则整个工业流程中共生成
II.
 、
、 、
、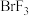 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是
(2)溴化碘(
 )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为(3)已知某些离子的还原性强弱顺序为
 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某化学小组研究草酸(H2C2O4)及其盐的性质。
(1)已知: ,
,
①将等物质的量浓度、等体积的H2C2O4溶液与KOH溶液混合,反应的离子方程式是_______ 。
②向①中继续加入KOH溶液至恰好完全反应,得到K2C2O4溶液。下列关系正确的是_______ (填字母)。
a.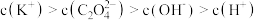
b.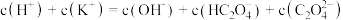
c.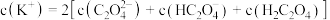
(2) 中碳元素的化合价是+3 价,推测其有还原性。文献表明:相同条件下,
中碳元素的化合价是+3 价,推测其有还原性。文献表明:相同条件下, 的还原性强于 Fe2+。为验证此结论,小组同学完成了如下实验:向10 mL0.5 mol·L−1FeCl3溶液中缓慢加入0.5mol·L−1K2C2O4溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
的还原性强于 Fe2+。为验证此结论,小组同学完成了如下实验:向10 mL0.5 mol·L−1FeCl3溶液中缓慢加入0.5mol·L−1K2C2O4溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
资料:三水三草酸合铁酸钾[K3Fe(C2O4)3·3H2O]为翠绿色晶体,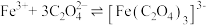 ,
,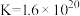 。
。
取少量晶体洗净,配成溶液,滴加KSCN溶液,不变红,继续加入硫酸,溶液变红。用平衡移动原理解释溶液变红的原因是_______ 。
(1)已知:
 ,
,
①将等物质的量浓度、等体积的H2C2O4溶液与KOH溶液混合,反应的离子方程式是
②向①中继续加入KOH溶液至恰好完全反应,得到K2C2O4溶液。下列关系正确的是
a.
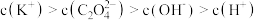
b.
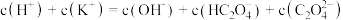
c.
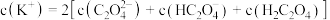
(2)
 中碳元素的化合价是+3 价,推测其有还原性。文献表明:相同条件下,
中碳元素的化合价是+3 价,推测其有还原性。文献表明:相同条件下, 的还原性强于 Fe2+。为验证此结论,小组同学完成了如下实验:向10 mL0.5 mol·L−1FeCl3溶液中缓慢加入0.5mol·L−1K2C2O4溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
的还原性强于 Fe2+。为验证此结论,小组同学完成了如下实验:向10 mL0.5 mol·L−1FeCl3溶液中缓慢加入0.5mol·L−1K2C2O4溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。资料:三水三草酸合铁酸钾[K3Fe(C2O4)3·3H2O]为翠绿色晶体,
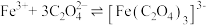 ,
,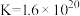 。
。取少量晶体洗净,配成溶液,滴加KSCN溶液,不变红,继续加入硫酸,溶液变红。用平衡移动原理解释溶液变红的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(一)一种工业制硝酸的方法经历下列几个步骤:
 △H1<0
△H1<0
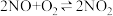 △H2<0
△H2<0
 △H3<0
△H3<0
已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有_______________ 目的;
(2)实验发现,单位时间内NH3的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因________________ 。

(3) 的反应历程如下:
的反应历程如下:
反应Ⅰ: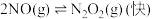 △H1<0
△H1<0

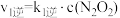
反应Ⅱ: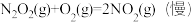 △H2<0
△H2<0
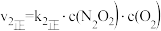
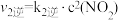
①一定条件下,反应 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=________________ 。(用含k1正、k1逆、k2正、k2逆的代数式表示);
②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数________________ k2逆增大的倍数(填“大于”“小于”或“等于”)。
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为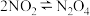 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
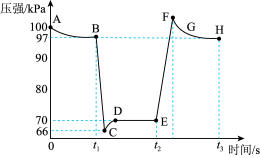
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是_______________ 。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=_______________ (不必化成小数);
(6)图像中C、E两点气体平均摩尔质量最大的点为_______________ (填代号)。
 △H1<0
△H1<0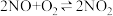 △H2<0
△H2<0 △H3<0
△H3<0已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
(2)实验发现,单位时间内NH3的氧化率[
 ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
(3)
 的反应历程如下:
的反应历程如下:反应Ⅰ:
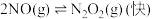 △H1<0
△H1<0 
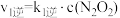
反应Ⅱ:
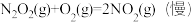 △H2<0
△H2<0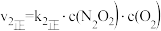
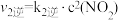
①一定条件下,反应
 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为
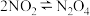 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=
(6)图像中C、E两点气体平均摩尔质量最大的点为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】CO2甲烷化反应为:CO2+4H2⇌CH4+2H2O,易发生副反应生成CO,CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+41kJ/mol。不同条件下,按照n(CO2):n(H2)=1:4投料同时发生CO2甲烷化反应和副反应,CO2的平衡转化率如图所示。
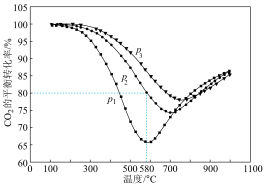
(1)CO2甲烷化反应的ΔH_______ 0(填“>”“<"或“=”)。
(2)压强p1、p2、p3由大到小的顺序是_______ 。压强为p2时,随着温度升高,CO2平衡转化率先减小后增大的原因是_______ 。
(3)580℃,压强为p2条件下,CH4的选择性为80%[CH4选择性=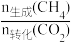 ×100%],则该温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=
×100%],则该温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=_______ 。

(1)CO2甲烷化反应的ΔH
(2)压强p1、p2、p3由大到小的顺序是
(3)580℃,压强为p2条件下,CH4的选择性为80%[CH4选择性=
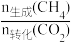 ×100%],则该温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=
×100%],则该温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】一氧化碳是一种重要的化工原料。
(1)高炉炼铁中发生的反应之一是:
FeO(s)+CO(g)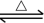 Fe(s)+CO2(g) △H=-1kJ/mol。
Fe(s)+CO2(g) △H=-1kJ/mol。
温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将______
(填“增大”、“减小”或“不变”)。
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应_______ .
A.向正反应向向进行 B.处于平衡状态 C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去。在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)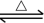 CO2(g)+H2(g) K=1.0
CO2(g)+H2(g) K=1.0
若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为_______ 。
(3)用CO和H2经如下两步反应制得甲酸甲醛:
CO+2H2→CH3OH
CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程)。_______
(1)高炉炼铁中发生的反应之一是:
FeO(s)+CO(g)
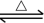 Fe(s)+CO2(g) △H=-1kJ/mol。
Fe(s)+CO2(g) △H=-1kJ/mol。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将
(填“增大”、“减小”或“不变”)。
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应
A.向正反应向向进行 B.处于平衡状态 C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去。在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)
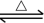 CO2(g)+H2(g) K=1.0
CO2(g)+H2(g) K=1.0若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为
(3)用CO和H2经如下两步反应制得甲酸甲醛:
CO+2H2→CH3OH
CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g) H2(g)+CO(g) ΔH=+131.3 kJ·mol-1。写出该反应的平衡常数表达式
H2(g)+CO(g) ΔH=+131.3 kJ·mol-1。写出该反应的平衡常数表达式_________________ 。
(2)已知在400℃时,N2(g)+3H2(g) 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。
①在400℃时,2NH3(g) N2(g)+3H2(g)的K'=
N2(g)+3H2(g)的K'=______ (填数值)。
②400℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应v正(N2)_____ v逆(N2)(填“>”、“<”“=”或“不能确定”)。
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡_____ 移动(填“向左”、“向右”或“不”);加入催化剂,反应的ΔH_______ (填“增大”、“减小”或“不改变”)。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g)
 H2(g)+CO(g) ΔH=+131.3 kJ·mol-1。写出该反应的平衡常数表达式
H2(g)+CO(g) ΔH=+131.3 kJ·mol-1。写出该反应的平衡常数表达式(2)已知在400℃时,N2(g)+3H2(g)
 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。①在400℃时,2NH3(g)
 N2(g)+3H2(g)的K'=
N2(g)+3H2(g)的K'=②400℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应v正(N2)
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】向2L密闭容器中通入amol 气体 A和bmol气体B,在一定条件下发生反应:2A(g) + 3B(g)  C(g) +6D(g) +Q,已知:反应2min 时,A的浓度减少了
C(g) +6D(g) +Q,已知:反应2min 时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol。回答下列问题:
mol。回答下列问题:
①反应2min内,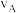 =
=___ ,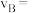
__________ 。
②反应平衡时,D为2a mol,则B的转化率为_________________ 。
③如果只升高反应温度,其他反应条件不变,平衡时D为 1.5a mol,则该反应的Q________ 0(填“>”、“<”或“=”)。
④如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较:
Ⅰ.反应速率__ (填“增大”、“减小”或“不变”),理由是_____ ;
Ⅱ.平衡时反应物的转化率__ (填“增大”、“减小”或“不变”),理由是___________________________________________________ 。
 C(g) +6D(g) +Q,已知:反应2min 时,A的浓度减少了
C(g) +6D(g) +Q,已知:反应2min 时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol。回答下列问题:
mol。回答下列问题:①反应2min内,
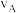 =
=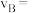
②反应平衡时,D为2a mol,则B的转化率为
③如果只升高反应温度,其他反应条件不变,平衡时D为 1.5a mol,则该反应的Q
④如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较:
Ⅰ.反应速率
Ⅱ.平衡时反应物的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某合成气的主要成分是一氧化碳和氢气,可用于合成甲醚等清洁燃料。由天然气获得该合成气过程中可能发生的反应有
①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
②CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。

反应进行的前5 min内,v(H2)=___________ ;10 min时,改变的外界条件可能是___________ 。
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象___________ 。

①CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1②CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1③CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。

反应进行的前5 min内,v(H2)=
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为___________ 热反应,且m+n___________ p(填“>”“=”“<”)。
(2)减压时,A的质量分数___________ 。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率___________ ,B的转化率___________ 。
(4)若升高温度,则平衡时B、C的浓度之比将___________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量___________ 。
(6)若B是有色物质,A、C均无色,维持容器内压强不变,充入氖气时,混合物颜色___________ (填“变深”“变浅”或“不变”)。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应的逆反应为
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若升高温度,则平衡时B、C的浓度之比将
(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若B是有色物质,A、C均无色,维持容器内压强不变,充入氖气时,混合物颜色
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)一定条件下1 L的密闭容器中,反应mA(g)+nB(g)  pC(g)+qD(g)达到平衡。若起始时A为1 mol,反应2min达到平衡,A剩余0.4 mol,则在0~2min内A的平均反应速率为
pC(g)+qD(g)达到平衡。若起始时A为1 mol,反应2min达到平衡,A剩余0.4 mol,则在0~2min内A的平均反应速率为______ mol/(L∙min)。
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,m+n______ p+q(选填“>”、“<”或“=”),v逆______ (选填“增大”、“减小”或“不变”)。
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是________ 。(选填编号,下同)
a.增大A的浓度 b. 缩小容器体积
c. 加入催化剂 d.升高温度
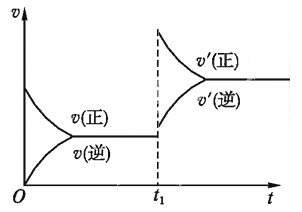
(4)若nV正(A)=mV逆(B),则该反应________ 。
a.向正反应方向进行 b. 向逆反应方向进行 c.处于平衡状态 d.无法判断
 pC(g)+qD(g)达到平衡。若起始时A为1 mol,反应2min达到平衡,A剩余0.4 mol,则在0~2min内A的平均反应速率为
pC(g)+qD(g)达到平衡。若起始时A为1 mol,反应2min达到平衡,A剩余0.4 mol,则在0~2min内A的平均反应速率为(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,m+n
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是
a.增大A的浓度 b. 缩小容器体积
c. 加入催化剂 d.升高温度

(4)若nV正(A)=mV逆(B),则该反应
a.向正反应方向进行 b. 向逆反应方向进行 c.处于平衡状态 d.无法判断
您最近一年使用:0次



