回答下列问题
(1)一定温度下,在0.5L密闭容器中充入 1molN2和 3molH2 发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0
2NH3(g) ΔH<0
①判断该反应的ΔS_____ 0 (填“>”、“<”或“=”);
②若容器容积恒定,达到平衡状态时,N2的物质的量为0.5mol,计算N2的转化率为__________ ,该反应的化学平衡常数K=________ 。
(2)对于反应 2NO(g)+O2(g) 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
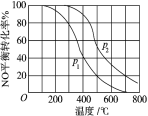
比较 P1、P2 的大小关系:P1________ P2(填“>”、“<”或“=”)。
②该反应的平衡常数 K 的表达式 为________ ,随温度升高,该反应平衡常数变化的趋势是________ 。(填“增大”、
“减小”或“不变”)。
③下列措施中能够同时满足增大反应速率和提高 NO 转化率的是________ 。(填写相应字母)
A.使用高效催化剂 B.保持容器体积不变加入惰性气体 C.保持容器体积不变加入 O2 D.降低温度 E.压缩容器体积
(3)已知同温同压下,下列反应的焓变和平衡常数分别表示为
式1:2SO2(g)+O2(g) 2SO3(g) ΔH1= - 197 kJ·mol-1 K1=a
2SO3(g) ΔH1= - 197 kJ·mol-1 K1=a
式2:2NO(g)+O2(g) 2NO2(g) ΔH2= -144 kJ·mol-1 K2=b
2NO2(g) ΔH2= -144 kJ·mol-1 K2=b
式3:NO2(g)+SO2(g) SO3(g)+NO(g) ΔH3=m kJ·mol-1 K3=c
SO3(g)+NO(g) ΔH3=m kJ·mol-1 K3=c
则m的数值为________ ,c与a、b之间的关系为__________ 。
(4)目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
在体积为2L的密闭容器中,充入1molCO2和3molH2,在相同温度、容积不变的条件下,能说明该反应已达平衡状态的是__________ (填序号)。
A.CO2、H2、CH3OH、H2O的浓度均不再变化 B.v生成(CH3OH)=v消耗(CO2)
C.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶1∶1∶1 D.容器中混合气体的密度保持不变
E.H2的消耗速率与CH3OH的消耗速率之比为3∶1
(1)一定温度下,在0.5L密闭容器中充入 1molN2和 3molH2 发生反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0
2NH3(g) ΔH<0 ①判断该反应的ΔS
②若容器容积恒定,达到平衡状态时,N2的物质的量为0.5mol,计算N2的转化率为
(2)对于反应 2NO(g)+O2(g)
 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
比较 P1、P2 的大小关系:P1
②该反应的平衡常数 K 的
“减小”或“不变”)。
③下列措施中能够同时满足增大反应速率和提高 NO 转化率的是
A.使用高效催化剂 B.保持容器体积不变加入惰性气体 C.保持容器体积不变加入 O2 D.降低温度 E.压缩容器体积
(3)已知同温同压下,下列反应的焓变和平衡常数分别表示为
式1:2SO2(g)+O2(g)
 2SO3(g) ΔH1= - 197 kJ·mol-1 K1=a
2SO3(g) ΔH1= - 197 kJ·mol-1 K1=a式2:2NO(g)+O2(g)
 2NO2(g) ΔH2= -144 kJ·mol-1 K2=b
2NO2(g) ΔH2= -144 kJ·mol-1 K2=b式3:NO2(g)+SO2(g)
 SO3(g)+NO(g) ΔH3=m kJ·mol-1 K3=c
SO3(g)+NO(g) ΔH3=m kJ·mol-1 K3=c则m的数值为
(4)目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。在体积为2L的密闭容器中,充入1molCO2和3molH2,在相同温度、容积不变的条件下,能说明该反应已达平衡状态的是
A.CO2、H2、CH3OH、H2O的浓度均不再变化 B.v生成(CH3OH)=v消耗(CO2)
C.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶1∶1∶1 D.容器中混合气体的密度保持不变
E.H2的消耗速率与CH3OH的消耗速率之比为3∶1
更新时间:2022-12-09 15:56:14
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】 资源化利用是实现
资源化利用是实现 减排的首要途径。已知
减排的首要途径。已知 加氢制甲醇反应体系中,主要反应有
加氢制甲醇反应体系中,主要反应有
Ⅰ.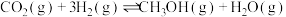


Ⅱ.


Ⅲ.


回答下列问题:
(1)
_______ 。
(2)在一定温度范围和压强范围内,只发生反应Ⅰ和Ⅱ,为了增大甲醇产率,理论上可采取的措施是_______ (写2点);
(3)已知反应Ⅰ和Ⅱ的 ,随温度的变化如图所示:
,随温度的变化如图所示:
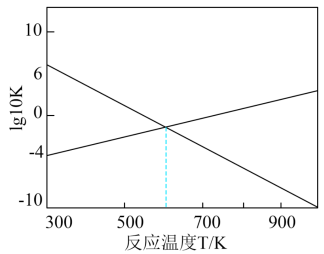
①300K时, 、
、 、
、 由大到小的顺序为
由大到小的顺序为_______ 。
②在600K、3MPa下,向密闭容器中充入2mol 和1mol
和1mol ,只发生反应Ⅰ和Ⅱ,开始时甲醇与CO的生成速率之比为6∶1,达到平衡时,生成速率之比为3∶1,甲醇的生成速率方程
,只发生反应Ⅰ和Ⅱ,开始时甲醇与CO的生成速率之比为6∶1,达到平衡时,生成速率之比为3∶1,甲醇的生成速率方程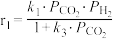 ,CO的生成速率方程
,CO的生成速率方程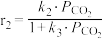 ,
, 、
、 为速率方程常数、
为速率方程常数、 为常数。体系达到平衡时,
为常数。体系达到平衡时,
_______ , 的平衡转化率为
的平衡转化率为_______ 。
(4) 电池的研究取得了新的进展,在TAPP-Mn(Ⅱ)作用下,其电池结构和正极反应历程如下:
电池的研究取得了新的进展,在TAPP-Mn(Ⅱ)作用下,其电池结构和正极反应历程如下:
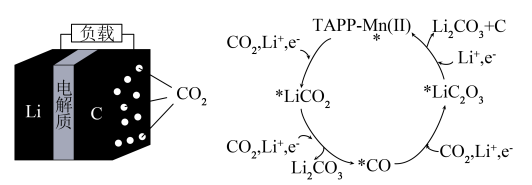
①该正极反应历程中有_______ 种中间产物;
②放电时,该电池的正极反应式为_______ 。
 资源化利用是实现
资源化利用是实现 减排的首要途径。已知
减排的首要途径。已知 加氢制甲醇反应体系中,主要反应有
加氢制甲醇反应体系中,主要反应有Ⅰ.
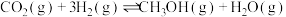


Ⅱ.



Ⅲ.



回答下列问题:
(1)

(2)在一定温度范围和压强范围内,只发生反应Ⅰ和Ⅱ,为了增大甲醇产率,理论上可采取的措施是
(3)已知反应Ⅰ和Ⅱ的
 ,随温度的变化如图所示:
,随温度的变化如图所示:
①300K时,
 、
、 、
、 由大到小的顺序为
由大到小的顺序为②在600K、3MPa下,向密闭容器中充入2mol
 和1mol
和1mol ,只发生反应Ⅰ和Ⅱ,开始时甲醇与CO的生成速率之比为6∶1,达到平衡时,生成速率之比为3∶1,甲醇的生成速率方程
,只发生反应Ⅰ和Ⅱ,开始时甲醇与CO的生成速率之比为6∶1,达到平衡时,生成速率之比为3∶1,甲醇的生成速率方程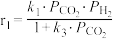 ,CO的生成速率方程
,CO的生成速率方程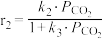 ,
, 、
、 为速率方程常数、
为速率方程常数、 为常数。体系达到平衡时,
为常数。体系达到平衡时,
 的平衡转化率为
的平衡转化率为(4)
 电池的研究取得了新的进展,在TAPP-Mn(Ⅱ)作用下,其电池结构和正极反应历程如下:
电池的研究取得了新的进展,在TAPP-Mn(Ⅱ)作用下,其电池结构和正极反应历程如下:
①该正极反应历程中有
②放电时,该电池的正极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca。
(1)Ca的原子结构示意图______________ 。
(2)配平用钙线氧脱鳞的化学方程式:
___ P +____ FeO +____ CaO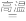
_____ Ca3(PO4)2+____ Fe。
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n。则金属M为_________ ,检测Mn+的方法是_____________________ (用离子方程式表达)。
(4)取1.6g钙线试样,与水充分反应,生成224mLH2(标准状况),再向溶液中通入适量的CO2,最多能得到CaCO3_________ g。
(5)处理炼钢厂含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知:CO(g) + O2(g) =CO2(g)
O2(g) =CO2(g) H=-283.0 kJ·mol-2
H=-283.0 kJ·mol-2
S(s) + O2(g) =SO2(g) H=-296.0 kJ·mol-1
H=-296.0 kJ·mol-1
此反应的热化学方程式是_________________________ 。
(1)Ca的原子结构示意图
(2)配平用钙线氧脱鳞的化学方程式:
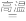
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n。则金属M为
(4)取1.6g钙线试样,与水充分反应,生成224mLH2(标准状况),再向溶液中通入适量的CO2,最多能得到CaCO3
(5)处理炼钢厂含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知:CO(g) +
 O2(g) =CO2(g)
O2(g) =CO2(g) H=-283.0 kJ·mol-2
H=-283.0 kJ·mol-2S(s) + O2(g) =SO2(g)
 H=-296.0 kJ·mol-1
H=-296.0 kJ·mol-1此反应的热化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】CO2和H2一定条件下可以合成甲醇,该过程存在副反应二
反应一:
反应二:
(1)已知25℃和101kPa下,H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0kJ·mol-1,
H2O(1)=H2O(g)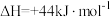 ,
,
则ΔH2=___________ kJ/mol。
(2)工业上可用CO2来制甲醇。
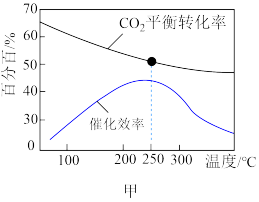
① 。根据图甲分析,实际工业生产中,反应温度选择250℃的理由是
。根据图甲分析,实际工业生产中,反应温度选择250℃的理由是___________ 。
②利用光电催化原理,由CO2和H2O制备CH3OH的装置如图乙。写出右侧的电极反应式:___________

(3)在恒容密闭容器内,充入1molCO2和3molH2,测得平衡时CO2转化率,CO和CH3OH选择性随温度变化如图所示【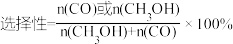 】。250℃下达平衡时,n(H2O)=
】。250℃下达平衡时,n(H2O)=___________ mol,其他条件不变,210℃比230℃平衡时生成的CH3OH___________ (填“多”或“少”)。

(4)在某密闭容器中充入n(CO2):n(H2)=5:17的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。
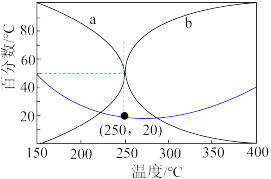
①表示平衡时CH3OH在含碳产物中物质的量百分数的曲线是___________ (填“a”或“b”)。
②CO2平衡转化率随温度的升高先减小后增大,增大的原因可能是___________ 。
反应一:

反应二:

(1)已知25℃和101kPa下,H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0kJ·mol-1,
H2O(1)=H2O(g)
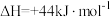 ,
,则ΔH2=
(2)工业上可用CO2来制甲醇。
①
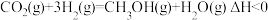 。根据图甲分析,实际工业生产中,反应温度选择250℃的理由是
。根据图甲分析,实际工业生产中,反应温度选择250℃的理由是
②利用光电催化原理,由CO2和H2O制备CH3OH的装置如图乙。写出右侧的电极反应式:

(3)在恒容密闭容器内,充入1molCO2和3molH2,测得平衡时CO2转化率,CO和CH3OH选择性随温度变化如图所示【
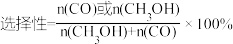 】。250℃下达平衡时,n(H2O)=
】。250℃下达平衡时,n(H2O)=
(4)在某密闭容器中充入n(CO2):n(H2)=5:17的混合气体,于5.0MPa和催化剂作用下发生反应,平衡时CO和CH3OH在含碳产物中物质的量百分数及CO2的转化率随温度的变化如图所示。

①表示平衡时CH3OH在含碳产物中物质的量百分数的曲线是
②CO2平衡转化率随温度的升高先减小后增大,增大的原因可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】甲醇被称为21世纪的新型燃料,研究和合成甲醇有着重要的意义。一种合成甲醇的方法为:CO(g)+2H2(g) CH3OH(g)△H1,在10 L恒容密闭容器中加入4 moLCO和8 mol H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g)△H1,在10 L恒容密闭容器中加入4 moLCO和8 mol H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如下表所示:
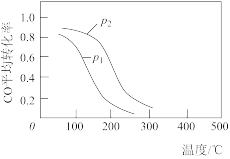
(1)△H1_______ (填“>”“<”或“=”)0。
(2)下列说法正确的是_____ (填标号)。
a温度越高,该反应的平衡常数越大
b若其它条件不变,反应改在绝热条件下进行,CO转化率比在恒温条件下转化率大
c容器内气体压强不再变化时,反应达到最大限度
d图中压强p1>p2
(3)0~3 min内用CH3OH表示的反应速率v(CH3OH)=______ (保留三位小数)。
(4)若达平衡状态时,再向容器中投入2 molCH3OH重新达平衡后甲醇的体积分数与原平衡时相比_______ (填变大、变小或不变)。
(5)200℃时,该反应的平衡常数K=______ 。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡_____ (填“正向”“逆向”或“不”)移动。
 CH3OH(g)△H1,在10 L恒容密闭容器中加入4 moLCO和8 mol H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g)△H1,在10 L恒容密闭容器中加入4 moLCO和8 mol H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如下表所示:| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |

(1)△H1
(2)下列说法正确的是
a温度越高,该反应的平衡常数越大
b若其它条件不变,反应改在绝热条件下进行,CO转化率比在恒温条件下转化率大
c容器内气体压强不再变化时,反应达到最大限度
d图中压强p1>p2
(3)0~3 min内用CH3OH表示的反应速率v(CH3OH)=
(4)若达平衡状态时,再向容器中投入2 molCH3OH重新达平衡后甲醇的体积分数与原平衡时相比
(5)200℃时,该反应的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g) CH3OH(g) ΔH2=-90.4kJ·mol-1
CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
回答下列问题:
(1)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的浓度为_____ mol·L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为_____ 。
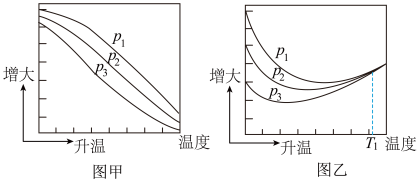
(2)不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。
已知:
CO2的平衡转化率=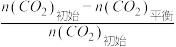 ×100%
×100%
CH3OH的平衡产率=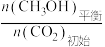 ×100%
×100%
其中纵坐标表示CO2平衡转化率的是图_____ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为_____ ;图乙中T1温度时,三条曲线几乎交于一点的原因是_____ 。
(3)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_____(填标号)。
Ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1Ⅱ.CO(g)+2H2(g)
 CH3OH(g) ΔH2=-90.4kJ·mol-1
CH3OH(g) ΔH2=-90.4kJ·mol-1Ⅲ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1回答下列问题:
(1)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的浓度为
(2)不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

已知:
CO2的平衡转化率=
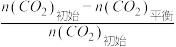 ×100%
×100%CH3OH的平衡产率=
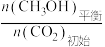 ×100%
×100%其中纵坐标表示CO2平衡转化率的是图
(3)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_____(填标号)。
| A.低温、高压 | B.高温、低压 |
| C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】环境问题,能源问题事关人类生存,社会可持续发展。回答下列问题:
(1)氮硫的氧化物的转化:
①已知:NO(g)+ O2(g)⇌NO2(g) ∆H=-56.5kJ•mol-1;
O2(g)⇌NO2(g) ∆H=-56.5kJ•mol-1;
2SO2(g)+O2(g)⇌2SO3(g) ∆H=-196.6kJ•mol-1;
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g) ∆H=___________ kJ•mol-1;
②一定条件下,将NO2与SO2以一定比例(不是等物质的量)置于恒温恒容的密闭容器中发生上述反应,下列能说明反应一定达到平衡状态的有___________ 。
a、混合气体的密度不变
b、反应速率v(NO2):v(SO2):v(SO3):v(NO)=1:1:1:1
c、NO2和SO2的浓度保持不变
d、混合气体颜色保持不变
(2)通常合成甲醇的主要反应为:CO(g)+2H2(g)⇌CH3OH(g) ∆H<0,起始时容器中只有1mol/LCO和2mol/LH2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。

①压强为p1温度为T1和T2时对应的平衡常数分别为K1、K2,则K1___________ K2(填“>”、“<”、“=”)请说明理由___________ 。
②若在温度为T1、压强为p1的条件下向密闭容器中加入等物质的量的CO、H2气体,则反应开始时v(CO)正___________ v(CO)逆。(填“>”、“<”、“=”、“无法确定”)
(3)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体CO2,其产物之一是NH4HCO3.常温下碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,NH3•H2O的电离常数Kb=1.8×10-5,则NH4HCO3溶液中c(NH )
)___________ c(HCO )。(填“>”、“<”“=”)
)。(填“>”、“<”“=”)
(1)氮硫的氧化物的转化:
①已知:NO(g)+
 O2(g)⇌NO2(g) ∆H=-56.5kJ•mol-1;
O2(g)⇌NO2(g) ∆H=-56.5kJ•mol-1;2SO2(g)+O2(g)⇌2SO3(g) ∆H=-196.6kJ•mol-1;
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g) ∆H=
②一定条件下,将NO2与SO2以一定比例(不是等物质的量)置于恒温恒容的密闭容器中发生上述反应,下列能说明反应一定达到平衡状态的有
a、混合气体的密度不变
b、反应速率v(NO2):v(SO2):v(SO3):v(NO)=1:1:1:1
c、NO2和SO2的浓度保持不变
d、混合气体颜色保持不变
(2)通常合成甲醇的主要反应为:CO(g)+2H2(g)⇌CH3OH(g) ∆H<0,起始时容器中只有1mol/LCO和2mol/LH2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。

①压强为p1温度为T1和T2时对应的平衡常数分别为K1、K2,则K1
②若在温度为T1、压强为p1的条件下向密闭容器中加入等物质的量的CO、H2气体,则反应开始时v(CO)正
(3)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体CO2,其产物之一是NH4HCO3.常温下碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,NH3•H2O的电离常数Kb=1.8×10-5,则NH4HCO3溶液中c(NH
 )
) )。(填“>”、“<”“=”)
)。(填“>”、“<”“=”)
您最近一年使用:0次
【推荐1】合成氨的反应对人类解决粮食问题贡献巨大,德国化学家F.Haber因合成氨而获得诺贝尔奖。合成氨反应热化学方程式如下:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
(1)已知N2(g)+3H2(g) 2NH3(g)不加入催化剂时正反应的活化能为326kJ/mol,则该反应逆反应的活化能为
2NH3(g)不加入催化剂时正反应的活化能为326kJ/mol,则该反应逆反应的活化能为_______ kJ/mol。
(2)已知N2(g)+O2(g)=2NO(g) △H=+180kJ/mol
H2的燃烧热△H=-285.8kJ/mol
则NH3(g)+ O2(g)=NO(g)+
O2(g)=NO(g)+ H2O(l) △H=
H2O(l) △H=_______ kJ/mol。
(3)一定温度下,向恒容的密闭容器中充入一定量的N2和H2发生反应,测得各组分浓度随时间变化如图所示。
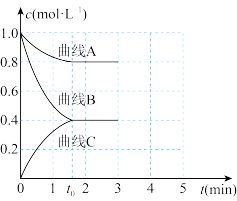
①表示c(H2)变化的曲线是_______ (填“曲线A”“曲线B”或“曲线C”)。
②0~t0时用NH3表示的化学反应速率为v(NH3)=_______ mol·L-1·min-1。
③下列能说明该反应达到平衡状态的是_______ (填标号)。
A.容器中混合气体的密度不随时间变化
B.容器中的n(N2)与n(H2)的比值不随时间变化
C.断裂3molH-H的同时断裂6molN-H键
D.3v正(H2)=2v逆(NH3)
(4)合成氨反应在某催化剂条件下的相对能量-反应历程如图所示(ad为吸附态):
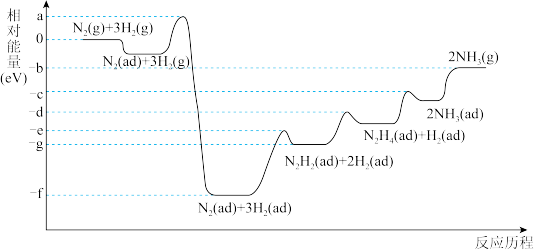
①该过程中含氮的中间产物有_______ 种(填数字)。
②活化能最大的那一步基元反应方程式为_______ 。
③下列说法正确的是_______ (填标号)。
A.最后一步NH3(ad)变为NH3(g)为吸热过程。
B.催化剂参与反应,但不改变合成氨反应的△H
C.催化剂和升温都能降低反应的活化能,加快合成氨的反应速率
D.使用催化剂和压缩容器体积加压都能增大活化分子百分数,加快合成氨反应速率
 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol(1)已知N2(g)+3H2(g)
 2NH3(g)不加入催化剂时正反应的活化能为326kJ/mol,则该反应逆反应的活化能为
2NH3(g)不加入催化剂时正反应的活化能为326kJ/mol,则该反应逆反应的活化能为(2)已知N2(g)+O2(g)=2NO(g) △H=+180kJ/mol
H2的燃烧热△H=-285.8kJ/mol
则NH3(g)+
 O2(g)=NO(g)+
O2(g)=NO(g)+ H2O(l) △H=
H2O(l) △H=(3)一定温度下,向恒容的密闭容器中充入一定量的N2和H2发生反应,测得各组分浓度随时间变化如图所示。

①表示c(H2)变化的曲线是
②0~t0时用NH3表示的化学反应速率为v(NH3)=
③下列能说明该反应达到平衡状态的是
A.容器中混合气体的密度不随时间变化
B.容器中的n(N2)与n(H2)的比值不随时间变化
C.断裂3molH-H的同时断裂6molN-H键
D.3v正(H2)=2v逆(NH3)
(4)合成氨反应在某催化剂条件下的相对能量-反应历程如图所示(ad为吸附态):

①该过程中含氮的中间产物有
②活化能最大的那一步基元反应方程式为
③下列说法正确的是
A.最后一步NH3(ad)变为NH3(g)为吸热过程。
B.催化剂参与反应,但不改变合成氨反应的△H
C.催化剂和升温都能降低反应的活化能,加快合成氨的反应速率
D.使用催化剂和压缩容器体积加压都能增大活化分子百分数,加快合成氨反应速率
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】Ⅰ.为了实现“碳达峰和碳中和”目标,科学家利用C3N4/Cu催化剂(CuNPs)加氢还原CO2制备烃类和烃类含氧衍生物,实现太阳能综合利用。如图所示:
(1)上述装置中能量转化形式主要是________
太阳能→___________能→___________能。
(2)图中采用___________ (填“质子”或“阴离子”)交换膜。
(3)下列措施不利于绿色低碳发展的是___________。
Ⅱ.CO2催化加氢制甲醇(CH3OH)是实现碳达峰、碳中和的途径之一,其反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
(4)写出该反应的平衡常数表达式K=___________ 。
(5)该反应分两步进行,反应过程能量变化如图所示,所有物质均为气态。 =
=___________ kJ/mol。第①步反应的热化学方程式为___________ 。
(6)一定温度下,在一体积固定的密闭容器中投入一定量的CO2和H2进行上述总反应,达到平衡后,改变下列1个条件,反应速率和CO2平衡转化率都增大的是___________。
(7)下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO2,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
Ⅲ.该反应的产物甲醇燃烧电池具有很多优点。
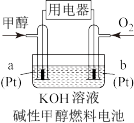
(8)在碱性甲醇燃料电池中,Pt(a)发生___________ (填“氧化”或“还原”)反应:在酸性甲醇燃料电池中,电极b上发生的电极反应式为___________ 。

(1)上述装置中能量转化形式主要是
太阳能→___________能→___________能。
(2)图中采用
(3)下列措施不利于绿色低碳发展的是___________。
| A.使用氢能源车 | B.杭州西站光伏发电 |
| C.使用脱硫煤发电 | D.使用可循环快递箱 |
Ⅱ.CO2催化加氢制甲醇(CH3OH)是实现碳达峰、碳中和的途径之一,其反应可表示为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
(4)写出该反应的平衡常数表达式K=
(5)该反应分两步进行,反应过程能量变化如图所示,所有物质均为气态。
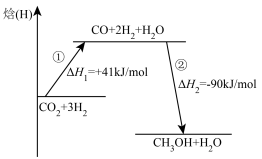
 =
=(6)一定温度下,在一体积固定的密闭容器中投入一定量的CO2和H2进行上述总反应,达到平衡后,改变下列1个条件,反应速率和CO2平衡转化率都增大的是___________。
| A.加入高效催化剂 | B.增大CO2浓度 | C.缩小容器容积 | D.升高温度 |
(7)下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO2,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
Ⅲ.该反应的产物甲醇燃烧电池具有很多优点。
(8)在碱性甲醇燃料电池中,Pt(a)发生

您最近一年使用:0次
【推荐3】甲烷水汽重整反应是我国主要的制氢技术,有关反应如下:
反应i:CH4(g)+H2O(g) CO(g)+3H2(g) △H1=akJ·mol-1;
CO(g)+3H2(g) △H1=akJ·mol-1;
反应ii:CO(g)+H2O(g) CO2(g)+H2(g) △H2=bkJ·mol-1。
CO2(g)+H2(g) △H2=bkJ·mol-1。
回答下列问题:
(1)反应i、反应ii的平衡常数分别为K1=1.198×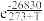 、K2=1.767×
、K2=1.767× ,反应温度为T℃。
,反应温度为T℃。
①随着温度的升高,K1____ (填“增大”“减小”或“不变”),△H2____ (填“<”或“>”)0。
②对于反应i,v正=k正c(CH4)•c(H2O),v逆=k逆c(CO)•c3(H2)(k正、k逆为速率常数,仅与温度有关)。向等压密闭容器中充入2molCH4、2molH2O仅发生反应i,达到平衡后生成1molCO和3molH2。下列说法正确的是____ (填字母)。
A.CO的体积分数保持不变能判断反应处于平衡状态
B.及时分离出CO,有利于提高甲烷的转化率和正反应速率
C.温度升高,k正和k逆均增大,且k正增大的倍数大于k逆增大的倍数
D.其他条件不变,达平衡后再向容器中充入1molCH4、1molH2O、1molCO、3molH2,则v正>v逆
(2)一定温度下,向恒容密闭反应器中通入CH4和H2O(g),起始时CH4和H2O(g)的分压分别为1MPa、3MPa,发生反应i和反应ii。反应进行t1min时达到平衡状态,此时CO、CO2的分压分别为mMPa、nMPa。
①H2(g)的平衡分压为_____ MPa(用含m、n的代数式表示,下同)。
②反应i前tmin的平均速率v(CH4)=_____ MPa·min-1。
③反应ii的Kp=____ (用平衡时各物质的分压代替物质的量浓度)。
(3)载氧体Fe2O3、载氧体CeO2和复合载氧体均可以氧化甲烷制取合成气(CO、H2),载氧体的质量与时间的关系如图所示(一定条件下有积碳反应发生:CH4=C+2H2)。
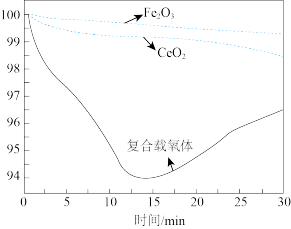
①由图可知反应性能最好的是_____ (填“Fe2O3”“CeO2”或“复合载氧体”)。
②从开始到13min的时候,曲线呈下降趋势的原因主要是甲烷还原载氧体,载氧体失去氧而出现失重的情况;反应在13~15min时,出现了一个短暂的小平台,其主要的原因是____ 。
反应i:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=akJ·mol-1;
CO(g)+3H2(g) △H1=akJ·mol-1;反应ii:CO(g)+H2O(g)
 CO2(g)+H2(g) △H2=bkJ·mol-1。
CO2(g)+H2(g) △H2=bkJ·mol-1。回答下列问题:
(1)反应i、反应ii的平衡常数分别为K1=1.198×
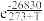 、K2=1.767×
、K2=1.767× ,反应温度为T℃。
,反应温度为T℃。①随着温度的升高,K1
②对于反应i,v正=k正c(CH4)•c(H2O),v逆=k逆c(CO)•c3(H2)(k正、k逆为速率常数,仅与温度有关)。向等压密闭容器中充入2molCH4、2molH2O仅发生反应i,达到平衡后生成1molCO和3molH2。下列说法正确的是
A.CO的体积分数保持不变能判断反应处于平衡状态
B.及时分离出CO,有利于提高甲烷的转化率和正反应速率
C.温度升高,k正和k逆均增大,且k正增大的倍数大于k逆增大的倍数
D.其他条件不变,达平衡后再向容器中充入1molCH4、1molH2O、1molCO、3molH2,则v正>v逆
(2)一定温度下,向恒容密闭反应器中通入CH4和H2O(g),起始时CH4和H2O(g)的分压分别为1MPa、3MPa,发生反应i和反应ii。反应进行t1min时达到平衡状态,此时CO、CO2的分压分别为mMPa、nMPa。
①H2(g)的平衡分压为
②反应i前tmin的平均速率v(CH4)=
③反应ii的Kp=
(3)载氧体Fe2O3、载氧体CeO2和复合载氧体均可以氧化甲烷制取合成气(CO、H2),载氧体的质量与时间的关系如图所示(一定条件下有积碳反应发生:CH4=C+2H2)。

①由图可知反应性能最好的是
②从开始到13min的时候,曲线呈下降趋势的原因主要是甲烷还原载氧体,载氧体失去氧而出现失重的情况;反应在13~15min时,出现了一个短暂的小平台,其主要的原因是
您最近一年使用:0次
【推荐1】乙烯被广泛用于合成聚乙烯等聚合产品。工业生产的乙烯中含有的少量乙炔会导致聚合催化剂中毒失活,含有的乙烷会使聚合过程终止。因此乙炔的选择加氢制乙烯在生产中有重大经济意义。反应原理如下:
反应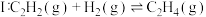 (主反应)
(主反应)
反应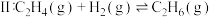 (副反应)
(副反应)
回答下列问题:
(1)分别以 乙炔和
乙炔和  氢气或
氢气或  乙烯为初始原料,在
乙烯为初始原料,在 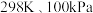 下,使用对反应
下,使用对反应  选择性好的催化剂,分别在恒压容器中反应,达平衡时,以乙炔和氢气为原料,体系向环境放热
选择性好的催化剂,分别在恒压容器中反应,达平衡时,以乙炔和氢气为原料,体系向环境放热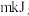 以乙烯为原料,体系从环境吸热
以乙烯为原料,体系从环境吸热 ,忽略副反应热效应,反应焓变
,忽略副反应热效应,反应焓变
___________  。
。
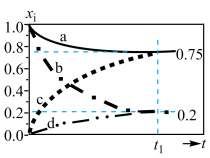
(2)初始条件同上,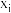 表示某物种
表示某物种  的物质的量与除
的物质的量与除  外其它各物种总物质的量之比,
外其它各物种总物质的量之比,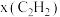 和
和  随时间
随时间 变化关系如图所示,实验测得
变化关系如图所示,实验测得 ,则图中表示
,则图中表示 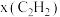 变化的曲线是
变化的曲线是___________ ;反应I平衡常数Kp=___________  ;以乙炔和氢气为原料时,
;以乙炔和氢气为原料时, 时刻
时刻 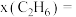
___________ 。
(3) 在催化剂表面逐步加氢,当变成
在催化剂表面逐步加氢,当变成  时,
时, 可从催化剂表面脱附生成
可从催化剂表面脱附生成 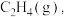 也可以继续加氢。清华大学李亚林团队找到一种催化剂,可使
也可以继续加氢。清华大学李亚林团队找到一种催化剂,可使  脱附生成
脱附生成  而不继续加氢,使催化产物停留在乙烯而不继续加氢生成乙烷。下面是两种催化剂(①
而不继续加氢,使催化产物停留在乙烯而不继续加氢生成乙烷。下面是两种催化剂(① 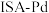 和②
和②  )分别催化乙炔加氢的反应机理:
)分别催化乙炔加氢的反应机理:
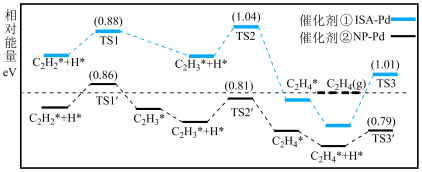
在催化剂② 作用下,
作用下, 倾向于
倾向于___________ (填“脱附”或“加氢”),结合图中数据,推测清华大学团队找到的理想催化剂是___________ (填“①”或“②”),原因是在该催化剂上 的脱附能
的脱附能___________ (填“高于”或“低于”)  进一步加氢需要突破的能垒,该催化剂具有好的选择性。
进一步加氢需要突破的能垒,该催化剂具有好的选择性。
反应
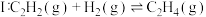 (主反应)
(主反应)反应
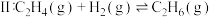 (副反应)
(副反应)回答下列问题:
(1)分别以
 乙炔和
乙炔和  氢气或
氢气或  乙烯为初始原料,在
乙烯为初始原料,在 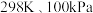 下,使用对反应
下,使用对反应  选择性好的催化剂,分别在恒压容器中反应,达平衡时,以乙炔和氢气为原料,体系向环境放热
选择性好的催化剂,分别在恒压容器中反应,达平衡时,以乙炔和氢气为原料,体系向环境放热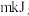 以乙烯为原料,体系从环境吸热
以乙烯为原料,体系从环境吸热 ,忽略副反应热效应,反应焓变
,忽略副反应热效应,反应焓变
 。
。(2)初始条件同上,
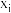 表示某物种
表示某物种  的物质的量与除
的物质的量与除  外其它各物种总物质的量之比,
外其它各物种总物质的量之比,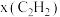 和
和  随时间
随时间 变化关系如图所示,实验测得
变化关系如图所示,实验测得 ,则图中表示
,则图中表示 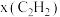 变化的曲线是
变化的曲线是 ;以乙炔和氢气为原料时,
;以乙炔和氢气为原料时, 时刻
时刻 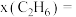

(3)
 在催化剂表面逐步加氢,当变成
在催化剂表面逐步加氢,当变成  时,
时, 可从催化剂表面脱附生成
可从催化剂表面脱附生成 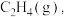 也可以继续加氢。清华大学李亚林团队找到一种催化剂,可使
也可以继续加氢。清华大学李亚林团队找到一种催化剂,可使  脱附生成
脱附生成  而不继续加氢,使催化产物停留在乙烯而不继续加氢生成乙烷。下面是两种催化剂(①
而不继续加氢,使催化产物停留在乙烯而不继续加氢生成乙烷。下面是两种催化剂(① 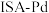 和②
和②  )分别催化乙炔加氢的反应机理:
)分别催化乙炔加氢的反应机理:
在催化剂②
 作用下,
作用下, 倾向于
倾向于 的脱附能
的脱附能 进一步加氢需要突破的能垒,该催化剂具有好的选择性。
进一步加氢需要突破的能垒,该催化剂具有好的选择性。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】乙醇是一种重要的工业原料,被广泛应用于能源、化工、食品等领域,以下两种方法可实现乙醇的制备。
I.采用催化乙烯水合制乙醇,该反应过程中能量变化如下图所示:
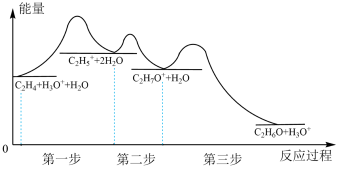
(1)反应物分子有效碰撞几率最大的步骤对应的基元反应为_______ 。
(2)制备的无水乙醇在25℃,101kPa下,完全燃烧时放出热量QkJ,其燃烧生成的 用过量饱和石灰水吸收可得100g
用过量饱和石灰水吸收可得100g 沉淀,则乙醇燃烧热的热化学方程式为
沉淀,则乙醇燃烧热的热化学方程式为_______ 。
Ⅱ.以合成气催化合成乙醇是近年来研究的热点,其中乙酸甲酯 催化加氢是制取乙醇的关键步骤之一,包括以下主要反应:
催化加氢是制取乙醇的关键步骤之一,包括以下主要反应:
①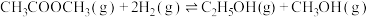
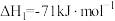
②
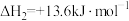
(3)反应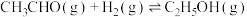 的ΔH=
的ΔH= _______  。
。
(4)若在体积为2L的密闭容器中,控制 流速为
流速为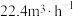 (已换算为标准状况),
(已换算为标准状况), 的转化率为80.0%,则
的转化率为80.0%,则 的反应速率为
的反应速率为_______ mol∙L-1∙min-1(保留三位有效数字), 流速过大时乙酸甲酯的转化率下降,原因是
流速过大时乙酸甲酯的转化率下降,原因是_______ 。
(5)向恒温恒压的两个密闭容器甲(25℃、 )、乙(25℃、
)、乙(25℃、 )放入物质的量均为amol的
)放入物质的量均为amol的 和
和 ,若只发生反应②,其正反应速率
,若只发生反应②,其正反应速率 ,p为物质分压,若容器甲与乙中平衡时正反应速率之比
,p为物质分压,若容器甲与乙中平衡时正反应速率之比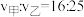 ,则甲、乙容器的体积之比为
,则甲、乙容器的体积之比为_______ 。
(6)一定条件下在1L密闭容器内通入2.00mol 和3.96mol
和3.96mol 发生反应①和②,测得不同温度下达平衡时
发生反应①和②,测得不同温度下达平衡时 转化率和乙醇的选择性如下图所示,260℃时反应①的平衡常数
转化率和乙醇的选择性如下图所示,260℃时反应①的平衡常数
_______ ;温度高于240℃时,随温度升高乙醇的选择性降低的原因可能是_______ 。
[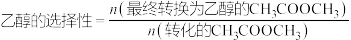 ]
]

I.采用催化乙烯水合制乙醇,该反应过程中能量变化如下图所示:

(1)反应物分子有效碰撞几率最大的步骤对应的基元反应为
(2)制备的无水乙醇在25℃,101kPa下,完全燃烧时放出热量QkJ,其燃烧生成的
 用过量饱和石灰水吸收可得100g
用过量饱和石灰水吸收可得100g 沉淀,则乙醇燃烧热的热化学方程式为
沉淀,则乙醇燃烧热的热化学方程式为Ⅱ.以合成气催化合成乙醇是近年来研究的热点,其中乙酸甲酯
 催化加氢是制取乙醇的关键步骤之一,包括以下主要反应:
催化加氢是制取乙醇的关键步骤之一,包括以下主要反应:①
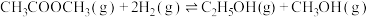
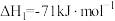
②

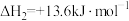
(3)反应
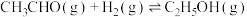 的ΔH=
的ΔH=  。
。(4)若在体积为2L的密闭容器中,控制
 流速为
流速为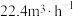 (已换算为标准状况),
(已换算为标准状况), 的转化率为80.0%,则
的转化率为80.0%,则 的反应速率为
的反应速率为 流速过大时乙酸甲酯的转化率下降,原因是
流速过大时乙酸甲酯的转化率下降,原因是(5)向恒温恒压的两个密闭容器甲(25℃、
 )、乙(25℃、
)、乙(25℃、 )放入物质的量均为amol的
)放入物质的量均为amol的 和
和 ,若只发生反应②,其正反应速率
,若只发生反应②,其正反应速率 ,p为物质分压,若容器甲与乙中平衡时正反应速率之比
,p为物质分压,若容器甲与乙中平衡时正反应速率之比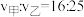 ,则甲、乙容器的体积之比为
,则甲、乙容器的体积之比为(6)一定条件下在1L密闭容器内通入2.00mol
 和3.96mol
和3.96mol 发生反应①和②,测得不同温度下达平衡时
发生反应①和②,测得不同温度下达平衡时 转化率和乙醇的选择性如下图所示,260℃时反应①的平衡常数
转化率和乙醇的选择性如下图所示,260℃时反应①的平衡常数
[
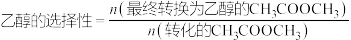 ]
]
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
反应I:4NH3(g) +5O2(g) 4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g) 2N2(g) +6H2O(g) △H
2N2(g) +6H2O(g) △H
(1)
△H=_______________ 。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是______________ 。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内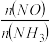 =1时,说明反应已达平衡
=1时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如下图:
①该催化剂在高温时选择反应_____________ (填“ I ”或“ II”)。
②520℃时,4NH3(g)+5O2 4NO(g) +6H2O(g)的平衡常数K=
4NO(g) +6H2O(g)的平衡常数K=________ (不要求得出计算结果,只需列出数字计算式)。
③有利于提高NH3转化为N2平衡转化率的措施有_______________
A.使用催化剂Pt/Ru
B.使用催化剂Cu/TiO2
C.增大NH3和O2的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)采用氨水吸收烟气中的SO2,
①若氨水与SO2恰好完全反应生成正盐,则此时溶液呈_____ 性(填“酸”或“碱”)常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10ˉ5mol·Lˉ1;H2SO3 :Ka1=1.3×10ˉ2mol·Lˉ1,Ka2=6.3×10ˉ8mol·Lˉ1
②上述溶液中通入______ 气体可使溶液呈中性(填“SO2”或NH3”),此时溶液c(NH4+)_______ c(SO32-)(填“>”“<”或“=”)
反应I:4NH3(g) +5O2(g)
 4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1反应 II:4NH3(g)+3O2(g)
 2N2(g) +6H2O(g) △H
2N2(g) +6H2O(g) △H(1)
化学键 | H—O | O===O | N≡N | N—H |
键能kJ·molˉ1 | 463 | 496 | 942 | 391 |
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内
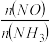 =1时,说明反应已达平衡
=1时,说明反应已达平衡(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如下图:
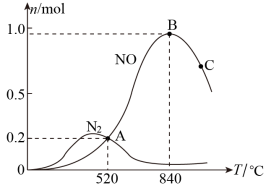
①该催化剂在高温时选择反应
②520℃时,4NH3(g)+5O2
 4NO(g) +6H2O(g)的平衡常数K=
4NO(g) +6H2O(g)的平衡常数K=③有利于提高NH3转化为N2平衡转化率的措施有
A.使用催化剂Pt/Ru
B.使用催化剂Cu/TiO2
C.增大NH3和O2的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)采用氨水吸收烟气中的SO2,
①若氨水与SO2恰好完全反应生成正盐,则此时溶液呈
②上述溶液中通入
您最近一年使用:0次



