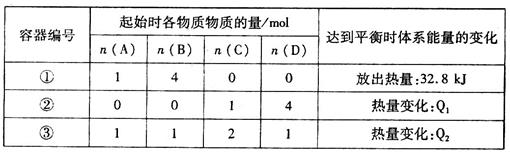
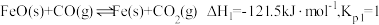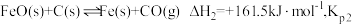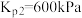已知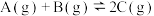
 ,反应平衡常数K与温度的关系如表所示,已知900℃时,向2L的密闭容器中充入0.40molA和0.40molB,经10s反应达到平衡状态。以下说法
,反应平衡常数K与温度的关系如表所示,已知900℃时,向2L的密闭容器中充入0.40molA和0.40molB,经10s反应达到平衡状态。以下说法不正确 的是
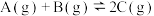
 ,反应平衡常数K与温度的关系如表所示,已知900℃时,向2L的密闭容器中充入0.40molA和0.40molB,经10s反应达到平衡状态。以下说法
,反应平衡常数K与温度的关系如表所示,已知900℃时,向2L的密闭容器中充入0.40molA和0.40molB,经10s反应达到平衡状态。以下说法| 温度/℃ | 750 | 900 | 1100 |
| K | 5.6 | 4 | 2.8 |
A. |
B.平衡时,C的物质的量浓度为 |
C.0~10s内,A的反应速率是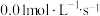 |
| D.平衡后若将容器容积缩小为原来的一半,则B的转化率为50% |
更新时间:2023-01-14 13:57:50
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】对于化学反应3W(g)+2X(g) 4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
 4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
4Y(g)+3Z(g),下列反应速率关系中,正确的是( )| A.v(X)=v(Y) | B.3v(W)=2v(X) | C.2v(X)=v(Y) | D.2v(X)=3v(Z) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】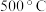 ,将
,将 和
和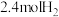 充入体积为
充入体积为 的已装有催化剂的恒容密闭容器中发生合成氨反应
的已装有催化剂的恒容密闭容器中发生合成氨反应 ,“此反应放热,下列说法正确的是
,“此反应放热,下列说法正确的是
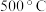 ,将
,将 和
和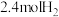 充入体积为
充入体积为 的已装有催化剂的恒容密闭容器中发生合成氨反应
的已装有催化剂的恒容密闭容器中发生合成氨反应 ,“此反应放热,下列说法正确的是
,“此反应放热,下列说法正确的是A.平衡时, 的浓度可能为 的浓度可能为 |
| B.容器内气体的密度不再随时间改变说明该反应已达到平衡状态 |
C.若已知生成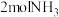 放出 放出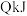 的热量,则该反应达平衡时放出的热量小于 的热量,则该反应达平衡时放出的热量小于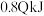 |
D.反应平衡后,向容器中充入一定体积的氨气,使容器中气体总压强增大,则 、 、 均增大 均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】X(g)+3Y(s) 2Z(g) ΔH=-a kJ·molˉ1,一定条件下,1 mol X和3 mol Y通入2 L的恒容密闭容器中,反应10 min,测得Y物质的量为2.4 mol。下列说法正确的是
2Z(g) ΔH=-a kJ·molˉ1,一定条件下,1 mol X和3 mol Y通入2 L的恒容密闭容器中,反应10 min,测得Y物质的量为2.4 mol。下列说法正确的是
 2Z(g) ΔH=-a kJ·molˉ1,一定条件下,1 mol X和3 mol Y通入2 L的恒容密闭容器中,反应10 min,测得Y物质的量为2.4 mol。下列说法正确的是
2Z(g) ΔH=-a kJ·molˉ1,一定条件下,1 mol X和3 mol Y通入2 L的恒容密闭容器中,反应10 min,测得Y物质的量为2.4 mol。下列说法正确的是| A.10 min内,Y的平均反应速率为0.03 mol·Lˉ1·minˉ1 |
| B.第10 min时,X的反应速率为0.01 mol·Lˉ1·minˉ1 |
| C.10 min内,消耗0.2 mol X,生成0.4 mol Z |
| D.10 min内,X和Y反应放出的热量为a kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知化合物A与H2O在一定条件下反应生成化合物B与 ,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法错误的是
,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法错误的是

 ,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法错误的是
,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法错误的是
| A.中间体I1比中间体I2更稳定 |
| B.该历程中的反应③为该反应的决速步 |
| C.平衡状态时,升温使反应逆向移动 |
| D.使用更高效的催化剂可降低反应所需的活化能和反应热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】甲硫醇是一种重要的原料和化工试剂,硫化氢与甲醇合成甲硫醇的催化过程如下。下列说法中不正确 的是
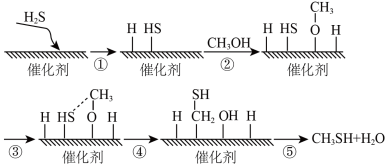

| A.过程①吸收能量 |
| B.过程④中,形成了O—H键和C—S键 |
| C.该催化剂可降低反应活化能从而有效提高反应物的平衡转化率 |
| D.硫化氢与甲醇合成甲硫醇的反应类型为取代反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组在学习完温度对盐类水解的影响后,测定了0.1mol·L-1Na2CO3溶液的pH随温度的变化,结果如下图所示。下列分析正确的是

A.升温前溶液呈碱性的原因是:CO +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
B.常温下,0.1 mol·L-1Na2CO3溶液中:c(Na+)>2c(CO )+c(HCO )+c(HCO ) ) |
| C.温度升高,Na2CO3水解程度增大,溶液pH增大,故图1实验数据一定错误 |
| D.降低温度,Na2CO3水解平衡移动和水的电离平衡移动对溶液pH的影响一致 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:3A(g)+B(g) 2C(g)+xD(g),达到平衡时,生成了2 mol C,经测定,D的浓度为0.5 mol·L-1,下列判断正确的是。
2C(g)+xD(g),达到平衡时,生成了2 mol C,经测定,D的浓度为0.5 mol·L-1,下列判断正确的是。
 2C(g)+xD(g),达到平衡时,生成了2 mol C,经测定,D的浓度为0.5 mol·L-1,下列判断正确的是。
2C(g)+xD(g),达到平衡时,生成了2 mol C,经测定,D的浓度为0.5 mol·L-1,下列判断正确的是。| A.x=1 |
| B.达到平衡时,在相同温度下容器内混合气体的压强是反应前的85% |
| C.平衡时A的浓度为1.50 mol·L-1 |
| D.B的转化率为20% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在一密闭容器中进行反应: 。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4
。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4 、0.2
、0.2 、0.4
、0.4 ,当反应达到平衡时,可能存在的数据是( )
,当反应达到平衡时,可能存在的数据是( )
 。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4
。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4 、0.2
、0.2 、0.4
、0.4 ,当反应达到平衡时,可能存在的数据是( )
,当反应达到平衡时,可能存在的数据是( )A. SO2的浓度为0.8 ,O2为0.4 ,O2为0.4 | B. SO2的浓度为0.5 |
C. SO3的浓度为0.8 | D. SO2、SO3的浓度一定均为0.3 |
您最近一年使用:0次
【推荐1】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
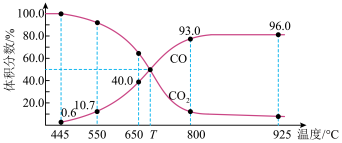
已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是
 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是
| A.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0P总 |
| B.550℃时,若充入惰性气体,v正,v逆均减小,平衡不移动 |
| C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 |
| D.650℃时,反应达平衡后CO2的转化率为25.0% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】将2molX和0.8molY置于体积为2L的恒容密闭容器中,发生反应:2X(g)+Y(s) M(g)+N(g) △H。反应过程中测得N的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
M(g)+N(g) △H。反应过程中测得N的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
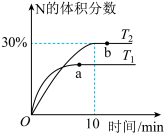
 M(g)+N(g) △H。反应过程中测得N的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
M(g)+N(g) △H。反应过程中测得N的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
| A.无论温度为T1还是T2,当容器中气体密度不变或压强不变时,反应达平衡状态 |
| B.温度为T2时,X的平衡转化率为60%,平衡常数K=5.625 |
| C.T1、T2的平衡常数分别为K1、K2,则K1<K2 |
| D.降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率 |
您最近一年使用:0次

 C(g)+D(g)
C(g)+D(g)  kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下: