为了研究 溶于铵盐溶液的原因,进行如下实验:
溶于铵盐溶液的原因,进行如下实验:
①向2 mL 0.2
 溶液中滴加1
溶液中滴加1  NaOH溶液至不再产生沉淀,将浊液分为2等份。
NaOH溶液至不再产生沉淀,将浊液分为2等份。
②向一份中逐滴加入4
 溶液,另一份中逐滴加入4
溶液,另一份中逐滴加入4 
 溶液
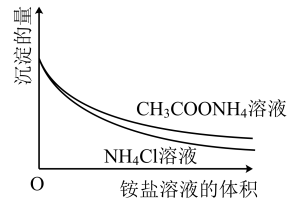
溶液 ,边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。
,边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。
③将①中的NaOH溶液用氨水替换,重复上述实验。
下列说法不正确 的是
 溶于铵盐溶液的原因,进行如下实验:
溶于铵盐溶液的原因,进行如下实验:①向2 mL 0.2

 溶液中滴加1
溶液中滴加1  NaOH溶液至不再产生沉淀,将浊液分为2等份。
NaOH溶液至不再产生沉淀,将浊液分为2等份。②向一份中逐滴加入4

 溶液,另一份中逐滴加入4
溶液,另一份中逐滴加入4 
 溶液
溶液 ,边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。
,边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。③将①中的NaOH溶液用氨水替换,重复上述实验。
下列说法

A. 浊液中存在: 浊液中存在: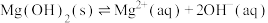 |
B.②中两组实验中均存在反应: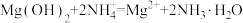 |
C.溶解 的过程中, 的过程中, 比 比 贡献更大 贡献更大 |
| D.实验③中获得的图像与②不同 |
更新时间:2023-01-14 09:57:44
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】Ga与Al同为第ⅢA族元素,溶液中Ga3+及其与OH-形成的微粒的浓度分数a随溶液pH变化的关系如下图所示。已知CH3COOH的电离平衡常数Ka=1.8×10-5,向NaGa(OH)4溶液中滴加醋酸溶液,关于该过程的说法不正确 的是
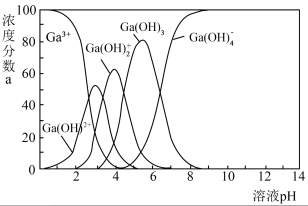

| A.[Ga(OH)4]-的浓度分数一直减小 |
B.Ga3++H2O Ga(OH)2++H+,该平衡常数K的数量级为10-3 Ga(OH)2++H+,该平衡常数K的数量级为10-3 |
C.pH=7时,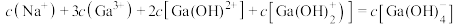 |
| D.当溶液中Ga3+与Ga(OH)3的浓度相等时,c(CH3COO-)<c(CH3COOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,通过下列实验探究一定浓度Na2CO3溶液的性质。
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测得溶液的pH约为10 |
| 2 | 向溶液中滴加几滴酚酞,加水稀释,溶液红色变浅 |
| 3 | 向溶液中通入过量的CO2,无明显现象 |
| 4 | 向实验3所得溶液中滴加少量Ba(OH)2溶液,产生白色沉淀 |
A.实验1溶液中存在: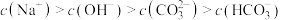 |
B.实验2中随蒸馏水的不断加入,溶液中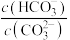 的值逐渐变大 的值逐渐变大 |
C.实验3所得溶液中存在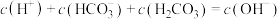 |
D.实验4反应的离子方程式为: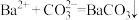 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某废旧锂电池材料含有钴酸锂(LiCoO2)、导电剂石墨和铝粉等。回收废旧锂电池中钴的工艺流程如图:

已知:①Ksp(CoC2O4)=2.5×10-9,Ksp(CoCO3)=1.5×10-13;
②“浸出液”的主要成分是LiHC2O4、Al(HC2O4)3,“浸出渣”的主要成分是CoC2O4。
下列说法正确的是

已知:①Ksp(CoC2O4)=2.5×10-9,Ksp(CoCO3)=1.5×10-13;
②“浸出液”的主要成分是LiHC2O4、Al(HC2O4)3,“浸出渣”的主要成分是CoC2O4。
下列说法正确的是
| A.H2C2O4用量越大,CoC2O4的产率越高 |
| B.“转化”中加入Na2CO3溶液发生反应的平衡常数数值为6×105 |
| C.“电解”时阳极的电极反应式为2H2O-4e-=O2↑+4H+ |
D.将m kg该废料(LiCoO2的质量分数为w)进行回收利用,电解得到钴n kg,钴的回收率为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究化学反应是否可逆 | 向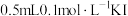 溶液中滴加1~2滴 溶液中滴加1~2滴 的 的 溶液,充分反应后,滴入1~2滴 溶液,充分反应后,滴入1~2滴 的 的 溶液,生成黄色沉淀 溶液,生成黄色沉淀 |
| B | 探究浓度对盐类水解平衡的影响 | 向滴有酚酞的碳酸钠溶液中滴加氯化钡溶液,观察现象 |
| C | 比较AgI和AgCl溶度积大小 | 向 的硝酸银溶液中先滴加2~3滴浓度为 的硝酸银溶液中先滴加2~3滴浓度为 的NaCl溶液,再滴加2~3滴相同浓度的NaI溶液,观察生成沉淀的颜色 的NaCl溶液,再滴加2~3滴相同浓度的NaI溶液,观察生成沉淀的颜色 |
| D | 比较HClO和 酸性强弱 酸性强弱 | 用pH试纸测定NaClO溶液和 溶液的pH 溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验或措施、现象、结论均正确的是
| 实验或措施 | 现象 | 结论 | |
| A | 将纯水加热到95℃ | pH<7 | 加热可导致水呈酸性 |
| B | 用4mL0.01mol·L-1的H2C2O4分别与2mL0.1mol·L-1的酸性KMnO4溶液和2mL0.2mol·L-1的酸性KMnO4溶液反应 | 0.2mol·L-1的酸性KMnO4溶液褪色快 | 研究浓度对反应速率的影响 |
| C | 将石蜡油分解产生的气体通入溴的CCl4溶液中 | 溶液褪色 | 产生的气体是乙烯 |
| D | 向1mL0.1mol·L-1MgCl2溶液中滴加1~2滴NaOH溶液,再滴加2滴0.1mol·L-1FeCl3溶液 | 先产生白色沉淀,后沉淀变为红褐色 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 )>c(
)>c( )>c(OH-)=c(H+)
)>c(OH-)=c(H+)

