我国明确提出2030年“碳达峰”与2060年“碳中和”目标,“碳中和”对我国意味着:一是能源转型首当其冲;二是通过工艺改造、节能等措施减少二氧化碳的排放在能源的产生、转换、消费过程。减少二氧化碳排放的方法之一是将CO2催化还原,比如:
反应1: CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
反应2: CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
都是目前处理CO2的重要方法。回答下列问题:
(1)反应1在_______ 的条件下能自发发生。(填低温、高温、任意温度)
(2)已知:①CO和H2的标准燃烧热分别为-283.0 kJ·mol-1和-285.8 kJ·mol-1
②H2O(1)=H2O(g) ΔH3=44.0 kJ·mol-1,
则 ΔH2=_______ kJ·mol-1。
(3)恒温恒容的密闭容器中,投入物质的量之比为1:3的CO2和H2发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1达到平衡,下列有关叙述正确的是_______。
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1达到平衡,下列有关叙述正确的是_______。
(4)一定条件下,在1L密闭容器中加入2molCO2和2molH2只发生反应2: CO2(g)+H2(g)  CO(g)+H2O(g),如图是随着反应的进行,CO2的浓度随时间改变的变化图。若在t1时刻再加入lmolCO2, t2时刻到达新的平衡。
CO(g)+H2O(g),如图是随着反应的进行,CO2的浓度随时间改变的变化图。若在t1时刻再加入lmolCO2, t2时刻到达新的平衡。
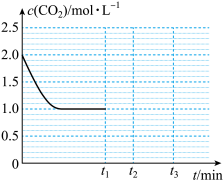
请你画出t1~t3内时刻CO2的物质的量浓度随时间改变的变化图:______
反应1: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1反应2: CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2都是目前处理CO2的重要方法。回答下列问题:
(1)反应1在
(2)已知:①CO和H2的标准燃烧热分别为-283.0 kJ·mol-1和-285.8 kJ·mol-1
②H2O(1)=H2O(g) ΔH3=44.0 kJ·mol-1,
则 ΔH2=
(3)恒温恒容的密闭容器中,投入物质的量之比为1:3的CO2和H2发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1达到平衡,下列有关叙述正确的是_______。
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1达到平衡,下列有关叙述正确的是_______。| A.升高温度,逆反应速率增加,平衡常数减小 |
| B.再加入一定量的CO2和H2, CO2和H2的转化率不可能同时都增大 |
| C.加入合适的催化剂可以提高CO2的平衡转化率 |
| D.其他条件不变,改为恒温恒压,可以提高平衡时CH3OH的百分含量 |
 CO(g)+H2O(g),如图是随着反应的进行,CO2的浓度随时间改变的变化图。若在t1时刻再加入lmolCO2, t2时刻到达新的平衡。
CO(g)+H2O(g),如图是随着反应的进行,CO2的浓度随时间改变的变化图。若在t1时刻再加入lmolCO2, t2时刻到达新的平衡。
请你画出t1~t3内时刻CO2的物质的量浓度随时间改变的变化图:
更新时间:2023-01-25 20:14:49
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】(1)金刚石和石墨灼为碳的同素异形体,它们在氧气不足时烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示:
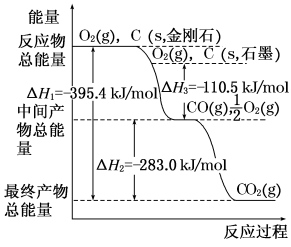
等物质的量的金刚石和石墨完全燃烧___ (填“金刚石”或“石墨”)放出热量更多。在通常状况下,金刚石和石墨相比_____ (填“金刚石”或“石墨”)更稳定。请写出表示石墨燃烧热的热化学方程式_________ 。
(2)已知: Fe2O3(s)+ C(石墨,s)=
C(石墨,s)= CO2(g)+2Fe(s)
CO2(g)+2Fe(s)  =+2341 kJ/mol,则 Fe2O3(s)=
=+2341 kJ/mol,则 Fe2O3(s)= O2(g)+2Fe(s)
O2(g)+2Fe(s)  =
=_________ kJ/mol。
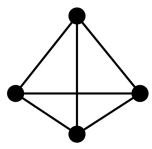
(3)意大利科学家FulviCacace 等获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 mol N—N吸收 167 kJ热量,生成1 mol 放出942 kJ。根据以上信息和数据,计算1 mol N4气体转变为N2的
放出942 kJ。根据以上信息和数据,计算1 mol N4气体转变为N2的  =
=_________ kJ/mol。

等物质的量的金刚石和石墨完全燃烧
(2)已知: Fe2O3(s)+
 C(石墨,s)=
C(石墨,s)= CO2(g)+2Fe(s)
CO2(g)+2Fe(s)  =+2341 kJ/mol,则 Fe2O3(s)=
=+2341 kJ/mol,则 Fe2O3(s)= O2(g)+2Fe(s)
O2(g)+2Fe(s)  =
=(3)意大利科学家FulviCacace 等获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 mol N—N吸收 167 kJ热量,生成1 mol
 放出942 kJ。根据以上信息和数据,计算1 mol N4气体转变为N2的
放出942 kJ。根据以上信息和数据,计算1 mol N4气体转变为N2的  =
=
您最近一年使用:0次
【推荐2】汽车尾气净化反应:2NO(g)+2CO(g) N2(g)+2CO2(g),请回答下列问题:
N2(g)+2CO2(g),请回答下列问题:
(1)对于气相反应,用某组分B平衡时的分压p(B)代替物质的量浓度c(B)也可表示平衡常数,记作KP,则该反应的平衡常数KP表达式为___ ;
(2)已知:N2(g) + O2(g) =2NO(g)△H=+180.5kJ·mol-1
C(s) + O2(g) = CO2(g) △H=-393.5 kJ·mol-1
2C(s) + O2(g) =2CO(g)△H=-221kJ·mol-1
则2NO(g)+2CO(g) N2(g)+2CO2(g)的△H=
N2(g)+2CO2(g)的△H=____ ,该反应能自发进行的条件_______ (填“高温”、“低温”或“任意温度”);
(3)在一定温度下,向体积为 V L的密闭容器中充入一定量的NO和CO。在t1时刻达到平衡状态,此时n(CO)=amol,n(NO)=2a mol,n(N2)=bmol。
①若保持体积不变,再向容器中充入n(CO2)= bmol,n(NO)=amol,则此时v正_____ v逆(填“>”、“=”或“<”);
②在t2时刻,将容器迅速压缩到原容积的 ,在其它条件不变的情况下,t3时刻达到新的平衡状态。请在下图中补充画出t2-t3-t4时段N2物质的量的变化曲线
,在其它条件不变的情况下,t3时刻达到新的平衡状态。请在下图中补充画出t2-t3-t4时段N2物质的量的变化曲线___________ 。
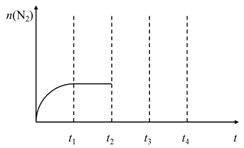
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。
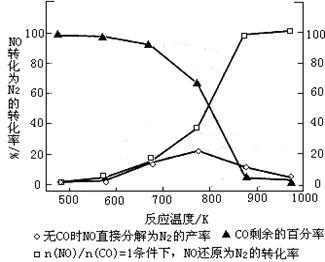
①若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为______ ;在 =1的条件下,应控制的最佳温度在
=1的条件下,应控制的最佳温度在______ 左右;
②目前对氮氧化物(NOx)进行治理的方法比较多,其中吸附/吸收法广受欢迎。下列物质适合作为NOx吸收剂的是____
A.活性炭 B.氨水 C.酸性尿素溶液 D.硫酸
 N2(g)+2CO2(g),请回答下列问题:
N2(g)+2CO2(g),请回答下列问题:(1)对于气相反应,用某组分B平衡时的分压p(B)代替物质的量浓度c(B)也可表示平衡常数,记作KP,则该反应的平衡常数KP表达式为
(2)已知:N2(g) + O2(g) =2NO(g)△H=+180.5kJ·mol-1
C(s) + O2(g) = CO2(g) △H=-393.5 kJ·mol-1
2C(s) + O2(g) =2CO(g)△H=-221kJ·mol-1
则2NO(g)+2CO(g)
 N2(g)+2CO2(g)的△H=
N2(g)+2CO2(g)的△H=(3)在一定温度下,向体积为 V L的密闭容器中充入一定量的NO和CO。在t1时刻达到平衡状态,此时n(CO)=amol,n(NO)=2a mol,n(N2)=bmol。
①若保持体积不变,再向容器中充入n(CO2)= bmol,n(NO)=amol,则此时v正
②在t2时刻,将容器迅速压缩到原容积的
 ,在其它条件不变的情况下,t3时刻达到新的平衡状态。请在下图中补充画出t2-t3-t4时段N2物质的量的变化曲线
,在其它条件不变的情况下,t3时刻达到新的平衡状态。请在下图中补充画出t2-t3-t4时段N2物质的量的变化曲线
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。

①若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为
 =1的条件下,应控制的最佳温度在
=1的条件下,应控制的最佳温度在②目前对氮氧化物(NOx)进行治理的方法比较多,其中吸附/吸收法广受欢迎。下列物质适合作为NOx吸收剂的是
A.活性炭 B.氨水 C.酸性尿素溶液 D.硫酸
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】(1)甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g)+2H2(g) CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图一所示。
CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图一所示。

下列说法正确的是____________ (填字母序号)。
A.达到平衡时,H2的转化率为65%
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氩气,反应速率减小
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)碳与水蒸气反应制取H2的相关反应如下:
Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H= - 43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(s) △H= - 178.3kJ/mol
计算反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g)的△H=
CaCO3(s)+2H2(g)的△H=__________ kJ/mol;
①若K1、K2、K3分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,该平衡常数K=__________ (用K1、K2、K3表示)。
②对于可逆反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是________ 。(填字母)
A.降低体系的温度 B.压缩容器的体积 C.增加CaO的量 D.选用适当的催化剂
 CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图一所示。
CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图一所示。
下列说法正确的是
A.达到平衡时,H2的转化率为65%
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氩气,反应速率减小
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)碳与水蒸气反应制取H2的相关反应如下:
Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H= - 43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(s) △H= - 178.3kJ/mol
计算反应C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+2H2(g)的△H=
CaCO3(s)+2H2(g)的△H=①若K1、K2、K3分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,该平衡常数K=
②对于可逆反应C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是A.降低体系的温度 B.压缩容器的体积 C.增加CaO的量 D.选用适当的催化剂
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氨基甲酸铵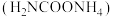 为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
已知:I.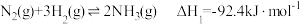
II.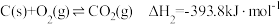
III.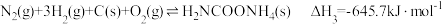
回答下列问题:
(1)写出 分解生成
分解生成 与
与 气体的热化学方程式:
气体的热化学方程式:_______ 。
(2)恒容条件下,实验测得数据如下表所示:
①恒温恒容时,下列能够说明该反应已达到化学平衡状态的是_______ (填标号)。
A.容器内总压强不再改变 B.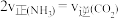
C.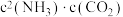 的值不再改变 D.
的值不再改变 D. 的体积分数不再改变
的体积分数不再改变
②某温度下,该反应达到平衡时容器内总压强为p,写出该反应的压强平衡常数的计算式
_______ (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
③随着温度升高, 逐渐
逐渐_______ (填“增大”“减小”或“不变”),其主要原因是_______ 。
④某温度下,达到平衡后,欲增加 的平衡浓度,可采取的措施有
的平衡浓度,可采取的措施有_______ (填标号)。
A.加 B.加催化剂 C.减小体积增大压强 D.移走
B.加催化剂 C.减小体积增大压强 D.移走
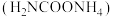 为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。已知:I.
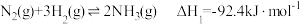
II.
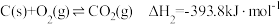
III.
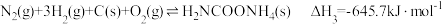
回答下列问题:
(1)写出
 分解生成
分解生成 与
与 气体的热化学方程式:
气体的热化学方程式:(2)恒容条件下,实验测得数据如下表所示:
 | 293 | 298 | 303 | 308 | 313 |
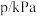 | 8.60 | 11.40 | 16.24 | 20.86 | 30.66 |
A.容器内总压强不再改变 B.
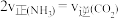
C.
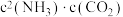 的值不再改变 D.
的值不再改变 D. 的体积分数不再改变
的体积分数不再改变②某温度下,该反应达到平衡时容器内总压强为p,写出该反应的压强平衡常数的计算式

③随着温度升高,
 逐渐
逐渐④某温度下,达到平衡后,欲增加
 的平衡浓度,可采取的措施有
的平衡浓度,可采取的措施有A.加
 B.加催化剂 C.减小体积增大压强 D.移走
B.加催化剂 C.减小体积增大压强 D.移走
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氧化铜、氯化亚铜是重要的化工原料,广泛用作有机合成的催化剂。
Ⅰ.实验室用右图所示装置,利用还原铜粉和氯气来制备氧化铜。

(1)石棉绒的作用是_______________ 。
(2)装置B中的试剂是_______________ 。
(3)所得产品中CuCl2的质量分数为90%,则其中可能含有的杂质是_______________ (写一种即可)。
Ⅱ.另取纯净CuCl2固体用于制备CuCl。
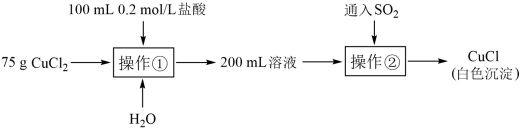
(4)操作①中加入盐酸的目的主要是_______________ 。
(5)操作②中反应的离子方程式为_______________ 。
(6)操作①中若用10mol/L盐酸代替0.2mol/L盐酸,再通入SO2后,无白色沉淀产生。对此现象有如下两种猜想:
猜想一:c(H+)过大导致白色沉淀溶解。
为验证此猜想,取75gCuCl2固体、100mL0.2mol/L盐酸及_______________ mL9.8mol/LH2SO4配制成200mL溶液,再进行操作②,观察是否有白色沉淀产生。
猜想二:c(Cl-)过大导致白色沉淀溶解。
[资料显示:存在平衡2Cl-(aq)+CuCl(s)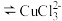 (aq)]
(aq)]
请设计实验说明该猜想是否成立:________________ 。
Ⅰ.实验室用右图所示装置,利用还原铜粉和氯气来制备氧化铜。

(1)石棉绒的作用是
(2)装置B中的试剂是
(3)所得产品中CuCl2的质量分数为90%,则其中可能含有的杂质是
Ⅱ.另取纯净CuCl2固体用于制备CuCl。

(4)操作①中加入盐酸的目的主要是
(5)操作②中反应的离子方程式为
(6)操作①中若用10mol/L盐酸代替0.2mol/L盐酸,再通入SO2后,无白色沉淀产生。对此现象有如下两种猜想:
猜想一:c(H+)过大导致白色沉淀溶解。
为验证此猜想,取75gCuCl2固体、100mL0.2mol/L盐酸及
猜想二:c(Cl-)过大导致白色沉淀溶解。
[资料显示:存在平衡2Cl-(aq)+CuCl(s)
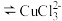 (aq)]
(aq)]请设计实验说明该猜想是否成立:
您最近一年使用:0次
【推荐3】化石能源的脱硫处理是环保热点问题。 用臭氧处理燃煤烟气脱硫的主要反应如下:
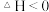 ,向1L反应装置充入
,向1L反应装置充入 和
和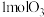 ,经过相同反应时间t后剩余
,经过相同反应时间t后剩余 的物质的量与温度关系如图所示:
的物质的量与温度关系如图所示:
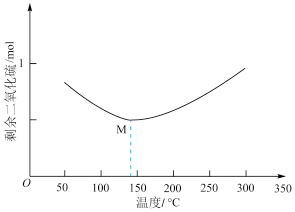
已知臭氧会转化成氧气: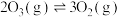 ,在上述反应条件下臭氧分解率与温度关系如下:
,在上述反应条件下臭氧分解率与温度关系如下:
(1)关于脱硫的主要反应,下列说法错误的是______________ 。
A. 50℃时,缩小反应装置的体积可以提高相同时间t内SO2的转化率
B.M点该反应处于平衡状态
C.温度越高,该反应的平衡常数越小
D.随温度的升高,正反应速率变大,逆反应速率减小
(2)200℃以后随着温度升高,SO2的物质的量增多的原因可能是______________________ 。
(3)已知250℃时 的平衡常数
的平衡常数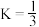 ,求该温度下反应
,求该温度下反应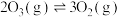 的平衡常数
的平衡常数
__________ 。
(4)其他条件不变,经过相同反应时间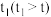 ,在图中画出剩余SO2的物质的量在
,在图中画出剩余SO2的物质的量在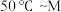 点温度范围内的关系趋势图
点温度范围内的关系趋势图____________ 。
(5)烟气脱硫后续还需用碱液吸收 形成
形成 ,溶液pH为
,溶液pH为 之间时
之间时 在电解池阴极上被还原成连二硫酸根
在电解池阴极上被还原成连二硫酸根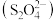 ,写出该电极反应式:
,写出该电极反应式:____________ 。

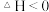 ,向1L反应装置充入
,向1L反应装置充入 和
和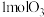 ,经过相同反应时间t后剩余
,经过相同反应时间t后剩余 的物质的量与温度关系如图所示:
的物质的量与温度关系如图所示:
已知臭氧会转化成氧气:
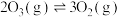 ,在上述反应条件下臭氧分解率与温度关系如下:
,在上述反应条件下臭氧分解率与温度关系如下:温度 | 50 | 100 | 150 | 200 | 250 | 300 |
 分解率 分解率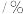 | 0 | 0 | 0 | 4 | 20 | 81 |
A. 50℃时,缩小反应装置的体积可以提高相同时间t内SO2的转化率
B.M点该反应处于平衡状态
C.温度越高,该反应的平衡常数越小
D.随温度的升高,正反应速率变大,逆反应速率减小
(2)200℃以后随着温度升高,SO2的物质的量增多的原因可能是
(3)已知250℃时
 的平衡常数
的平衡常数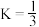 ,求该温度下反应
,求该温度下反应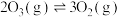 的平衡常数
的平衡常数
(4)其他条件不变,经过相同反应时间
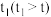 ,在图中画出剩余SO2的物质的量在
,在图中画出剩余SO2的物质的量在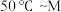 点温度范围内的关系趋势图
点温度范围内的关系趋势图(5)烟气脱硫后续还需用碱液吸收
 形成
形成 ,溶液pH为
,溶液pH为 之间时
之间时 在电解池阴极上被还原成连二硫酸根
在电解池阴极上被还原成连二硫酸根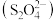 ,写出该电极反应式:
,写出该电极反应式:
您最近一年使用:0次
【推荐1】Ⅰ.将 CO2转化为有价值的化工原料,正成为科学家们研究的重要领域。回答下列问题:
(1)已知:
①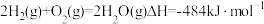
②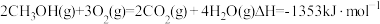
则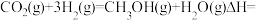
_____ 
(2)在恒压密闭容器中通入 CO2和 H2的混合气体制备甲醇。过程中测得甲醇的时空收率(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
在 220°C 和 170 °C 条件下,该反应速率之比: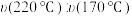
___ 。
(3)CO2催化加氢制甲醇过程中,存在竞争的副反应主要是: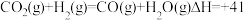
 在恒温密闭容器中,CO2的平衡转化率[α(CO2)%]和甲醇选择性[CH3OH%=
在恒温密闭容器中,CO2的平衡转化率[α(CO2)%]和甲醇选择性[CH3OH%= 随着温度变化关系如图所示。
随着温度变化关系如图所示。
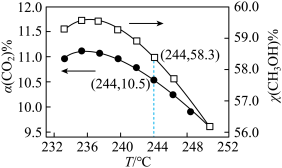
①分析温度高于 236°C 时图中曲线下降的原因_____ 。
②按 1 mol CO2(g)、3 mol H2(g)投料反应,计算 244°C 时反应生成 CH3OH 的物质的量为_____ mol。 (保留两位有效数字)
③在压强为p 的反应条件下,1 mol CO2(g)和 3 mol H2(g)反应并达到平衡状态,CO2平衡转化率为 20%,甲醇选择性为 50%,该温度下主反应的平衡常数 Kp=_____ 。 ( 列出计 算式即可,用平衡分压代替平衡浓度,分压=总压×物质的量分数)
Ⅱ.
(4)工业上也可用 H2还原 CO 电化学法制备甲醇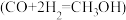 的工作原理如上图所示。电池工作过程中 H+通过质子膜向
的工作原理如上图所示。电池工作过程中 H+通过质子膜向_____ (填“左”或者“右”)移动,通入 CO 的一端发生的电极反应为_____ 。

(1)已知:
①
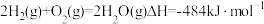
②
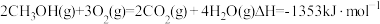
则
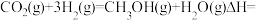

(2)在恒压密闭容器中通入 CO2和 H2的混合气体制备甲醇。过程中测得甲醇的时空收率(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
| T/°C | 170 | 180 | 1 90 | 200 | 210 | 220 | 230 |
| STY/[mol/(mol·h)] | 0.10 | 0.15 | 0.20 | 0.25 | 0.28 | 0.20 | 0.15 |
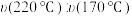
(3)CO2催化加氢制甲醇过程中,存在竞争的副反应主要是:
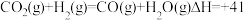
 在恒温密闭容器中,CO2的平衡转化率[α(CO2)%]和甲醇选择性[CH3OH%=
在恒温密闭容器中,CO2的平衡转化率[α(CO2)%]和甲醇选择性[CH3OH%= 随着温度变化关系如图所示。
随着温度变化关系如图所示。
①分析温度高于 236°C 时图中曲线下降的原因
②按 1 mol CO2(g)、3 mol H2(g)投料反应,计算 244°C 时反应生成 CH3OH 的物质的量为
③在压强为p 的反应条件下,1 mol CO2(g)和 3 mol H2(g)反应并达到平衡状态,CO2平衡转化率为 20%,甲醇选择性为 50%,该温度下主反应的平衡常数 Kp=
Ⅱ.
(4)工业上也可用 H2还原 CO 电化学法制备甲醇
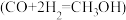 的工作原理如上图所示。电池工作过程中 H+通过质子膜向
的工作原理如上图所示。电池工作过程中 H+通过质子膜向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】在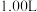 的密闭容器中,通入一定量的
的密闭容器中,通入一定量的 ,发生反应
,发生反应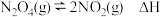 ,随温度升高,混合气体的颜色变深。回答下列问题:
,随温度升高,混合气体的颜色变深。回答下列问题:
(1)
___________ (填“>”或“<”)0。
(2)图甲为该反应过程中有关物理量Y随温度X(其他条件不变)变化的关系图。Y可表示___________ (填字母)。
A.逆反应速率 B.气体的密度 C.平衡常数 D. 的转化率 E.气体的平均摩尔质量
的转化率 E.气体的平均摩尔质量
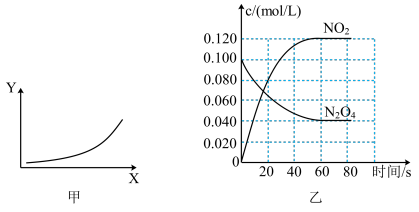
(3)图乙为100℃时,体系中各物质的物质的量浓度随时间变化关系。
①在 时段,反应速率
时段,反应速率 为
为___________  。
。
② 后,改变反应温度为
后,改变反应温度为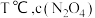 以
以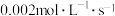 的平均速率降低,经
的平均速率降低,经 后又达到平衡。T
后又达到平衡。T___________ (填“>”或“<”)100℃,判断理由是___________ 。在 时反应达平衡后,将反应容器的容积缩小一半,平衡向
时反应达平衡后,将反应容器的容积缩小一半,平衡向___________ (填“正反应”或“逆反应”)方向移动,判断的理由是___________ 。
(4)对于上述反应,用平衡时各物质分压表示的平衡常数为 。在一定条件下
。在一定条件下 、
、 的消耗速率与分压关系为
的消耗速率与分压关系为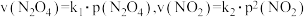 。其中,
。其中,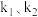 是与温度有关的常数,则
是与温度有关的常数,则
___________ (用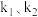 表示)。
表示)。
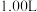 的密闭容器中,通入一定量的
的密闭容器中,通入一定量的 ,发生反应
,发生反应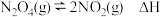 ,随温度升高,混合气体的颜色变深。回答下列问题:
,随温度升高,混合气体的颜色变深。回答下列问题:(1)

(2)图甲为该反应过程中有关物理量Y随温度X(其他条件不变)变化的关系图。Y可表示
A.逆反应速率 B.气体的密度 C.平衡常数 D.
 的转化率 E.气体的平均摩尔质量
的转化率 E.气体的平均摩尔质量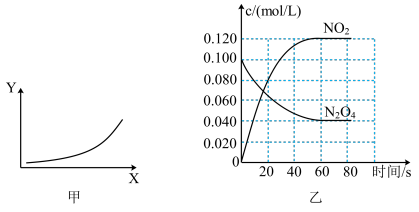
(3)图乙为100℃时,体系中各物质的物质的量浓度随时间变化关系。
①在
 时段,反应速率
时段,反应速率 为
为 。
。②
 后,改变反应温度为
后,改变反应温度为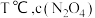 以
以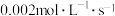 的平均速率降低,经
的平均速率降低,经 后又达到平衡。T
后又达到平衡。T 时反应达平衡后,将反应容器的容积缩小一半,平衡向
时反应达平衡后,将反应容器的容积缩小一半,平衡向(4)对于上述反应,用平衡时各物质分压表示的平衡常数为
 。在一定条件下
。在一定条件下 、
、 的消耗速率与分压关系为
的消耗速率与分压关系为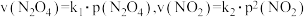 。其中,
。其中,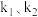 是与温度有关的常数,则
是与温度有关的常数,则
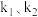 表示)。
表示)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氮、碳氧化物的无害化处理是研究的热点。一定条件下N2O发生如下反应:
Ⅰ.2N2O(g) 2N2(g)+O2(g)+164kJ
2N2(g)+O2(g)+164kJ
Ⅱ.N2O(g)+CO(g) N2(g)+CO2(g)+356 kJ
N2(g)+CO2(g)+356 kJ
完成下列填空:
(1)反应I平衡常数的表达式K=_______ 。
某温度下,反应Ⅰ的K=0.16,该温度下,测得容器中N2O、N2、O2的浓度分别为0.5mol·L-1、0.5mol·L-1、0.25mol·L-1,此时,反应I是否处于平衡状态?若不是,预测反应的方向。_______ 。
(2)甲为10L 的恒温容器。盛有1mol N2O和lmolCO,发生反应Ⅰ和反应Ⅱ,5min 时,测得CO转化率为60%,n(N2):n(O2)=8:1,则n(N2O)=_______ mol;0~5min, O2的平均反应速率v(O2)=_______ mol · L-1·min-1。
(3)乙为10L的绝热容器。向其中充入1mol N2O和1molCO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间_______ 甲;此时乙中n(N2O)比甲中_______ (以上两空选填“>”“<”或“=”),理由是:_______ 。
(4)不同压强的密闭容器中,分别充入1mol N2O和1lmolCO,发生反应Ⅰ和反应Ⅱ,测得N2O的平衡转化率与温度的关系如图所示。
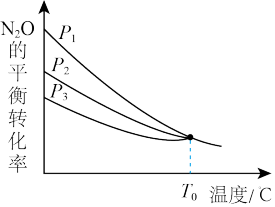
P1、P2、 P3由小到大的顺序为_______ ;温度高于T°C时,容器内发生的主要反应为_______ (填 “Ⅰ”“Ⅱ”)。
Ⅰ.2N2O(g)
 2N2(g)+O2(g)+164kJ
2N2(g)+O2(g)+164kJⅡ.N2O(g)+CO(g)
 N2(g)+CO2(g)+356 kJ
N2(g)+CO2(g)+356 kJ完成下列填空:
(1)反应I平衡常数的表达式K=
某温度下,反应Ⅰ的K=0.16,该温度下,测得容器中N2O、N2、O2的浓度分别为0.5mol·L-1、0.5mol·L-1、0.25mol·L-1,此时,反应I是否处于平衡状态?若不是,预测反应的方向。
(2)甲为10L 的恒温容器。盛有1mol N2O和lmolCO,发生反应Ⅰ和反应Ⅱ,5min 时,测得CO转化率为60%,n(N2):n(O2)=8:1,则n(N2O)=
(3)乙为10L的绝热容器。向其中充入1mol N2O和1molCO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时间
(4)不同压强的密闭容器中,分别充入1mol N2O和1lmolCO,发生反应Ⅰ和反应Ⅱ,测得N2O的平衡转化率与温度的关系如图所示。

P1、P2、 P3由小到大的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】运用化学反应原理研究与氨气有关反应有重要意义。请回答下列问题。
I.已知合成氨反应的热化学方程式为:
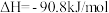 。
。
(1)近期,我国科学家为了解决合成氨反应速率和平衡产率的矛盾,选择使用Fe-TiO2-xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2-xHy的温度为415℃)。结合图示解释该双催化剂的工作原理(已知:常温下氮氮三键不易断裂):___________ 。
热Fe冷Ti双温催化原理如下:

II.催化氧化法除尾气中氨气的反应为:
a.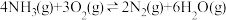
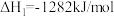
在实际反应中还伴随如下副反应发生:
b.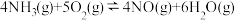
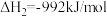
c.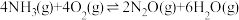
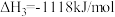
(2)反应a在常压下自发进行的温度条件是___________ 。(填“高温”“低温”或“任意温度”)
(3)其他条件不变,升高温度,NH3的平衡转化率___________ (填“增大”、“减小”或“不变”)。原因为___________ 。
(4)将一定比例的NH3和O2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、生成N2的选择率与温度的关系如图所示。
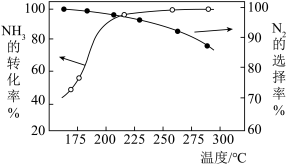
①其他条件不变,在175℃~300℃范围,催化氧化除去尾气中的NH3应选择反应温度范围为200℃~225℃之间,理由是___________ 。
②随温度的升高,N2选择率下降的原因可能为___________ 。
III.请回答:
(5)含氮化合物对工业生产有多种影响,化学工作者设计了如下再利用的方案:
以NH3和CO2为原料合成尿素[CO(NH2)2],两步反应的能量变化如图:

①已知第二步反应决定了生产尿素的快慢,可推测E1___________ E3(填“>”“<”或“=”)。
②该反应达到化学平衡后,下列措施能提高NH3转化率的是___________ 。
A.选用更有效的催化剂 B.及时从体系转移出生成的尿素
C.降低反应体系的温度 D.增大二氧化碳的浓度
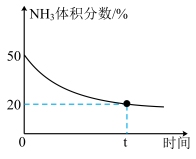
(6)某实验小组为了模拟工业合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应: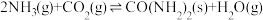 ,反应过程中NH3的体积分数如图所示。实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数Kp=
,反应过程中NH3的体积分数如图所示。实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数Kp=___________ (MPa)-2(已知: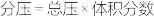 )。
)。
I.已知合成氨反应的热化学方程式为:

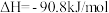 。
。(1)近期,我国科学家为了解决合成氨反应速率和平衡产率的矛盾,选择使用Fe-TiO2-xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2-xHy的温度为415℃)。结合图示解释该双催化剂的工作原理(已知:常温下氮氮三键不易断裂):
热Fe冷Ti双温催化原理如下:

II.催化氧化法除尾气中氨气的反应为:
a.
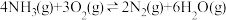
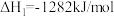
在实际反应中还伴随如下副反应发生:
b.
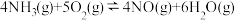
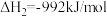
c.
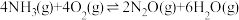
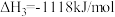
(2)反应a在常压下自发进行的温度条件是
(3)其他条件不变,升高温度,NH3的平衡转化率
(4)将一定比例的NH3和O2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、生成N2的选择率与温度的关系如图所示。

①其他条件不变,在175℃~300℃范围,催化氧化除去尾气中的NH3应选择反应温度范围为200℃~225℃之间,理由是
②随温度的升高,N2选择率下降的原因可能为
III.请回答:
(5)含氮化合物对工业生产有多种影响,化学工作者设计了如下再利用的方案:
以NH3和CO2为原料合成尿素[CO(NH2)2],两步反应的能量变化如图:

①已知第二步反应决定了生产尿素的快慢,可推测E1
②该反应达到化学平衡后,下列措施能提高NH3转化率的是
A.选用更有效的催化剂 B.及时从体系转移出生成的尿素
C.降低反应体系的温度 D.增大二氧化碳的浓度
(6)某实验小组为了模拟工业合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应:
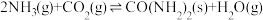 ,反应过程中NH3的体积分数如图所示。实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数Kp=
,反应过程中NH3的体积分数如图所示。实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数Kp=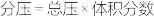 )。
)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】(1)用太阳能分解水制备 是一项新技术,其过程如下。
是一项新技术,其过程如下。

已知: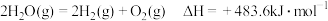
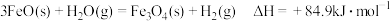
过程I的热化学方程式是_______
(2)已知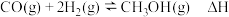 ,经测定不同温度下反应的化学平衡常数如下:
,经测定不同温度下反应的化学平衡常数如下:
①该反应在_______ 条件下易自发。(填“高温”或“低温”)
②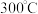 ,某时刻
,某时刻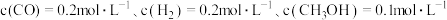 ,此时
,此时 正
正_______  逆(填“>”、“<”或“=”)
逆(填“>”、“<”或“=”)
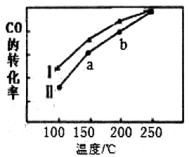
③其他条件不变,在不同催化剂(Ⅰ、Ⅱ)作用下,反应 进行相同时间后,
进行相同时间后, 的转化率随反应温度的变化如图所示。b点
的转化率随反应温度的变化如图所示。b点 的转化率高于a点,原因是
的转化率高于a点,原因是_______
(3)在一体积为 密闭容器中,加入催化剂并加热到一定温度时,使其发生反应
密闭容器中,加入催化剂并加热到一定温度时,使其发生反应 ,起始
,起始 和
和 的物质的量分别为
的物质的量分别为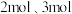 :
:
①达到平衡后测得体系压强是起始时的0.6倍,则该反应的平衡常数
_______ 
②一氧化碳催化加氢合成甲醇反应往往伴随着副反应,生成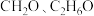 等有机物。一定温度和压强条件下,为了提高反应速率和合成甲醇的选择性,应当
等有机物。一定温度和压强条件下,为了提高反应速率和合成甲醇的选择性,应当_______ 。
(4)在不同的电压下,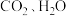 混合电解转化为
混合电解转化为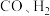 的电流效率如图所示
的电流效率如图所示
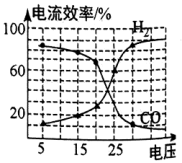
(注: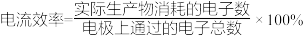 )
)
①由图可知生成 和
和 有相互
有相互_______ (填“促进”、“抑制”或“无影响”)作用。
②用此法生产的 和
和 合成
合成 ,为使利用率最高,电解时应控制电压在
,为使利用率最高,电解时应控制电压在_______ V左右(选填5、15、25)
 是一项新技术,其过程如下。
是一项新技术,其过程如下。
已知:
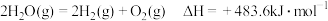
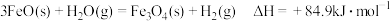
过程I的热化学方程式是
(2)已知
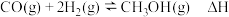 ,经测定不同温度下反应的化学平衡常数如下:
,经测定不同温度下反应的化学平衡常数如下:温度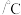 | 250 | 300 | 350 |
| K | 2.04 | 0.27 | 0.012 |
①该反应在
②
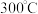 ,某时刻
,某时刻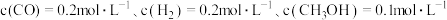 ,此时
,此时 正
正 逆(填“>”、“<”或“=”)
逆(填“>”、“<”或“=”)③其他条件不变,在不同催化剂(Ⅰ、Ⅱ)作用下,反应
 进行相同时间后,
进行相同时间后, 的转化率随反应温度的变化如图所示。b点
的转化率随反应温度的变化如图所示。b点 的转化率高于a点,原因是
的转化率高于a点,原因是
(3)在一体积为
 密闭容器中,加入催化剂并加热到一定温度时,使其发生反应
密闭容器中,加入催化剂并加热到一定温度时,使其发生反应 ,起始
,起始 和
和 的物质的量分别为
的物质的量分别为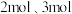 :
:①达到平衡后测得体系压强是起始时的0.6倍,则该反应的平衡常数


②一氧化碳催化加氢合成甲醇反应往往伴随着副反应,生成
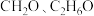 等有机物。一定温度和压强条件下,为了提高反应速率和合成甲醇的选择性,应当
等有机物。一定温度和压强条件下,为了提高反应速率和合成甲醇的选择性,应当(4)在不同的电压下,
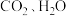 混合电解转化为
混合电解转化为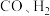 的电流效率如图所示
的电流效率如图所示
(注:
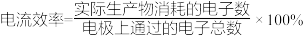 )
)①由图可知生成
 和
和 有相互
有相互②用此法生产的
 和
和 合成
合成 ,为使利用率最高,电解时应控制电压在
,为使利用率最高,电解时应控制电压在
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】氮及化合物用途广泛,可制化肥、燃料、医药等化学工业。
(1)氨气易溶于水可电离出 和OH-、易液化,液氨也与水一样发生双聚电离,但比水弱,能溶解一些金属等性质。下列说法不正确的是
和OH-、易液化,液氨也与水一样发生双聚电离,但比水弱,能溶解一些金属等性质。下列说法不正确的是__________ 。
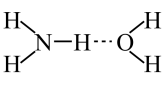
A.NH3可看作比水弱的电解质
B.NH3的双聚电离为2NH3
 +
+
C.NH3易溶于水是由于与水形成氢键,如图所示
D.NH3可与Na反应2NH3+2Na=2NaNH2+H2↑
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g) 4NO2(g)+O2(g)
4NO2(g)+O2(g)  >0
>0
①该反应自发进行的条件是___________ 。
②下表为反应在T1温度下的部分实验数据:
若在T2温度下进行实验,1000s时测得反应体系中NO2浓度为4.98mol·L-1,则T2__________ T1(填“>”、“<”或“=”)。
(3)N2H4是二元弱碱,其水溶液呈碱性的原因是(用电离方程式表示)__________ 。N2H4的制法可用过量NH3与CH3CHO的混合物与氯气进行气相反应合成出异肼(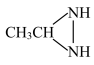 ),异肼水解得到肼,写出第一步的化学反应方程式
),异肼水解得到肼,写出第一步的化学反应方程式__________ 。
(4)有一种化合物NH4H,据推断NH4H不能稳定存在,原因是__________ 。
(1)氨气易溶于水可电离出
 和OH-、易液化,液氨也与水一样发生双聚电离,但比水弱,能溶解一些金属等性质。下列说法不正确的是
和OH-、易液化,液氨也与水一样发生双聚电离,但比水弱,能溶解一些金属等性质。下列说法不正确的是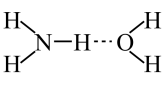
A.NH3可看作比水弱的电解质
B.NH3的双聚电离为2NH3

 +
+
C.NH3易溶于水是由于与水形成氢键,如图所示
D.NH3可与Na反应2NH3+2Na=2NaNH2+H2↑
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)
 4NO2(g)+O2(g)
4NO2(g)+O2(g)  >0
>0①该反应自发进行的条件是
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
(3)N2H4是二元弱碱,其水溶液呈碱性的原因是(用电离方程式表示)
 ),异肼水解得到肼,写出第一步的化学反应方程式
),异肼水解得到肼,写出第一步的化学反应方程式(4)有一种化合物NH4H,据推断NH4H不能稳定存在,原因是
您最近一年使用:0次



