 N2(g)+2CO2(g),请回答下列问题:
N2(g)+2CO2(g),请回答下列问题:(1)对于气相反应,用某组分B平衡时的分压p(B)代替物质的量浓度c(B)也可表示平衡常数,记作KP,则该反应的平衡常数KP表达式为
(2)已知:N2(g) + O2(g) =2NO(g)△H=+180.5kJ·mol-1
C(s) + O2(g) = CO2(g) △H=-393.5 kJ·mol-1
2C(s) + O2(g) =2CO(g)△H=-221kJ·mol-1
则2NO(g)+2CO(g)
 N2(g)+2CO2(g)的△H=
N2(g)+2CO2(g)的△H=(3)在一定温度下,向体积为 V L的密闭容器中充入一定量的NO和CO。在t1时刻达到平衡状态,此时n(CO)=amol,n(NO)=2a mol,n(N2)=bmol。
①若保持体积不变,再向容器中充入n(CO2)= bmol,n(NO)=amol,则此时v正
②在t2时刻,将容器迅速压缩到原容积的
 ,在其它条件不变的情况下,t3时刻达到新的平衡状态。请在下图中补充画出t2-t3-t4时段N2物质的量的变化曲线
,在其它条件不变的情况下,t3时刻达到新的平衡状态。请在下图中补充画出t2-t3-t4时段N2物质的量的变化曲线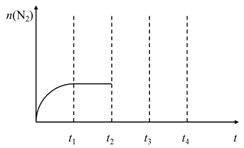
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。
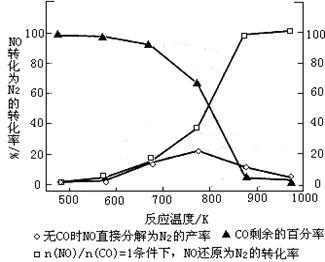
①若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为
 =1的条件下,应控制的最佳温度在
=1的条件下,应控制的最佳温度在②目前对氮氧化物(NOx)进行治理的方法比较多,其中吸附/吸收法广受欢迎。下列物质适合作为NOx吸收剂的是
A.活性炭 B.氨水 C.酸性尿素溶液 D.硫酸
相似题推荐
(1)不同温度、压强下.合破氦平衡体系NH3的物质的量分数如图 (N2和H2的起始物质的量之比为1:3)。
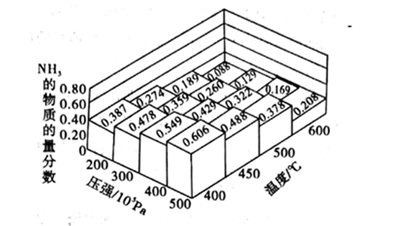
①分析图中数据,升商温度,该反应的平衡常数K值
②下列关于合成氨的说法正确的是
A.工业上合成氨,为了提高氨的含量压强越大越好
B.使用催化剂可以提高氨气的产率
C.合成氨反应△H<0、△S<0,该反应高温条件下一定能自发进行
D.减小n(N2): n(H2) 的比值,有利于提高N2 的转化率
③如果开始时向密闭容器中投入1.0mol N2 和3.0mol H2,则在500C、3×107Pa条件下达到平衡时N2 的平衡 转 化率=
(2)以氨气代替氢气研发氨燃料电池是当前科研的一一个热点。氨燃料电池使用的电解质溶液是KOH溶液。该电池负极的电极反应式为
(3)NH3也是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的NH3转化为氮气除去,其相关反应的热化学方程式如下:
反应I: NH3 (aq)+HClO(aq)=NH2Cl(aq)+H2O(l) △H1=akJ/mol;
反应II :NH2Cl(aq)+HClO(aq)=NHCl2(aq)+H2O(l) △H2=bkJ/mol;
反应III: 2NHCl2(aq) +H2O(l)=N2(g)+HClO( aq)+3HCl( aq) △H3=ckJ/mol。
①2NH3(aq)+3HClO(aq)==N2(g)+ H2O(l) △H=
②已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件不变的情况下,改变
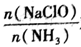 对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量) 的影响如图l4所示。a点之前溶液中发生的主要反应为
对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量) 的影响如图l4所示。a点之前溶液中发生的主要反应为A.反应I、I I B.反应I
③除氨氮过程中最佳的
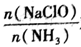 值约为
值约为
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1II.2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2
CH3OCH3(g)+H2O(g) △H2III.CO(g)+H2O(g)
 CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3则3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g) △H=
CH3OCH3(g)+CO2(g) △H=(2)在1 L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示: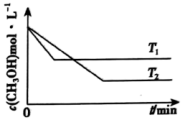
①△H
②在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)
 CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1II.CO(g)+2H2(g)
 CH3OH(g) △H2=-90.4 kJ·mol-1
CH3OH(g) △H2=-90.4 kJ·mol-1III.CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol,此时H2O(g)的浓度为
Ⅰ脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) △H=+l33kJ·mol-1
H2O(g)=H2O(l) △H=-44kJ·mol-1
在催化剂存在下,H2还原NO2可生成水蒸气和其它无毒物质的热化学方程式为:
Ⅱ.脱碳:在2L的密闭容器中充入2mol CO2和6mol H2,在适当的催化剂作用下发生反应:
CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) △H<0
CH3OH(l)+H2O(l) △H<0①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均摩尔质量保持不变
b. CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d. 混合气体的密度保持不变
e. 1mol CO2生成的同时有3 mul H―H键断裂
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,请画出t2~t4CO2浓度随时间的变化。

(2)改变温度,使反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) △H<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I:恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| l0min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ:绝热恒容 | 0min | 0 | 0 | 2 | 2 |
① 达到平衡时,反应I、Ⅱ对比:平衡常数K(I)
②对反应I,前10min内的平均反应速率v(CH3OH)=
(1)制取甲胺CH3NH2的反应为是一个可逆的过程,以甲醇蒸气、氨气为原料合成,另一产物为水蒸气。已知该反应中相关化学键的键能数据如下:
| 共价键 | C—O | H—O | N—H | C—N |
| 键能/(kJ/mol) | 351 | 463 | 393 | 293 |
则该反应的热化学方程式为:
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为CO(g)+2H2(g)
 CH3OH(g) ΔH<0在一定条件下,将1molCO和2molH2通入一个3L的密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g) ΔH<0在一定条件下,将1molCO和2molH2通入一个3L的密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示: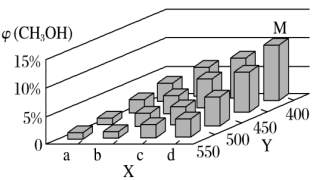
①平衡时,M点CH3OH的体积分数为10%,求该反应在400℃时的平衡常数K=
②某同学认为上图中X轴表示压强,你认为他判断的理由是
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,同时生成I2,写出发生的化学反应方程式
(4)HI的制备:将0.8molI2(g)和1.2molH2(g)置于某1L密闭容器中,在P0MPa、T℃的条件下发生反应:I2(g)+H2(g)
 2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:
2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| HI体积分数 | 26% | 42% | 52% | 57% | 60% | 60% | 60% |
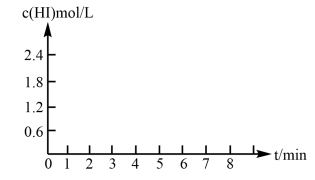
①该反应进行到6min时体系内H2的分压为
②反应达到平衡后,在7min时将容器体积压缩为原来的一半,请在图中画出c(HI)随时间变化的曲线。
I.CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) △H1
CO2(g)+3H2(g) △H1II.CH3OH(g)
 CO(g)+2H2(g) △H2=+90kJ•mol-1
CO(g)+2H2(g) △H2=+90kJ•mol-1(1)已知CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1反应I的△H1=
(2)将组成(物质的量分数)为25%CH3OH(g)、35%H2O(g)和40%N2(g)(N2不参与反应)的气体通入恒容容器中反应相同时间,测得CH3OH转化率和产物的物质的量分数随温度变化关系如图所示。
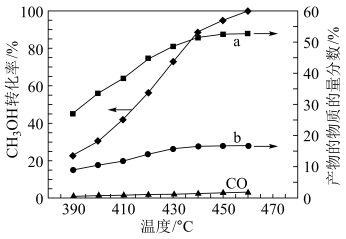
①曲线a和b分别代表产物
②下列对甲醇水蒸气重整制氢反应体系的说法合理的有
A.增大N2的浓度,反应I、II的正反应速率都增加
B.移除CO2能提高CH3OH的平衡转化率
C.升高温度,N2的物质的量分数保持不变
D.440℃~460℃时,升高温度,H2的产率增大
③反应I活化能小于反应II,结合图中信息解释判断依据
(3)一定条件下,向2L的恒容密闭容器中通入1molCH3OH(g)和1molH2O(g)发生上述反应,达到平衡时,容器中CO2为0.8mol,CO为0.1mol,此时H2的浓度为
(4)研究发现以铜作催化剂时,反应I经历三步:
①CH3OH→HCHO+H2,
②HCHO+H2O→HCOOH+H2,
③
①CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g)ΔH1=+210.5 kJ·mol-1
CaO(s)+SO2(g)+CO2(g)ΔH1=+210.5 kJ·mol-1 ②
 CaSO4(s)+CO(g)
CaSO4(s)+CO(g) 
 CaS(s)+CO2(g) ΔH2=-47.3 kJ·mol-1
CaS(s)+CO2(g) ΔH2=-47.3 kJ·mol-1请回答下列问题:
反应CaO(s)+3CO(g)+SO2(g)
 CaS(s)+3CO2(g) ΔH3=
CaS(s)+3CO2(g) ΔH3=(2)有机物加氢反应中镍是常用的催化剂,但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资料如下:
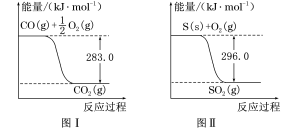
则:①不用通入O2氧化的方法除去CO的原因是
②SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=
(3)汽车发动机工作时会引发N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,其能量变化示意图如下:
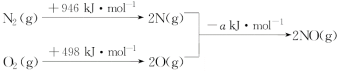
则NO中氮氧键的键能为

(1)氨与氧气生成一氧化氮反应的化学方程式是
(2)在800℃时,向容积为1L的密闭容器中充入0.020 mol NO和0.010 mol O2,发生反应2NO(g)+O2(g)
 2NO2(g),反应过程中O2的浓度随时间变化情况如下图所示。
2NO2(g),反应过程中O2的浓度随时间变化情况如下图所示。
①2min时,c(NO2)=
②800℃时,该反应的化学平衡常数数值是
③已知:

NO生成NO2热化学方程式是
(3)可用电解法处理含氮氧化物的废气。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极)。电解过程中NO转化为硝酸的电极反应式是

 N2(g)+2CO2(g) ΔH<0。
N2(g)+2CO2(g) ΔH<0。(1)假设在密闭容器中发生上述反应,达到平衡时,下列措施能提高NO转化率的是_______(填序号)。
| A.选用更有效的催化剂 | B.升高反应体系的温度 |
| C.降低反应体系的温度 | D.缩小容器的容积 |

(3)已知上述反应中NO的平衡转化率与压强、温度的关系如图所示。工业上催化装置中比较适合的温度和压强是

(1)中科院兰州化学物理研究所用
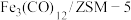 催化
催化 加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂
加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂 (也起催化作用)后可改变反应的选择性。
(也起催化作用)后可改变反应的选择性。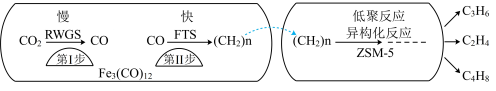
下列说法正确的是
a.第1步所发生的反应为:
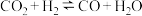
b.第1步反应的活化能低于第2步
c.
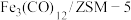 使
使 加氢合成低碳烯烃的
加氢合成低碳烯烃的 减小
减小d.添加不同助剂后,各反应的平衡常数不变
(2)纳米铁是重要的储氢材料,可用反应
 制得。在
制得。在 恒容密闭容器中加入足量铁粉和
恒容密闭容器中加入足量铁粉和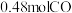 ,在
,在 不同温度下进行反应,测得
不同温度下进行反应,测得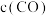 与温度、时间的关系如图所示。
与温度、时间的关系如图所示。

(3)
 温度下,平衡时体系的压强为
温度下,平衡时体系的压强为 ,反应的标准平衡常数
,反应的标准平衡常数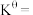
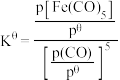 ,其中
,其中 为标准压强
为标准压强 为各组分的平衡分压。)
为各组分的平衡分压。)(4)高铁酸钾
 被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。
被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。①电解法可制得
 ,装置如图,阳极电极反应式为
,装置如图,阳极电极反应式为
②
 在水解过程中铁元素形成的微粒分布分数与
在水解过程中铁元素形成的微粒分布分数与 的关系如图所示,向
的关系如图所示,向 的溶液中加入
的溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为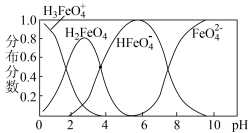
(5)复合氧化物铁酸锰
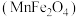 可用于热化学循环分解制氢气,原理如下:
可用于热化学循环分解制氢气,原理如下: ①


②


③


则:
 与
与 、
、 的关系为
的关系为
ⅰ.CO(g)+2H2(g)
 CH3OH(g) ΔH=a kJ/mol;
CH3OH(g) ΔH=a kJ/mol;ⅱ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=b kJ/mol;
CH3OH(g)+H2O(g) ΔH=b kJ/mol;ⅲ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=−c kJ/mol。
CO(g)+H2O(g) ΔH=−c kJ/mol。回答下列问题:
(1)a=
(2)在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2与H2,在催化剂的作用下仅发生反应ⅲ。该反应达到平衡时,其他条件不变,通入CO2时,则v(正)
(3)一定温度下,向体积为2L的恒容密闭容器中通入CO、H2、CH3OH,发生反应ⅰ,其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。
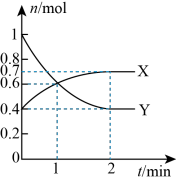
①Y为
②0~1min时v(CO)为
③该温度下,该反应的平衡常数Kc=
(4)工业上以
 和
和 为原料可制备合成气(CO、H2),已知
为原料可制备合成气(CO、H2),已知 、
、 、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应
、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应

 ,
, (
(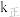 、
、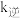 为速率常数,只与温度有关),平衡后降低温度,则
为速率常数,只与温度有关),平衡后降低温度,则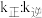
(5)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cm△T计算获得。
①热量的测定:取0.5000mol/LNaOH溶液和0.5500mol/L盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,(c和
 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
 。
。②下列操作会使所测得的焓变
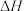 偏小的是
偏小的是a.用等物质的量浓度的醋酸代替盐酸实验 b.量热装置绝热效果欠佳 c.NaOH溶液量多了
【推荐2】阿根廷科学家MasVeronica等人利用Ni(Ⅱ)Al(Ⅲ)层状复合催化剂进行了乙醇水蒸气重整制氢的研究。其主要反应为
反应I.C2H5OH(g)+3H2O(g)=2CO2(g)+6H2(g) △H1=+173.3kJ/mol △S=+362.7J/(K•mol)
反应Ⅱ.C2H5OH(g)+H2O(g)=2CO(g)+4H2(g) △H2=+255.7kJ/mol
若在恒容密闭容器中发生上述反应。
(1)反应I在常温下
(2)对上述恒容密闭容器中的体系,下列说法正确的是
| A.增大H2O(g)的浓度,有利于提高C2H5OH平衡转化率 |
| B.一定温度下,增大C2H5OH的浓度可以提高C2H5OH的平衡转化率 |
| C.若气体的平均相对分子质量保持不变,说明反应体系已达平衡 |
| D.升高温度可以使反应I、Ⅱ的正反应速率加快,逆反应速率减小,平衡向正反应方向移动 |
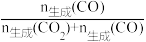 ×100%。
×100%。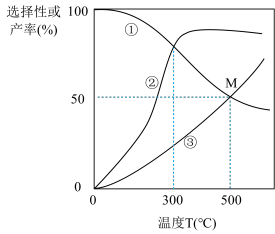
①图中曲线表示平衡时H2产率随温度变化的曲线是
②在密闭容器中,以投料比n(C2H5OH):n(H2O)=3:8通入混合气体,此时C2H5OH的转化率为66.67%,求交点M坐标为(500℃,50%)时反应Ⅱ的平衡常数Kp=
③一定能提高CO选择性的关键因素是
④请分析说明曲线②随温度变化的原因
(4)对乙醇水蒸气重整制氢反应I进行反应机理分析如下,“*”表示催化剂表面的活性中心,请补充完成基元反应iii。
i.C2H6O(g)+(*)→C2H6O*
ii.C2H6O*+(*)→CH4O*+CH2*
ⅲ.
iv.CH2*+2H2O(g)→CO2(g)+3H2(g)+(*)
(1)“可燃冰”晶体中平均每46个H2O分子构建8个笼,其中6个笼分别容纳1个CH4分子,另外2个笼分别容纳1个H2O分子,则“可燃冰”平均组成可表示为
(2)已知:
CO2(g)+nH2O(l)=CO2·nH2O(s) △H=-57.98kJ·mol-1
CH4(g)+nH2O(l)=CH4·nH2O(s) △H=-54.49kJ·mol-1
反应CO2(g)+CH4·nH2O(s)=CH4(g)+CO2·nH2O(s)的△H=
(3)科学家提出用CO2“置换”CH4开采海底“可燃冰”的设想,提出该设想的理论依据是
(4)图中显示,CO2·nH2O的生产速率明显大于 CH4·nH2O释放出的速率,其原因是
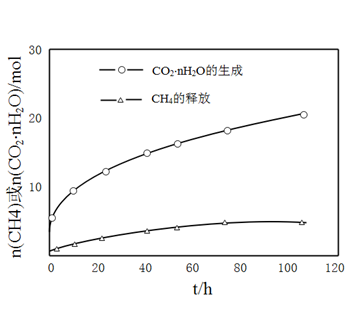
(5)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图。
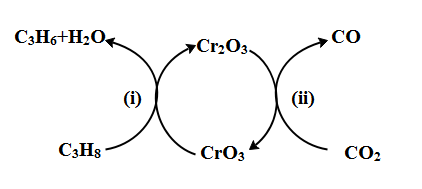
①反应(i)的化学方程式为
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是



