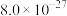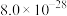钒(V)广泛应用于冶金、化工、航天等领域。一种以钒渣(主要成分是 、
、 、
、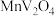 等)为原料制取金属钒的工艺流程如图所示:
等)为原料制取金属钒的工艺流程如图所示:
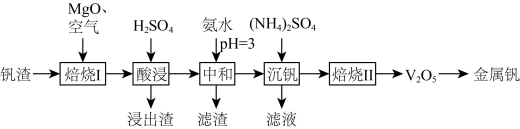
已知:① 具有强氧化性,主要存在于pH<2的溶液中,pH>2时转化成酸式多钒酸盐。
具有强氧化性,主要存在于pH<2的溶液中,pH>2时转化成酸式多钒酸盐。
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)基态V原子的价电子轨道表示式为_______ 。
(2)“焙烧Ⅰ”中 (Fe为+2价)转化为
(Fe为+2价)转化为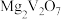 和
和 的化学方程式为
的化学方程式为_______ 。
(3)“酸浸”所得浸出液中除含有 、
、 外,还含有的金属阳离子有
外,还含有的金属阳离子有_______ 。
(4)“沉钒”可得到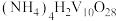 沉淀,“焙烧Ⅱ”中发生反应的化学方程式为
沉淀,“焙烧Ⅱ”中发生反应的化学方程式为_______ 。
(5)“沉钒”所得滤液中加入氨水调节溶液pH=x,过滤得到 沉淀和溶液A,溶液A中
沉淀和溶液A,溶液A中 浓度为
浓度为 ,为尽可能多地回收
,为尽可能多地回收 ,并避免
,并避免 中混入
中混入 ,应控制x=
,应控制x=_______ 。
(6)溶液A经加氨沉淀除镁后,溶液中的溶质可再生循环到_______ 工序使用。
(7)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如下图所示:

①该钒的硫化物的化学式是_______ 。
②该钒的硫化物的晶体中,与每个V原子最近且等距的S原子的个数是_______ 。
 、
、 、
、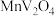 等)为原料制取金属钒的工艺流程如图所示:
等)为原料制取金属钒的工艺流程如图所示:
已知:①
 具有强氧化性,主要存在于pH<2的溶液中,pH>2时转化成酸式多钒酸盐。
具有强氧化性,主要存在于pH<2的溶液中,pH>2时转化成酸式多钒酸盐。②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
开始沉淀时 的pH 的pH | 1.9 | 7.0 | 8.1 | 8.9 |
沉淀完全时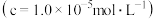 的pH 的pH | 3.2 | 9.0 | 10.1 | 10.9 |
(1)基态V原子的价电子轨道表示式为
(2)“焙烧Ⅰ”中
 (Fe为+2价)转化为
(Fe为+2价)转化为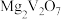 和
和 的化学方程式为
的化学方程式为(3)“酸浸”所得浸出液中除含有
 、
、 外,还含有的金属阳离子有
外,还含有的金属阳离子有(4)“沉钒”可得到
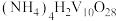 沉淀,“焙烧Ⅱ”中发生反应的化学方程式为
沉淀,“焙烧Ⅱ”中发生反应的化学方程式为(5)“沉钒”所得滤液中加入氨水调节溶液pH=x,过滤得到
 沉淀和溶液A,溶液A中
沉淀和溶液A,溶液A中 浓度为
浓度为 ,为尽可能多地回收
,为尽可能多地回收 ,并避免
,并避免 中混入
中混入 ,应控制x=
,应控制x=(6)溶液A经加氨沉淀除镁后,溶液中的溶质可再生循环到
(7)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如下图所示:

①该钒的硫化物的化学式是
②该钒的硫化物的晶体中,与每个V原子最近且等距的S原子的个数是
更新时间:2023-02-02 11:35:04
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体按如下图装置进行制取。
(1)已知装置B中的产物有ClO2气体,则装置B中反应的化学方程式为___________ ;装置D中反应生成NaClO2的化学方程式为________________________ ;
(2)装置B中反应后的溶液中阴离子除了ClO2﹣、ClO3﹣、Cl﹣、ClO﹣、OH﹣外还肯定含有的一种阴离子是________________ ;检验该离子的方法是________________________ ;
(3)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②__________ ;③用38℃~60℃热水洗涤;④低于60℃干燥;得到成品。
(4)如果撤去D中的冷水浴,可能导致产品中混有的杂质是________________________ ;
实验Ⅱ:样品杂质分析与纯度测定
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2﹣+4I﹣+4H+=2H2O+2I2+Cl﹣,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L﹣1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL
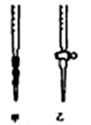
①用Na2S2O3标准溶液滴定时,应将Na2S2O3标准溶液注入________ (填“甲”或“乙”)中。
②观察Na2S2O3标准溶液滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致待测溶液浓度测定值___________ (选填“偏大”“偏小”或“无影响”)。
③(已知:I2+2S2O32﹣=2I﹣+S4O62﹣)。请计算所称取的样品中NaClO2的物质的量为________ 。
实验Ⅰ:制取NaClO2晶体按如下图装置进行制取。

(1)已知装置B中的产物有ClO2气体,则装置B中反应的化学方程式为
(2)装置B中反应后的溶液中阴离子除了ClO2﹣、ClO3﹣、Cl﹣、ClO﹣、OH﹣外还肯定含有的一种阴离子是
(3)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②
(4)如果撤去D中的冷水浴,可能导致产品中混有的杂质是
实验Ⅱ:样品杂质分析与纯度测定
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2﹣+4I﹣+4H+=2H2O+2I2+Cl﹣,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L﹣1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL
①用Na2S2O3标准溶液滴定时,应将Na2S2O3标准溶液注入
②观察Na2S2O3标准溶液滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致待测溶液浓度测定值
③(已知:I2+2S2O32﹣=2I﹣+S4O62﹣)。请计算所称取的样品中NaClO2的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】过氧化钙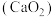 在水中能缓慢放出氧气,是一种用途广泛的供氧剂,可用于鱼塘养殖。
在水中能缓慢放出氧气,是一种用途广泛的供氧剂,可用于鱼塘养殖。
(1) 中所含化学键的类型是
中所含化学键的类型是___________ 、___________ 。
(2) 与水反应的化学方程式是
与水反应的化学方程式是___________ 。
(3)由电石渣(主要成分为氢氧化钙)制备过氧化钙可实现工业废渣的资源化,其制备流程如下:
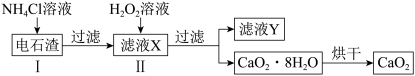
①滤液Y可循环使用,其主要溶质的质量与反应前的加入量几乎没有变化,该溶质是___________ 。解释其质量不变的原因:___________ (用化学方程式表示)。
②Ⅰ和Ⅱ的反应装置均需置于冰水浴中,解释Ⅱ中冰水浴的作用:___________ (答出一点即可)。
(4) 样品纯度测定
样品纯度测定
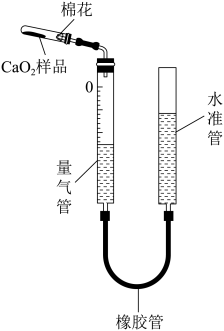
ⅰ.按上图连接装置(夹持和加热装置均略去),从水准管口加入适量水,并检查气密性;
ⅱ.准确称量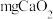 样品加入试管,并使其在试管底部均匀铺成薄层;
样品加入试管,并使其在试管底部均匀铺成薄层;
ⅲ.上下移动水准管,使水准管中液面与量气管中液面平齐;读取量气管中液面对应的刻度,记为 ;
;
ⅳ.加热发生反应: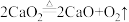 ,充分反应至不再有气体产生,停止加热,___________;再次读取量气管中液面对应的刻度,记为
,充分反应至不再有气体产生,停止加热,___________;再次读取量气管中液面对应的刻度,记为 ;
;
Ⅴ.计算样品中 的纯度。
的纯度。
①补全ⅳ中操作:___________ 。
②该实验条件下,气体摩尔体积为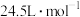 ,样品中
,样品中 的纯度为
的纯度为___________ (用质量分数表示)。
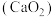 在水中能缓慢放出氧气,是一种用途广泛的供氧剂,可用于鱼塘养殖。
在水中能缓慢放出氧气,是一种用途广泛的供氧剂,可用于鱼塘养殖。(1)
 中所含化学键的类型是
中所含化学键的类型是(2)
 与水反应的化学方程式是
与水反应的化学方程式是(3)由电石渣(主要成分为氢氧化钙)制备过氧化钙可实现工业废渣的资源化,其制备流程如下:

①滤液Y可循环使用,其主要溶质的质量与反应前的加入量几乎没有变化,该溶质是
②Ⅰ和Ⅱ的反应装置均需置于冰水浴中,解释Ⅱ中冰水浴的作用:
(4)
 样品纯度测定
样品纯度测定
ⅰ.按上图连接装置(夹持和加热装置均略去),从水准管口加入适量水,并检查气密性;
ⅱ.准确称量
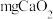 样品加入试管,并使其在试管底部均匀铺成薄层;
样品加入试管,并使其在试管底部均匀铺成薄层;ⅲ.上下移动水准管,使水准管中液面与量气管中液面平齐;读取量气管中液面对应的刻度,记为
 ;
;ⅳ.加热发生反应:
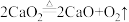 ,充分反应至不再有气体产生,停止加热,___________;再次读取量气管中液面对应的刻度,记为
,充分反应至不再有气体产生,停止加热,___________;再次读取量气管中液面对应的刻度,记为 ;
;Ⅴ.计算样品中
 的纯度。
的纯度。①补全ⅳ中操作:
②该实验条件下,气体摩尔体积为
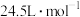 ,样品中
,样品中 的纯度为
的纯度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】钼和钨同属第ⅤIB族元素,性质有一定的相似性,在自然界中常形成共生矿。某钼钨矿的主要成分为RWO4、RMoO4(其中R为Fe、Mn等),同时还含有少量SiO2。工业上由钼钨矿冶炼金属钼和钨并获取副产物,流程如图所示。(已知常温下,钨酸是难溶于水的弱酸)

请回答下列问题:
(1)焙烧所得固体物质的主要成分除了Fe2O3、MnO2、Na2WO4、Na2MoO4外,还有______ 。
(2)MnMoO4在焙烧条件下与纯碱、空气反应的化学方程式为:_____ 。
(3)“沉钼”过程中,加入Na2S固体太多,可能的后果是:_____ 。
(4)“沉钨”过程中,判断钨酸已完全沉淀的方法是_____ 。
(5)若在实验室中进行“操作1”,用到的玻璃仪器除烧杯外,还有_____ ,若滤渣1用稀盐酸浸泡,则固体A主要成分的化学式为_____ 。
(6)MnO2与硫酸、草酸(H2C2O4)溶液反应的离子方程式为_____ 。

请回答下列问题:
(1)焙烧所得固体物质的主要成分除了Fe2O3、MnO2、Na2WO4、Na2MoO4外,还有
(2)MnMoO4在焙烧条件下与纯碱、空气反应的化学方程式为:
(3)“沉钼”过程中,加入Na2S固体太多,可能的后果是:
(4)“沉钨”过程中,判断钨酸已完全沉淀的方法是
(5)若在实验室中进行“操作1”,用到的玻璃仪器除烧杯外,还有
(6)MnO2与硫酸、草酸(H2C2O4)溶液反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】电子工业中,可用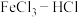 溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
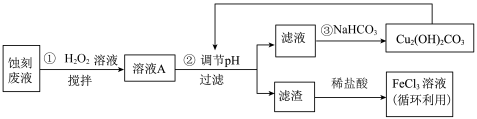
回答下列问题:
(1)把 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是___________ 。(填写化学式)
(2) 蚀刻液中加入盐酸的目的是
蚀刻液中加入盐酸的目的是___________ 。
(3)步骤①中加入 溶液的目的是(用离子方程式表示)
溶液的目的是(用离子方程式表示)___________ 。
(4)已知:生成氢氧化物沉淀的 如下表。
如下表。
根据表中数据推测调节 的范围是
的范围是___________ 。
(5)上述流程路线中,除 溶液外,还可用于循环利用的物质是
溶液外,还可用于循环利用的物质是___________ 。
(6)在 ,向浓度均为
,向浓度均为 的
的 溶液中逐滴加入氨水,若镁离子浓度为
溶液中逐滴加入氨水,若镁离子浓度为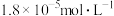 时溶液的
时溶液的 为
为___________ 。(已知 时
时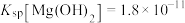 )。
)。
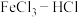 溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
回答下列问题:
(1)把
 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是(2)
 蚀刻液中加入盐酸的目的是
蚀刻液中加入盐酸的目的是(3)步骤①中加入
 溶液的目的是(用离子方程式表示)
溶液的目的是(用离子方程式表示)(4)已知:生成氢氧化物沉淀的
 如下表。
如下表。| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.2 |
 的范围是
的范围是(5)上述流程路线中,除
 溶液外,还可用于循环利用的物质是
溶液外,还可用于循环利用的物质是(6)在
 ,向浓度均为
,向浓度均为 的
的 溶液中逐滴加入氨水,若镁离子浓度为
溶液中逐滴加入氨水,若镁离子浓度为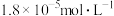 时溶液的
时溶液的 为
为 时
时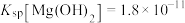 )。
)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
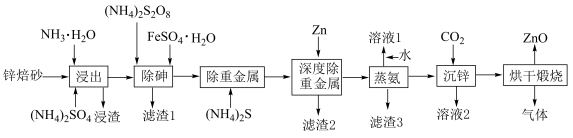
【推荐2】氧化锌是一种功能材料。利用锌焙砂(主要成分为ZnO,含As2O3及铅、铜、镉的氧化物)生产高纯氧化锌的工业流程如图所示。
② 中存在一个过氧键(—O—O—)
中存在一个过氧键(—O—O—)
③常温下,相关硫化物的 如下表所示。
如下表所示。
回答下列问题:
(1)“浸出”时生成 的离子方程式为
的离子方程式为____________________ 。
(2)“除砷”过程中,需加入过量的 ,其中S的化合价为
,其中S的化合价为______ 。滤渣1的主要成分是______ (填化学式)。
(3)“除重金属”过程中,涉及的部分反应为:
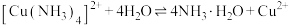

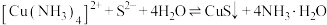
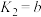
 的加入量[
的加入量[ ]对锌的回收率及溶液中铜锌比[
]对锌的回收率及溶液中铜锌比[ ]的影响如图所示。
]的影响如图所示。 、
、 对应的数值,则a、b之间存在的等式关系是
对应的数值,则a、b之间存在的等式关系是______ 。
② 较为合理的加入量约为120%。当
较为合理的加入量约为120%。当 加入量超过100%时,锌的回收率下降的原因可能是
加入量超过100%时,锌的回收率下降的原因可能是______ (用离子方程式表示)。
③“除重金属”后,测得溶液中 为
为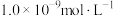 ,此时
,此时 是否完全沉淀
是否完全沉淀______ (填“是”或“否”)。
(4)“蒸氨”后,锌元素以 存在,写出CO2“沉锌”的化学方程式
存在,写出CO2“沉锌”的化学方程式______ 。
(5)流程中可循环利用的物质有______ (填化学式)。
②
 中存在一个过氧键(—O—O—)
中存在一个过氧键(—O—O—)③常温下,相关硫化物的
 如下表所示。
如下表所示。物质 | ZnS | CdS | PbS | CuS |
|
|
|
|
|
(1)“浸出”时生成
 的离子方程式为
的离子方程式为(2)“除砷”过程中,需加入过量的
 ,其中S的化合价为
,其中S的化合价为(3)“除重金属”过程中,涉及的部分反应为:
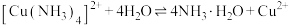

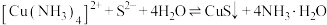
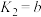
 的加入量[
的加入量[ ]对锌的回收率及溶液中铜锌比[
]对锌的回收率及溶液中铜锌比[ ]的影响如图所示。
]的影响如图所示。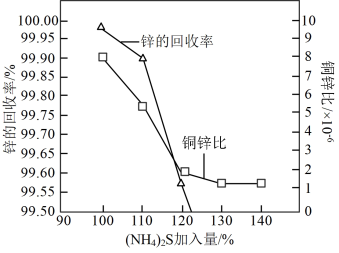
 、
、 对应的数值,则a、b之间存在的等式关系是
对应的数值,则a、b之间存在的等式关系是②
 较为合理的加入量约为120%。当
较为合理的加入量约为120%。当 加入量超过100%时,锌的回收率下降的原因可能是
加入量超过100%时,锌的回收率下降的原因可能是③“除重金属”后,测得溶液中
 为
为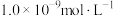 ,此时
,此时 是否完全沉淀
是否完全沉淀(4)“蒸氨”后,锌元素以
 存在,写出CO2“沉锌”的化学方程式
存在,写出CO2“沉锌”的化学方程式(5)流程中可循环利用的物质有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】一种工业上利用废旧三元锂离子电池正极材料(主要成分为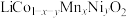 ,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示:
,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示: 的溶解度随温度升高而减小;
的溶解度随温度升高而减小;
②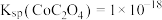 ,
,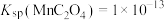 ,
,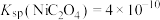 。
。
回答下列问题:
(1)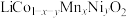 中
中 、
、 元素的化合价分别为+2价、+3价,若
元素的化合价分别为+2价、+3价,若 ,则
,则 元素的化合价为
元素的化合价为___________ 。锂离子电池中的电解质 与水相遇会生成
与水相遇会生成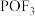 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“酸浸”时,下列试剂中最适宜替换 的是
的是___________ 。
a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.浓盐酸
溶液 d.浓盐酸
(3)若“酸浸”后溶液中 、
、 、
、 浓度均为
浓度均为 ,欲使
,欲使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而不沉淀
)而不沉淀 、
、 ,理论上需调节溶液
,理论上需调节溶液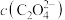 范围为
范围为___________ ;实际“沉钴”时,在加入 之后溶液中
之后溶液中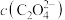 超出
超出 完全沉淀所需浓度,须先加入一定量氨水,所加氨水的作用为
完全沉淀所需浓度,须先加入一定量氨水,所加氨水的作用为___________ 。
(4)“沉锰”过程中加入 溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,紫红色褪去的原因为
溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,紫红色褪去的原因为___________ (用离子方程式表示)。
(5)“沉锂”操作中需将温度升高到 ,原因是:①加快反应速率;②
,原因是:①加快反应速率;②___________ 。
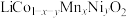 ,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示:
,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示: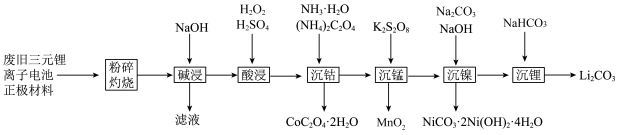
 的溶解度随温度升高而减小;
的溶解度随温度升高而减小;②
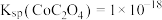 ,
,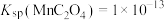 ,
,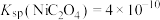 。
。回答下列问题:
(1)
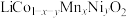 中
中 、
、 元素的化合价分别为+2价、+3价,若
元素的化合价分别为+2价、+3价,若 ,则
,则 元素的化合价为
元素的化合价为 与水相遇会生成
与水相遇会生成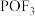 ,该反应的化学方程式为
,该反应的化学方程式为(2)“酸浸”时,下列试剂中最适宜替换
 的是
的是a.
 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.浓盐酸
溶液 d.浓盐酸(3)若“酸浸”后溶液中
 、
、 、
、 浓度均为
浓度均为 ,欲使
,欲使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而不沉淀
)而不沉淀 、
、 ,理论上需调节溶液
,理论上需调节溶液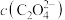 范围为
范围为 之后溶液中
之后溶液中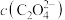 超出
超出 完全沉淀所需浓度,须先加入一定量氨水,所加氨水的作用为
完全沉淀所需浓度,须先加入一定量氨水,所加氨水的作用为(4)“沉锰”过程中加入
 溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,紫红色褪去的原因为
溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,紫红色褪去的原因为(5)“沉锂”操作中需将温度升高到
 ,原因是:①加快反应速率;②
,原因是:①加快反应速率;②
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】Ⅰ.Fe3+可以与SCN-、CN-、F-、有机分子等形成很多的配合物。请回答下列问题:
(1)基态Fe3+的电子排布式可表示为__________________ 。
(2)与CN-互为等电子体的分子有___________ (写出2种)。
(3)金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=_____ 。
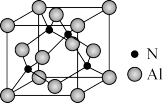
Ⅱ.已知氮化铝的晶胞结构如图所示。请回答下列问题:
(4)下列说法正确的是__________ (填序号)。
(5)NH3空间构型为______ ;已知(CH3)3Al为非极性分子,则其中铝原子的杂化方式为__________ 。
(6)若氮化铝可由(CH3)3Al和NH3在一定条件下反应制得,则反应的方程式为_________ 。
(7)若Al与N 原子最近的距离为a cm,则该晶体的密度为____ g/cm。(阿伏加德罗常数用NA表示)
(1)基态Fe3+的电子排布式可表示为
(2)与CN-互为等电子体的分子有
(3)金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=
Ⅱ.已知氮化铝的晶胞结构如图所示。请回答下列问题:

(4)下列说法正确的是
| A.氮化铝晶胞结构与NaCl相同 | B.第一电离能 N>Al |
| C.电负性N>Al | D.原子半径 N>Al |
(6)若氮化铝可由(CH3)3Al和NH3在一定条件下反应制得,则反应的方程式为
(7)若Al与N 原子最近的距离为a cm,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】W、X、Y、Z(W、X、Y、Z分别代表元素符号)均为元素周期表中前四周期的元素,其原子序数依次增大,其中W、X、Y、Z为短周期元素,它们的单质在通常情况下均为无色气体。X元素的基态原子在同周期元素基态原子中含有的未成对电子数最多,Y元素的基态原子中s能级上的电子数等于p能级上的电子数,Z为金属元素,其基态原子是具有4s1结构的基态原子中质子数最多的原子,试回答下列问题:
(1)写出X的基态原子的价电子排布式_________________ ;
(2)比较X、Y两元素基态原子的第一电离能大小:X__________ Y(填“>”、“<”或“=”),理由是________ ;
(3)W、X两元素能写出一种常见气体M,每个M分子中含有10个电子,M分子中心原子的杂化方式为_________ ;WX两种元素还能写出一种常见阳离子N,每个N中也含有10个电子,但在N与M中所含化学键的键角大小不同,其原因是__________ ;
(4)Z2+可与M分子在谁溶液中形成[Z(M)4]2+,其中M分子和Z2+通过__________ -结合;
(5)单质Z的警报结构如图所示,已知两个最近的Z原子距离为a,Z的相对原子质量用Mr表示,则该晶体密度为_______________ (只列计算式)。
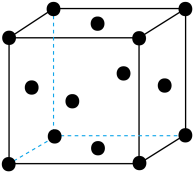
(1)写出X的基态原子的价电子排布式
(2)比较X、Y两元素基态原子的第一电离能大小:X
(3)W、X两元素能写出一种常见气体M,每个M分子中含有10个电子,M分子中心原子的杂化方式为
(4)Z2+可与M分子在谁溶液中形成[Z(M)4]2+,其中M分子和Z2+通过
(5)单质Z的警报结构如图所示,已知两个最近的Z原子距离为a,Z的相对原子质量用Mr表示,则该晶体密度为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】利用炼锌钴渣[主要含Co(OH)2、FeSO4、NiSO4和Zn、Cu单质]协同制备Co(OH)3和高纯Zn的流程如下。___________ 。
(2)“沉铁”过程CaCO3的作用有___________ 。
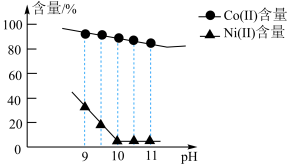
(3)“沉镍”过程pH对溶液中Co(Ⅱ)、Ni(Ⅱ)含量的影响如图。___________ 。
②该过程Co可能发生的反应如下:
Co2++6NH3·H2O=[Co(NH3)6]2++6H2O K1=105
Co2++2NH3·H2O=Co(OH)2↓+2 K2
K2
则K2=___________ ,[Co(NH3)6]2+为___________ (填“热力学”或“动力学”)产物。
(已知:25℃时,Kb(NH3·H2O)=10-4.8,Ksp[Co(OH)2]=10-15)
(4)“沉钴”过程生成Co(OH)3的离子方程式为___________ 。
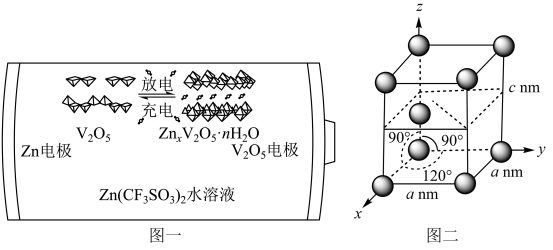
(5)一种以Zn和V2O5为电极、Zn(CF3SO3)2水溶液为电解质的电池,其示意图如下图一所示。放电时,Zn2+可插入V2O5层间形成ZnxV2O5·nH2O。___________ 。
②上述电池充电时阳极的电极反应式为___________ 。
③金属Zn的晶胞如图二,密度为ρg/cm3,则阿伏加德罗常数NA=___________ (列代数式即可,下同),晶胞空间占有率为___________ 。

(2)“沉铁”过程CaCO3的作用有
(3)“沉镍”过程pH对溶液中Co(Ⅱ)、Ni(Ⅱ)含量的影响如图。
②该过程Co可能发生的反应如下:
Co2++6NH3·H2O=[Co(NH3)6]2++6H2O K1=105
Co2++2NH3·H2O=Co(OH)2↓+2
 K2
K2则K2=
(已知:25℃时,Kb(NH3·H2O)=10-4.8,Ksp[Co(OH)2]=10-15)
(4)“沉钴”过程生成Co(OH)3的离子方程式为
(5)一种以Zn和V2O5为电极、Zn(CF3SO3)2水溶液为电解质的电池,其示意图如下图一所示。放电时,Zn2+可插入V2O5层间形成ZnxV2O5·nH2O。
②上述电池充电时阳极的电极反应式为
③金属Zn的晶胞如图二,密度为ρg/cm3,则阿伏加德罗常数NA=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】“钢是虎,钒是翼,钢含钒犹如虎添翼”,金属钒被誉为“合金的维生素”。从废钒(主要成分为V2O5、Fe2O3、SiO2等)中回收V2O5的一种工艺流程如下图所示: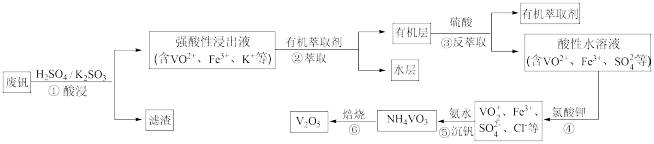
已知:步骤②、③中的变化过程可简化为:Rn+(水层)+nHA(有机层)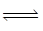 RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。
RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。
回答下列问题:
(1)步骤①酸浸过程中发生氧化还原反应的化学方程式为______________ 。
(2)萃取时应加入适量碱的作用是___________________ 。
(3)步骤④中反应的离子方程式为___________________ 。
(4)步骤⑤25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
通过表中数据分析,在实际生产中,⑤中加入氨水,调节溶液的最佳pH范围为______ ;
若加入氨水调节溶液pH=2,钒沉淀率达到93%且不产生Fe(OH)3沉淀,则此时溶液中c(Fe3+)<_____ mol/L(按25℃计算,25℃时Ksp[Fe(OH)3]=2.6×10-39)。
(5)V2O5是两性氧化物,在强酸性溶液中以VO2+形式存在,VO2+具有强氧化性,能将I-氧化为I2,本身被还原为VO+,则V2O5与氢碘酸反应的离子方程式为_________________ 。
(6)为提高钒的回收率,步骤②和③需多次进行,假设酸浸所得“强酸性浸出液”中c(VO2+)=amol/L,步骤②和③每进行一次,VO2+萃取率为80%,4次操作后,“强酸性浸出液中”c(VO2+)=_______ mol/L(萃取率=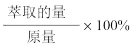 )
)

已知:步骤②、③中的变化过程可简化为:Rn+(水层)+nHA(有机层)
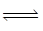 RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。
RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。回答下列问题:
(1)步骤①酸浸过程中发生氧化还原反应的化学方程式为
(2)萃取时应加入适量碱的作用是
(3)步骤④中反应的离子方程式为
(4)步骤⑤25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
若加入氨水调节溶液pH=2,钒沉淀率达到93%且不产生Fe(OH)3沉淀,则此时溶液中c(Fe3+)<
(5)V2O5是两性氧化物,在强酸性溶液中以VO2+形式存在,VO2+具有强氧化性,能将I-氧化为I2,本身被还原为VO+,则V2O5与氢碘酸反应的离子方程式为
(6)为提高钒的回收率,步骤②和③需多次进行,假设酸浸所得“强酸性浸出液”中c(VO2+)=amol/L,步骤②和③每进行一次,VO2+萃取率为80%,4次操作后,“强酸性浸出液中”c(VO2+)=
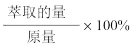 )
)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】某工业废料的主要成分有 、
、 、
、 、
、 、
、 等,现欲利用以下工艺流程回收混合物中的金属化合物(部分条件未给出):
等,现欲利用以下工艺流程回收混合物中的金属化合物(部分条件未给出):

已知:常温下,部分阳离子沉淀时的pH
回答下列问题:
(1)“混合研磨”的目的为:_____ ,“滤渣1”的主要成分为:_____ 。
(2) 有氧化性,请写出“酸溶”时绿矾发生反应的离子方程式:
有氧化性,请写出“酸溶”时绿矾发生反应的离子方程式:_____ 。
(3)“氧化、调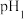 ”时若不加
”时若不加 ,可能造成的后果为:
,可能造成的后果为:_____ ,也可用 代替,此时环境酸性
代替,此时环境酸性 转化为
转化为 ,请写出反应的离子方程式:
,请写出反应的离子方程式:_____ 。
(4)“调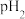 ”的范围为
”的范围为_____ 。
(5)“沉锰”时的离子方程式为:_____ 。
(6)请说出“沉锰”后的滤液主要成分在生活中的用途:_____ 。
 、
、 、
、 、
、 、
、 等,现欲利用以下工艺流程回收混合物中的金属化合物(部分条件未给出):
等,现欲利用以下工艺流程回收混合物中的金属化合物(部分条件未给出):
已知:常温下,部分阳离子沉淀时的pH
 |  |  |  | |
| 开始沉淀 | 3.9 | 2.2 | 6.9 | 8.6 |
| 沉淀完全 | 4.7 | 3.2 | 8.3 | 10.6 |
(1)“混合研磨”的目的为:
(2)
 有氧化性,请写出“酸溶”时绿矾发生反应的离子方程式:
有氧化性,请写出“酸溶”时绿矾发生反应的离子方程式:(3)“氧化、调
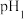 ”时若不加
”时若不加 ,可能造成的后果为:
,可能造成的后果为: 代替,此时环境酸性
代替,此时环境酸性 转化为
转化为 ,请写出反应的离子方程式:
,请写出反应的离子方程式:(4)“调
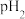 ”的范围为
”的范围为(5)“沉锰”时的离子方程式为:
(6)请说出“沉锰”后的滤液主要成分在生活中的用途:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】辛烯醛是重要化工原料,某小组拟用正丁醛制备辛烯醛并探究其结构。
[制备实验]
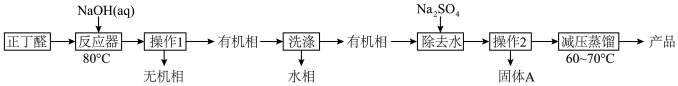
已知:①正丁醛的沸点为75.7℃。辛烯醛沸点为177℃,密度为0.848 g·cm-3,不溶于水。
②CH3CH2CH2CHO
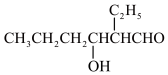

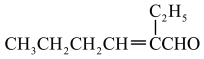
(1)在如图1三颈瓶中加入12.6 mL 2% NaOH溶液,在充分搅拌下,从恒压滴液漏斗慢慢滴入10 mL正丁醛。最适宜的加热方式是___________ ;使用冷凝管的目的是____________ 。
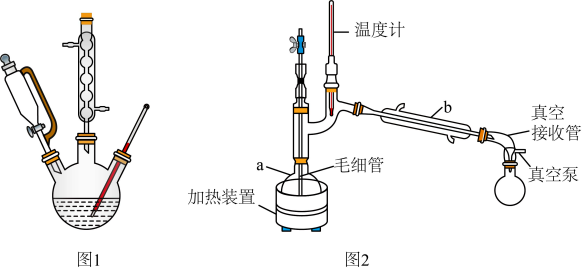
(2)操作1中使用的主要仪器名称是___________ ,有机相从___________ (填“上”或“下”)口取出。
(3)判断有机相已洗涤至中性的操作方法:___________ 。
(4)操作2的名称是_____________ ;固体A的摩尔质量为322 g·mol-1,固体A的化学式为___________ 。
(5)利用图2装置进行“减压蒸馏”。下列有关说法错误的是___________ 。(填选项)
A 温度计示数为177℃,指示馏分温度
B 随着温度计液泡高度的提升,所得液体的沸点升高
C 毛细管的作用和沸石相似,防止液体暴沸
D 实验结束后,应先关闭冷凝水,再关闭真空泵
[性质实验]
资料显示:醛类(RCHO)在常温下能与溴水、酸性高锰酸钾溶液反应;在加热条件下能与银氨溶液、新制氢氧化铜浊液反应。
(6)为了证明辛烯醛含有碳碳双键,设计如下方案,能达到实验目的的是________ 。(填选项)
a 取少量溴水,滴加辛烯醛,振荡,溶液褪色
b 取少量酸性高锰酸钾溶液,滴加辛烯醛,振荡,溶液褪色
c 取少量辛烯醛,加入足量的银氨溶液,水浴加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
d 取少量辛烯醛,加入足量的新制Cu(OH)2浊液,加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
[制备实验]

已知:①正丁醛的沸点为75.7℃。辛烯醛沸点为177℃,密度为0.848 g·cm-3,不溶于水。
②CH3CH2CH2CHO

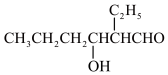

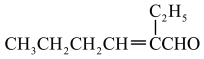
(1)在如图1三颈瓶中加入12.6 mL 2% NaOH溶液,在充分搅拌下,从恒压滴液漏斗慢慢滴入10 mL正丁醛。最适宜的加热方式是

(2)操作1中使用的主要仪器名称是
(3)判断有机相已洗涤至中性的操作方法:
(4)操作2的名称是
(5)利用图2装置进行“减压蒸馏”。下列有关说法错误的是
A 温度计示数为177℃,指示馏分温度
B 随着温度计液泡高度的提升,所得液体的沸点升高
C 毛细管的作用和沸石相似,防止液体暴沸
D 实验结束后,应先关闭冷凝水,再关闭真空泵
[性质实验]
资料显示:醛类(RCHO)在常温下能与溴水、酸性高锰酸钾溶液反应;在加热条件下能与银氨溶液、新制氢氧化铜浊液反应。
(6)为了证明辛烯醛含有碳碳双键,设计如下方案,能达到实验目的的是
a 取少量溴水,滴加辛烯醛,振荡,溶液褪色
b 取少量酸性高锰酸钾溶液,滴加辛烯醛,振荡,溶液褪色
c 取少量辛烯醛,加入足量的银氨溶液,水浴加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
d 取少量辛烯醛,加入足量的新制Cu(OH)2浊液,加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
您最近一年使用:0次