下列叙述与图对应的是
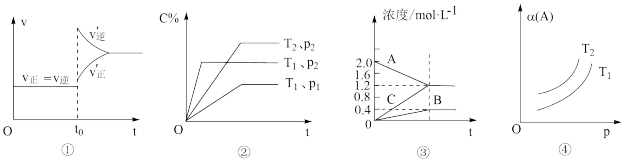

A.已达平衡状态的反应:N2(g)+3H2(g)  2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 |
B.由图②可知,P2>P1、T1>T2满足反应:2A(g)+B(g)  2C(g) ΔH<0 2C(g) ΔH<0 |
| C.图③表示的反应方程式为:2A(g)=B(g)+3C(g) |
D.由图④可知,对于反应aA(g) bB(g)+cC(g),该反应用于工业生产时,采用的压强越大越好 bB(g)+cC(g),该反应用于工业生产时,采用的压强越大越好 |
更新时间:2023-02-02 20:23:47
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】已知某可逆反应在密闭容器中进行:A(g)+2B(g) 3C(g)+D(s) ΔH<0,如图中曲线a、b代表一定条件下该反应的进程。若使b曲线变为曲线a,可采取的措施是
3C(g)+D(s) ΔH<0,如图中曲线a、b代表一定条件下该反应的进程。若使b曲线变为曲线a,可采取的措施是
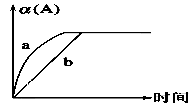
①增大A的浓度 ②缩小容器的容积 ③增大B的浓度 ④增大容器的容积 ⑤加入合适正催化剂
 3C(g)+D(s) ΔH<0,如图中曲线a、b代表一定条件下该反应的进程。若使b曲线变为曲线a,可采取的措施是
3C(g)+D(s) ΔH<0,如图中曲线a、b代表一定条件下该反应的进程。若使b曲线变为曲线a,可采取的措施是 
①增大A的浓度 ②缩小容器的容积 ③增大B的浓度 ④增大容器的容积 ⑤加入合适正催化剂
| A.① | B.②⑤ | C.④ | D.②③ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2NO2(g)  N2O4(g) ΔH = -QkJ·mol-1(Q>0),测得反应的相关数据如下,下列说法正确的是
N2O4(g) ΔH = -QkJ·mol-1(Q>0),测得反应的相关数据如下,下列说法正确的是
 N2O4(g) ΔH = -QkJ·mol-1(Q>0),测得反应的相关数据如下,下列说法正确的是
N2O4(g) ΔH = -QkJ·mol-1(Q>0),测得反应的相关数据如下,下列说法正确的是| 甲 | 乙 | 丙 | |
| 应温度T/K | 500 | 500 | 700 |
| 反应物投入量 | 2molNO2 | 2mol N2O4 | 1 mol N2O4 |
| 平衡v正(NO2)/mol·L-1·S-1 | v1 | v2 | v3 |
| 平衡c(N2O4)/mol·L-1 | c1 | c2 | c3 |
| 平衡体系系总压强p/Pa | p1 | p2 | p3 |
| 反应能量变化 | 放出xkJ | 吸收ykJ | 吸收zkJ |
| 物质的平衡转化率α | α1(NO2) | α2(N2O4) | α3(N2O4) |
| 平衡常数K | K1 | K2 | K3 |
| A.K1> K3,p2>2p3 | B.v1< v3,x+0.5y=Q |
| C.v1< v2,c2<2c1 | D.c2>2c3,α1(NO2)+ α3(N2O4)>1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】二氧化碳催化加氢可合成乙烯:
 。当原料初始组成
。当原料初始组成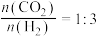 ,体系压强为
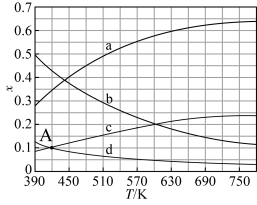
,体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是

 。当原料初始组成
。当原料初始组成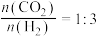 ,体系压强为
,体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是
A.该反应的 |
B.表示 、 、 变化的曲线分别为c、d 变化的曲线分别为c、d |
C.A点对应温度为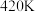 ,此时 ,此时 的转化率为66.7% 的转化率为66.7% |
| D.选择合适的催化剂可提高反应速率和乙烯的平衡产率 |
您最近一年使用:0次
【推荐2】一定温度下,在三个容积均为1.0L的恒容密闭容器中发生反应:CH3OH(g)+CO(g) CH3COOH(g) △H< 0。下列说法不正确的是
CH3COOH(g) △H< 0。下列说法不正确的是
 CH3COOH(g) △H< 0。下列说法不正确的是
CH3COOH(g) △H< 0。下列说法不正确的是| 容器编号 | 温度(K) | 起始物质的量(mol) | 平衡时CH3COOH的物质的量(mol) | 平衡常数 | ||
| n(CH3OH) | n (CO) | n (CH3COOH) | ||||
| Ⅰ | 530 | 0.05 | 0.05 | 0 | 0.025 | K1 |
| Ⅱ | 530 | 0.03 | 0.03 | 0.006 | K2 | |
| Ⅲ | 510 | 0 | 0 | 0.05 | K3 | |
| A.达平衡时,容器Ⅰ中平衡常数K1 =40 |
| B.达平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小 |
| C.达平街时,容器Ⅰ中CH3OH转化率与容器Ⅲ中CH3COOH转化率之和小于1 |
| D.K1>K2>K3 |
您最近一年使用:0次
【推荐1】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s) ⇌2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列见表,下列说法错误的是
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3 mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增大 |
| B.当混合气体平均相对分子质量为26时说明该反应已达平衡 |
| C.根据表中数据,计算25.0 ℃时分解的浓度平衡常数约为1.6×10-8 mol3/L3 |
| D.若保持温度和容器体积不变,平衡后再充入n(NH3)∶n(CO2)=2∶1,则再次达到平衡时c(NH3)不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】以CO2、H2为原料合成CH3OH涉及的主要反应如下:
①

②

CO2的平衡转化率(X-CO2)、的选择(S-CH3OH)随温度、压强变化如下:
下列叙述正确的是
①


②


CO2的平衡转化率(X-CO2)、的选择(S-CH3OH)随温度、压强变化如下:


下列叙述正确的是
A.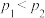 |
| B.400℃左右,体系发生的反应主要是反应① |
C.由图可知, , , |
D.起始 、 、 ,平衡后 ,平衡后 , , ,若只发生反应①、②,则 ,若只发生反应①、②,则 的平衡转化率为25% 的平衡转化率为25% |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】在相同温度相同体积的甲、乙两密闭容器中,分别充入1molN2和3molH2,甲保持恒温恒压,乙保持恒温恒容,发生反应:N2(g) + 3H2(g)⇌2NH3(g) ΔH<0。下列说法错误的是
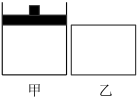

| A.甲容器中反应达到平衡时,再向容器内充入1 mol 稀有气体,平衡逆向移动 |
| B.两容器内的反应达到化学平衡状态所需时间: t甲>t乙 |
| C.当甲中N2的平衡转化率为10%时,乙中N2的转化率小于10% |
| D.乙容器中反应达到平衡时,再向容器内充入1 mol N2,则平衡正向移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】我国科学家用下列实验研究硫酸盐会加剧雾霾的原因:以N2或空气为载气,将SO2和NO2按一定比例混合,通入不同吸收液,相同时间后,检测吸收液中的 含量,数据如下:
含量,数据如下:
下列说法正确的是
 含量,数据如下:
含量,数据如下:| 反应 | 载气 | 吸收液 |  含量 含量 | 数据分析 |
| ① | N2 | 蒸馏水 | a | i. ii.若起始不通入NO2,则最终检测不到  |
| ② | 3%氨水 | b | ||
| ③ | 空气 | 蒸馏水 | c | |
| ④ | 3%氨水 | d |
| A.SO2和NO2都属于酸性氧化物 |
| B.反应①中还原产物可能是HNO2 |
C.产生 的反应中NO2既是氧化剂,又是还原剂 的反应中NO2既是氧化剂,又是还原剂 |
| D.实验表明硫酸盐的形成主要与空气中的O2有关 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害。某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示。下列判断不正确的是
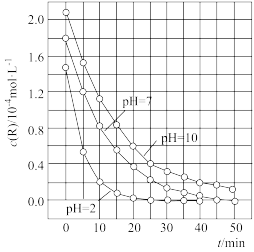

| A.在0~20min之间,pH=7时R的降解速率为7×10-6mol·L-1·min-1 |
| B.R的起始浓度不同,无法判断溶液的酸碱性对R的降解速率的影响 |
| C.在这三种pH条件下,二氧化钛对pH=2的R溶液催化降解效率最好 |
| D.在0~50 min之间,R的降解百分率pH=2等于pH=7 |
您最近一年使用:0次

 2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验: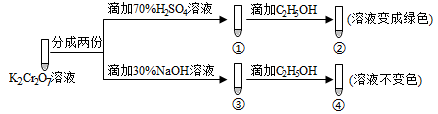
 ,发生反应
,发生反应 。
。


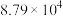

 如
如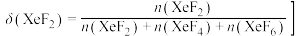 随温度的变化如图。下列说法不正确的是
随温度的变化如图。下列说法不正确的是
 与
与 的投料比为1:1时,平衡转化率:
的投料比为1:1时,平衡转化率: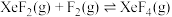 正向移动
正向移动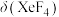 在
在 后减小的原因是反应ⅱ逆向移动的程度较大
后减小的原因是反应ⅱ逆向移动的程度较大 ),每2个
),每2个 参与反应机理如图所示,其中吸附在催化剂表面上的物种用*标注,下列说法错误的是
参与反应机理如图所示,其中吸附在催化剂表面上的物种用*标注,下列说法错误的是




 降低反应的活化能,提高化学反应速率
降低反应的活化能,提高化学反应速率

