在相同温度相同体积的甲、乙两密闭容器中,分别充入1molN2和3molH2,甲保持恒温恒压,乙保持恒温恒容,发生反应:N2(g) + 3H2(g)⇌2NH3(g) ΔH<0。下列说法错误的是
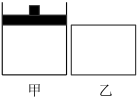

| A.甲容器中反应达到平衡时,再向容器内充入1 mol 稀有气体,平衡逆向移动 |
| B.两容器内的反应达到化学平衡状态所需时间: t甲>t乙 |
| C.当甲中N2的平衡转化率为10%时,乙中N2的转化率小于10% |
| D.乙容器中反应达到平衡时,再向容器内充入1 mol N2,则平衡正向移动 |
更新时间:2020-11-07 17:25:40
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
| A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.活化分子间所发生的碰撞为有效碰撞 |
| D.升高温度能使化学反应速率增大的主要原因是增加了反应物中活化分子的百分数 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】利用传感技术可探究压强对化学平衡 的影响。往注射器中充入适量
的影响。往注射器中充入适量 气体保持活塞位置不变达到平衡(图甲);恒定温度下,分别在
气体保持活塞位置不变达到平衡(图甲);恒定温度下,分别在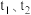 时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化如图乙。下列说法错误的是
时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化如图乙。下列说法错误的是
 的影响。往注射器中充入适量
的影响。往注射器中充入适量 气体保持活塞位置不变达到平衡(图甲);恒定温度下,分别在
气体保持活塞位置不变达到平衡(图甲);恒定温度下,分别在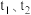 时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化如图乙。下列说法错误的是
时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化如图乙。下列说法错误的是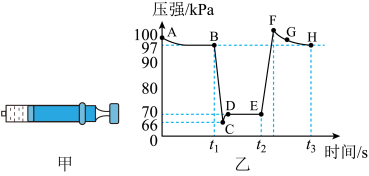
A. 两点对应的反应速率: 两点对应的反应速率: |
B.B点对应的分压平衡常数为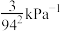 |
| C.C点到D点平衡逆向移动,针筒内气体颜色D点比B点深 |
D.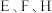 三点中, 三点中, 点的气体平均相对分子质量最大 点的气体平均相对分子质量最大 |
您最近一年使用:0次
【推荐3】下列装置图或曲线图与对应的叙述相符的是( )
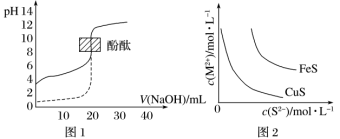



| A.如图1所示,用0.1 mol/L NaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 |
| B.某温度下FeS、CuS的沉淀溶解平衡曲线如图2所示,纵坐标c(M2+)代表Fe2+或Cu2+的浓度,横坐标c(S2-)代表S2-的浓度。在物质的量浓度相等的Fe2+和Cu2+的溶液中滴加硫化钠溶液,首先沉淀的离子为Fe2+ |
| C.图3表示N2(g)+3H2(g)⇌2NH3(g)的v逆随时间变化曲线,由图知t1时刻可能减小了容器内的压强 |
| D.图4表示温度为T℃,体积不等的恒容密闭容器中发生反应: 2C(s)+2NO2(g)⇌N2(g)+2CO2(g),相同时间测得各容器中NO2的转化率与容器体积的关系,图中c点所示条件下,v正=v逆 |
您最近一年使用:0次
单选题
|
较难
(0.4)
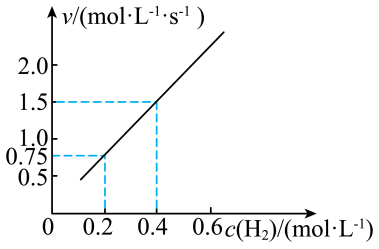
【推荐1】在恒温恒容密闭容器中发生反应2H2(g)+2NO(g) 2H2O(g)+N2(g),N2的瞬时生成速率v=k·cm(H2)·c2(NO)。控制NO起始浓度为0.5mol•L-1,N2的瞬时生成速率和H2起始浓度的关系如图所示,下列说法正确的是
2H2O(g)+N2(g),N2的瞬时生成速率v=k·cm(H2)·c2(NO)。控制NO起始浓度为0.5mol•L-1,N2的瞬时生成速率和H2起始浓度的关系如图所示,下列说法正确的是
 2H2O(g)+N2(g),N2的瞬时生成速率v=k·cm(H2)·c2(NO)。控制NO起始浓度为0.5mol•L-1,N2的瞬时生成速率和H2起始浓度的关系如图所示,下列说法正确的是
2H2O(g)+N2(g),N2的瞬时生成速率v=k·cm(H2)·c2(NO)。控制NO起始浓度为0.5mol•L-1,N2的瞬时生成速率和H2起始浓度的关系如图所示,下列说法正确的是
| A.该反应的速率常数k为15L2·mol-2•s-1 |
| B.随着H2起始浓度增大,达平衡时N2的物质的量分数增大 |
| C.反应达平衡后,H2和NO的浓度均增加一倍,则NO转化率减小 |
| D.H2起始浓度为0.2mol•L-1,某时刻NO的浓度为0.4mol•L-1,则此时N2的瞬时生成速率为0.24mol•L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知:t℃下的某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: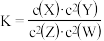 ,有关该平衡的说法中正确的是
,有关该平衡的说法中正确的是
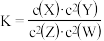 ,有关该平衡的说法中正确的是
,有关该平衡的说法中正确的是| A.升高温度,平衡常数K变大 |
| B.增大压强,W(g)物质的量分数变大 |
| C.升温,若混合气体的平均相对分子质量变小,则正反应放热 |
| D.增大X浓度,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列实验中,对现象的解释不正确 的是
| 选项 | A | B | C | D |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 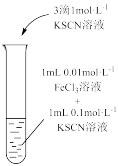 | 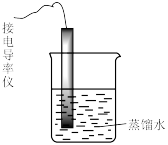 分别测定20℃和80℃蒸馏水的电导率 | 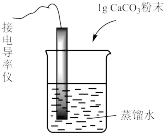 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在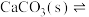  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】根据实验目的,下列实验及现象、结论正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 探究温度对平衡移动的影响 | 向试管中加入2mL CuCl2溶液,CuCl2溶液存在 CuCl2溶液,CuCl2溶液存在   ,加热试管,溶液由蓝绿色变为黄绿色 ,加热试管,溶液由蓝绿色变为黄绿色 | 其他条件不变时,升高温度,平衡向吸热反应方向移动 |
| B | 探究氢离子浓度对 、 、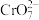 相互转化的影响 相互转化的影响 | 向2mL K2Cr2O7溶液中滴加5~10滴 K2Cr2O7溶液中滴加5~10滴 NaOH溶液,溶液变为黄色 NaOH溶液,溶液变为黄色 | 其他条件不变时,减小氢离子浓度,平衡向生成 的方向移动 的方向移动 |
| C | 探究压强对平衡移动的影响 | 用注射器吸入20mLNO2和N2O4混合气体,向内推动注射器,混合气体颜色加深 | 其他条件不变时,加压,平衡向生成NO2的方向移动 |
| D | 验证CH3COOH和H2CO3的酸性 | 向盛有2mL1mol/L的Na2CO3溶液中,逐滴加入同体积同浓度的CH3COOH溶液,无气泡产生 | 酸性强弱: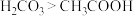 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】反应:2X(g)+Y(g)⇌2Z(g)在不同温度和压强下的产物Z的物质的量和反应时间t的关系如图所示,下列判断正确的是( )
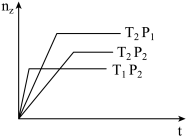

| A.P1>P2 T1>T2 ΔH<0 |
| B.P1>P2 T1<T2 ΔH<0 |
| C.P1<P2 T1>T2 ΔH>0 |
| D.P1<P2 T1<T2 ΔH>0 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列反应不能用勒夏特例原理解释的是( )
| A.光照新制的氯水时 溶液的 pH逐渐减小 |
| B.锌与稀硫酸反应,加入少量硫酸铜反应速率加快 |
| C.可用浓氨水和氢氧化钠固体快速制取氨气 |
| D.增大压强,有利于SO2和O2反应生成 SO3 |
您最近一年使用:0次

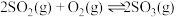 ,
, 。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
 的体积分数:Ⅱ>Ⅲ
的体积分数:Ⅱ>Ⅲ
 ,恒压条件下,按
,恒压条件下,按 进行反应,达平衡时各组分的物质的量分数随温度变化曲线如图所示。下列说法错误的是
进行反应,达平衡时各组分的物质的量分数随温度变化曲线如图所示。下列说法错误的是
 的物质的量分数随温度的变化
的物质的量分数随温度的变化 的平衡转化率为60%
的平衡转化率为60% 的物质的量分数比在恒温密闭容器中的低
的物质的量分数比在恒温密闭容器中的低

