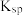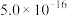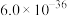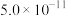镍钛钯废靶材含钛55%、镍25%、钯18%和杂质铝2%。从镍钛钯废靶材回收有关金属的工艺流程如下:
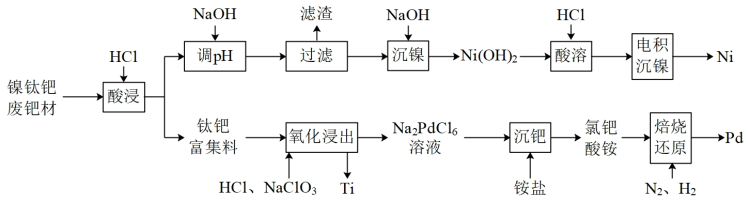
已知:Ⅰ.常温下,钛与钯均不溶于盐酸。
Ⅱ. 在溶液中存在配位平衡:
在溶液中存在配位平衡: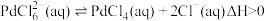
回答下列问题:
(1)镍元素在周期表中的位置为_______ ,请写出其基态原子的核外电子排布式_______ 。
(2)“调pH”除铝、钛时,pH对溶液中金属离子质量浓度影响如下表,根据表中数据判断除铝、钛时pH应调节至_______ 为宜。
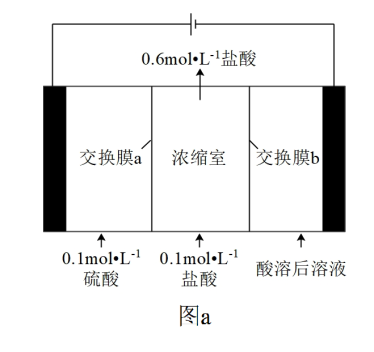
(3)“酸溶”所得溶液,经电积可得单质镍,电积沉镍装置如图a所示。电积装置中,交换膜b应为_______ 离子交换膜(填“阳”或“阴”)。电解时浓缩室溶液体积保持不变,当浓缩室得到 的盐酸时,阴极得到Ni的质量小于14.75g,其原因为
的盐酸时,阴极得到Ni的质量小于14.75g,其原因为_______ 。
(4)“氧化浸出”时,钯(Pd)被氧化生成配位离子 的离子方程式为
的离子方程式为_______ 。
(5)“沉钯”时,温度保持在55~65℃,温度不易过高,其原因除防止铵盐分解外,还有_______ 。“沉钯”时,铵盐最好选用_______ (填该物质的电子式),有利于钯的沉淀。
(6)氯钯酸铵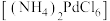 在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在
在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在_______ 操作中循环使用(填操作单元名称)。

已知:Ⅰ.常温下,钛与钯均不溶于盐酸。
Ⅱ.
 在溶液中存在配位平衡:
在溶液中存在配位平衡: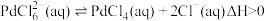
回答下列问题:
(1)镍元素在周期表中的位置为
(2)“调pH”除铝、钛时,pH对溶液中金属离子质量浓度影响如下表,根据表中数据判断除铝、钛时pH应调节至
| pH | 溶液中金属离子质量浓度( ) ) | ||
 |  |  | |
| 1.1 | 6100 | 7780 | 46 |
| 2.1 | 5960 | 7430 | 3 |
| 3.4 | 212 | 6080 | 1 |
| 4.2 | 202 | 5870 | 1 |
| 5.2 | 107 | 3720 | 1 |

(3)“酸溶”所得溶液,经电积可得单质镍,电积沉镍装置如图a所示。电积装置中,交换膜b应为
 的盐酸时,阴极得到Ni的质量小于14.75g,其原因为
的盐酸时,阴极得到Ni的质量小于14.75g,其原因为(4)“氧化浸出”时,钯(Pd)被氧化生成配位离子
 的离子方程式为
的离子方程式为(5)“沉钯”时,温度保持在55~65℃,温度不易过高,其原因除防止铵盐分解外,还有
(6)氯钯酸铵
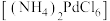 在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在
在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析出,该固体可在
更新时间:2023-02-09 12:43:42
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为 ,含少量
,含少量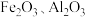 、
、 等)制取
等)制取 工艺流程如下:
工艺流程如下:

已知:①浸出液含有的阳离子主要有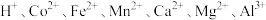 等;
等;
②部分阳离子以氢氧化物形式沉淀时溶液的 见表:
见表:
(1) 中
中 的化合价是
的化合价是_______ 。
(2)写出浸出过程中 与
与 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(3)浸出液中加入 的目的是
的目的是_______ 。
(4)加 能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除
能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除 外,还有的成分是
外,还有的成分是_______ (填化学式),试用离子方程式和必要的文字简述其原理:_______ 。
(5)萃取剂对金属离子的萃取率与 的关系如图,萃取剂的作用是
的关系如图,萃取剂的作用是_______ ;其使用的适宜 范围是
范围是_______ 。
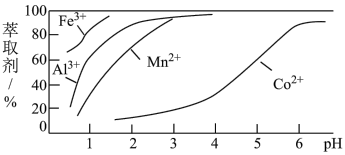
A.接近2.0B.接近3.0C.接近5.0
(6)用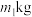 水钴矿(含
水钴矿(含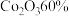 )制备
)制备 ,最终得到产品
,最终得到产品 ,产率(实际产量/理论产量
,产率(实际产量/理论产量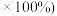 为
为_______ 。(已知: ,仅列数字计算式)。
,仅列数字计算式)。
 ,含少量
,含少量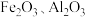 、
、 等)制取
等)制取 工艺流程如下:
工艺流程如下:
已知:①浸出液含有的阳离子主要有
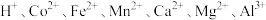 等;
等;②部分阳离子以氢氧化物形式沉淀时溶液的
 见表:
见表:| 沉淀物 |  |  |  |  |  |
完全沉淀的 | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)
 中
中 的化合价是
的化合价是(2)写出浸出过程中
 与
与 发生反应的离子方程式:
发生反应的离子方程式:(3)浸出液中加入
 的目的是
的目的是(4)加
 能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除
能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除 外,还有的成分是
外,还有的成分是(5)萃取剂对金属离子的萃取率与
 的关系如图,萃取剂的作用是
的关系如图,萃取剂的作用是 范围是
范围是
A.接近2.0B.接近3.0C.接近5.0
(6)用
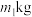 水钴矿(含
水钴矿(含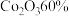 )制备
)制备 ,最终得到产品
,最终得到产品 ,产率(实际产量/理论产量
,产率(实际产量/理论产量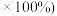 为
为 ,仅列数字计算式)。
,仅列数字计算式)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】铝灰主要含有Al2O3、Al,以及少量硅石和Fe的氧化物,利用铝灰制备净水剂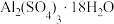 的工艺流程如图。
的工艺流程如图。

已知:金属离子浓度为0.1mol∙L-1时生成氢氧化物沉淀的pH
回答相关问题:
(1)酸浸时为确保安全应注意_______ ,酸浸充分后溶液中的金属阳离子是_______ 。
(2)操作I和II的名称是_______ 。
(3)若无氧化步骤,对实验的影响是_______ 。
(4)棕色沉淀含MnO2,操作①加入MnSO4反应的离子方程式是_______ ,判断该反应完成的现象是_______ 。
(5)操作②调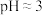 的原因是
的原因是_______ 。
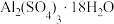 的工艺流程如图。
的工艺流程如图。
已知:金属离子浓度为0.1mol∙L-1时生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
(1)酸浸时为确保安全应注意
(2)操作I和II的名称是
(3)若无氧化步骤,对实验的影响是
(4)棕色沉淀含MnO2,操作①加入MnSO4反应的离子方程式是
(5)操作②调
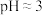 的原因是
的原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】 应用广泛。利用工业废碱渣(主要成分
应用广泛。利用工业废碱渣(主要成分 )吸收硫酸厂尾气中的
)吸收硫酸厂尾气中的 制备无水
制备无水 的成本低、优势明显,其流程如下:
的成本低、优势明显,其流程如下:

已知:① 溶液的pH约为4.7;
溶液的pH约为4.7;
②吸收过程中,当吸收塔中pH约为5时吸收液进入中和器。
(1)举例说明向大气中排放 导致的环境问题
导致的环境问题___________ 。
(2)中和器中发生的主要反应的化学方程式是___________ 。
(3)为了促进 结晶,中和器中加入过量的NaOH.请
结晶,中和器中加入过量的NaOH.请结合 化学用语,从平衡移动的角度解释___________ 。
(4)写出生产过程中吸收塔内发生反应的离子方程式___________ 。
(5)检验成品质量。
①取少量成品溶解,___________ ,说明成品中含 。请
。请补全操作与现象 。
②可用碘量法测定成品中 的含量,过程如下:
的含量,过程如下:
ⅰ.将mg成品溶于水配成100mL溶液,取25mL于碘量瓶中,并调至弱酸性;
ⅱ.加入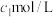 的碘标准液
的碘标准液 ,盖上瓶塞,缓慢振荡使其充分反应;
,盖上瓶塞,缓慢振荡使其充分反应;
ⅲ.用 的
的 标准液滴定至溶液呈淡黄色时,加入1mL淀粉指示剂,继续滴定至终点,消耗
标准液滴定至溶液呈淡黄色时,加入1mL淀粉指示剂,继续滴定至终点,消耗 标准液
标准液 。(已知:
。(已知: )
)
a.滴定终点的现象是___________ 。
b.成品中 的质量分数是
的质量分数是___________ 。
 应用广泛。利用工业废碱渣(主要成分
应用广泛。利用工业废碱渣(主要成分 )吸收硫酸厂尾气中的
)吸收硫酸厂尾气中的 制备无水
制备无水 的成本低、优势明显,其流程如下:
的成本低、优势明显,其流程如下:
已知:①
 溶液的pH约为4.7;
溶液的pH约为4.7;②吸收过程中,当吸收塔中pH约为5时吸收液进入中和器。
(1)举例说明向大气中排放
 导致的环境问题
导致的环境问题(2)中和器中发生的主要反应的化学方程式是
(3)为了促进
 结晶,中和器中加入过量的NaOH.请
结晶,中和器中加入过量的NaOH.请(4)写出生产过程中吸收塔内发生反应的离子方程式
(5)检验成品质量。
①取少量成品溶解,
 。请
。请②可用碘量法测定成品中
 的含量,过程如下:
的含量,过程如下:ⅰ.将mg成品溶于水配成100mL溶液,取25mL于碘量瓶中,并调至弱酸性;
ⅱ.加入
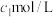 的碘标准液
的碘标准液 ,盖上瓶塞,缓慢振荡使其充分反应;
,盖上瓶塞,缓慢振荡使其充分反应;ⅲ.用
 的
的 标准液滴定至溶液呈淡黄色时,加入1mL淀粉指示剂,继续滴定至终点,消耗
标准液滴定至溶液呈淡黄色时,加入1mL淀粉指示剂,继续滴定至终点,消耗 标准液
标准液 。(已知:
。(已知: )
)a.滴定终点的现象是
b.成品中
 的质量分数是
的质量分数是
您最近一年使用:0次
【推荐1】有效去除大气中的 是环境保护的重要课题。
是环境保护的重要课题。
(1)用水吸收 的相关热化学方程式如下:
的相关热化学方程式如下:
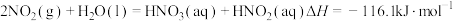
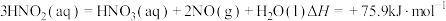
反应 的
的
___________  。
。
(2)用稀硝酸吸收 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:___________ 。( 是弱酸)
是弱酸)
(3)用酸性 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 生成
生成 和
和 的反应,写出该反应的化学方程式:
的反应,写出该反应的化学方程式:___________ 。
(4)在有氧条件下,新型催化剂 能催化
能催化 与
与 反应生成
反应生成 。
。
① 与
与 生成
生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为___________  。
。
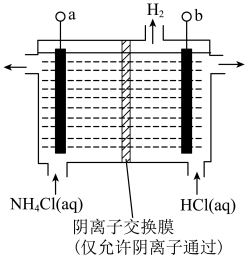
②将一定比例的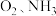 和
和 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器中反应(装置见图):
的反应器中反应(装置见图): 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在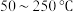 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后缓慢上升的主要原因是
的去除率先迅速上升后缓慢上升的主要原因是___________ 。 (氯的化合价为
(氯的化合价为 价),其原理是
价),其原理是
 接电源的
接电源的___________ (填“正”或“负”)极。
②阳极反应式是___________ 。
 是环境保护的重要课题。
是环境保护的重要课题。(1)用水吸收
 的相关热化学方程式如下:
的相关热化学方程式如下: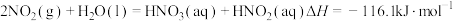
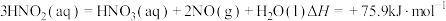
反应
 的
的
 。
。(2)用稀硝酸吸收
 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式: 是弱酸)
是弱酸)(3)用酸性
 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 生成
生成 和
和 的反应,写出该反应的化学方程式:
的反应,写出该反应的化学方程式:(4)在有氧条件下,新型催化剂
 能催化
能催化 与
与 反应生成
反应生成 。
。①
 与
与 生成
生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为 。
。②将一定比例的
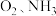 和
和 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器中反应(装置见图):
的反应器中反应(装置见图):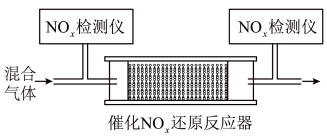
 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在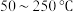 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后缓慢上升的主要原因是
的去除率先迅速上升后缓慢上升的主要原因是
 (氯的化合价为
(氯的化合价为 价),其原理是
价),其原理是
 接电源的
接电源的②阳极反应式是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】乙烯是一种重要的基本化工原料,乙烯的产量可以衡量一个国家的石油化工发展水平,研究工业制取乙烯有重要的意义。
Ⅰ.工业用 和
和 在一定条件下合成乙烯:
在一定条件下合成乙烯: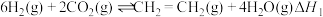
已知:①
②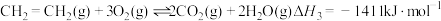
(1)
___________ 
(2)在刚性密闭容器中充入体积比为 的
的 和
和 ,在一定条件下模拟工业合成乙烯,不同温度对
,在一定条件下模拟工业合成乙烯,不同温度对 的平衡转化率和催化剂催化效率的影响如图所示,下列说法
的平衡转化率和催化剂催化效率的影响如图所示,下列说法不正确 的是___________(填字母)。
Ⅱ.工业用甲烷催化法制取乙烯: ,T℃时,向3L的恒容反应器中充入
,T℃时,向3L的恒容反应器中充入 ,仅发生上述反应,反应过程中的物质的量随时间变化如图所示:
,仅发生上述反应,反应过程中的物质的量随时间变化如图所示: ,
,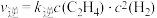 ,
, 、
、 为速率常数,只与温度有关,T℃时,平衡时容器内
为速率常数,只与温度有关,T℃时,平衡时容器内 的物质的量为
的物质的量为 ,则
,则 与
与 的比值为
的比值为___________ (用含a的代数式表示);若将温度降低,速率常数减少的倍数:
___________ (填“>”、“=”或“<”) 。
。
Ⅲ.乙烷裂解制乙烯:
(4)T℃时,将乙烷与氦气体积比 混合后,通入一密闭容器中发生反应。平衡时容器压强为
混合后,通入一密闭容器中发生反应。平衡时容器压强为 ,若乙烷的平衡转化率为80%,反应的平衡常数
,若乙烷的平衡转化率为80%,反应的平衡常数
___________ kPa(用分压表示,分压=总压×物质的量分数)。
Ⅳ.电解法还原二氧化碳制乙烯原理如图所示(AB表示直流电源)。___________ 。
Ⅰ.工业用
 和
和 在一定条件下合成乙烯:
在一定条件下合成乙烯: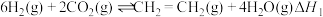
已知:①

②
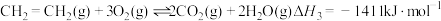
(1)


(2)在刚性密闭容器中充入体积比为
 的
的 和
和 ,在一定条件下模拟工业合成乙烯,不同温度对
,在一定条件下模拟工业合成乙烯,不同温度对 的平衡转化率和催化剂催化效率的影响如图所示,下列说法
的平衡转化率和催化剂催化效率的影响如图所示,下列说法
A.平衡常数: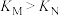 |
B.消耗 的速率: 的速率: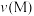 可能小于 可能小于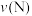 |
C.为了提高 的平衡转化率,选择温度越低越好 的平衡转化率,选择温度越低越好 |
| D.M点时的压强一定小于N点时的压强 |
Ⅱ.工业用甲烷催化法制取乙烯:
 ,T℃时,向3L的恒容反应器中充入
,T℃时,向3L的恒容反应器中充入 ,仅发生上述反应,反应过程中的物质的量随时间变化如图所示:
,仅发生上述反应,反应过程中的物质的量随时间变化如图所示: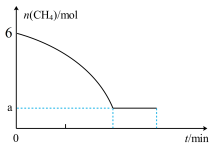
 ,
,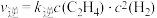 ,
, 、
、 为速率常数,只与温度有关,T℃时,平衡时容器内
为速率常数,只与温度有关,T℃时,平衡时容器内 的物质的量为
的物质的量为 ,则
,则 与
与 的比值为
的比值为
 。
。Ⅲ.乙烷裂解制乙烯:

(4)T℃时,将乙烷与氦气体积比
 混合后,通入一密闭容器中发生反应。平衡时容器压强为
混合后,通入一密闭容器中发生反应。平衡时容器压强为 ,若乙烷的平衡转化率为80%,反应的平衡常数
,若乙烷的平衡转化率为80%,反应的平衡常数
Ⅳ.电解法还原二氧化碳制乙烯原理如图所示(AB表示直流电源)。

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】氟化镨(PrF3)常用于电弧碳棒添加剂。利用方镨矿精矿(Pr2S3,难溶于水)制备氟化镨的流程如下:
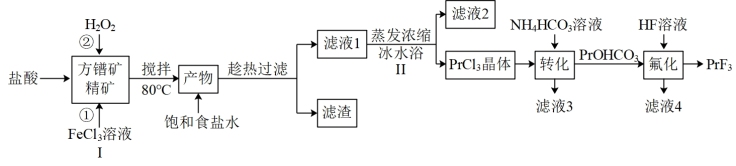
已知:① ;
;
② 、
、 以氢氧化物的形式完全沉淀时,溶液的pH分别为3.2、10.1。
以氢氧化物的形式完全沉淀时,溶液的pH分别为3.2、10.1。
(1)步骤I中加入 溶液后生成
溶液后生成 和S,该反应中氧化剂与还原剂的物质的量之比为
和S,该反应中氧化剂与还原剂的物质的量之比为_______ ,加入盐酸的另一个目的是控制pH在0.5~1.0,原因是_______ 。
(2)请用离子方程式解释反应②中加入 的作用:
的作用:_______ 。
(3)请用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因:_______ 。
(4)完成 溶液转化为
溶液转化为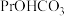 沉淀的离子方程式:□
沉淀的离子方程式:□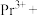 □
□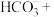 □
□ □
□ □
□ 。
。_______
(5)滤液3可用作_______ 。
(6)镨蓄电池具有稳定性高等有点,充电后两个电极上沉积的 分别转化为
分别转化为 和Pr,充电时阴极的电极反应式为
和Pr,充电时阴极的电极反应式为_______ 。

已知:①
 ;
;②
 、
、 以氢氧化物的形式完全沉淀时,溶液的pH分别为3.2、10.1。
以氢氧化物的形式完全沉淀时,溶液的pH分别为3.2、10.1。(1)步骤I中加入
 溶液后生成
溶液后生成 和S,该反应中氧化剂与还原剂的物质的量之比为
和S,该反应中氧化剂与还原剂的物质的量之比为(2)请用离子方程式解释反应②中加入
 的作用:
的作用:(3)请用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因:
(4)完成
 溶液转化为
溶液转化为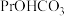 沉淀的离子方程式:□
沉淀的离子方程式:□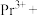 □
□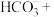 □
□ □
□ □
□ 。
。(5)滤液3可用作
(6)镨蓄电池具有稳定性高等有点,充电后两个电极上沉积的
 分别转化为
分别转化为 和Pr,充电时阴极的电极反应式为
和Pr,充电时阴极的电极反应式为
您最近一年使用:0次
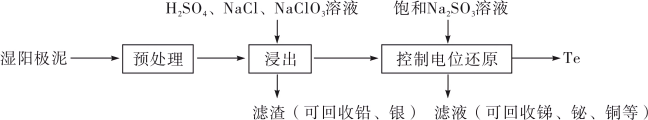
【推荐1】碲(Te)是一种重要的稀有分散元素,广泛应用于冶金、石油、化工、航空、电子等领域。以某冶炼厂的湿阳极泥(含水26%,主要含锑、砷、铅、铋、银和少量铜、碲等)为原料回收碲的流程如下:
请回答下列问题:
(1) 的基态原子的电子排布式为
的基态原子的电子排布式为___________ 。
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是___________ ;氧化后的原料还需粉碎、过筛,目的是___________ 。
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为___________ 、___________ ;添加 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式___________ 。
(4)电解时为防止除Te以外的单质生成,需控制电位的范围为___________ ;加入饱和 溶液还原
溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成___________ (填化学式)。
(5)碲可用于制备半导体材料碲化锌,其立方晶胞结构如图所示。以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。A点碲原子坐标为 ,C点锌原子坐标为
,C点锌原子坐标为 ,则B点锌原子坐标为
,则B点锌原子坐标为___________ 。若Te的原子半径为rpm,碲化锌晶胞中面心与顶点的碲原子相切,晶体的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
___________  (列出计算式)。
(列出计算式)。
| 物质 | 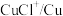 | 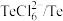 | 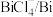 | 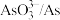 | 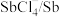 |
| 氧化还原电位(E)/V | 0.342 | 0.568 | 0.16 | 小于0.16 | 小于0.16 |
(1)
 的基态原子的电子排布式为
的基态原子的电子排布式为(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为
 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式(4)电解时为防止除Te以外的单质生成,需控制电位的范围为
 溶液还原
溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成(5)碲可用于制备半导体材料碲化锌,其立方晶胞结构如图所示。以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。A点碲原子坐标为
 ,C点锌原子坐标为
,C点锌原子坐标为 ,则B点锌原子坐标为
,则B点锌原子坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数
 (列出计算式)。
(列出计算式)。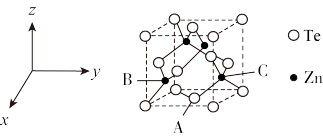
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】一种磁性材料的磨削废料主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物,由该废料制备纯度较高的氢氧化镍的工艺流程如图,回答下列问题:
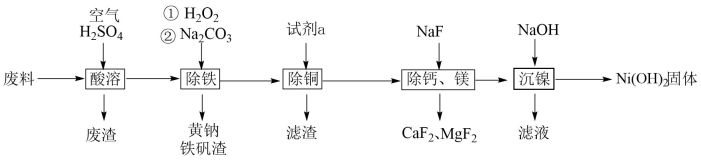
(1)镍元素所在的第四周期中3d轨道上没有未成对电子的过渡元素离子的水合离子为无色,下列离子形成的水合离子为无色的是 (填序号)。
(2)“酸溶”时产生的废渣主要成分为______________________ 。
(3)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢通入空气,写出金属镍溶解生成 的离子方程式:
的离子方程式:____________________ 。
(4)“除铁”时为了证明添加的 已足量,应选择的试剂是
已足量,应选择的试剂是___________ 。
(5)“除铜”时,试剂a最好选用_______ (填序号),其优点有_________ (至少答两点)。
A. B.
B. C.NaOH D.FeS
C.NaOH D.FeS
(6)“除钙、镁”时,在完全除去钙、镁离子时,溶液中
___________ 。
(7)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下: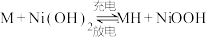 中M为储氢合金),写出电池放电过程中正极的电极反应式:
中M为储氢合金),写出电池放电过程中正极的电极反应式:___________________________________ ,用该电池及惰性电极电解一定量饱和食盐水,在阴阳两极分别收集到784L和336L气体(标准状况下),则电池负极质量变化量为_____________ 。

物质 |
|
| CuS |
|
|
|
|
|
|
|
|
A. | B. | C.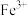 | D. |
(3)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢通入空气,写出金属镍溶解生成
 的离子方程式:
的离子方程式:(4)“除铁”时为了证明添加的
 已足量,应选择的试剂是
已足量,应选择的试剂是(5)“除铜”时,试剂a最好选用
A.
 B.
B. C.NaOH D.FeS
C.NaOH D.FeS(6)“除钙、镁”时,在完全除去钙、镁离子时,溶液中

(7)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:
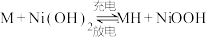 中M为储氢合金),写出电池放电过程中正极的电极反应式:
中M为储氢合金),写出电池放电过程中正极的电极反应式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】砷化镓(GaAs)、碲化镉(CdTe)等太阳能电池适合光电转换,可以直接把光能转化成电能。回答下列问题:
(1)元素As与N同族,预测As的氢化物分子的立体结构为____ ,其基态原子最外层p轨道电子的自旋状态____ (填“相同”或“相反”)。
(2)元素Cd与Zn是同一副族的相邻元素,Cd的价层电子排布为4d105s2,Cd2+的价层电子排布为___ 。
(3)经X射线衍射实验证明在碲酸(H6TeO6)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为____ 。
(4)Te、Se都是第ⅥA族的元素,SeF6与SF6具有相似的结构,则熔沸点SeF6___ SF6(填“>”或“<”或“=");二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用如图表示,已知光的波长与其能量成反比,则图中实现光响应的波长:λ1____ λ2(填“>”或“<”或“="),其原因是____ 。

(5)CdTe的晶胞属立方晶系,晶胞参数如图1所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。如原子M的坐标为(0,0,0),则原子N的坐标为____ 。

该晶胞沿其面对角线方向上的投影如图2所示,则代表Te原子的位置是____ (填序号),晶胞中原子6和11之间的距离为____ pm(用含a的代数式表示)。
(1)元素As与N同族,预测As的氢化物分子的立体结构为
(2)元素Cd与Zn是同一副族的相邻元素,Cd的价层电子排布为4d105s2,Cd2+的价层电子排布为
(3)经X射线衍射实验证明在碲酸(H6TeO6)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
(4)Te、Se都是第ⅥA族的元素,SeF6与SF6具有相似的结构,则熔沸点SeF6

(5)CdTe的晶胞属立方晶系,晶胞参数如图1所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。如原子M的坐标为(0,0,0),则原子N的坐标为

该晶胞沿其面对角线方向上的投影如图2所示,则代表Te原子的位置是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】钨酸铋(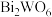 )是一种新型的光催化剂。一种以铜转炉白烟灰(主要成分是
)是一种新型的光催化剂。一种以铜转炉白烟灰(主要成分是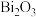 ,还含
,还含 、
、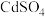 、
、 、
、 及CuO、
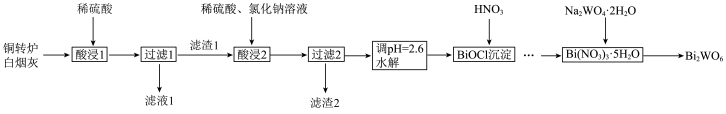
及CuO、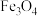 )为原料制备钨酸铋的工艺流程如图所示:
)为原料制备钨酸铋的工艺流程如图所示:
已知: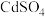 溶于水,
溶于水,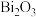 不溶于稀硫酸,溶于稀盐酸。
不溶于稀硫酸,溶于稀盐酸。
请回答下列问题:
(1)“酸浸1”时,铜转炉白烟灰与稀硫酸逆向加入,硫酸以喷雾形式,其目的是___________ 。
(2)滤渣1的成分是___________ (填化学式);在实验室进行“过滤1”需要的玻璃仪器为___________ 。
(3)“酸浸1”中生成 的化学方程式为
的化学方程式为___________ 。
(4)“酸浸2”中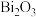 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(5)洗涤BiOCl沉淀的操作方法是___________ 。
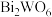 )是一种新型的光催化剂。一种以铜转炉白烟灰(主要成分是
)是一种新型的光催化剂。一种以铜转炉白烟灰(主要成分是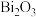 ,还含
,还含 、
、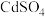 、
、 、
、 及CuO、
及CuO、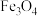 )为原料制备钨酸铋的工艺流程如图所示:
)为原料制备钨酸铋的工艺流程如图所示:
已知:
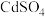 溶于水,
溶于水,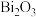 不溶于稀硫酸,溶于稀盐酸。
不溶于稀硫酸,溶于稀盐酸。请回答下列问题:
(1)“酸浸1”时,铜转炉白烟灰与稀硫酸逆向加入,硫酸以喷雾形式,其目的是
(2)滤渣1的成分是
(3)“酸浸1”中生成
 的化学方程式为
的化学方程式为(4)“酸浸2”中
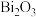 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为(5)洗涤BiOCl沉淀的操作方法是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】氢氧化铍可用作核技术和制备含铍材料的中间体等。以硅铍石(主要成分Be2SiO4含少量Al2O3)和方解石(主要成分CaCO3,含少量FeCO3、SiO2)为原料,制备Be(OH)2的工艺流程如图所示:

已知:I.硅铍石不易被硫酸直接分解;铍的性质与铝相似;粗Be(OH)2含有少量Al(OH)3;
II.生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
(1)“熔炼”时加入方解石粉的作用为_______ ;生成气体的电子式为_______ 。
(2)浸渣中除含有CaSiO3、H2SiO3外,还含有_______ (填化学式)。
(3)滤渣1中含有NH4Al(SO4)2·12H2O、(NH4)2 Fe(SO4)2·6H2O。NH4Al(SO4)2 ·12H2O能用作净水剂,原因为_______ (用离子方程式表示);(NH4)2 Fe(SO4)2·6H2O可用于测定KMnO4的含量,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)根据已知II信息可知,“深度除铁”的适宜方案为_______ 。
(5)“调pH”所得母液中的主要溶质可返回到_______ 工序循环利用。
(6)“洗涤”的目的是除去粗Be(OH)2中所含的Al(OH)3,若用足量NaOH浓溶液代替NaOH稀溶液,会导致的后果为_______ (用离子方程式表示)。

已知:I.硅铍石不易被硫酸直接分解;铍的性质与铝相似;粗Be(OH)2含有少量Al(OH)3;
II.生成氢氧化物沉淀的pH如下表所示:
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Be(OH)2 |
| 开始沉淀的pH | 7.7 | 2.5 | 3.5 | 4.6 |
| 沉淀完全的pH (溶液中金属离子浓度等于10-5 mol·L-1) | 8.7 | 3.2 | 4.7 | 5.9 |
回答下列问题:
(1)“熔炼”时加入方解石粉的作用为
(2)浸渣中除含有CaSiO3、H2SiO3外,还含有
(3)滤渣1中含有NH4Al(SO4)2·12H2O、(NH4)2 Fe(SO4)2·6H2O。NH4Al(SO4)2 ·12H2O能用作净水剂,原因为
(4)根据已知II信息可知,“深度除铁”的适宜方案为
(5)“调pH”所得母液中的主要溶质可返回到
(6)“洗涤”的目的是除去粗Be(OH)2中所含的Al(OH)3,若用足量NaOH浓溶液代替NaOH稀溶液,会导致的后果为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
真题
解题方法
【推荐3】以铅精矿(含 ,
, 等)为主要原料提取金属
等)为主要原料提取金属 和
和 的工艺流程如下:
的工艺流程如下:
(1)“热浸”时,难溶的 和
和 转化为
转化为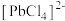 和
和 及单质硫。溶解等物质的量的
及单质硫。溶解等物质的量的 和
和 时,消耗
时,消耗 物质的量之比为
物质的量之比为_______ ;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发外,另一目的是防止产生
挥发外,另一目的是防止产生_______ (填化学式)。
(2)将“过滤Ⅱ”得到的 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属
沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属 “电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为
“电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为_______ 。
(3)“还原”中加入铅精矿的目的是_______ 。
(4)“置换”中可选用的试剂X为_______ (填标号)。
A. B.
B. C.
C. D.
D.
“置换”反应的离子方程式为_______ 。
(5)“电解II”中将富银铅泥制成电极板,用作_______ (填“阴极”或“阳极”)。
 ,
, 等)为主要原料提取金属
等)为主要原料提取金属 和
和 的工艺流程如下:
的工艺流程如下: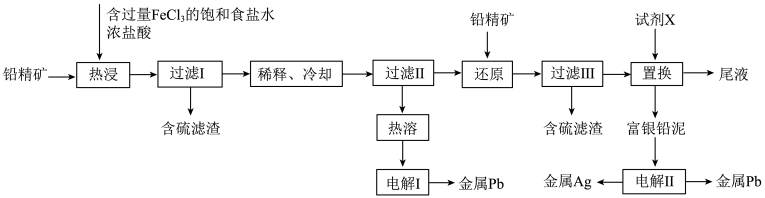
(1)“热浸”时,难溶的
 和
和 转化为
转化为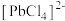 和
和 及单质硫。溶解等物质的量的
及单质硫。溶解等物质的量的 和
和 时,消耗
时,消耗 物质的量之比为
物质的量之比为 挥发外,另一目的是防止产生
挥发外,另一目的是防止产生(2)将“过滤Ⅱ”得到的
 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属
沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属 “电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为
“电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为(3)“还原”中加入铅精矿的目的是
(4)“置换”中可选用的试剂X为
A.
 B.
B. C.
C. D.
D.
“置换”反应的离子方程式为
(5)“电解II”中将富银铅泥制成电极板,用作
您最近一年使用:0次