已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是nsnnp2n;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:A_______ ;B_______ ;C_______ ;D_______ 。
②A、B、C三种元素的电负性由大到小的顺序为:_______ 。
③B、C、D、E四种元素的第一电离能由大到小的顺序为:_______ 。
(2)以下是A、B、C、D、E、F元素中某种元素的部分电离能,由此可推断该元素是_______ 。(填元素名称)
(3)F元素位于周期表的_______ 区,未成对电子对数为_______ ,最外层电子所占能级轨道电子云轮廓图的形状为_______ ,与F元素同周期的元素中未成对电子数最多的是_______ 。(填元素符号)
(1)请用元素符号完成下列空白:
①元素:A
②A、B、C三种元素的电负性由大到小的顺序为:
③B、C、D、E四种元素的第一电离能由大到小的顺序为:
(2)以下是A、B、C、D、E、F元素中某种元素的部分电离能,由此可推断该元素是
| I1 | I2 | I3 | I4 | I5 |
| 578 kJ·mol-1 | 1817 kJ·mol-1 | 2745 kJ·mol-1 | 11575 kJ·mol-1 | 14830 kJ·mol-1 |
更新时间:2023-03-06 08:20:42
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期中的位置为_____ ,G的原子结构示意图是_____ 。
(2)D与E按原子个数比1∶1形成化合物甲,其化学式为_____ ,向甲中滴加足量水时发生反应的化学方程式是_____ 。
(3)E、F、G形成的简单离子,半径由大到小顺序是_____ (用离子符号表示)。
(4)B、C、D的简单氢化物的还原性强弱顺序为_____ (填分子式,下同),热稳定性强弱顺序为_____ 。
(5)F、G的最高价氧化物的水化物的分子式为_____ ,酸性较强的为_____ 。
(1)C在元素周期中的位置为
(2)D与E按原子个数比1∶1形成化合物甲,其化学式为
(3)E、F、G形成的简单离子,半径由大到小顺序是
(4)B、C、D的简单氢化物的还原性强弱顺序为
(5)F、G的最高价氧化物的水化物的分子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知X、Y、Z、W 是中学化学中常见的四种不同粒子,其中X、W 为分子,Y、Z为离子它们之间存在如下所示的转化关系:
X+Y→Z+W Z+H+ →X Y+H+ →W
(1)如果X、Y、Z、W 均是10电子的粒子,请写出:
X的电子式:____________ ; W 的电子式:_________________ 。
(2)如果X和Z均是18电子的粒子,Y 和 W 均是10电子的粒子,请写出:
①X与Y(足量)在溶液中反应的离子方程式:______________________ 。
②根据上述离子方程式,可判断Z与 Y 结合质子(H+ )的能力大小是________ >_____ 。(用化学式或离子符号表示)
X+Y→Z+W Z+H+ →X Y+H+ →W
(1)如果X、Y、Z、W 均是10电子的粒子,请写出:
X的电子式:
(2)如果X和Z均是18电子的粒子,Y 和 W 均是10电子的粒子,请写出:
①X与Y(足量)在溶液中反应的离子方程式:
②根据上述离子方程式,可判断Z与 Y 结合质子(H+ )的能力大小是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D为原子序数依次增大的四种短周期元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C的最高正价为+5价,核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是___________ (填元素符号),C原子价电子运动状态有___________ 种。
(2)单质A有两种同素异形体,其中沸点高的是_____ (填分子式);B的氢化物所属的晶体类型为______ 。
(3)C和D反应可生成组成比为1︰3的化合物E,E的立体构型为_____ ,中心原子的杂化轨道类型为_____ 。
(4)A和B能够形成化合物F,其晶胞结构如图所示,F的化学式为______ ,晶胞中A的配位数为______ ,A原子和B原子的最近距离为______ pm,晶胞参数a=apm,阿伏加德罗常数的值为NA,晶体F的密度为____ g·cm-3(列出计算式)。

(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1︰3的化合物E,E的立体构型为
(4)A和B能够形成化合物F,其晶胞结构如图所示,F的化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铜阳极泥含有金属( 、
、 、
、 等)及它们的化合物,其中银在铜阳极泥中的存在状态有
等)及它们的化合物,其中银在铜阳极泥中的存在状态有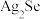 、
、 、
、 等。下图是从铜阳极泥提取银的一种工艺:
等。下图是从铜阳极泥提取银的一种工艺:

已知:Ag++2NH3 [Ag(NH3)2]+
[Ag(NH3)2]+
(1)基态Se原子的核外电子排布式是_______ 。
(2)炉气中的 可与
可与 、
、 反应生成硒单质。写出该反应方程式
反应生成硒单质。写出该反应方程式_______ 。
(3)溶液a的主要成分是_______ 。
(4)水氯化浸金过程中,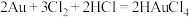 。
。 配离子中提供空轨道的是
配离子中提供空轨道的是_______ (填元素符号),配位数是_______ 。
(5)加入氨气后, 溶解,请写出氨浸分银的离子方程式
溶解,请写出氨浸分银的离子方程式_______ 。
(6)SO 的孤电子对数为
的孤电子对数为_______ 。
(7)Au的晶胞为面心立方体结构、如图所示棱长为apm(1pm=1×10-10cm)晶体金的密度
_______  。(NA为阿伏加德罗常数)
。(NA为阿伏加德罗常数)

 、
、 、
、 等)及它们的化合物,其中银在铜阳极泥中的存在状态有
等)及它们的化合物,其中银在铜阳极泥中的存在状态有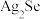 、
、 、
、 等。下图是从铜阳极泥提取银的一种工艺:
等。下图是从铜阳极泥提取银的一种工艺:
已知:Ag++2NH3
 [Ag(NH3)2]+
[Ag(NH3)2]+(1)基态Se原子的核外电子排布式是
(2)炉气中的
 可与
可与 、
、 反应生成硒单质。写出该反应方程式
反应生成硒单质。写出该反应方程式(3)溶液a的主要成分是
(4)水氯化浸金过程中,
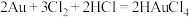 。
。 配离子中提供空轨道的是
配离子中提供空轨道的是(5)加入氨气后,
 溶解,请写出氨浸分银的离子方程式
溶解,请写出氨浸分银的离子方程式(6)SO
 的孤电子对数为
的孤电子对数为(7)Au的晶胞为面心立方体结构、如图所示棱长为apm(1pm=1×10-10cm)晶体金的密度

 。(NA为阿伏加德罗常数)
。(NA为阿伏加德罗常数)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某锂离子电池正极由钴酸锂(LiCoO2)、铝箔、石墨等组成。某研究小组利用该锂离子电池正极材料回收制备Co3O4,同时回收锂,流程如下:

某些物质的溶解度(s)如下表所示:
请回答下列问题:
(1)写出钴元素基态原子的价层电子排布式___________ ,Co在周期表中的位置为___________ ,Co3+中有多少种运动状态的电子___________ 。
(2)过程Ⅰ浸出液产生气泡,钴酸锂发生反应的化学方程式为___________ 。
(3)过程Ⅱ中,不同pH下金属离子的去除效果如图所示。该过程加碱调节pH的范围是___________ 。

(4)过程Ⅳ中操作方法为:向滤液中加入稍过量的___________ ,充分搅拌,加热浓缩,___________ ,用热水洗涤后干燥。
(5)过程Ⅴ中,常温下CoC2O4开始转化为Co(OH)2的pH为___________ 。(已知:Ksp[Co(OH)2]=2.0×10-15,Ksp[CoC2O4]=4.0×10-8)

某些物质的溶解度(s)如下表所示:
| t/℃ | 20 | 40 | 60 | 80 |
| s(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| s(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)写出钴元素基态原子的价层电子排布式
(2)过程Ⅰ浸出液产生气泡,钴酸锂发生反应的化学方程式为
(3)过程Ⅱ中,不同pH下金属离子的去除效果如图所示。该过程加碱调节pH的范围是

(4)过程Ⅳ中操作方法为:向滤液中加入稍过量的
(5)过程Ⅴ中,常温下CoC2O4开始转化为Co(OH)2的pH为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(物质结构与性质)
Ⅰ.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素D的基态原子电子排布式___________________ 。
(2)元素A、B形成的单质中,______ 对应的单质熔点更高,原因是_________________ 。
(3)写出C的最高价氧化物的水化物与B的最高价氧化物的水化物反应的化学方程式_______________ 。
(4)元素D可以形成化学式为D(NH3)5BrSO4,配位数均为6的两种配合物。若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为____________ 。
Ⅱ.钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。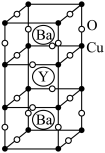
(5)根据图示晶胞结构,推算晶体中Y,Ba,Cu和O原子个数比,确定其化学式为________ 。
Ⅲ.BF3与一定量的水形成晶体Q [(H2O)2·BF3],Q在一定条件下可转化为R:
(6)晶体Q中各种微粒间的作用力不涉及________ (填字母)。
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.范德华力
(7)R中阳离子的空间构型为________ ,阴离子的中心原子轨道采用_____ 杂化。
Ⅰ.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素D的基态原子电子排布式
(2)元素A、B形成的单质中,
(3)写出C的最高价氧化物的水化物与B的最高价氧化物的水化物反应的化学方程式
(4)元素D可以形成化学式为D(NH3)5BrSO4,配位数均为6的两种配合物。若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为
Ⅱ.钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。

(5)根据图示晶胞结构,推算晶体中Y,Ba,Cu和O原子个数比,确定其化学式为
Ⅲ.BF3与一定量的水形成晶体Q [(H2O)2·BF3],Q在一定条件下可转化为R:

(6)晶体Q中各种微粒间的作用力不涉及
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.范德华力
(7)R中阳离子的空间构型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第4周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题。
(1)B元素基态原子核外电子有_______ 种不同的空间运动状态,能量最高的电子所在原子轨道在空间有_______ 个伸展方向。
(2)根据上述信息,画出C元素基态原子的轨道表示式_______ 。
(3)F在元素周期表中属于_______ 区元素,其基态原子核外共有_______ 个未成对电子。
(4)D、E两元素的第一电离能大小关系是_______ (用元素符号表示,下同),B、D两元素的电负性大小关系是_______ 。
(5)写出DA3的电子式:_______ (用元素符号表示)。
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738kJ/mol、I2=1451kJ/mol、I3=7733kJ/mol、I4=10540kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)D、E两元素的第一电离能大小关系是
(5)写出DA3的电子式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、M、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)基态Y原子的价电子排布图是______ ;Z所在周期中第一电离能最大的主族元素是_______ (元素名称)
(2)XY2¯离子的立体构型是________ ;R2+的水合离子[R(H2O)4]2+中,提供孤电子对的原子是________ (元素符号)。
(3)已知XH3易与R2+形成配离子,但XM3不易与R2+形成配离子,其原因是_______________ 。
(4)Y与R所形成的化合物晶体晶胞如图所示,该晶体的化学式:_____________ ;晶胞参数如图所示,则该晶胞密度是___________ g‧cm-3(列式并计算结果,保留小数点儿后一位)。

(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是________ (填标号)。

a.CF4 b.CH4 c.NH4+ d.H2O
(1)基态Y原子的价电子排布图是
(2)XY2¯离子的立体构型是
(3)已知XH3易与R2+形成配离子,但XM3不易与R2+形成配离子,其原因是
(4)Y与R所形成的化合物晶体晶胞如图所示,该晶体的化学式:

(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是

a.CF4 b.CH4 c.NH4+ d.H2O
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】I.2022年4月,大型运输机运−20向塞尔维亚远程运送“常规军事物资”,展示了大国重器“鲲鹏”的突出性能,为世人瞩目。
(1)运−20的外壳大量使用了AM系列Mg−Al−Mn,铝的价电子排布图为___________ ,第一电离能铝___________ (填“大于”、“等于”或“小于”)镁,镁原子核外有___________ 种不同运动状态的电子。
(2)为了减轻飞机的起飞重量并保持机身强度,运-20使用了大量的树脂材料,其中一种树脂材料的部分结构如图1所示,其中碳原子的杂化方式为___________ ,其个数比为___________ 。

Ⅱ.大型飞机的高推重比发动机被誉为航空工业皇冠上的“宝石”,采用大量的金属钨作为耐高温耐磨损材料。
(3)钨元素位于第六周期第VIB族,价电子排布的能级与Cr相同,但排布方式与Cr有所不同,请写出钨原子的价层电子排布式___________ 。
(4)图2为碳和钨形成的一种化合物的晶胞模型,碳原子和钨原子个数比为___________ ,其中一个钨原子周围距离最近且相等的碳原子有___________ 个。

(5)已知该晶胞边长为acm,高为hcm,NA为阿伏加德罗常数。摩尔质量为M g∙mol−1。该晶体密度为___________ g∙cm−3。
(1)运−20的外壳大量使用了AM系列Mg−Al−Mn,铝的价电子排布图为
(2)为了减轻飞机的起飞重量并保持机身强度,运-20使用了大量的树脂材料,其中一种树脂材料的部分结构如图1所示,其中碳原子的杂化方式为

Ⅱ.大型飞机的高推重比发动机被誉为航空工业皇冠上的“宝石”,采用大量的金属钨作为耐高温耐磨损材料。
(3)钨元素位于第六周期第VIB族,价电子排布的能级与Cr相同,但排布方式与Cr有所不同,请写出钨原子的价层电子排布式
(4)图2为碳和钨形成的一种化合物的晶胞模型,碳原子和钨原子个数比为

(5)已知该晶胞边长为acm,高为hcm,NA为阿伏加德罗常数。摩尔质量为M g∙mol−1。该晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铜是重要的过渡元素,其单质及化合物具有广泛用途。回答下列问题:
(1)铜元素基态原子的价电子排布式为________ 。
(2)铜元素能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。
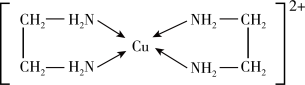
①Cu2+与乙二胺所形成的配离子内部粒子间的作用力类型有________ 。
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
②乙二胺分子中氮原子的杂化轨道类型为________ ,C、N、H三种元素的电负性由大到小顺序是 ___ 。
③乙二胺和三甲胺 [N(CH3)3]均属于胺,乙二胺的沸点比三甲胺高很多,原因是________ 。
(3)Cu2+在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+,其原因是______ 。
(4)Cu和S形成某种晶体的晶胞如图所示。
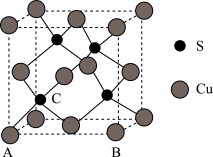
①该晶体的化学式为________ 。
②该晶胞原子坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为________
③已知该晶体的密度为 dg•cm-3,Cu2+和S2-的半径分别为apm和bpm,阿伏加 德罗常数值为NA。列式表示该晶体中原子的空间利用率________ 。
(1)铜元素基态原子的价电子排布式为
(2)铜元素能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。

①Cu2+与乙二胺所形成的配离子内部粒子间的作用力类型有
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
②乙二胺分子中氮原子的杂化轨道类型为
③乙二胺和三甲胺 [N(CH3)3]均属于胺,乙二胺的沸点比三甲胺高很多,原因是
(3)Cu2+在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+,其原因是
(4)Cu和S形成某种晶体的晶胞如图所示。

①该晶体的化学式为
②该晶胞原子坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为
③已知该晶体的密度为 dg•cm-3,Cu2+和S2-的半径分别为apm和bpm,阿伏加 德罗常数值为NA。列式表示该晶体中原子的空间利用率
您最近一年使用:0次
【推荐2】氢气的生产、存储是氢能应用的核心。目前较成熟的生产、存储路线之一为:利用甲醇(CH3OH)和H2O在Cu/Zn—Al催化剂存在下生产H2,H2与Mg在一定条件下化合制得储氢物质MgH2。
回答问题:
(1)根据原子核外电子排布特征
①Al在元素周期表中位于_______ 区(填“s”“p”“d”或“ds”)。
②基态Al原子的轨道表示式是_______ 。
③基态29Cu原子的价层电子排布式是_______ 。
(2)组成CH3OH分子的三种元素中,电负性最大的元素是_______ 。
(3)键能是衡量共价键稳定性的参数之一、甲醇的结构式为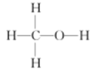 (可看作甲烷分子中的一个H原子被羟基取代的产物)。
(可看作甲烷分子中的一个H原子被羟基取代的产物)。
①甲醇分子的键参数中有_______ 种键能数据。
②由甲醇与水分子中都含有H-O键,解释“甲醇为非电解质,而水为弱电解质”的原因_______ 。
(4)作为储氢材料的MgH2,能发生水解反应产生氢气,该反应的化学方程式是_______ 。
回答问题:
(1)根据原子核外电子排布特征
①Al在元素周期表中位于
②基态Al原子的轨道表示式是
③基态29Cu原子的价层电子排布式是
(2)组成CH3OH分子的三种元素中,电负性最大的元素是
(3)键能是衡量共价键稳定性的参数之一、甲醇的结构式为
 (可看作甲烷分子中的一个H原子被羟基取代的产物)。
(可看作甲烷分子中的一个H原子被羟基取代的产物)。①甲醇分子的键参数中有
②由甲醇与水分子中都含有H-O键,解释“甲醇为非电解质,而水为弱电解质”的原因
(4)作为储氢材料的MgH2,能发生水解反应产生氢气,该反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】金属钛(22Ti)、铁(26Fe)及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为_____________ ,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有_________ 种。
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+ 易被氧化成Fe3+的原因是_____________ 。
(3)SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C N)和异硫氰酸(H-N=C=S)。
N)和异硫氰酸(H-N=C=S)。
①写出与SCN-互为等电子体的一种微粒______________ (分子或离子);
②硫氰酸分子中π键和σ键的个数之比为______________ ;
③异硫氰酸的沸点比硫氰酸沸点高的原因是__________________________________ 。
(4)TiCl3可用作烯烃定向聚合的催化剂,如:nCH3CH=CH2 。该反应涉及的物质中碳原子的杂化轨道类型有
。该反应涉及的物质中碳原子的杂化轨道类型有_______________________ ;反应涉及的元素中电负性最大的是_____________________________ 。
(5)Ti 的某氧化物和CaO相互作用能形成钛酸盐的晶胞结构如图所示(Ti4+ 位于立方体的顶点,Ca2+ 处于立方体的中心)。该晶体中,Ti4+和周围________ 个O2-紧邻;若该晶胞的密度为dg/cm3 则钛氧键的键长为________ cm(用含NA 的代数式表示)。
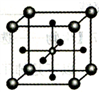
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+ 易被氧化成Fe3+的原因是
(3)SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C
 N)和异硫氰酸(H-N=C=S)。
N)和异硫氰酸(H-N=C=S)。①写出与SCN-互为等电子体的一种微粒
②硫氰酸分子中π键和σ键的个数之比为
③异硫氰酸的沸点比硫氰酸沸点高的原因是
(4)TiCl3可用作烯烃定向聚合的催化剂,如:nCH3CH=CH2
 。该反应涉及的物质中碳原子的杂化轨道类型有
。该反应涉及的物质中碳原子的杂化轨道类型有(5)Ti 的某氧化物和CaO相互作用能形成钛酸盐的晶胞结构如图所示(Ti4+ 位于立方体的顶点,Ca2+ 处于立方体的中心)。该晶体中,Ti4+和周围

您最近一年使用:0次



