下列实验能得出相关结论的是
| 实验操作 | 实验结论 | |
| A | 向NaHA溶液中滴加紫色石蕊溶液,溶液变为蓝色 | Kw>Ka1(H2A)·Ka2(H2A) |
| B | 常温下将铝片投入浓硝酸中,无明显现象 | 铝与浓硝酸不反应 |
| C | 向10mL0.1mol·L-1FeCl3溶液中加入5mL0.1mol·L-1KSCN溶液,溶液显红色,再滴加少量1mol·L-1KSCN溶液,红色加深 | Fe3+和SCN-的反应是可逆反应 |
| D | 向FeCl2溶液中滴加少量的酸性KMnO4溶液,KMnO4溶液褪色 | 氧化性: >Cl2 >Cl2 |
| A.A | B.B | C.C | D.D |
更新时间:2023-03-09 10:01:03
|
相似题推荐
单选题
|
困难
(0.15)
名校
解题方法
【推荐1】向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如下图所示。下列有关说法中正确的是
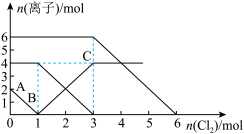

| A.离子的还原性顺序为:Fe2+>Br->I- |
| B.原混合溶液中FeBr2的物质的量为4mol |
| C.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3 |
| D.当通入2 mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐2】向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.则下列说法中不正确的是
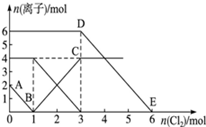

| A.还原性:I->Fe2+>Br- |
| B.原混合溶液中FeBr2的物质的量为3mol |
| C.线段AB表示Fe2+被氯气氧化 |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)═2:1:3 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐1】将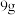 铜和铁的混合物投入
铜和铁的混合物投入 稀硝酸中,充分反应后得到标准状况下
稀硝酸中,充分反应后得到标准状况下 ,剩余
,剩余 金属;继续加入
金属;继续加入 等浓度的稀硝酸,金属完全溶解,又得到标准状况下
等浓度的稀硝酸,金属完全溶解,又得到标准状况下 。若向反应后的溶液中加入
。若向反应后的溶液中加入 溶液,溶液不变红,则下列说法不正确的是
溶液,溶液不变红,则下列说法不正确的是
A.原混合物中铜和铁各 |
B.稀硝酸的物质的量浓度为 |
C.第一次剩余的 金属为铜 金属为铜 |
D.向反应后的溶液中再加入该稀硝酸 ,又得到标准状况下的 ,又得到标准状况下的 |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐2】将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应;反应过程中放出 气体,向所得溶液中加入物质的量浓度为
气体,向所得溶液中加入物质的量浓度为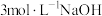 溶液至恰好沉淀完全,测得生成沉淀的质量比原合金的质量增加了
溶液至恰好沉淀完全,测得生成沉淀的质量比原合金的质量增加了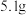 ,由此推断
,由此推断
 气体,向所得溶液中加入物质的量浓度为
气体,向所得溶液中加入物质的量浓度为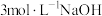 溶液至恰好沉淀完全,测得生成沉淀的质量比原合金的质量增加了
溶液至恰好沉淀完全,测得生成沉淀的质量比原合金的质量增加了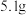 ,由此推断
,由此推断A.沉淀完全时消耗 溶液的体积为 溶液的体积为 |
B.参与反应的 的物质的量为 的物质的量为 |
C.合金的质量可能为 |
D.标准状况下,溶解合金时收集到 气体的体积为 气体的体积为 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
【推荐3】将 FeO 和Cu(NO3)2的混合物9.08 g加入到150 mL 1.0 mol ·L-1的稀硫酸中,待固体完全溶解后得到溶液 X。向溶液 X 中通入448 mL(已换算为标准状况)的Cl2得到溶液Y,此时溶液中的Fe2+恰好被完全氧化。下列叙述正确的是
| A.溶液X中的阳离子一定有Cu2+、Fe2+、H+,可能有Fe3+ |
| B.原混合物中 FeO 的质量为2.88 g |
| C.向溶液Y中加入足量铁粉,充分反应后产生标准状况下224 mL的H2 |
| D.向溶液Y中加入5 g铁粉,充分反应后得到不溶固体1.08g |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐1】在常温下,向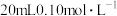 的
的 溶液中滴加
溶液中滴加 的盐酸,溶液pH随滴定百分率(%)的变化如图所示。下列说法
的盐酸,溶液pH随滴定百分率(%)的变化如图所示。下列说法不正确 的是

 的
的 溶液中滴加
溶液中滴加 的盐酸,溶液pH随滴定百分率(%)的变化如图所示。下列说法
的盐酸,溶液pH随滴定百分率(%)的变化如图所示。下列说法
A.在a点的溶液中,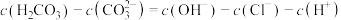 |
B.在b点的溶液中,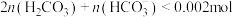 |
C.煮沸的目的是除去 ,使突跃变大,冷却后继续滴定到终点 ,使突跃变大,冷却后继续滴定到终点 |
D.若将 的盐酸换成同浓度的 的盐酸换成同浓度的 ,当滴至溶液的 ,当滴至溶液的 时, 时,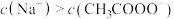 |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐2】常温下,用NaOH溶液滴定二元弱酸亚磷酸溶液,溶液中- 和-lgc(
和-lgc(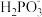 )或-
)或- 和-lgc(
和-lgc( )的关系如图所示,下列说法错误的是
)的关系如图所示,下列说法错误的是

 和-lgc(
和-lgc(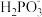 )或-
)或- 和-lgc(
和-lgc( )的关系如图所示,下列说法错误的是
)的关系如图所示,下列说法错误的是
A.L2表示- 和-lgc( 和-lgc( )的关系 )的关系 |
| B.H3PO3的电离常数Ka1(H3PO3)的数量级为10-2 |
C.等浓度等体积的H3PO3溶液与NaOH溶液充分混合,c( )<c(H3PO3) )<c(H3PO3) |
D.pH=6.54时,c(Na+ )<3c( ) ) |
您最近一年使用:0次
【推荐3】二元有机酸(H2X)的电离常数Ka1=1.67×10-8、Ka2=3.34×10-17。BaX难溶于水,常温下,将一定浓度的HY溶液,逐滴加入盛有一定量BaX固体的试管中,直到BaX全部溶解,测得混合液中c2(H+)与c2(Ba2+)的关系如图所示。下列说法错误的是
②0.192=0.0361,0.382=0.1444
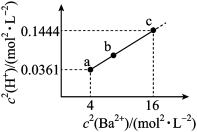
②0.192=0.0361,0.382=0.1444
| A.NaHX溶液显碱性 |
| B.溶度积Ksp(BaX)≈6.18×10-21mol2•L-2 |
| C.b点:2c(Ba2+)+c(H+)=2c(X2-)+c(HX-)+c(OH-)+c(Y-) |
| D.若0.1molBaX溶于25mLxmol•L-1HY溶液中得到c点溶液,则x≈8.38 |
您最近一年使用:0次




