2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1)要证明月壤中含有这些元素,可采用的方法是___________ 。
(2)写出铜的基态原子的电子排布式:___________ 。
(3)月球表面的月海玄武岩中富含钛和铁,将月海玄武岩用硝酸溶解,所得溶液用 检验,溶液呈红色。
检验,溶液呈红色。 中K、C、N的电负性从大到小的顺序是
中K、C、N的电负性从大到小的顺序是___________ ,C原子的杂化轨道类型是___________ , 的空间构型是
的空间构型是___________ 形,1
 中含有的
中含有的 键数目是
键数目是___________ 。
(4)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝( ,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于
,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于___________ (填晶体类型)。氮化铝可用氧化铝(熔点为2054℃)为原料来制取,从晶体类型角度分析 的熔点比氧化铝高的原因是
的熔点比氧化铝高的原因是___________ 。
②氮化铝的晶体结构如图所示,其中铝原子的配位数是___________ , 与N原子最近的距离为a
与N原子最近的距离为a ,则该晶体的密度为
,则该晶体的密度为___________  。(
。( 为阿伏加德罗常数的值,列出表达式即可)
为阿伏加德罗常数的值,列出表达式即可)

(1)要证明月壤中含有这些元素,可采用的方法是
(2)写出铜的基态原子的电子排布式:
(3)月球表面的月海玄武岩中富含钛和铁,将月海玄武岩用硝酸溶解,所得溶液用
 检验,溶液呈红色。
检验,溶液呈红色。 中K、C、N的电负性从大到小的顺序是
中K、C、N的电负性从大到小的顺序是 的空间构型是
的空间构型是
 中含有的
中含有的 键数目是
键数目是(4)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝(
 ,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于
,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于 的熔点比氧化铝高的原因是
的熔点比氧化铝高的原因是②氮化铝的晶体结构如图所示,其中铝原子的配位数是
 与N原子最近的距离为a
与N原子最近的距离为a ,则该晶体的密度为
,则该晶体的密度为 。(
。( 为阿伏加德罗常数的值,列出表达式即可)
为阿伏加德罗常数的值,列出表达式即可)
更新时间:2023-03-12 10:45:38
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式:_______ 。
(2)B元素基态原子中能量最高的电子,其电子云在空间有_______ 个方向,原子轨道呈_______ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为: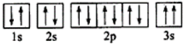 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了_______ 。
(4)G位于_______ 族_______ 区,该元素的核外电子排布式为_______ 。
(5)DE3中心原子的杂化方式为_______ ,用价层电子对互斥理论推测其空间构型为____ 。
(6)检验F元素的方法是_______
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: I1=738kJ·mol﹣1 I2=1451kJ·mol﹣1 I3=7733kJ·mol﹣1 I4=10540kJ·mol﹣1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:
(2)B元素基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为:
 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了(4)G位于
(5)DE3中心原子的杂化方式为
(6)检验F元素的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F是原子序数依次增大的6种短周期元素,A元素原子的2p原子轨道上有2个未成对的电子,B元素在同周期元素中原子半径最大,与A可形成原子个数比为1:1和2:1的两种化合物,C单质是一种常见的半导体材料,F有9个原子轨道,且只有一个未成对电子,没有空轨道。
(1)C元素在元素周期表中的位置_______
(2)EF2中心原子杂化轨道类型为_______ 杂化,VSEPR模型为_______ ,空间结构为_______
(3)P4S3可用于制造火柴,其分子结构如图所示。

①P4S3分子中硫原子的杂化轨道类型为_______ 。
②每个P4S3分子中含孤电子对的数目为_______ 。
③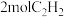 分子中含有
分子中含有_______  键
键
(1)C元素在元素周期表中的位置
(2)EF2中心原子杂化轨道类型为
(3)P4S3可用于制造火柴,其分子结构如图所示。

①P4S3分子中硫原子的杂化轨道类型为
②每个P4S3分子中含孤电子对的数目为
③
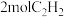 分子中含有
分子中含有 键
键
您最近一年使用:0次
【推荐3】有五种短周期元素,它们的结构或性质等信息如下表所示:
请根据表中信息回答下列问题:
(1)A元素基态原子的核外电子排布式为______________ 。
(2)B元素在元素周期表中的位置为_________ ;离子半径:B___________ (填“>”或“<”)A。
(3)C元素基态原子的核外电子轨道表示式为________ ,其原子核外有_______ 个未成对电子,能量最高的电子排布在_______ 轨道上。
(4)D元素基态原子的核外电子排布式为______  的结构示意图为
的结构示意图为__________ 。
(5)C、E元素的第一电离能的大小关系是_______ (用元素符号表示)。
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是______ (填元素符号),CD3与水反应后的产物是______ (填化学式)。
| 元素 | 结构或性质 |
| A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
| E | 元素原子的L电子层上有2对成对电子 |
(1)A元素基态原子的核外电子排布式为
(2)B元素在元素周期表中的位置为
(3)C元素基态原子的核外电子轨道表示式为
(4)D元素基态原子的核外电子排布式为
 的结构示意图为
的结构示意图为(5)C、E元素的第一电离能的大小关系是
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是
您最近一年使用:0次
【推荐1】有五种短周期元素,它们的结构或性质等信息如下表所示:
请根据表中信息回答下列问题:
(1)A元素基态原子的核外电子排布式为______________ 。
(2)B元素在元素周期表中的位置为_________ ;离子半径:B___________ (填“>”或“<”)A。
(3)C元素基态原子的核外电子轨道表示式为________ ,其原子核外有_______ 个未成对电子,能量最高的电子排布在_______ 轨道上。
(4)D元素基态原子的核外电子排布式为______  的结构示意图为
的结构示意图为__________ 。
(5)C、E元素的第一电离能的大小关系是_______ (用元素符号表示)。
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是______ (填元素符号),CD3与水反应后的产物是______ (填化学式)。
| 元素 | 结构或性质 |
| A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
| E | 元素原子的L电子层上有2对成对电子 |
(1)A元素基态原子的核外电子排布式为
(2)B元素在元素周期表中的位置为
(3)C元素基态原子的核外电子轨道表示式为
(4)D元素基态原子的核外电子排布式为
 的结构示意图为
的结构示意图为(5)C、E元素的第一电离能的大小关系是
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】据媒体报道,法国一家公司Tiamat日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池,预计从2020年开始实现工业生产。该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。
回答下列问题:
(1)Te属于元素周期表中_____ 区元素,其基态原子的价电子排布式为_____ 。
(2)基态Na原子中,核外电子占据的原子轨道总数为____ ,最高能层电子云轮廓图形状为_____
(3)结合题中信息判断:C、O、Cl的电负性由大到小的顺序为_____ (用元素符号表示)。
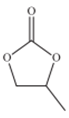
(4)CO32-的几何构型为______ ;碳酸丙烯酯的结构简式如图所示,则其中碳原子的杂化轨道类型为_________ ,1mol碳酸丙烯酯中键的数目为________ .
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是_____ ,该配离子包含的作用力为__ (填选项字母)。
A.离子键 B.极性键 C.配位键 D.氢键 E.金属键
(6)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为______ ,该晶胞的密度为ρg/cm3,阿伏伽德罗常数的值为NA,则Na与O之间的最短距离为_____ cm(用含ρ、NA的代数式表示)。
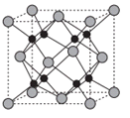
回答下列问题:
(1)Te属于元素周期表中
(2)基态Na原子中,核外电子占据的原子轨道总数为
(3)结合题中信息判断:C、O、Cl的电负性由大到小的顺序为
(4)CO32-的几何构型为

(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是
A.离子键 B.极性键 C.配位键 D.氢键 E.金属键
(6)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】VCU研发的锂超离子导体Li3SBF4,提升了固态电解质导电性,其制备反应为LiBF4+Li2S=Li3SBF4。
回答下列问题:
(1)基态硫原子中核外电子有____ 种运动状态;组成锂超离子导体的四种元素中,电负性最大的元素的价层电子排布式为____ 。
(2)S的常见含氧酸有H2SO3和H2SO4,其中酸根离子呈三角锥形结构的酸是____ (填化学式),该分子的中心原子的价层电子对数是____ ;含F有机酸CF3COOH比CCl3COOH的酸性____ (填“强”或“弱”),原因为____ 。
(3)BF3与F-形成 时,二者形成的化学键为
时,二者形成的化学键为____ 键,提供电子对的原子为____ (填元素符号), 中B的杂化方式为
中B的杂化方式为____ 。
(4)另一种含锂电极材料LiFePO4的晶胞结构如图所示,晶胞参数分别为anm、bnm、cnm,其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构,每个晶胞中含Fe和P的数目分别为___ 、___ ;设NA为阿伏加德罗常数的值,LiFePO4的密度ρ=___ g•cm-3(用含a、b、c、NA的代数式表示)。
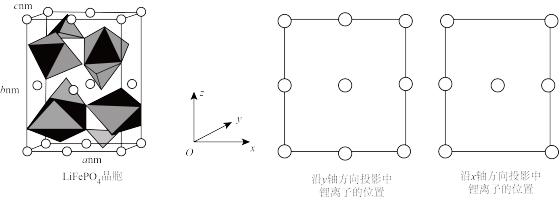
回答下列问题:
(1)基态硫原子中核外电子有
(2)S的常见含氧酸有H2SO3和H2SO4,其中酸根离子呈三角锥形结构的酸是
(3)BF3与F-形成
 时,二者形成的化学键为
时,二者形成的化学键为 中B的杂化方式为
中B的杂化方式为(4)另一种含锂电极材料LiFePO4的晶胞结构如图所示,晶胞参数分别为anm、bnm、cnm,其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构,每个晶胞中含Fe和P的数目分别为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】黄铜矿(CuFeS2)是炼铜的最主要矿物,火法炼铜时发生反应:2CuFeS2+O2=Cu2S+2FeS+SO2。
(1)Fe在周期表中的位置为__________ ;Fe、S、O原子的第一电离能由大到小的顺序是____________ 。
(2)CuFeS2中Cu元素有________ 个未成对电子,Cu2S中Cu元素基态时电子排布式为_____________ 。
(3)SO2分子的立体构型为________ ,SO2可氧化生成SO3,SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图,此固态SO3中S原子的杂化轨道类型是________ 。
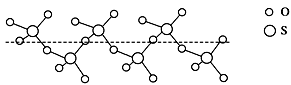
(4)已知FeO、FeS熔点分别为1369℃、1193℃,解释熔点FeO高于FeS 的原因__________________ 。
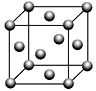
(5)Cu的晶胞如图所示,晶体密度为ρ g·cm-3。晶胞中等距最近的Cu原子有________ 个,晶胞的边长为____________________ (用含ρ和NA的式子表示)。
(1)Fe在周期表中的位置为
(2)CuFeS2中Cu元素有
(3)SO2分子的立体构型为

(4)已知FeO、FeS熔点分别为1369℃、1193℃,解释熔点FeO高于FeS 的原因

(5)Cu的晶胞如图所示,晶体密度为ρ g·cm-3。晶胞中等距最近的Cu原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】碳和硅是中学常见元素,其单质及化合物有独特的性质和用途。回答问题:
(1)基态碳原子的电子排布图为___ ,CO2属于___ 分子(选填“极性”或“非极性”);
(2)60克SiO2晶体中含有的Si-O键数目为___ (用NA表示);
(3)有机物M( )中碳的杂化类型有
)中碳的杂化类型有__ ,除氢原子之外的其它元素原子的第一电离能由大到小的顺序为__ ;
(4)碳元素能形成多种单质如金刚石、石墨、C60等,回答下列问题:
(Ⅰ)C60的晶体类型是__ 晶体。
(Ⅱ)石墨是一种混合晶型,结构中具有的作用力有___ 。
a.共价键 b.分子间作用力 c.氢键 d.金属键 e.离子键
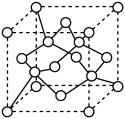
(Ⅲ)金刚石晶胞结构如图所示,假设金刚石晶胞的边长为a cm,阿伏加 德罗常数为NA,则金刚石的密度可以表示为___ g/cm3。
(1)基态碳原子的电子排布图为
(2)60克SiO2晶体中含有的Si-O键数目为
(3)有机物M(
 )中碳的杂化类型有
)中碳的杂化类型有(4)碳元素能形成多种单质如金刚石、石墨、C60等,回答下列问题:
(Ⅰ)C60的晶体类型是
(Ⅱ)石墨是一种混合晶型,结构中具有的作用力有
a.共价键 b.分子间作用力 c.氢键 d.金属键 e.离子键
(Ⅲ)金刚石晶胞结构如图所示,假设金刚石晶胞的边长为a cm,阿伏加 德罗常数为NA,则金刚石的密度可以表示为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
(1)某同学根据上述信息,推断B的核外电子排布如右图所示,该同学所画的电子排布图违背了_________ 。

(2)ACl2分子中A的杂化类型为________ 。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确____ ,并阐述理由______________________ 。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式_________ ,该物质的K原子和C60分子的个数比为__________ 。

(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是__________ ,NCl3分子的VSEPR模型为________ 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为______ 。
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |

(2)ACl2分子中A的杂化类型为
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式

(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】海洋是元素的摇篮,海水中含有的大量元素在生产、生活、科学研究等多方面具有重要作用。回答下列问题:
(1)写出基态溴原子的价电子排布式_______ ,氟、氯、溴、氧四种元素中,电负性由大到小的顺序为_______ (填元素符号)
(2)X射线衍射测定等发现,I3AsF6中存在I 离子。I
离子。I 离子的几何构型为
离子的几何构型为_______ ,中心原子的杂化类型为_______
(3)C原子可以形成多种有机物,如图所示是一种吡啶和一种嘌呤的结构,两种分子中所有原子都在一个平面上
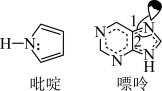
①1 mol吡啶分子中含有σ键数目是_______ NA
②嘌呤中轨道之间的夹角∠1比∠2大,解释原因_______
③分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 )。该吡啶和嘌呤中都含有大π键,则该吡啶中的大π键表示为
)。该吡啶和嘌呤中都含有大π键,则该吡啶中的大π键表示为_______
(4)CaF2可用于冶金、化工和建材等很多行业,为立方晶胞,结构如下图所示:

①“原子坐标参数”可表示晶胞内部各原子的相对位置,已知A、B两点的原子坐标参数如图所示,则C点的“原子坐标参数”为(_______,_______, ),
),_______
②已知晶胞参数为0.5462 nm,阿伏加德罗常数的值为NA,则其密度为_______ g·cm-3 (列出计算式即可)
(1)写出基态溴原子的价电子排布式
(2)X射线衍射测定等发现,I3AsF6中存在I
 离子。I
离子。I 离子的几何构型为
离子的几何构型为(3)C原子可以形成多种有机物,如图所示是一种吡啶和一种嘌呤的结构,两种分子中所有原子都在一个平面上

①1 mol吡啶分子中含有σ键数目是
②嘌呤中轨道之间的夹角∠1比∠2大,解释原因
③分子中的大π键可以用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 )。该吡啶和嘌呤中都含有大π键,则该吡啶中的大π键表示为
)。该吡啶和嘌呤中都含有大π键,则该吡啶中的大π键表示为(4)CaF2可用于冶金、化工和建材等很多行业,为立方晶胞,结构如下图所示:

①“原子坐标参数”可表示晶胞内部各原子的相对位置,已知A、B两点的原子坐标参数如图所示,则C点的“原子坐标参数”为(_______,_______,
 ),
),②已知晶胞参数为0.5462 nm,阿伏加德罗常数的值为NA,则其密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硼和硼的化合物在工业上有着广泛的用途。
(1)基态硼原子的电子排布式为___________________________ 。
(2)晶体硼的基本结构单元是由硼原子构成的正二十面体(如下图),其中有20个等边三角形的面和一定数目的顶点,每个顶点各有一个硼原子。此结构单元中含有硼原子的数目为________________ 。

(3)氮化硼(BN)晶体有多种结构。六方氮化硼与石墨相似,具有层状结构,可作高温润滑剂。立方氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。关于这两种晶体的说法中,正确的是____ (填标号)。

a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的 B—N 键均为共价键
d.两种晶体均为分子晶体
(4)六方氮化硼晶体内硼原子的杂化方式为________ ,该晶体不导电的原因是___________ 。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。与BF4—互为等电子体的一种分子的化学式为__ , lmolNH4BF4晶体中含有配位键的数目为_____________ 。
(6)立方氮化硼的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,则立方氮化硼的一个晶胞中含有______ 个硼原子,立方氮化硼的密度是____ g•cm-3(只要求列算式,不必计算出数值,阿伏加 德罗常数为NA)。
(1)基态硼原子的电子排布式为
(2)晶体硼的基本结构单元是由硼原子构成的正二十面体(如下图),其中有20个等边三角形的面和一定数目的顶点,每个顶点各有一个硼原子。此结构单元中含有硼原子的数目为

(3)氮化硼(BN)晶体有多种结构。六方氮化硼与石墨相似,具有层状结构,可作高温润滑剂。立方氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。关于这两种晶体的说法中,正确的是

a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的 B—N 键均为共价键
d.两种晶体均为分子晶体
(4)六方氮化硼晶体内硼原子的杂化方式为
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。与BF4—互为等电子体的一种分子的化学式为
(6)立方氮化硼的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,则立方氮化硼的一个晶胞中含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】周期表中前四周期的元素A、Z、Q、R、T的原子序数依次增大,且A、Z、Q同周期。A共有两个原子轨道上有电子,且电子数目相同。Z、Q相邻,且Z中的未成对电子数为3个,R元素在地壳中含量位于金属元素的第二位。T是人类最早使用的元素,并以这种元素命名了我国的一个时代。请回答下面的问题:
(1)A、Z、Q第一电离能从小到大的顺序为:_______________ (填元素符号),T的价层电子排布图为:__________________________ 。
(2)Q的基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈_______ 形。
(3)Z3-的立体构型为____________ ,写出与Z3-互为等电子体的一种非极性分子化学式____________ 。
(4)在不同的温度下,A以ACl2和二聚体A2Cl4两种形式存在,二聚体的结构式如图所示:

①ACl2中A的杂化方式为______________________ 。
②1mol A2Cl4中含配位键的数目为____________ 。
(5)R单质的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。体心立方晶胞和面心立方晶胞的棱边长分别为acm、bcm,则R单质的体心立方晶胞和面心立方晶胞的密度之比为_________ ,R原子配位数之比为_____________ 。

(1)A、Z、Q第一电离能从小到大的顺序为:
(2)Q的基态原子中能量最高的电子,其电子云在空间有
(3)Z3-的立体构型为
(4)在不同的温度下,A以ACl2和二聚体A2Cl4两种形式存在,二聚体的结构式如图所示:

①ACl2中A的杂化方式为
②1mol A2Cl4中含配位键的数目为
(5)R单质的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。体心立方晶胞和面心立方晶胞的棱边长分别为acm、bcm,则R单质的体心立方晶胞和面心立方晶胞的密度之比为

您最近一年使用:0次



