(1)选择合适的催化剂,一定条件下可直接光催化分解
 ,发生反应:
,发生反应: ,该反应的
,该反应的
(2)写出氯碱工业原理的离子反应方程式:
(3)亚硫酸
 溶液存在电离平衡:
溶液存在电离平衡: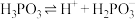 ,
,
①已知25℃时,
 的
的 溶液中,
溶液中, 的电离度为
的电离度为 ,
, 的一级电离平衡常数
的一级电离平衡常数
 的计算式表示,
的计算式表示, 第二步电离忽略不计,忽略水的电离)。
第二步电离忽略不计,忽略水的电离)。②常温下,将NaOH溶液滴加到亚硝酸
 溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示
溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示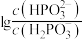 的是曲线
的是曲线 的
的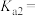
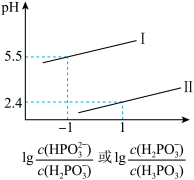
③请结合相关的平衡常数判断
 稀溶液显
稀溶液显(4)25℃时,HF的电离常数
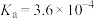 ;
; 的电离常数为
的电离常数为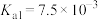 ,
, ,
,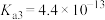 。足量NaF溶液和
。足量NaF溶液和 溶液反应的离子方程式为:
溶液反应的离子方程式为:相似题推荐
 、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。
、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。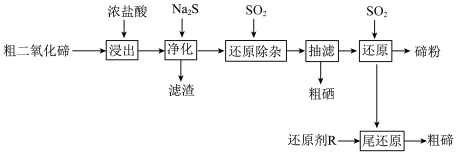
(1)“浸出”步骤中,碲和硒两种元素分别转化为
 和
和 。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是
。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是(2)
 的沸点(387℃)高于
的沸点(387℃)高于 的沸点(191.4℃),原因是
的沸点(191.4℃),原因是(3)“净化”步骤中产生的滤渣主要含
(4)化学反应的吉布斯自由能变
 。
。 还原
还原 和
和 的
的 随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过
随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过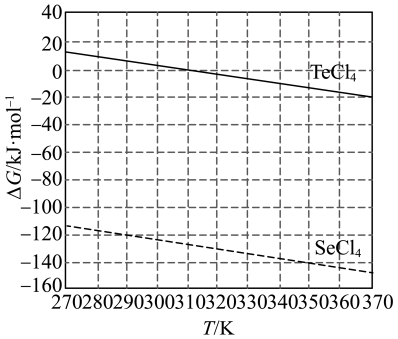
(6)“还原”后的酸性还原尾液中含有少量未被还原的碲,加入还原剂R进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是
A.铁粉 B.氢气 C.硫化钠
(1)已知在101kPa、150℃时,各1mol的碳、一氧化碳和氢气在足量的氧气充分燃烧并恢复至原温度,所放出的热量分别为393.7kJ/mol、283.0kJ/mol、242.0 kJ/mol,请写出煤的气化反应的热化学方程式
(2)在恒容密闭容器里,按物质的量比1:1加入一定量的碳和水蒸气反应生成水煤气。一定条件下达到平衡,当改变反应的某一条件时,下列变化能说明平衡一定向正反应方向移动的是
A.正反应速率先增大后减少 B.化学平衡常数K减少
C.混合气体的平均相对分子质量减少 D.反应物气体体积分数增大
(3)一定条件下煤的气化产物还可以发生反应,700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g)+ H2(g) 反应过程中测定的部分数据见下表:
CO2(g)+ H2(g) 反应过程中测定的部分数据见下表:
反应时间/ min | n(CO)/ mol | n(H2O)/ mol |
0 | 1.20 | 0.60 |
5 | 0.80 | |
10 | 0.20 |
请根据表格回答下列问题:
①计算反应在5min内由氢气表示的平均速率为:
②列式并计算该反应在700℃时的化学平衡常数K=
③将上表中达平衡后的混合气体恢复至室温,用200mL2mol/LNaOH溶液进行吸收,充分反应后假设溶液体积不变,下列说法不正确的是:(已知HCO3-电离常数约为4 10-11,CaCO3的溶度积常数约为3
10-11,CaCO3的溶度积常数约为3 10-9)___________
10-9)___________
A.c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
B.c(H2CO3)<c(CO32-)
C.c(Na+)+c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D.向该溶液中加入等体积等浓度的CaCl2溶液产生白色沉淀
(1)氨热分解法制氢:反应原理为
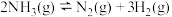
 ,一定温度下,向2L恒容密闭容器(含有适量催化剂,其体积忽略不计)中充入2
,一定温度下,向2L恒容密闭容器(含有适量催化剂,其体积忽略不计)中充入2
 发生上述反应,5min末达到平衡状态,此时
发生上述反应,5min末达到平衡状态,此时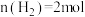 。
。①该反应正反应的活化能
②0~5min内该反应的平均速率

 ,平衡常数
,平衡常数
 。
。③该反应达到平衡状态时,若其他条件不变,向容器中再充入1

 时,
时,
 ,达到新平衡时,
,达到新平衡时, 的转化率小于原平衡的转化率,其原因是
的转化率小于原平衡的转化率,其原因是(2)氨电解法制氢:利用电解原理,将氨转化为高纯氢气,其工作原理如图所示。
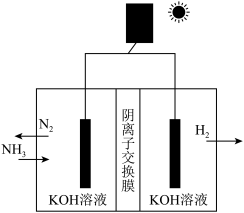
①图中太阳能电池的主要材料是
②阳极电极反应式为
(1)将0.10mol/L NH3•H2O溶液稀释10倍,则稀释后的溶液中c(OH﹣)
(2)实验测得0.10mol/L CH3COONH4溶液的pH=7,则c(CH3COO-)
(3)利用反应:I2+2Na2S2O3=Na2S4O6+2NaI可以定量测定市售硫代硫酸钠(M=158)的纯度,现在称取7.900g硫代硫酸钠固体样品,配成250mL的溶液,取25.00mL置于锥形瓶中,加入指示剂,用含有I2为 0.1000mol/L的碘水滴定,消耗碘水20.00mL,则:
①滴定应选择的指示剂是
②对于该滴定实验的有关操作或误差分析正确的是
A.滴定前,应对滴定管、锥形瓶进行润洗操作
B.滴定过程中,标准液滴到锥形瓶外,会使所测结果偏大
C.滴定管在滴定开始时尖嘴有气泡,滴定完成后气泡消失,则所测得的纯度将会偏小
D.滴定前仰视读数而滴定结束时平视读数,则所测得的纯度将会偏小
③样品中硫代硫酸钠纯度为
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀加入CaCl2溶液的最小浓度为
I.探究Na2SO3溶液与FeCl3溶液的反应原理
某兴趣小组进行了如下实验:
| 装置 | 现象 |
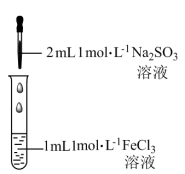 | 现象i:一开始液体颜色加深,由棕黄色变为红褐色。 现象ii:一段时间后液体颜色变浅,变为浅黄色。 |
(2)针对上述现象,小组成员展开讨论,甲同学认为Fe3+与SO
 发生了相互促进的水解反应得到一种胶体,其离子方程式为
发生了相互促进的水解反应得到一种胶体,其离子方程式为 还发生了氧化还原反应,并依据反应现象判断出两种反应活化能较大的是
还发生了氧化还原反应,并依据反应现象判断出两种反应活化能较大的是经查阅资料和进一步实验探究,证实了SO
 与Fe3+既发生了水解反应又发生了氧化还原反应。
与Fe3+既发生了水解反应又发生了氧化还原反应。II.Na2SO3溶液作吸收剂
工业上可用Na2SO3溶液吸收SO2。已知25°C时,H2SO3的电离常数Ka1=1.0×10-2,Ka2=6.2×10-8。
(3)25°C时,NaHSO3的水解常数为Kh=
(4)25°C时,用Na2SO3溶液吸收SO2至pH=7时,溶液中各离子浓度的大小关系为
 将
将(1)25℃时,物质的量浓度均为0.1mol/L的几种盐溶液的pH如下表所示。
| 序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 溶液 | NaClO溶液 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |
| pH | 10.3 | 8.4 | 7 | 5 |
②溶液Ⅱ中阴离子浓度由大到小的顺序:
③溶液Ⅲ中,
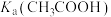
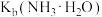 。
。④溶液Ⅳ中,由水电离产生的

 。
。(2)几种离子开始沉淀时的pH如下表所示。
| 离子 |  |  |  |
| pH | 7.6 | 4.4 | 10.4 |
 、
、 、
、 的溶液中滴加氢氧化钠溶液,
的溶液中滴加氢氧化钠溶液,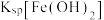
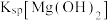 。
。②25℃时,若要使
 硫酸铜溶液中的
硫酸铜溶液中的 沉淀较为完全[使
沉淀较为完全[使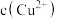 降至原来的千分之一],则应向溶液中加入氢氧化钠溶液,使溶液的pH为
降至原来的千分之一],则应向溶液中加入氢氧化钠溶液,使溶液的pH为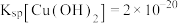 )
)(3)该小组同学利用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
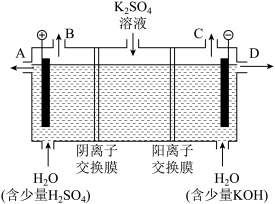
该电解池的阳极反应式为

(1)打开分液漏斗a的旋塞,浓硫酸不能顺利流下,原因可能是
(2)实验室通常使用亚硫酸钠固体与70%硫酸溶液反应制备SO2,此方法与用浓硫酸与铜反应制备SO2相比,优点是:①
(3)装置B的作用是
(4)探究实验:向NaHSO3溶液中加入NaClO溶液时,反应有二种可能的情况:
I.NaHSO4与NaClO恰好完全反应,此时反应的离子方程式为
II.NaHSO3过量;
III.NaClO过量。
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪种情况,请完成下表:
(已知: H2SO3;Ka1=1.54×10-2,Ka2=1.02×10-7;H2CO3:Ka1=4.3×10-7,Ka2=5.61×10-11;HClO:Ka=3×10-8)
| 序号 | 实验操作 | 现象 | 结论 |
| ① | 加入少量CaCO3粉末 | I或II | |
| ② | 滴加少量淀粉-KI溶液,振荡 | 溶液先变蓝后褪色 | |
| ③ | II |
 ,会引起酸雨、光化学烟雾等问题。
,会引起酸雨、光化学烟雾等问题。(1)
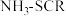 脱硝。该技术是在催化剂的作用下将烟气中的
脱硝。该技术是在催化剂的作用下将烟气中的 还原为无污染的
还原为无污染的 、
、 。该过程涉及的主要反应为:
。该过程涉及的主要反应为:ⅰ.
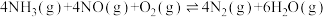

ⅱ.


ⅲ.
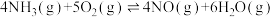
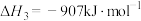
①


②保持温度为T,在2L密闭容器中发生反应ⅱ,投料比
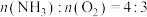 ,投料量相同,测得不同催化剂对
,投料量相同,测得不同催化剂对 生成量的影响如下图所示。下列说法正确的有
生成量的影响如下图所示。下列说法正确的有

B.反应活化能:
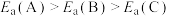
C.平衡后,使用催化剂A的容器内压强最大
D.反应物的转化率:
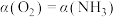
(2)络合脱硝法。利用过渡金属与配体螯合形成的络合液将NO由气相络合转为液相。研究表明乙二胺四乙酸(EDTA,可简写为
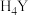 )鳌合亚铁生成的络合液
)鳌合亚铁生成的络合液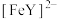 对NO具有较高脱除效率。
对NO具有较高脱除效率。①已知
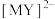 结构如图(
结构如图(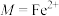 、
、 ……),则提供孤电子对的原子是
……),则提供孤电子对的原子是
 键。
键。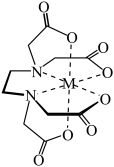
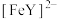 )络合脱硝反应过程如下:
)络合脱硝反应过程如下:(a)
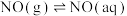
(b)
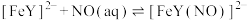
(c)
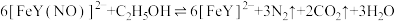 (Fe(Ⅱ)-EDTA再生)
(Fe(Ⅱ)-EDTA再生)(d)
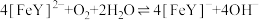 (副反应)
(副反应)步骤(c)所用试剂除
 外,还可选择
外,还可选择 ”或“NaClO”)。
”或“NaClO”)。③
 会与溶液中的
会与溶液中的 形成多种配合物。当
形成多种配合物。当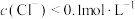 时,溶液中主要存在下列两个平衡:
时,溶液中主要存在下列两个平衡: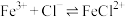
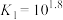
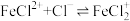
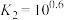
改变
 起始浓度,测得平衡时
起始浓度,测得平衡时 、
、 和
和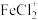 的物质的量分数
的物质的量分数 随
随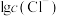 的部分变化如图所示。
的部分变化如图所示。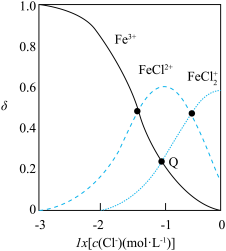
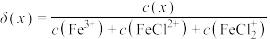 ,若Q点
,若Q点 对应的起始浓度
对应的起始浓度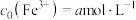
(Ⅰ)求Q点溶液中
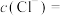
 ;
;(Ⅱ)计算Q点溶液中
 的平衡转化率
的平衡转化率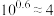 )
)
| 化学式 | CH3COOH | H2CO3 | HCN | HClO | NH3∙H2O |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=6.2×10-10 | Ka=3.0×10-8 | Kb=1.8×10-5 |
| A.CH3COONa | B.Na2CO3 | C.NaCN | D.NaClO |
A.c(H+) B.
 C.c(H+)∙c(OH-) D.
C.c(H+)∙c(OH-) D. E.
E.
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将amol•L-1的醋酸溶液与bmol•L-1氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=
(5)标准状况下将2.24LCO2通入100mL 1mol•L-1NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=c(H2CO3)+
(6)25℃,氨水的浓度为2.0mol•L-1,溶液中的c(OH-)=
 )=
)= )。(填“>”、“<”或“=”)
)。(填“>”、“<”或“=”)



