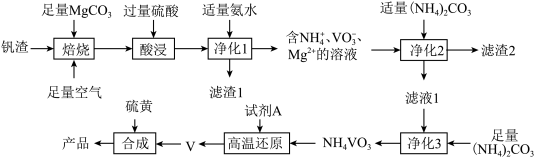
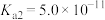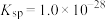科学家最近合成了VS2和VS相互交叉排列晶体.某小组以钒渣(含72%V2O3、14%Fe2O3、9%Al2O3、3%CuO,其余为有机杂质)为原料制备VS、VS2的流程如图:
已知部分信息如下:
含钒离子在溶液中的主要存在形式与pH的关系如表所示。
②常温下,几种难溶电解质的溶度积如表:
③NH4VO3是白色粉末,微溶于冷水。
回答下列问题:
(1)基态V原子的核外电子排布式为______ ,NH 的空间结构为
的空间结构为______ 。
(2)“焙烧”时通入足量空气的目的是_____ 。
(3)“净化1”中,如果氨水过量,可能产生的影响是______ (填一种)。
(4)若“净化1”中调节pH=5,则c(Cu2+)=______ mol•L-1。
(5)“净化3”中洗涤NH4VO3时选择的洗涤剂为______ (填“冷水”或“热水”)。
(6)当试剂A为CO时,写出“高温还原”时发生反应的化学方程式:______ 。
(7)某工厂用1吨该钒渣制备VS、VS2,若该工艺流程中,V的损耗率为5%,则最终得到产品的质量为______ kg。[已知产品中n(VS):n(VS2)=1:1]。

已知部分信息如下:
含钒离子在溶液中的主要存在形式与pH的关系如表所示。
| pH | 4~6 | 6~8 | 8~10 |
| 主要离子 | VO | VO | V2O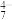 |
②常温下,几种难溶电解质的溶度积如表:
| 难溶电解质 | Cu(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| Ksp | 2.2×10-22 | 4.0×10-38 | 1.3×10-33 | 1.8×10-11 |
③NH4VO3是白色粉末,微溶于冷水。
回答下列问题:
(1)基态V原子的核外电子排布式为
 的空间结构为
的空间结构为(2)“焙烧”时通入足量空气的目的是
(3)“净化1”中,如果氨水过量,可能产生的影响是
(4)若“净化1”中调节pH=5,则c(Cu2+)=
(5)“净化3”中洗涤NH4VO3时选择的洗涤剂为
(6)当试剂A为CO时,写出“高温还原”时发生反应的化学方程式:
(7)某工厂用1吨该钒渣制备VS、VS2,若该工艺流程中,V的损耗率为5%,则最终得到产品的质量为
更新时间:2023-04-30 12:11:18
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
【推荐1】铬盐广泛应用于冶金、电镀、军工等行业。工业上以铬铁矿(主要成分为 和FeO,含有少量
和FeO,含有少量 、
、 、CaO和MgO杂质)为原料,制备重铬酸钠以及草酸亚铁,工艺流程如下:
、CaO和MgO杂质)为原料,制备重铬酸钠以及草酸亚铁,工艺流程如下: 易转化为
易转化为 。
。
② ;
;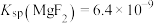 。
。
(1)基态Cr的价层电子排布式为___________ 。
(2)煅烧过程中,铬、铝、硅转化为相应最高价态含氧酸盐,写出 反应的化学方程式
反应的化学方程式___________ 。
(3)滤渣1的主要成分为___________ ,调pH时,pH值不宜过小的原因是___________ 。
(4)加入氟化钠溶液可将 、
、 沉淀除去,若“沉钙、沉镁”后所得滤液中
沉淀除去,若“沉钙、沉镁”后所得滤液中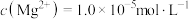 时,则滤液中
时,则滤液中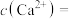
___________  。
。
(5)“沉铁”步骤中加入草酸氢铵溶液,反应的离子方程式为___________ 。
(6)氧化亚铁属于立方晶系(晶体结构类似于氯化钠晶体),其晶胞参数为a nm。距离 最近的
最近的 有
有___________ 个,该晶胞的密度
___________  (列出计算式即可,
(列出计算式即可, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
 和FeO,含有少量
和FeO,含有少量 、
、 、CaO和MgO杂质)为原料,制备重铬酸钠以及草酸亚铁,工艺流程如下:
、CaO和MgO杂质)为原料,制备重铬酸钠以及草酸亚铁,工艺流程如下: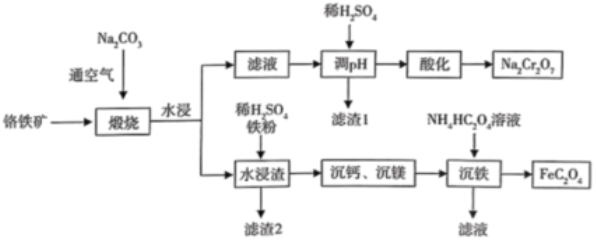
 易转化为
易转化为 。
。②
 ;
;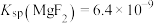 。
。(1)基态Cr的价层电子排布式为
(2)煅烧过程中,铬、铝、硅转化为相应最高价态含氧酸盐,写出
 反应的化学方程式
反应的化学方程式(3)滤渣1的主要成分为
(4)加入氟化钠溶液可将
 、
、 沉淀除去,若“沉钙、沉镁”后所得滤液中
沉淀除去,若“沉钙、沉镁”后所得滤液中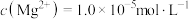 时,则滤液中
时,则滤液中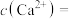
 。
。(5)“沉铁”步骤中加入草酸氢铵溶液,反应的离子方程式为
(6)氧化亚铁属于立方晶系(晶体结构类似于氯化钠晶体),其晶胞参数为a nm。距离
 最近的
最近的 有
有
 (列出计算式即可,
(列出计算式即可, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】碳酸铈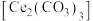 ]是一种稀土材料,工业上常以氟碳铈矿(主要成分为
]是一种稀土材料,工业上常以氟碳铈矿(主要成分为 、
、 、
、 )为原料制备碳酸铈,其工艺流程如图所示:
)为原料制备碳酸铈,其工艺流程如图所示:
①“酸浸”后铈元素主要以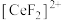 的形式存在;
的形式存在;
② 在空气中易被氧化为
在空气中易被氧化为 ,两者均能形成氢氧化物沉淀。
,两者均能形成氢氧化物沉淀。
(1)“焙烧”时,从焙烧室的底部通入空气的目的是____________________ 。
(2)“滤渣1”的主要成分为__________ 。
(3)“还原”时,加入硫脲( )的目的是将
)的目的是将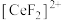 还原为
还原为 ,硫脲被氧化为
,硫脲被氧化为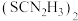 。
。
①该反应的离子方程式为____________________ 。
②硫脲属于__________ (填“极性”或“非极性”)分子,该分子中键角
__________ 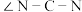 (填“>”“<”或“=”)
(填“>”“<”或“=”)
(4)“碱转酸浸”在加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为______________________________________________________________________ 。
(5)若“沉淀”后,溶液的pH为6,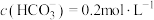 ,此时
,此时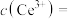
__________ 。已知常温下:
(6)某研究小组利用硫化锌锂电池电解含Ce(Ⅱ)的溶液,可将Ce(Ⅱ)转化为Ce(Ⅳ)。该硫化锌锂电池放电时,负极材料晶胞组成变化如图所示: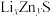 中,
中,
__________ 。
②ZnS晶胞中, 填充在
填充在 构成的部分正四面体空隙中,
构成的部分正四面体空隙中, 和
和 之间的核间距为apm,设
之间的核间距为apm,设 为阿伏加德罗常数的值,则晶体密度为
为阿伏加德罗常数的值,则晶体密度为__________  (列出计算式,ZnS的摩尔质量为
(列出计算式,ZnS的摩尔质量为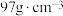 )。
)。
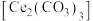 ]是一种稀土材料,工业上常以氟碳铈矿(主要成分为
]是一种稀土材料,工业上常以氟碳铈矿(主要成分为 、
、 、
、 )为原料制备碳酸铈,其工艺流程如图所示:
)为原料制备碳酸铈,其工艺流程如图所示: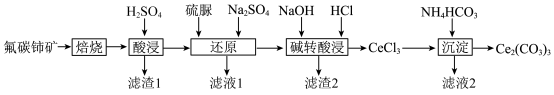
①“酸浸”后铈元素主要以
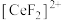 的形式存在;
的形式存在;②
 在空气中易被氧化为
在空气中易被氧化为 ,两者均能形成氢氧化物沉淀。
,两者均能形成氢氧化物沉淀。(1)“焙烧”时,从焙烧室的底部通入空气的目的是
(2)“滤渣1”的主要成分为
(3)“还原”时,加入硫脲(
 )的目的是将
)的目的是将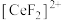 还原为
还原为 ,硫脲被氧化为
,硫脲被氧化为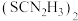 。
。①该反应的离子方程式为
②硫脲属于

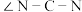 (填“>”“<”或“=”)
(填“>”“<”或“=”)(4)“碱转酸浸”在加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为
(5)若“沉淀”后,溶液的pH为6,
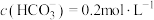 ,此时
,此时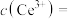
|
| |
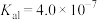 |
|
|
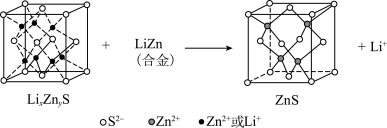
(6)某研究小组利用硫化锌锂电池电解含Ce(Ⅱ)的溶液,可将Ce(Ⅱ)转化为Ce(Ⅳ)。该硫化锌锂电池放电时,负极材料晶胞组成变化如图所示:
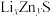 中,
中,
②ZnS晶胞中,
 填充在
填充在 构成的部分正四面体空隙中,
构成的部分正四面体空隙中, 和
和 之间的核间距为apm,设
之间的核间距为apm,设 为阿伏加德罗常数的值,则晶体密度为
为阿伏加德罗常数的值,则晶体密度为 (列出计算式,ZnS的摩尔质量为
(列出计算式,ZnS的摩尔质量为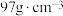 )。
)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】已知草酸镍晶体( )难溶于水,常用于制镍粉。工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍的流程如图所示:
)难溶于水,常用于制镍粉。工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍的流程如图所示: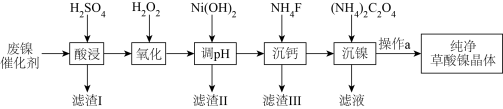
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
②Ksp(CaF2)=1.46 ③当某物质浓度小于1
③当某物质浓度小于1 时,视为完全沉淀
时,视为完全沉淀
回答下列问题:
(1)写出一种能提高“酸浸”速率的措施_______ 。滤渣Ⅰ的成分为 和
和_______ (填化学式)。
(2)“氧化”时反应的离子方程式为_______ 。
(3)“调 ”的范围为
”的范围为_______ ,用化学反应原理的相关知识简要说明滤渣Ⅱ的形成原因_______ 。
(4)“沉钙”过程中,当 沉淀完全时,溶液中
沉淀完全时,溶液中
_______  (列出计算式即可)。
(列出计算式即可)。
(5)“沉镍”时的离子方程式为_______ 。
(6)操作a包含过滤、用乙醇洗涤、110℃下烘干等步骤,其中用乙醇洗涤的目的是洗去杂质和_______ 。
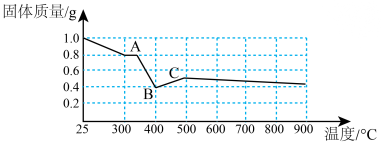
(7)某化学研究小组在文献中查阅到: 受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时,
受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时, 晶体受热分解的化学方程式为
晶体受热分解的化学方程式为_______ 。
 )难溶于水,常用于制镍粉。工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍的流程如图所示:
)难溶于水,常用于制镍粉。工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍的流程如图所示:
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
 ③当某物质浓度小于1
③当某物质浓度小于1 时,视为完全沉淀
时,视为完全沉淀回答下列问题:
(1)写出一种能提高“酸浸”速率的措施
 和
和(2)“氧化”时反应的离子方程式为
(3)“调
 ”的范围为
”的范围为(4)“沉钙”过程中,当
 沉淀完全时,溶液中
沉淀完全时,溶液中
 (列出计算式即可)。
(列出计算式即可)。(5)“沉镍”时的离子方程式为
(6)操作a包含过滤、用乙醇洗涤、110℃下烘干等步骤,其中用乙醇洗涤的目的是洗去杂质和
(7)某化学研究小组在文献中查阅到:
 受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时,
受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时, 晶体受热分解的化学方程式为
晶体受热分解的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】
H、C、N、O、W、Fe、V都是生活与化学工业中常见元素,请回答下列问题:
⑴碳负离子CH3-的空间构型为_______ ;根据等电子原理,NO+的电子式为________ 。
⑵N、Na+、Fe3+、Cu2+四种微粒基态的核外电子排布式中未成对电子数最多的是________ ;Cu2+在水中呈现蓝色是因为形成了水合铜离子,其化学式为______ 。
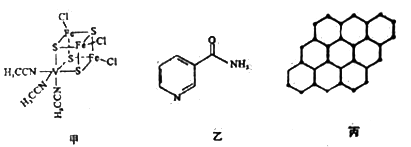
(3)钒可用于人工合成的二价钒固氮美酶(结构如图甲)。钒固氮酶中钒的配位原子有__________ (填元素符号)。
(4)烟酰胺(结构如图乙)可用于合成光合辅酶NADPH,烟酰胺分子中氮原子的杂化轨道类型有______ ,1 mol该分子中含σ键的数目为________________ 。
(5)下图为碳化钨晶体的一部分结构,碳原子嵌入金属钨的晶格的间隙,并不破坏原有金属的晶格,形成填隙+固溶体,也称为填隙化合物。在此结构中,其中钨原子有______ 个,1个钨原子周围距离钨原子最近的碳原子有______ 个,假设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g/mol,密度为b g/cm3,则阿伏伽德罗常数NA用上述数据可以表示为___________________ 。
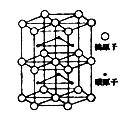
(6)12 g石墨烯(结构如图丙)中含有的正六边形的物质的量为_____ mol;请你预测硅是否容易形成类似石墨烯的结构,并说明理由____________________ 。
H、C、N、O、W、Fe、V都是生活与化学工业中常见元素,请回答下列问题:
⑴碳负离子CH3-的空间构型为
⑵N、Na+、Fe3+、Cu2+四种微粒基态的核外电子排布式中未成对电子数最多的是

(3)钒可用于人工合成的二价钒固氮美酶(结构如图甲)。钒固氮酶中钒的配位原子有
(4)烟酰胺(结构如图乙)可用于合成光合辅酶NADPH,烟酰胺分子中氮原子的杂化轨道类型有
(5)下图为碳化钨晶体的一部分结构,碳原子嵌入金属钨的晶格的间隙,并不破坏原有金属的晶格,形成填隙+固溶体,也称为填隙化合物。在此结构中,其中钨原子有

(6)12 g石墨烯(结构如图丙)中含有的正六边形的物质的量为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】硒化镍纳米材料可用于肿瘤的光热治疗研究。回答下列问题:
(1)基态Ni2+的核外电子排布式为_______ 。
(2)第一电离能:Br_______ (填“>”或“<”,下同)Se。未成对电子数:Br_______ Se。
(3)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是_______ 。在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_______ ,提供孤电子对的成键原子是_______ (用元素符号表示)。
(4)硒化镍材料也可作有机合成的催化剂,例如,苯甲醛被还原成环已基甲醇,反应如下:
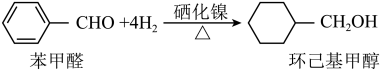
①环已基甲醇分子中采取sp3杂化方式的原子共有_______ 个。
②苯甲醛分子中的所有π电子形成了一个大π键,其中的π电子数目为_______ 个。
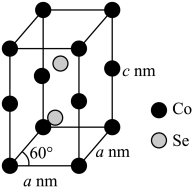
(5)我国科学家在真空条件下煅烧钴箔和硒粉,合成了具有优异电催化性能的硒化钴,其晶胞结构如图所示。该硒化钴的化学式为_______ ,晶体密度为_______ g·cm-3(用含a和c的式子表示,阿伏加德罗常数的值为NA)。
(1)基态Ni2+的核外电子排布式为
(2)第一电离能:Br
(3)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是
(4)硒化镍材料也可作有机合成的催化剂,例如,苯甲醛被还原成环已基甲醇,反应如下:

①环已基甲醇分子中采取sp3杂化方式的原子共有
②苯甲醛分子中的所有π电子形成了一个大π键,其中的π电子数目为
(5)我国科学家在真空条件下煅烧钴箔和硒粉,合成了具有优异电催化性能的硒化钴,其晶胞结构如图所示。该硒化钴的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】近日,厦门大学王野教授、谢顺吉教授综述了Cu基催化剂上CO2和CO制得C2H4、C2H5OH、CH3COOH等物质的原理。回答下列有关问题:
(1)基态Cu+的价电子排布式为____ 。
(2)C2H4、C2H5OH、CH3COOH三种物质中碳原子杂化形式有____ ,催化CO2还原的过程中可能产生CO ,该离子的空间构型为
,该离子的空间构型为____ 。
(3)与分子结构相似,配位化合物中心原子也存在轨道杂化现象,NH3可与Cu2+形成配离子的化学式为___ ,1mol该离子含有σ键___ mol,已知CuCl 空间结构为直线型,则Cu+的杂化形式为
空间结构为直线型,则Cu+的杂化形式为___ 。
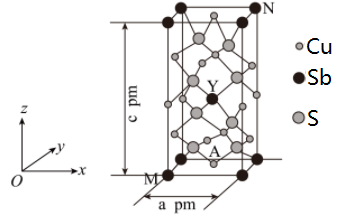
(4)某种含铜热电材料,晶胞结构如图,Cu位于棱、面上,Sb位于体心、顶点,S位于晶胞内,底部边长为a pm,高为c pm,该晶体的化学式为___ ,其中部分原子坐标为M(0,0,0)、A( ,
, ,0)、N(1,1,
,0)、N(1,1,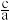 ),则Y点的原子坐标为
),则Y点的原子坐标为___ 。晶体的密度为ρ g/cm3,则c=___ pm(用a和ρ的式子表示)。设NA为阿伏加德罗常数的值。
(1)基态Cu+的价电子排布式为
(2)C2H4、C2H5OH、CH3COOH三种物质中碳原子杂化形式有
 ,该离子的空间构型为
,该离子的空间构型为(3)与分子结构相似,配位化合物中心原子也存在轨道杂化现象,NH3可与Cu2+形成配离子的化学式为
 空间结构为直线型,则Cu+的杂化形式为
空间结构为直线型,则Cu+的杂化形式为(4)某种含铜热电材料,晶胞结构如图,Cu位于棱、面上,Sb位于体心、顶点,S位于晶胞内,底部边长为a pm,高为c pm,该晶体的化学式为
 ,
, ,0)、N(1,1,
,0)、N(1,1,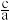 ),则Y点的原子坐标为
),则Y点的原子坐标为
您最近一年使用:0次
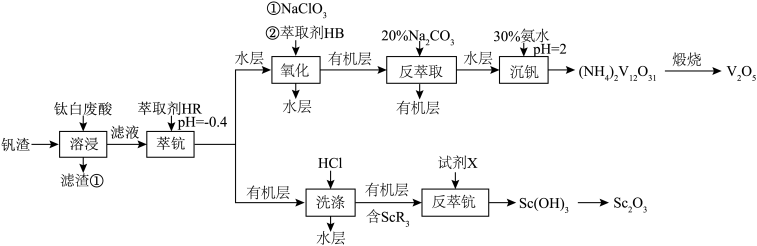
【推荐1】钒被称为金属“维生素”,钪用途广泛。以钒渣为原料,用钛白废酸浸出提取钒、钪,工艺流程如下。
已知:
I.钒渣中主要含Fe3O4、SiO2、V2O3,钛白废酸中含Sc3+、TiO2+、H+、SO 等离子。
等离子。
Ⅱ.表 反萃剂种类对钪反萃率的影响
(1)“溶浸”过程,可加快反应速率的措施有_______ (任写一项)。
(2)“溶浸”后,滤渣①主要成分是TiO2和_______ 。
(3)“氧化”过程,VO2+被氧化成VO ,同时还有
,同时还有_______ 离子被氧化。写出VO2+转化为VO ,反应的离子方程式
,反应的离子方程式_______ 。
(4)“萃钪”后“洗涤”,只有ScR3在有机层中,其他金属离子基本进入水层,水层可进入_______ 工序,充分利用资源。
(5)从上表中找出“反萃钪”过程的最佳试剂X和条件组合是_______ ,(填字母组合如“Aa”)“反萃钪”过程,发生反应的离子方程式是_______ 。
(6)常温下,各种形态五价钒粒子总浓度的对数[lgc总(V)]与pH关系如图。已知钛白废酸浸出液中c总(V)=0.2mol/L,“沉钒”过程控制pH=2.0,则五价钒粒子的存在形态为_______ (填化学式)。

(7)钒的价电子排布式_______ ,与钪的未成对电子数相同的同周期元素种类有_______ 种。
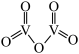
(8)五氧化二钒的结构简式如图所示,该结构中 键与
键与 键个数之比是
键个数之比是_______ 。
(9)催化剂V2O5溶于NaOH溶液中,可得到偏钒酸钠,偏钒酸钠的阴离子呈如图所示的无限链状结构,写出偏钒酸钠的化学式_______ 。

(10)单质钒的晶胞结构如图所示,若晶胞的棱长为anm,钒的相对原子质量为M,阿伏加德罗常数的值为NA,单质钒的密度为_______ (列出计算式即可)。


已知:
I.钒渣中主要含Fe3O4、SiO2、V2O3,钛白废酸中含Sc3+、TiO2+、H+、SO
 等离子。
等离子。Ⅱ.表 反萃剂种类对钪反萃率的影响
| 反萃剂种类/温度、时间 | a:常温5min | b:常温10min | c:常温15min | d:常温20min+40℃10min |
| A:2mol/LNa2CO3 | 20% | 30% | 32% | 45% |
| B:2mol/LNa2CO3+1mol/LNaCl | 13% | 20% | 25% | 28% |
| C:2mol/LNaOH | 56% | 60% | 57% | 57% |
| D:2mol/LNaOH+1mol/LNaCl | 60% | 58% | 56% | 99% |
(2)“溶浸”后,滤渣①主要成分是TiO2和
(3)“氧化”过程,VO2+被氧化成VO
 ,同时还有
,同时还有 ,反应的离子方程式
,反应的离子方程式(4)“萃钪”后“洗涤”,只有ScR3在有机层中,其他金属离子基本进入水层,水层可进入
(5)从上表中找出“反萃钪”过程的最佳试剂X和条件组合是
(6)常温下,各种形态五价钒粒子总浓度的对数[lgc总(V)]与pH关系如图。已知钛白废酸浸出液中c总(V)=0.2mol/L,“沉钒”过程控制pH=2.0,则五价钒粒子的存在形态为

(7)钒的价电子排布式
(8)五氧化二钒的结构简式如图所示,该结构中
 键与
键与 键个数之比是
键个数之比是
(9)催化剂V2O5溶于NaOH溶液中,可得到偏钒酸钠,偏钒酸钠的阴离子呈如图所示的无限链状结构,写出偏钒酸钠的化学式

(10)单质钒的晶胞结构如图所示,若晶胞的棱长为anm,钒的相对原子质量为M,阿伏加德罗常数的值为NA,单质钒的密度为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】碱式氯化铝[Al2(OH)nCl6-n]m (1≤n≤6,m≤10)(商业代号BAC),是一种比Al2(SO4)3效果更好的净水药剂。以下是用煤矸石(主要含Al2O3,SiO2及少量铁的氧化物)为原料生产碱式氯化铝过程中遇到的情况:
(1)在反应器中加入16%的硫酸和16%的盐酸,在不断搅拌过程中再加入经过焙烧后的煤矸石粉,反应器上部有一条长管子作为反应时气体的排放管。加热至沸腾(102℃)并保持一段时间,期间不断用精密pH试纸在排气管口上方检查排出气体的pH,记录如表:
试解释排气管中放出气体的pH变化的原因。如果把排气管加长一倍,排气的pH有无变化?_______ 为什么_______ 。
(2)观察反应器内溶液的颜色(取上面清液观察),在沸腾1h内,溶液逐渐呈黄绿色,以后逐渐转变为淡棕黄色,1.5h后呈棕红色。解释导致颜色变化的原因。_______ 。
(3)上述反应结束后,冷却,过滤弃渣,然后再加热至100℃,并在不断搅拌的条件下,向溶液慢慢地添加Ca(OH)2至适量,生成大量沉淀。过滤上述溶液,弃渣,得到澄清的BAC稀溶液。将此稀溶液加热蒸发浓缩,又产生白色细晶状沉淀,经化验分析,知此沉淀不是BAC固体,也不是AlCl3晶体或Al(OH)3。问:这是什么物质_______ ,为什么此时会有沉淀析出?_______ 。
(1)在反应器中加入16%的硫酸和16%的盐酸,在不断搅拌过程中再加入经过焙烧后的煤矸石粉,反应器上部有一条长管子作为反应时气体的排放管。加热至沸腾(102℃)并保持一段时间,期间不断用精密pH试纸在排气管口上方检查排出气体的pH,记录如表:
| 时间 | 起始 | 14min后 | 30min后 | 75min后 |
| pH | <2.0 | =2.5 | <3.5 | =3.5 |
(2)观察反应器内溶液的颜色(取上面清液观察),在沸腾1h内,溶液逐渐呈黄绿色,以后逐渐转变为淡棕黄色,1.5h后呈棕红色。解释导致颜色变化的原因。
(3)上述反应结束后,冷却,过滤弃渣,然后再加热至100℃,并在不断搅拌的条件下,向溶液慢慢地添加Ca(OH)2至适量,生成大量沉淀。过滤上述溶液,弃渣,得到澄清的BAC稀溶液。将此稀溶液加热蒸发浓缩,又产生白色细晶状沉淀,经化验分析,知此沉淀不是BAC固体,也不是AlCl3晶体或Al(OH)3。问:这是什么物质
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】绿色植物标本用醋酸铜[(CH3COO)2Cu]处理后颜色更鲜艳、稳定。某化学小组制备醋酸铜晶体并测定产品中铜的含量,实验如下。
Ⅰ.醋酸铜晶体的制备

(1)①中,用离子方程式表示产物里OH-的来源是__________ 。
(2)②中,化学方程式是__________ 。
(3)③中采用的实验方法依据醋酸铜的性质是_________ 。
Ⅱ.测定产品中铜的含量
ⅰ.取a g醋酸铜产品于具塞锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产生CuI沉淀,溶液呈棕黄色;
ⅱ.用b mol·L-1 Na2S2O3标准溶液滴定ⅰ中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;
ⅲ.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
ⅳ.继续用Na2S2O3 标准溶液滴定ⅲ中浊液至终点,消耗标准溶液v mL。
已知:① ,Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
,Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②CuI易吸附I2,CuSCN难溶于水且不吸附I2。被吸附的I2不与淀粉显色。
(4)ⅰ中发生反应的离子方程式是__________ 。
(5)结合离子方程式说明,ⅲ中加入KSCN的目的是__________ 。
(6)醋酸铜产品中铜元素的质量分数是__________ 。
Ⅰ.醋酸铜晶体的制备

(1)①中,用离子方程式表示产物里OH-的来源是
(2)②中,化学方程式是
(3)③中采用的实验方法依据醋酸铜的性质是
Ⅱ.测定产品中铜的含量
ⅰ.取a g醋酸铜产品于具塞锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产生CuI沉淀,溶液呈棕黄色;
ⅱ.用b mol·L-1 Na2S2O3标准溶液滴定ⅰ中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;
ⅲ.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
ⅳ.继续用Na2S2O3 标准溶液滴定ⅲ中浊液至终点,消耗标准溶液v mL。
已知:①
 ,Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
,Na2S2O3溶液和Na2S4O6溶液颜色均为无色;②CuI易吸附I2,CuSCN难溶于水且不吸附I2。被吸附的I2不与淀粉显色。
(4)ⅰ中发生反应的离子方程式是
(5)结合离子方程式说明,ⅲ中加入KSCN的目的是
(6)醋酸铜产品中铜元素的质量分数是
您最近一年使用:0次