Fe、Ni和铜等过渡元素在生活中被广泛应用。回答下列问题:
(1)下列状态的铁中,电离最外层一个电子所需能量最大的是___________。
(2)在分析化学中 常用于
常用于 的掩蔽剂,因为生成的
的掩蔽剂,因为生成的 十分稳定,但
十分稳定,但 却不能与
却不能与 形成配合物,其原因是
形成配合物,其原因是___________ 。
(3)基态Cu的价电子排布图为___________ ,位于___________ 区。元素 与
与 的第二电离能
的第二电离能 分别为
分别为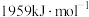 、
、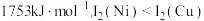 的原因是
的原因是___________ 。
(4)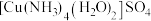 中各种微粒间的化学键有
中各种微粒间的化学键有___________  填序号
填序号 。
。
a.离子键 b.σ键 c.π键 d.配位键 e.氢键
1mol该物质中含有的σ键数为___________ 。其中与Cu2+配位更稳定的配体的分子构型为___________ 。
(5)镍和苯基硼酸在催化剂作用下可以合成丙烯醇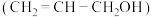 ,其相对分子质量等于丙醛
,其相对分子质量等于丙醛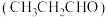 ,但两者沸点相差较大,原因是
,但两者沸点相差较大,原因是___________ 。
(6)铁单质的堆积方式有两种,其剖面图分别如图a、 所示。
所示。
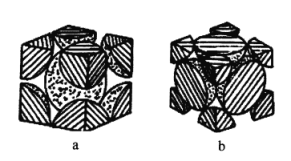
其中属于面心立方最密堆积的是___________ (填“ ”或“
”或“ ”),此晶体的空间利用率为
”),此晶体的空间利用率为___________  用含圆周率
用含圆周率 的代数式表示
的代数式表示
(1)下列状态的铁中,电离最外层一个电子所需能量最大的是___________。
A.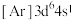 | B.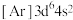 | C. | D.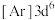 |
 常用于
常用于 的掩蔽剂,因为生成的
的掩蔽剂,因为生成的 十分稳定,但
十分稳定,但 却不能与
却不能与 形成配合物,其原因是
形成配合物,其原因是(3)基态Cu的价电子排布图为
 与
与 的第二电离能
的第二电离能 分别为
分别为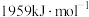 、
、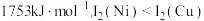 的原因是
的原因是(4)
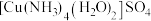 中各种微粒间的化学键有
中各种微粒间的化学键有 填序号
填序号 。
。a.离子键 b.σ键 c.π键 d.配位键 e.氢键
1mol该物质中含有的σ键数为
(5)镍和苯基硼酸在催化剂作用下可以合成丙烯醇
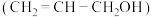 ,其相对分子质量等于丙醛
,其相对分子质量等于丙醛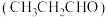 ,但两者沸点相差较大,原因是
,但两者沸点相差较大,原因是(6)铁单质的堆积方式有两种,其剖面图分别如图a、
 所示。
所示。
其中属于面心立方最密堆积的是
 ”或“
”或“ ”),此晶体的空间利用率为
”),此晶体的空间利用率为 用含圆周率
用含圆周率 的代数式表示
的代数式表示
更新时间:2023-05-23 22:06:50
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】光催化是一种能耗低、效率高、无二次污染、反应条件温和的绿色化学法。我国科学家使用乙二胺和水混合溶剂,合成带状纳米光催化剂Zn2GeO4.这类光催化材料广泛应用于水污染治理、CO2还原、空气净化等领域。回答下列问题:
(1)基态Zn原子的核外电子排布式为________ 。
(2)利用CO(NH2)2(尿素)在Zn2GeO4表面沉积非金属N,能够有效提高Zn2GeO4的光催化性能。尿素分子中σ键与π键数目比为________ ,C、N、O元素第一电离能大小顺序为________ ,原因是________ 。
(3)乙二胺(H2NCH2CH2NH2)所含C、N原子的杂化轨道类型分别为________ 、________ 。它能与Zn2+形成环状离子,原因是________ 。
(4)钙钛矿也是一种光催化剂,它的一种立方晶体的晶胞结构如图。其组成元素电负性最小的是________ 。与Ti4+距离最近的O2-数目为________ ,若晶胞参数为apm,该晶体密度为________ g▪cm-3(写出表达式)。

(1)基态Zn原子的核外电子排布式为
(2)利用CO(NH2)2(尿素)在Zn2GeO4表面沉积非金属N,能够有效提高Zn2GeO4的光催化性能。尿素分子中σ键与π键数目比为
(3)乙二胺(H2NCH2CH2NH2)所含C、N原子的杂化轨道类型分别为
(4)钙钛矿也是一种光催化剂,它的一种立方晶体的晶胞结构如图。其组成元素电负性最小的是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D、E、F为原子序数依次增大的短周期主族元素。A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级且每个能级上的电子数相同;A与C形成的分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F。
(1)A、C形成的分子极易溶于水,除因为它们都是极性分子外,还因为_____________________ 。
(2)比较E、F的第一电离能:E____ F 。(选填“>”或“<”)
(3) BD2在高温高压下所形成的晶胞如图所示:
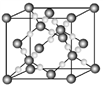
该晶体的类型属于____ 选填(分子晶体、原子晶体、离子晶体或金属晶体),该晶体中B原子的杂化形式____ 。
(4)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则 [F(OH)4]-中存在____ 。(填序号)
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(1)A、C形成的分子极易溶于水,除因为它们都是极性分子外,还因为
(2)比较E、F的第一电离能:E
(3) BD2在高温高压下所形成的晶胞如图所示:

该晶体的类型属于
(4)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则 [F(OH)4]-中存在
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
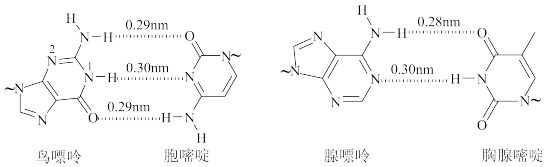
【推荐3】氢键对生命活动具有重要意义。DNA中四种碱基间的配对方式如下图。(~ 代表糖苷键)
(1)基态N的核外电子排布式为___________ ;N和O第一电离能较大的是___________ 。
(2)①碱基中的-NH2具有一定的碱性,可以结合H+形成-NH ,从结构角度解释可以结合的原因:
,从结构角度解释可以结合的原因:___________ 。
②写出甘氨酸(H2NCH2COOH)在pH=1和pH=13时的粒子存在形态:pH=1时___________ ,pH=13时___________ 。
(3)鸟嘌呤是一种常见的碱基。
①鸟嘌呤中2号N的杂化类型为___________ 。
②鸟嘌呤中N-H键的平均键长___________ (填“大于”“小于”或“等于”)0.29nm。
(4)氢键在DNA复制过程中起重要作用。
①碱基中,O、N能与H形成氢键而C不能,原因是___________ 。
②下列说法正确的是___________ (填序号)。
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比鸟嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
d.DNA在形成双螺旋结构时,碱基遵循互补配对原则,形成的氢键多,结构更稳定
(5)一定条件下鸟嘌呤会发生异构化,其1号N上的H会转移到O上形成-OH。
①鸟嘌呤异构化后的结构简式为___________ 。
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是___________ 。
(1)基态N的核外电子排布式为
(2)①碱基中的-NH2具有一定的碱性,可以结合H+形成-NH
 ,从结构角度解释可以结合的原因:
,从结构角度解释可以结合的原因:②写出甘氨酸(H2NCH2COOH)在pH=1和pH=13时的粒子存在形态:pH=1时
(3)鸟嘌呤是一种常见的碱基。
①鸟嘌呤中2号N的杂化类型为
②鸟嘌呤中N-H键的平均键长
(4)氢键在DNA复制过程中起重要作用。
①碱基中,O、N能与H形成氢键而C不能,原因是
②下列说法正确的是
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比鸟嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
d.DNA在形成双螺旋结构时,碱基遵循互补配对原则,形成的氢键多,结构更稳定
(5)一定条件下鸟嘌呤会发生异构化,其1号N上的H会转移到O上形成-OH。
①鸟嘌呤异构化后的结构简式为
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】电气石是一种具有保健作用的天然石材,其中含有的主要元素为 等元素。
等元素。
(1)上述元素中,原子半径最小的是_______ (用元素符号表示),与硫同周期的元素中简单离子半径最小的是_______ (用离子符号表示);
(2)用轨道表示式表示氧元素原子核外电子的运动状态_______ ;氧元素原子核外有_______ 种不同能量的电子;
(3) 分子中
分子中 为
为_______ 杂化,键角等于_______ ,可以判断出 分子为
分子为_______ 分子(选填“极性”或“非极性”); 晶体的熔点比
晶体的熔点比 晶体
晶体_______ (选填“高”、“低”),原因为_______ 。
 等元素。
等元素。(1)上述元素中,原子半径最小的是
(2)用轨道表示式表示氧元素原子核外电子的运动状态
(3)
 分子中
分子中 为
为 分子为
分子为 晶体的熔点比
晶体的熔点比 晶体
晶体
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为____________ ,3d能级上的未成对电子数为________ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是__________ 。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为________ ,提供孤电子对的成键原子是________ 。
③氨的沸点________ (填“高于”或“低于”)膦(PH3),原因是___________ ;氨是________ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为________ 。
(3)单质铜及镍都是由________ 键形成的晶体。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
③氨的沸点
(3)单质铜及镍都是由
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】完成下列填空
(1)甲烷的结构特点
甲烷分子中5个原子不在同一平面上,而是形成_________ 的空间结构,碳原子位于正四面体的_________ ,4个氢原子位于4个_________ ,分子中的4个C—H的长度和强度_________ ,相互之间的夹角_________ ,分子结构示意图: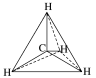 ,球棍模型为
,球棍模型为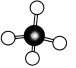 ,空间充填模型为
,空间充填模型为 。
。
(2)几种常见的烷烃
(3)烷烃结构的特点
①结构特点
a.单键:碳原子之间都以___________ 结合。
b.饱和:碳原子剩余价键全部跟___________ 结合。
c.结构:每个碳原子都与其他原子形成___________ 结构。
②链状烷烃通式:___________ 。
(1)甲烷的结构特点
甲烷分子中5个原子不在同一平面上,而是形成
 ,球棍模型为
,球棍模型为 ,空间充填模型为
,空间充填模型为 。
。(2)几种常见的烷烃
| 烷烃 | 乙烷 | 丙烷 | 正丁烷 |
| 分子式 | |||
| 结构式 | 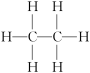 | 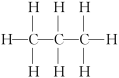 |  |
| 结构简式 |
①结构特点
a.单键:碳原子之间都以
b.饱和:碳原子剩余价键全部跟
c.结构:每个碳原子都与其他原子形成
②链状烷烃通式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】铜是生活中常见的金属,铜及其化合物在不同环境中能呈现出不同的颜色:

回答下列问题:
(1)Cu基态核外电子排布式为___ ;科学家通过X射线测得Cu(H2O)4SO4·H2O结构示意图可简单表示如图:
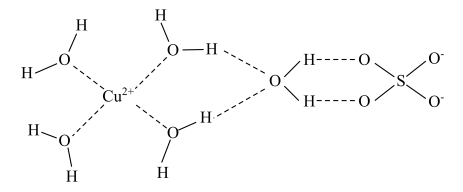
图中虚线表示的作用力为___ 。
(2)已知Cu+(SCN)2 Cu+(SCN)2,1mol(SCN)2分子中含有的π键数目为
Cu+(SCN)2,1mol(SCN)2分子中含有的π键数目为___ ,写出2个与SCN-互为等电子体的分子的化学式___ 。
(3)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是___ ,反应的化学方程式为___ 。
(4)在Cu(H2O)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是___ ,其中心原子的杂化轨道类型是___ 。
(5)已知Cu的晶胞结构如图所示,铜原子的配位数为___ ,又知晶胞边长为3.61×10-8cm,则Cu的密度为___ (保留三位有效数字)。


回答下列问题:
(1)Cu基态核外电子排布式为

图中虚线表示的作用力为
(2)已知Cu+(SCN)2
 Cu+(SCN)2,1mol(SCN)2分子中含有的π键数目为
Cu+(SCN)2,1mol(SCN)2分子中含有的π键数目为(3)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
(4)在Cu(H2O)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是
(5)已知Cu的晶胞结构如图所示,铜原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】硼单质及其化合物有重要的应用。阅读下列材料,回答问题:
硼晶体熔点为2076℃。乙硼烷(B2H6)具有还原性,易水解生成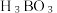 (一元弱酸);乙硼烷可与
(一元弱酸);乙硼烷可与 反应生成氨硼烷(
反应生成氨硼烷( ,其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成
,其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成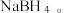
(1)下列说法正确的是_______(填字母)。
(2)根据对角线规则,B的一些化学性质与元素_______ 的相似;B 的空间结构是
的空间结构是_______ 。
(3)硼酸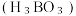 是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。
是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。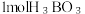 晶体中含有
晶体中含有_______ mol氢键;加热时,硼酸在水中溶解度增大,从结构角度分析,可能的原因为_______ 。
②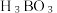 与NaOH溶液反应可以制备硼砂
与NaOH溶液反应可以制备硼砂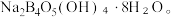 常温下,
常温下, 可以水解生成等物质的量浓度的
可以水解生成等物质的量浓度的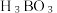 和
和 该水解反应的离子方程式为
该水解反应的离子方程式为_______ 。
(4)氮化硼(BN)晶体有多种相结构。一种立方BN晶体与金刚石结构相似,其晶胞结构如图: 则晶胞中含有BN的个数为
则晶胞中含有BN的个数为_______ (列出计算式,阿伏加德罗常数的数值为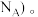
硼晶体熔点为2076℃。乙硼烷(B2H6)具有还原性,易水解生成
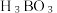 (一元弱酸);乙硼烷可与
(一元弱酸);乙硼烷可与 反应生成氨硼烷(
反应生成氨硼烷( ,其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成
,其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成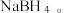
(1)下列说法正确的是_______(填字母)。
| A.元素的电负性大小顺序是O>N>B>H |
B.乙硼烷水解方程式为 |
| C.氨硼烷分子中N提供孤电子对,B提供空轨道形成配位键 |
D.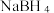 晶体中存在的相互作用有离子键、共价键、氢键 晶体中存在的相互作用有离子键、共价键、氢键 |
 的空间结构是
的空间结构是(3)硼酸
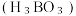 是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。
是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。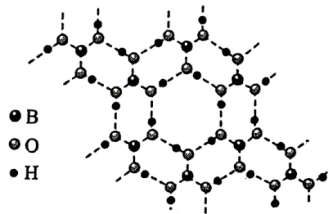
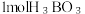 晶体中含有
晶体中含有②
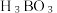 与NaOH溶液反应可以制备硼砂
与NaOH溶液反应可以制备硼砂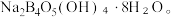 常温下,
常温下, 可以水解生成等物质的量浓度的
可以水解生成等物质的量浓度的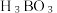 和
和 该水解反应的离子方程式为
该水解反应的离子方程式为(4)氮化硼(BN)晶体有多种相结构。一种立方BN晶体与金刚石结构相似,其晶胞结构如图:
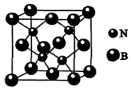
 则晶胞中含有BN的个数为
则晶胞中含有BN的个数为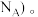
您最近一年使用:0次
【推荐3】在建国70周年阅兵仪式上,“歼20”“东风-41核导弹”等国之重器亮相,它们采用了大量合金材料。回答下列问题:
(1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是_____________ ,比较第一电离能Al______ Mg(填“>”“<”“=”)。
(2)查阅资料显示第二电离能Cu大于Zn,理由是_______________ 。
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为___________________ 。钛晶体在882 ℃以上为体心立方的β钛,其中钛原子的配位数为_______ 。
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的立体构型为___________ ,S的_______ 杂化轨道与O的2p轨道形成_____ 键(填“π”或“σ”)。
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为________ g/cm3(用含a、NA的计算式表示)。
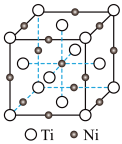
(6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于_________ 晶体,CO与Fe之间的化学键称为________ 。与CO互为等电子体的分子或离子是______ (只写一种)。
(1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是
(2)查阅资料显示第二电离能Cu大于Zn,理由是
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的立体构型为
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为

(6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】镓( )是非常重要的稀土金属,其化合物广泛应用于诸多领域。
)是非常重要的稀土金属,其化合物广泛应用于诸多领域。
(1)镓元素在元素周期表中的位置是___________ 。
(2)工业上利用炼锌矿渣[主要含可溶性铁酸镓 、铁酸锌
、铁酸锌 ]提取
]提取 。矿渣经“酸浸”后所得酸浸液含有
。矿渣经“酸浸”后所得酸浸液含有 、
、 、
、 等离子,经萃取富集其中的镓元素用于后续反应可制备氮化镓晶体。萃取工艺流程如下图所示。
等离子,经萃取富集其中的镓元素用于后续反应可制备氮化镓晶体。萃取工艺流程如下图所示。
①“酸浸”过程中 发生的反应的离子方程式为
发生的反应的离子方程式为___________ 。
②萃取剂水杨羟肟酸的结构简式如图1所示,萃取时分子中的 、
、 原子能与金属离子形成稳定的配位键。解释
原子能与金属离子形成稳定的配位键。解释 、
、 原子能作为配位原子的原因
原子能作为配位原子的原因___________ 。___________ (填试剂)充分反应后再进行萃取。
④“反萃取”后,溶液中镓元素的存在形式为___________ 。(填离子符号)
(3)氮化镓是非常重要的半导体材料,其立方晶胞如图2所示,与金刚石结构相似。 原子采用
原子采用___________ 杂化轨道成键。
②常压下,该晶体熔点为 ,其晶体类型为
,其晶体类型为___________ 。
③已知 晶体中距离最近的
晶体中距离最近的 原子间的核间距为
原子间的核间距为 ,
, 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为___________  。
。
 )是非常重要的稀土金属,其化合物广泛应用于诸多领域。
)是非常重要的稀土金属,其化合物广泛应用于诸多领域。(1)镓元素在元素周期表中的位置是
(2)工业上利用炼锌矿渣[主要含可溶性铁酸镓
 、铁酸锌
、铁酸锌 ]提取
]提取 。矿渣经“酸浸”后所得酸浸液含有
。矿渣经“酸浸”后所得酸浸液含有 、
、 、
、 等离子,经萃取富集其中的镓元素用于后续反应可制备氮化镓晶体。萃取工艺流程如下图所示。
等离子,经萃取富集其中的镓元素用于后续反应可制备氮化镓晶体。萃取工艺流程如下图所示。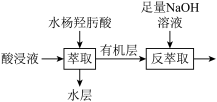
| 金属离子 |  |  |  |  |
| 萃取率/% | 0 | 0 | 99 | 97~98.5 |
 发生的反应的离子方程式为
发生的反应的离子方程式为②萃取剂水杨羟肟酸的结构简式如图1所示,萃取时分子中的
 、
、 原子能与金属离子形成稳定的配位键。解释
原子能与金属离子形成稳定的配位键。解释 、
、 原子能作为配位原子的原因
原子能作为配位原子的原因
④“反萃取”后,溶液中镓元素的存在形式为
(3)氮化镓是非常重要的半导体材料,其立方晶胞如图2所示,与金刚石结构相似。
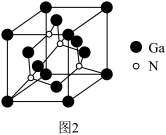
 原子采用
原子采用②常压下,该晶体熔点为
 ,其晶体类型为
,其晶体类型为③已知
 晶体中距离最近的
晶体中距离最近的 原子间的核间距为
原子间的核间距为 ,
, 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】锡、铬、钴、铜等金属及其化合物在工业上有重要用途。
(1)锡合金具有优异的抗蚀性能,可以用来生产制作各种精美合金饰品。
①基态Sn原子价层电子排布为_______
②Co元素在元素周期表中的位置是_______
③Cu元素位于元素周期表的_______ 区
(2)制备CrO2Cl2的反应为K2Cr2O7 + 3CCl4 = 2KCl + 2CrO2Cl2 + 3COCl2↑
①上述方程式中非金属元素电负性由小到大的顺序为_______ (用元素符号表示)。
②COCl2分子中π键和σ键的个数比为_______ ,中心原子的杂化方式为_______ ,COCl2属于_______ 分子(填“极性”或“非极性”)。
(3)Cu−Mn−Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:
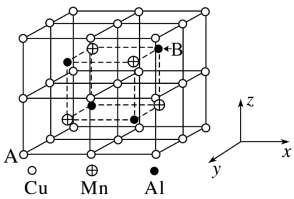
①合金的化学式为_______ 。
②A原子坐标参数为(0,1,0),则B原子坐标参数为_______ 。
③已知该合金晶体密度为ρg·cm-3,则两个Al原子间的最近距离为_______ nm (阿伏加德罗常数用NA表示,只列计算式)。
(1)锡合金具有优异的抗蚀性能,可以用来生产制作各种精美合金饰品。
①基态Sn原子价层电子排布为
②Co元素在元素周期表中的位置是
③Cu元素位于元素周期表的
(2)制备CrO2Cl2的反应为K2Cr2O7 + 3CCl4 = 2KCl + 2CrO2Cl2 + 3COCl2↑
①上述方程式中非金属元素电负性由小到大的顺序为
②COCl2分子中π键和σ键的个数比为
(3)Cu−Mn−Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:

①合金的化学式为
②A原子坐标参数为(0,1,0),则B原子坐标参数为
③已知该合金晶体密度为ρg·cm-3,则两个Al原子间的最近距离为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】美国芝加哥大学化学研究所近日揭示了WO3/CeO2-TiO2双催化剂在低温下催化氮的污染性气体转化为无毒气体,其过程如图所示
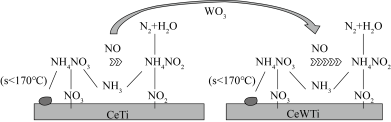
(1)Ti价电子排布式为______________ ,其能量最高的能层是___________ 。
(2)N、O、H三种原子的电负性由大到小的顺序为___________________ 。
(3)NO2-的空间构型为___________ ,与NO3-互为等电子体的分子为_______________
(4)WO3可作为苯乙烯氧化的催化剂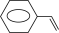 +H2O2
+H2O2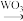
 +H2O
+H2O
① 中碳原子的杂化方式为
中碳原子的杂化方式为_________ 。
②1molH2O2中δ键个数为____________ 。
③ 属于
属于______________ 晶体。
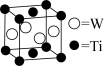
(5)W和Ti可形成金属互化物,某W和Ti的金属互化物如图所示,则该晶体的化学式为__________ 。
(6)金属钛的晶体堆积方式为____________

(1)Ti价电子排布式为
(2)N、O、H三种原子的电负性由大到小的顺序为
(3)NO2-的空间构型为
(4)WO3可作为苯乙烯氧化的催化剂
 +H2O2
+H2O2
 +H2O
+H2O①
 中碳原子的杂化方式为
中碳原子的杂化方式为②1molH2O2中δ键个数为
③
 属于
属于(5)W和Ti可形成金属互化物,某W和Ti的金属互化物如图所示,则该晶体的化学式为

(6)金属钛的晶体堆积方式为
您最近一年使用:0次



