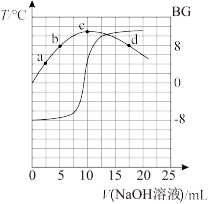
向20.00mL0.1000mol•L-1的某一元酸HA溶液中滴加未知浓度的NaOH溶液(初始温度为室温),混合溶液的温度、碱度BG[BG=lg ]随加入NaOH体积的变化如图所示。下列说法正确的是
]随加入NaOH体积的变化如图所示。下列说法正确的是
 ]随加入NaOH体积的变化如图所示。下列说法正确的是
]随加入NaOH体积的变化如图所示。下列说法正确的是
| A.NaOH溶液的浓度为0.1000mol•L-1 |
| B.b、c、d三点对应的溶液中,水的电离程度的大小关系是c>b>d |
| C.室温下,HA的电离常数的数量级约为10-6 |
| D.b点溶液中:2c(OH-)+c(HA)=2c(H+)+c(A-) |
更新时间:2023-05-25 16:06:37
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.硫酸铵溶液中c(NH4+)>c(SO42-)>c((H+)>c(OH-) |
| B.10 mL 0.1 mol/L醋酸溶液中加入等体积、等浓度的氢氧化钠后,溶液中离子浓度由大到小的顺序是:c(Na+)=c(CH3COO-);c(OH-)=c(H+) |
| C.pH=3的盐酸与pH=11的氨水等体积混合c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.碳酸钠溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是A. 时, 时,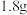 水中含有氢键的数目为 水中含有氢键的数目为 |
B. 时, 时, 乙烯中,含有 乙烯中,含有 键的数目为 键的数目为 |
C.标准状况下,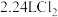 含有非极性键的数目为 含有非极性键的数目为 |
D.1L  醋酸中含有 醋酸中含有 和 和 数目之和为 数目之和为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,Ka(HCOOH)=1.77×10-4,Ka(CH3COOH)=1.75×10-5,Kb(NH3·H2O)=1.76×10-5,下列说法正确的是( )
A.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
| B.用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等 |
| C.0.2 mol/L HCOOH 与 0.1 mol/L NaOH 等体积混合后:c(HCOO-) + c(OH-)=c(HCOOH) + c(H+) |
| D.0.2 mol/L CH3COONa 与 0.1 mol/L盐酸等体积混合后 (pH<7):c(CH3COO-)>c(Cl- )>c(CH3COOH)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在常温下,有关下列四种溶液的叙述中正确的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A.在溶液①、②中分别加入适量的氯化铵晶体后,①溶液pH值变大,②溶液pH值变小 |
| B.将aL溶液④与bL溶液②混合后,若所得溶液的pH=4,则a:b=9:11 |
| C.分别取10mL溶液稀释至100mL,四种溶液的pH值:①>②>④>③ |
D.将溶液①、④等体积混合,所得溶液中:c(Cl-)>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在某温度时,将n mol/L氨水滴入10 mL 1.0mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是
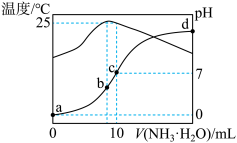
A.a点 |
| B.b点水的电离程度最大,c点水的电离程度最小 |
C.d点: |
D.25℃时, 水解平衡常数为 水解平衡常数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下 0.1mol/L的H2A溶液中H2A、HA-、A2-三者中所占物质的量分数(分布系数)随pH变化的关系如图所示。下列表述不正确 的是
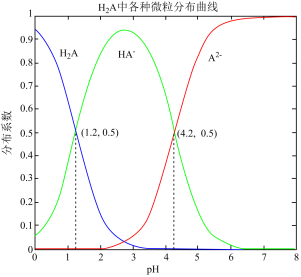

A.HA- H+ + A2- K=10-4.2 H+ + A2- K=10-4.2 |
| B.在 0.1mol/L NaHA 溶液中,各离子浓度大小关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C.已知25℃时HF的Ka=10-3.45,将少量H2A的溶液加入足量NaF溶液中,发生的反应为:H2A+F﹣═HF+HA﹣ |
| D.将等物质的量的NaHA、Na2A溶于水中,所得溶液pH恰好为4.2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】室温下,用0.100mol•L-1Na2SO3溶液吸收SO2的过程如图所示。已知Kal(H2SO3)=1.54×10-2,Ka2(H2SO3)=1.02×10-7,下列说法正确的是
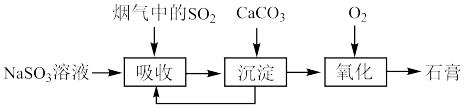
A.0.100mol•L-1NaHSO3溶液中:c(SO )<c(H2SO3) )<c(H2SO3) |
B.0.100mol•L-1Na2SO3溶液中:c(H+)+c(SO )+c(HSO )+c(HSO )+2c(H2SO3)=c(OH-) )+2c(H2SO3)=c(OH-) |
C.吸收烟气后的溶液中:c(Na+)<2c(SO )+2c(HSO )+2c(HSO )+2c(H2SO3) )+2c(H2SO3) |
D.沉淀得到的上层清液中:c(SO )< )< |
您最近一年使用:0次

 或
或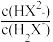 或
或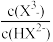 。下列说法正确的是(
。下列说法正确的是(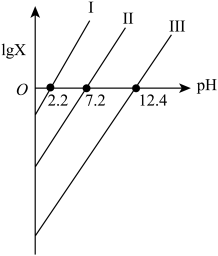
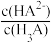 =100.6
=100.6
 );B点>F点
);B点>F点 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)

