工业制硫酸中的一步重要反应是二氧化硫在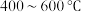 下的催化氧化:
下的催化氧化: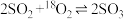 。如果反应在密闭容器中进行,下列有关的叙述正确的是
。如果反应在密闭容器中进行,下列有关的叙述正确的是
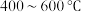 下的催化氧化:
下的催化氧化: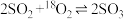 。如果反应在密闭容器中进行,下列有关的叙述正确的是
。如果反应在密闭容器中进行,下列有关的叙述正确的是| A.该反应属于吸热反应 |
| B.使用催化剂能提高反应的平衡转化率 |
C.一段时间后,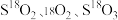 将共存于反应体系之中 将共存于反应体系之中 |
| D.当二氧化硫浓度和三氧化硫浓度相等时反应达到平衡 |
更新时间:2023-07-15 19:42:14
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于ΔH(焓变)的说法正确的是
| A.在恒压件下,化学反应的焓变等于化学反应的反应热 |
| B.ΔH>0时,反应放出热量;ΔH<0时,反应吸收热量 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.任何放热反应在常温下一定能发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】对于反应Zn+H2SO4=ZnSO4+H2↑,1 mol Zn反应时放出Q kJ热量。下列叙述不正确的是( )
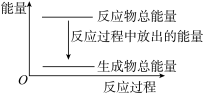

| A.反应过程中的能量关系可用如图表示 | B.滴入少许CuSO4溶液后反应速率减小 |
| C.若将该反应设计成原电池,则锌为负极 | D.理论上当转移4 mol电子时放出2QkJ热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述与图对应的是


A.对于达到平衡状态的反应:2SO2(g)+O2(g) 2SO3(g),图①表示在t0时刻又充入了一定量的SO3,平衡逆向移动 2SO3(g),图①表示在t0时刻又充入了一定量的SO3,平衡逆向移动 |
B.由图②可知,P2>P1、T1>T2满足反应:2A(g)+B(g) 2C(g) ∆H<0 2C(g) ∆H<0 |
| C.图③表示的反应方程式为: 2A=B+3C |
| D.图④表示0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L醋酸溶液的滴定曲线 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将BaO2放入密闭的真空容器中,反应2BaO2(s) 2BaO(s)+O2(g)达到平衡,保持温度不变,缩小一半容积,体系重新达到平衡,下列说法不正确的是
2BaO(s)+O2(g)达到平衡,保持温度不变,缩小一半容积,体系重新达到平衡,下列说法不正确的是
 2BaO(s)+O2(g)达到平衡,保持温度不变,缩小一半容积,体系重新达到平衡,下列说法不正确的是
2BaO(s)+O2(g)达到平衡,保持温度不变,缩小一半容积,体系重新达到平衡,下列说法不正确的是| A.气体的平均摩尔质量不变 | B.BaO量减小 |
| C.BaO2的转化率减小 | D.容器中气体浓度减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g) CH3OH,下列叙述中能说明上述反应在一定条件下
CH3OH,下列叙述中能说明上述反应在一定条件下一定 达到最大限度的是( )
 CH3OH,下列叙述中能说明上述反应在一定条件下
CH3OH,下列叙述中能说明上述反应在一定条件下| A.CO全部转化为乙醇 |
| B.正反应和逆反应的化学反应速率均为零 |
| C.CO和H2以1∶2的物质的量之比反应生成甲醇 |
| D.反应体系中甲醇的物质的量浓度不再变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】CO和H2在一定条件下可以合成乙醇(CH3CH2OH):2CO(g) +4H2 (g) CH3CH2OH(g)+H2O(g)。在2 L密闭容器中充入反应物,其中n(CO)随时间的变化如下表所示:
CH3CH2OH(g)+H2O(g)。在2 L密闭容器中充入反应物,其中n(CO)随时间的变化如下表所示:
下列说法中正确的是
 CH3CH2OH(g)+H2O(g)。在2 L密闭容器中充入反应物,其中n(CO)随时间的变化如下表所示:
CH3CH2OH(g)+H2O(g)。在2 L密闭容器中充入反应物,其中n(CO)随时间的变化如下表所示:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO)/mol | 3 | 2 | 1.5 | 1.25 | 1.125 | 1.125 |
| A.4s时,该反应恰好达到平衡状态 |
| B.前2 s,CO的平均反应速率为0.375 mol·L-1·s-1 |
| C.当v(CO)= 2v(CH3CH2OH),反应达到平衡状态 |
| D.达到平衡时,CO的转化率为37.5% |
您最近一年使用:0次
【推荐1】一定温度下,在一体积为2L的恒容密闭容器中充入2molSO2、1molO2,发生反应:2SO2(g)+O2(g)  2SO3(g) △H= - 196 kJ·mol-1,达到平衡后放出热量156.8kJ,下列说法不正确的是
2SO3(g) △H= - 196 kJ·mol-1,达到平衡后放出热量156.8kJ,下列说法不正确的是
 2SO3(g) △H= - 196 kJ·mol-1,达到平衡后放出热量156.8kJ,下列说法不正确的是
2SO3(g) △H= - 196 kJ·mol-1,达到平衡后放出热量156.8kJ,下列说法不正确的是| A.相同条件下初始若向容器中只充入2molSO3,达到平衡时吸收热量156.8kJ |
| B.若升高温度,该反应的平衡常数将减小 |
| C.反应过程中转移3.2mole- |
| D.平衡时SO2的转化率为80% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在373K时,把0.5molN2O4气体通入体积为5L 的恒容密闭容器中,发生反应: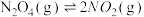 立即出现红棕色。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
立即出现红棕色。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
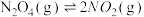 立即出现红棕色。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
立即出现红棕色。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是| A.前60秒,以N2O4的浓度变化表示的平均反应速率为0.01mol/(L·s) |
B.在 60秒时,  物质的量为0.2mol 物质的量为0.2mol |
| C.在平衡时体系内含N2O4的物质的量为0.2mol |
| D.60秒时,再充入一定量N2O4则可提高N2O4的转化率 |
您最近一年使用:0次

 为吸热反应,下列说法正确的是
为吸热反应,下列说法正确的是
 ,②
,② 。反应体系中组分X(g)、W(g)的物质的量浓度c随时间的变化情况如图所示{已知:Z(g)的选择性
。反应体系中组分X(g)、W(g)的物质的量浓度c随时间的变化情况如图所示{已知:Z(g)的选择性 。下列说法正确的是
。下列说法正确的是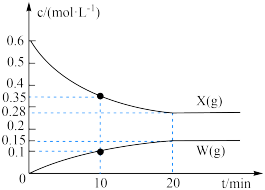
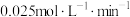
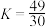
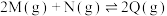
 ,在容器中以
,在容器中以 通入两种反应物,
通入两种反应物, 后M在不同温度下转化率如下表所示,且
后M在不同温度下转化率如下表所示,且 ,则下列说法正确的是
,则下列说法正确的是




 温度下(
温度下(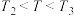 ),N的转化率是30%
),N的转化率是30%

