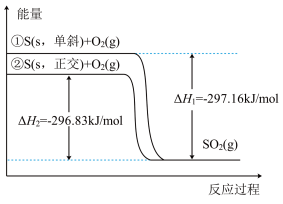
已知25℃时,某些物质的燃烧热数据如表:
下列热化学方程式书写正确的是
| 物质 |  |  |  |  |
燃烧热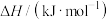 | -285.8 | -393.5 | -395.0 | -3267.5 |
A. 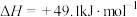 |
B. 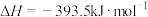 |
C.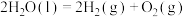  |
D.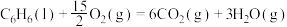 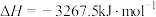 |
更新时间:2023-10-12 21:17:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知下列数据:
Fe(s)+ O2(g)=FeO(s) △H=-272kJ·mol-1
O2(g)=FeO(s) △H=-272kJ·mol-1
2Al(s)+ O2(g)=Al2O3(s) △H=-1675kJ·mol-1
O2(g)=Al2O3(s) △H=-1675kJ·mol-1
则2Al(s) +3FeO(s)=Al2O3(s) + 3Fe(s)的△H是
Fe(s)+
 O2(g)=FeO(s) △H=-272kJ·mol-1
O2(g)=FeO(s) △H=-272kJ·mol-12Al(s)+
 O2(g)=Al2O3(s) △H=-1675kJ·mol-1
O2(g)=Al2O3(s) △H=-1675kJ·mol-1则2Al(s) +3FeO(s)=Al2O3(s) + 3Fe(s)的△H是
| A.+859 kJ·mol-1 | B.-859 kJ·mol-1 |
| C.-1403 kJ·mol-1 | D.-2491 kJ·mol-1 |
您最近一年使用:0次
【推荐2】下列说法正确的是( )
A.若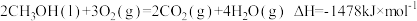 ,则CH3OH(l)的燃烧热为739kJ·mol-1 ,则CH3OH(l)的燃烧热为739kJ·mol-1 |
B.已知25℃、101KPa 下,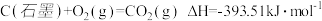 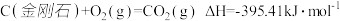 ,则石墨比金刚石更稳定 ,则石墨比金刚石更稳定 |
C.已知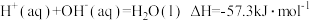 ,则20.0gNaOH固体与稀盐酸完全中和,放出28.65kJ的热量 ,则20.0gNaOH固体与稀盐酸完全中和,放出28.65kJ的热量 |
| D.中和热测定实验中,不可用环形铜质搅拌棒代替环形玻璃搅拌棒,实验至少需测3次温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列依据热化学方程式得出的结论正确的是( )
| A.已知P(白磷,s)=P(红磷,s)△H<0,则白磷比红磷稳定 |
| B.已知2H2(g)+O2(g)=2H2O(g)△H= -483.6kJ•mol-1,则氢气的标准燃烧热为241.8kJ•mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H=a kJ•mol-1,2C(s)+O2(g)=2CO(g)△H=b kJ•mol-1,则a>b |
| D.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则含40.0gNaOH的稀溶液与浓硫酸完全中和,放出大于57.3kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0 |
| B.已知2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1,则CO的燃烧热ΔH=-283kJ |
| C.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,则稀H2SO4溶液和稀Ba(OH)2溶液反应的反应热ΔH=2×(-57.3)kJ·mol-1 |
| D.甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列关于反应2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l) ΔH=-5 800 kJ·mol-1的叙述错误的是
| A.该反应的反应热ΔH=-5 800 kJ·mol-1,是放热反应 |
| B.该反应的ΔH与各物质的状态有关,与化学计量数也有关 |
| C.该热化学方程式表示在25 ℃、101 kPa下,2 mol C4H10气体完全燃烧生成CO2气体和液态水时放出热量5 800 kJ |
| D.该反应表明2 分子 C4H10气体完全燃烧时放出5 800 kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知热化学方程式:
H2O(g)=H2(g)+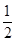 O2(g) ΔH=+241.8 kJ/mol
O2(g) ΔH=+241.8 kJ/mol
H2(g)+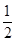 O2(g)=H2O(l) ΔH=-285.8 kJ/mol,当1 g液态水变为水蒸气时,其热量变化是( )
O2(g)=H2O(l) ΔH=-285.8 kJ/mol,当1 g液态水变为水蒸气时,其热量变化是( )
H2O(g)=H2(g)+
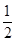 O2(g) ΔH=+241.8 kJ/mol
O2(g) ΔH=+241.8 kJ/molH2(g)+
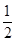 O2(g)=H2O(l) ΔH=-285.8 kJ/mol,当1 g液态水变为水蒸气时,其热量变化是( )
O2(g)=H2O(l) ΔH=-285.8 kJ/mol,当1 g液态水变为水蒸气时,其热量变化是( )| A.ΔH=+88 kJ/mol | B.ΔH=+2.44 kJ/mol |
| C.ΔH=-4.98 kJ/mol | D.ΔH=-44 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】通过以下两步反应可实现NH4Cl分解产物的分离。
NH4Cl(s)+MgO(s) NH3(g)+Mg(OH)Cl(s) △H=+61.34kJ·mol-1
NH3(g)+Mg(OH)Cl(s) △H=+61.34kJ·mol-1
Mg(OH)Cl(s) HCl(g)+MgO(s) △H=+97.50kJ·mol-1
HCl(g)+MgO(s) △H=+97.50kJ·mol-1
下列说法不正确的是
NH4Cl(s)+MgO(s)
 NH3(g)+Mg(OH)Cl(s) △H=+61.34kJ·mol-1
NH3(g)+Mg(OH)Cl(s) △H=+61.34kJ·mol-1Mg(OH)Cl(s)
 HCl(g)+MgO(s) △H=+97.50kJ·mol-1
HCl(g)+MgO(s) △H=+97.50kJ·mol-1下列说法不正确的是
| A.MgO是NH4Cl分解反应的催化剂 |
| B.两步反应的△S均大于0 |
| C.反应NH4Cl(s)=NH3(g)+HCl(g)的△H=+158.84kJ·mol-1 |
| D.10.7gNH4Cl完全分解理论上可获得标准状况下的HCl4.48L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应物的总键能与生成物的总键能之差。
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的反应热△H为 ( )
Si(s)+4HCl(g),该反应的反应热△H为 ( )
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/kJ·mol-1 | 46 | 360 | 436 | 431 | 176 | 347 |
 Si(s)+4HCl(g),该反应的反应热△H为 ( )
Si(s)+4HCl(g),该反应的反应热△H为 ( )| A.+412 kJ·mol-1 | B.-412 kJ·mol-1 |
| C.+236 kJ·mol-1 | D.-236 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知各物质的键能如下表所示,下列说法正确的是
| 共价键 |  | 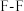 | 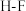 |  |  |
键能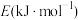 | 436 | 157 | 568 | 432 | 298 |
A.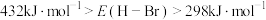 |
B. 能量最低,稳定性最强 能量最低,稳定性最强 |
C.稳定性: |
| D.H2(g)+F2(g)=2HF(g)的ΔH=+25kJ/mol |
您最近一年使用:0次

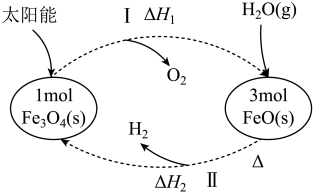
 、
、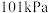 下:
下: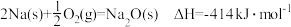
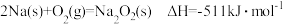
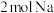 分别同时发生上述反应,转移电子数均为
分别同时发生上述反应,转移电子数均为
 与少量
与少量 点燃产物为
点燃产物为