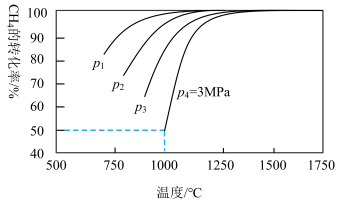
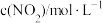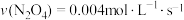工业合成氨的原料气来源于化石燃料,如采用甲烷与二氧化碳反应:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH=akJ·mol-1.在某容器中,充入等物质的量的CH4和CO2,下列说法正确的是
2CO(g)+2H2(g) ΔH=akJ·mol-1.在某容器中,充入等物质的量的CH4和CO2,下列说法正确的是
 2CO(g)+2H2(g) ΔH=akJ·mol-1.在某容器中,充入等物质的量的CH4和CO2,下列说法正确的是
2CO(g)+2H2(g) ΔH=akJ·mol-1.在某容器中,充入等物质的量的CH4和CO2,下列说法正确的是
| A.该原料气的制备反应为放热反应,a<0 |
| B.压强关系:p1>p2>p3>p4 |
| C.恒温恒压条件下,充入He,平衡逆向移动 |
| D.1000℃时的压强平衡常数Kp=4 |
2023高三·全国·专题练习 查看更多[1]
(已下线)第3讲 化学平衡计算 平衡常数
更新时间:2023-10-21 17:07:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】纳米二氧化钛催化剂可用于工业上合成甲醇: ,按
,按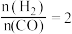 投料比将
投料比将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
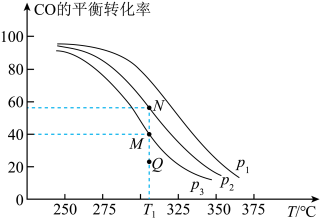
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
 ,按
,按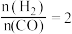 投料比将
投料比将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
A. |
B.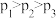 |
C.N点 转化率、平衡常数均大于M点 转化率、平衡常数均大于M点 |
D. 、 、 压强下,Q点对应的 压强下,Q点对应的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在某 恒容密闭容器中充入
恒容密闭容器中充入
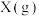 和
和
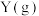 ,发生反应:
,发生反应: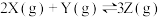 ,反应过程持续升高温度,测得混合体系中
,反应过程持续升高温度,测得混合体系中 的体积分数与温度的关系如图所示。下列推断正确的是
的体积分数与温度的关系如图所示。下列推断正确的是

 恒容密闭容器中充入
恒容密闭容器中充入
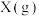 和
和
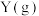 ,发生反应:
,发生反应: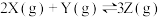 ,反应过程持续升高温度,测得混合体系中
,反应过程持续升高温度,测得混合体系中 的体积分数与温度的关系如图所示。下列推断正确的是
的体积分数与温度的关系如图所示。下列推断正确的是
| A.该反应为吸热反应 |
| B.升高温度,平衡右移,正反应速率减小,逆反应速率增大 |
| C.Q点时Z的体积分数最大 |
| D.W,M两点Y的正反应速率相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一密闭容器中,反应 a A(g) b B(g)+c C(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的70%,以下不正确的是( )
b B(g)+c C(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的70%,以下不正确的是( )
 b B(g)+c C(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的70%,以下不正确的是( )
b B(g)+c C(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的70%,以下不正确的是( )| A.平衡向正反应方向移动了 |
| B.物质A的转化率减少了 |
| C.物质B的质量分数增加了 |
| D.a<b+c |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实或操作不符合平衡移动原理的是( )
| A.开启啤酒有泡沫逸出 |
B.向FeCl3溶液中加KSCN,有 Fe(SCN)3(血红色)+3KCl反应,平衡后向体系中加入KCl固体,使体系红色变浅 Fe(SCN)3(血红色)+3KCl反应,平衡后向体系中加入KCl固体,使体系红色变浅 |
C.装有 的烧瓶置于热水中颜色加深 的烧瓶置于热水中颜色加深 |
| D.实验室用排饱和食盐水的方法收集氯气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】水气变换反应(CO+H2O H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。研究发现,在反应
H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。研究发现,在反应 、
、 中,
中, 仅对反应
仅对反应 有催化加速作用;反应
有催化加速作用;反应 速率远大于反应Ⅱ,近似认为反应
速率远大于反应Ⅱ,近似认为反应 建立平衡后始终处于平衡状态,T°C下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中,发生如下反应:
建立平衡后始终处于平衡状态,T°C下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中,发生如下反应:
Ⅰ.HCOOH(aq) CO(aq)+H2O(1)
CO(aq)+H2O(1)
Ⅱ.HCOOH(aq) CO2(aq)+H2(aq)
CO2(aq)+H2(aq)
含碳粒子浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式):
 H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。研究发现,在反应
H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。研究发现,在反应 、
、 中,
中, 仅对反应
仅对反应 有催化加速作用;反应
有催化加速作用;反应 速率远大于反应Ⅱ,近似认为反应
速率远大于反应Ⅱ,近似认为反应 建立平衡后始终处于平衡状态,T°C下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中,发生如下反应:
建立平衡后始终处于平衡状态,T°C下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中,发生如下反应:Ⅰ.HCOOH(aq)
 CO(aq)+H2O(1)
CO(aq)+H2O(1)Ⅱ.HCOOH(aq)
 CO2(aq)+H2(aq)
CO2(aq)+H2(aq)含碳粒子浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式):
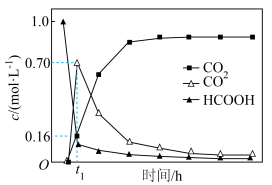
A.反应 活化能大于反应 活化能大于反应 |
| B.混合体系达平衡后:c(CO)+c(CO2)=1.0mol/L |
C. 时,反应 时,反应 正反应速率<逆反应速率 正反应速率<逆反应速率 |
D.若在起始溶液中加入盐酸,则CO达浓度峰值时, 的值与未加盐酸时相同 的值与未加盐酸时相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在某一体积可变的恒温密闭容器中发生反应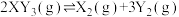
 。改变其中一个反应条件,得到逆反应速率(
。改变其中一个反应条件,得到逆反应速率( )与时间的关系如图所示。下列说法正确的是
)与时间的关系如图所示。下列说法正确的是
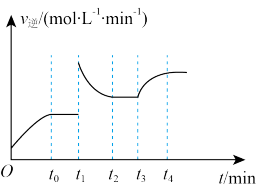
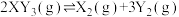
 。改变其中一个反应条件,得到逆反应速率(
。改变其中一个反应条件,得到逆反应速率( )与时间的关系如图所示。下列说法正确的是
)与时间的关系如图所示。下列说法正确的是
A.平衡常数: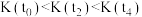 |
B.起始时,在容器中只充入了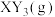 |
| C.t1时改变的反应条件可能是升高温度 |
D.图中,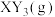 的平衡转化率最大的时间段是 的平衡转化率最大的时间段是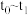 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 常用作有机反应中的还原剂,受热发生反应:
常用作有机反应中的还原剂,受热发生反应: 。一定温度时,向
。一定温度时,向 密闭容器中充入
密闭容器中充入 ,体系中
,体系中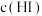 与反应时间t的关系如图。下列说法中,
与反应时间t的关系如图。下列说法中,不正确 的是
 常用作有机反应中的还原剂,受热发生反应:
常用作有机反应中的还原剂,受热发生反应: 。一定温度时,向
。一定温度时,向 密闭容器中充入
密闭容器中充入 ,体系中
,体系中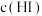 与反应时间t的关系如图。下列说法中,
与反应时间t的关系如图。下列说法中,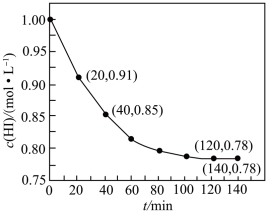
A. 的还原性与 的还原性与 价碘元素有关 价碘元素有关 |
B.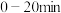 时, 时, 的反应速率为 的反应速率为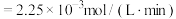 |
C. 时,有 时,有 的 的 发生分解 发生分解 |
D.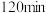 时,反应达到了平衡状态 时,反应达到了平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】高温下CO2和H2S发生如下反应:CO2(g) +H2S(g)⇌COS(g) +H2O(g)。有关实验数据如下:
下列说法不正确的是
| 实验 | 温度 | 物质的起始物质的量/(mol) | 平衡时COS物质的量/(mol) | |
| n(CO2) | n(H2S) | n(COS) | ||
| I | 337℃ | 0.10 | 0.40 | 0.01 |
| II | 347℃ | 0.10 | 0.40 | 0.015 |
| A.该反应为吸热反应 |
| B.实验I达平衡后COS的物质的量分数为5% |
C.实验I温度下,反应的平衡常数为 |
| D.平衡后向II中再充入0.10 mol CO2和0.40 mol H2S,相同温度下再达平衡时n(COS)=0.03mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
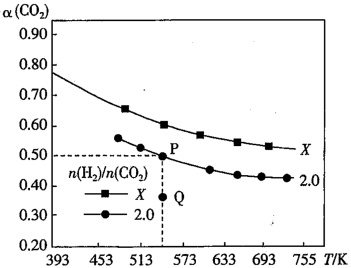
【推荐3】在两个固定体积均为1L密闭容器中以不同的氢碳比 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
| A.该反应在常温下不可能自发进行 |
| B.X的氢碳比X>2.0,在氢碳比为2.0时Q点v逆(H2)>P点v逆(H2) |
| C.若起始时CO2、H2浓度分别为0.5mol/L、1.0mol/L,则可得P点对应温度的平衡常数的值为512 |
| D.向处于P点状态的容器中,按2:4:1:4的比例再充入CO2、H2、C2H4、H2O,再次平衡后α(CO2)减小 |
您最近一年使用:0次

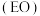 和乙醛
和乙醛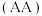 ,其反应过程中的能量变化如图所示(图中“
,其反应过程中的能量变化如图所示(图中“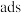 ”表示吸附态):
”表示吸附态):

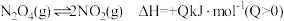 ,获得如下数据:
,获得如下数据: