I.已知尿酸是一种有机酸(以HUr表示),能溶于水。关节炎的原因归结
在关节滑液中形成了尿酸钠晶体(NaUr)。发生的反应如下:HUr Ur-+H+①;Ur-(aq)+Na+(aq)
Ur-+H+①;Ur-(aq)+Na+(aq) NaUr(s)②
NaUr(s)②
(1)关节炎大都是阴冷天气时发作,这说明反应②是_____ (填“放热”或“吸热”)反应。
(2)写出反应②的平衡常数表达式K=_____ 。
II.我国科学家研制出一种新型催化剂,实现了温和条件下“人工固氨”。在催化剂表面和常温常压下发生反应: 。
。
(3)改变下列一个条件,能提高活化分子百分数的是_____(填字母)。
(4)在某恒温恒容密闭容器中充入足量液态水和N2,达到平衡后,再充入少量N2,N2的平衡转化率_____ (填“增大”“减小”或“不变”)。
III
(5)在一密闭容器中进行反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206.1kJ·mol-1,测得CH4的物质的量浓度随反应时间的变化如图1所示。
CO(g)+3H2(g) ΔH1=+206.1kJ·mol-1,测得CH4的物质的量浓度随反应时间的变化如图1所示。
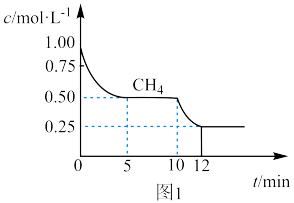
反应进行的前5min内,v(H2)=_____ ;10min时,改变的外界条件可能是_____ 。
(6)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g)并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像
2CO(g)+2H2(g)并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像_____ 。

在关节滑液中形成了尿酸钠晶体(NaUr)。发生的反应如下:HUr
 Ur-+H+①;Ur-(aq)+Na+(aq)
Ur-+H+①;Ur-(aq)+Na+(aq) NaUr(s)②
NaUr(s)②(1)关节炎大都是阴冷天气时发作,这说明反应②是
(2)写出反应②的平衡常数表达式K=
II.我国科学家研制出一种新型催化剂,实现了温和条件下“人工固氨”。在催化剂表面和常温常压下发生反应:
 。
。(3)改变下列一个条件,能提高活化分子百分数的是_____(填字母)。
| A.增大反应物浓度 |
| B.加入高效催化剂 |
| C.适当升温 |
| D.增大压强 |
(4)在某恒温恒容密闭容器中充入足量液态水和N2,达到平衡后,再充入少量N2,N2的平衡转化率
III
(5)在一密闭容器中进行反应CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+206.1kJ·mol-1,测得CH4的物质的量浓度随反应时间的变化如图1所示。
CO(g)+3H2(g) ΔH1=+206.1kJ·mol-1,测得CH4的物质的量浓度随反应时间的变化如图1所示。
反应进行的前5min内,v(H2)=
(6)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像
2CO(g)+2H2(g)并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像
更新时间:2023-11-01 22:16:43
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】如图是反应CO(g)+H2O(g) H2(g)+CO2(g) △H<0中CO和CO2的浓度随时间的变化关系图像。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2的浓度变化曲线,并标明物质(假设各物质状态均保持不变)
H2(g)+CO2(g) △H<0中CO和CO2的浓度随时间的变化关系图像。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2的浓度变化曲线,并标明物质(假设各物质状态均保持不变)______ 。
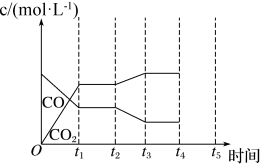
 H2(g)+CO2(g) △H<0中CO和CO2的浓度随时间的变化关系图像。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2的浓度变化曲线,并标明物质(假设各物质状态均保持不变)
H2(g)+CO2(g) △H<0中CO和CO2的浓度随时间的变化关系图像。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2的浓度变化曲线,并标明物质(假设各物质状态均保持不变)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)已知锌与稀硫酸反应为放热反应,某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气,实验记录如下:
①反应速率最大的(即0 min~1 min、1 min~2 min、2 min~3 min、3 min~4 min、4 min~
5 min)时间段为____________ ,原因是_____________________ 。②反应速率最小的时间段为____________ ,原因是________________________ 。
(2)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入以下物质以减缓反应速率:
A.蒸馏水 B.更加细小的锌粒 C.NaCl溶液
你认为他的做法可行的是______ (填相应字母);做法不可行的理由是______ 。
| 时间 (min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 30 | 120 | 280 | 350 | 370 |
①反应速率最大的(即0 min~1 min、1 min~2 min、2 min~3 min、3 min~4 min、4 min~
5 min)时间段为
(2)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入以下物质以减缓反应速率:
A.蒸馏水 B.更加细小的锌粒 C.NaCl溶液
你认为他的做法可行的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50 mL密度为 1.1 g/cm3的双氧水溶液中, 通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示。请依图回答下列问题:
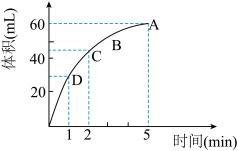
(1)放出一半气体所需要的时间为_____________ ;
(2)A、B、C、D各点反应速率快慢的顺序是______ 。
(3)在5min后,收集到的气体体积不再增加,原因是___________
(4)过氧化氢溶液的初始物质的量浓度为__________

(1)放出一半气体所需要的时间为
(2)A、B、C、D各点反应速率快慢的顺序是
(3)在5min后,收集到的气体体积不再增加,原因是
(4)过氧化氢溶液的初始物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)向盛有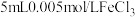 溶液的试管中加入
溶液的试管中加入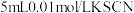 溶液,溶液呈红色。在这个反应体系中存在下述平衡:
溶液,溶液呈红色。在这个反应体系中存在下述平衡: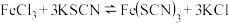
①向上述平衡体系中加入5滴浓的 溶液,溶液颜色
溶液,溶液颜色______ (填“变深”“变浅”或“不变”)。
②向上述平衡体系中加入少量 固体,溶液颜色
固体,溶液颜色______ (填“变深”“变浅”或“不变”)。
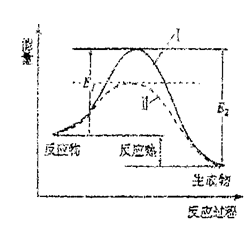
(2)氨是一种重要的化工原料,合成氨的反应: ,反应过程如图所示:
,反应过程如图所示:
①

______ (用含 、
、 的式子表示)。
的式子表示)。
②加催化剂的曲线______ (填“Ⅰ”或“Ⅱ”)。
③在一定条件下,能说明反应 一定达到平衡的是
一定达到平衡的是______ (填字母代号)。
A.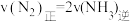
B.单位时间内消耗 的同时消耗
的同时消耗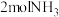
C.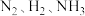 的物质的量之比为
的物质的量之比为
D.混合气体中 保持不变
保持不变
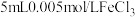 溶液的试管中加入
溶液的试管中加入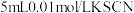 溶液,溶液呈红色。在这个反应体系中存在下述平衡:
溶液,溶液呈红色。在这个反应体系中存在下述平衡: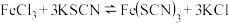
①向上述平衡体系中加入5滴浓的
 溶液,溶液颜色
溶液,溶液颜色②向上述平衡体系中加入少量
 固体,溶液颜色
固体,溶液颜色(2)氨是一种重要的化工原料,合成氨的反应:
 ,反应过程如图所示:
,反应过程如图所示:
①


 、
、 的式子表示)。
的式子表示)。②加催化剂的曲线
③在一定条件下,能说明反应
 一定达到平衡的是
一定达到平衡的是A.
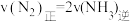
B.单位时间内消耗
 的同时消耗
的同时消耗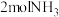
C.
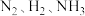 的物质的量之比为
的物质的量之比为
D.混合气体中
 保持不变
保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学知识在生产和生活中处处都有体现,请用化学知识解释。
(1)冰箱能够在一定时间内保鲜食物,原因是_____ 。
(2)乳酸饮料(含乳酸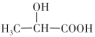 )显酸性的原因是
)显酸性的原因是_____ (用电离方程式表示)。
(3)工业上合成氨气时总是及时分离出反应器中的氨气,这样做的原因是_____ 。
(4)燃气灶具进风口通入的空气总是适当过量,这是为了_____ 。
(5)接近沸腾的纯净水pH<7,原因是_____ 。
(1)冰箱能够在一定时间内保鲜食物,原因是
(2)乳酸饮料(含乳酸
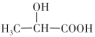 )显酸性的原因是
)显酸性的原因是(3)工业上合成氨气时总是及时分离出反应器中的氨气,这样做的原因是
(4)燃气灶具进风口通入的空气总是适当过量,这是为了
(5)接近沸腾的纯净水pH<7,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氯水中存在如下平衡:Cl2 +H2O HCl+HClO。向氯水中加入下列物质,回答各问题:
HCl+HClO。向氯水中加入下列物质,回答各问题:
(1)加入少量CaCO3(s),发生反应的离子方程式表示为__________________ ,平衡向________ 移动(填“正向”、“逆向”或“不”,下同),HClO的浓度______ (填“增大”、“减小”或“不变”,下同)。
(2)加入少量NaCl(s),平衡向_________ 移动,HClO的浓度___________ 。
(3)加入少量NaOH(s),平衡向__________ 移动,HClO的浓度____________ 。
(4)加入少量NaBr溶液,发生反应的离子方程式表示为____ ,HCl的物质的量_____ 。
(5)加入少量浓品红试液,实验现象为_____________ ,HCl的物质的量___________ 。
(6)加蒸馏水稀释,HClO的浓度__________ 。
 HCl+HClO。向氯水中加入下列物质,回答各问题:
HCl+HClO。向氯水中加入下列物质,回答各问题:(1)加入少量CaCO3(s),发生反应的离子方程式表示为
(2)加入少量NaCl(s),平衡向
(3)加入少量NaOH(s),平衡向
(4)加入少量NaBr溶液,发生反应的离子方程式表示为
(5)加入少量浓品红试液,实验现象为
(6)加蒸馏水稀释,HClO的浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
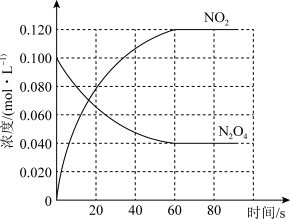
回答下列问题:
(1)100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为___________ mol·L-1·s-1,平衡时NO2的体积分数为___________ 。升高温度,混合气体的平均相对分子质量将___________ (填“增大”、“减小”或“不变”)
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10s又达到平衡。T___________ 100℃(填“大于”“小于”),判断理由是___________ 。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向(填“正反应”或“逆反应”)___________ 方向移动,判断理由是___________ 。
 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
(1)100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10s又达到平衡。T
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向(填“正反应”或“逆反应”)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】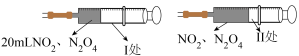
注射器活塞往里推到Ⅱ处时,为什么管内气体的颜色先变深又逐渐变浅________ ?由此得出的实验结论是什么________ ?

注射器活塞往里推到Ⅱ处时,为什么管内气体的颜色先变深又逐渐变浅
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在一定条件下,反应H2(g)+ I2(g) ⇌ 2HI(g) △H<0在一密闭体系中达到化学平衡。在448℃时,该反应的化学平衡常数为49。
(1)请写出该反应的平衡常数的表达式__________ 。
(2)下列说法中能说明该反应已达平衡状态的是______________ (用字母序号填空)
A.压强不再改变
B.速率之比 v(H2):v(I2):v(HI)=1:1:2
C.混合气体的颜色不再改变
D.混合气体的密度不再改变
(3)只改变下列条件,该化学平衡如何移动?①向正反应方向移动;②向逆反应方向移动;③不移动。升高温度__________ ;(用数字序号填空,下同)缩小容器的体积___________ ;保持体积不变,通入氢气___________ ;保持压强不变,通入氩气____________ 。
(1)请写出该反应的平衡常数的表达式
(2)下列说法中能说明该反应已达平衡状态的是
A.压强不再改变
B.速率之比 v(H2):v(I2):v(HI)=1:1:2
C.混合气体的颜色不再改变
D.混合气体的密度不再改变
(3)只改变下列条件,该化学平衡如何移动?①向正反应方向移动;②向逆反应方向移动;③不移动。升高温度
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
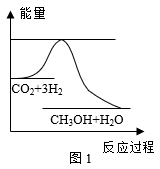
(1)该反应平衡常数K的表达式为___________ 。
(2)温度降低,平衡常数K___________ (填“增大”、“不变”或“减小”)。
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2)为___________ mol·L-1·min-1, CO2和H2的转化率比是___________

(4)下列措施中能使(3)题中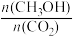 增大的有
增大的有___________ 。(填字母)
A.升高温度
B.加入催化剂
C.将H2O(g)从体系中分离
D.充入He(g),使体系总压强增大
E.再充入1mol CO2和3mol H2
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
(1)该反应平衡常数K的表达式为
(2)温度降低,平衡常数K
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2)为

(4)下列措施中能使(3)题中
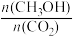 增大的有
增大的有A.升高温度
B.加入催化剂
C.将H2O(g)从体系中分离
D.充入He(g),使体系总压强增大
E.再充入1mol CO2和3mol H2
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】钾是—种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取。该反应为:Na(l)+KCl(l) NaCl(l)+K(g)(正反应吸热)
NaCl(l)+K(g)(正反应吸热)
该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见上表。
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为_______ ,而反应的最高温度应低于_______ 。
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是___________ 。
(3)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为:K=_____ 。
 NaCl(l)+K(g)(正反应吸热)
NaCl(l)+K(g)(正反应吸热)压强(kPa) | 13.33 | 53.32 | 101.3 |
K的沸点(℃) | 590 | 710 | 770 |
Na的沸点(℃) | 700 | 830 | 890 |
KCl的沸点(℃) | 1437 | ||
NaCl的沸点(℃) | 1465 |
该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见上表。
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是
(3)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为:K=
您最近一年使用:0次

 pC,某温度下达到平衡时,
pC,某温度下达到平衡时,

