Ⅰ.根据题意,写出下列反应的热化学方程式或填空:
(1)1mol氨气和1mol氯化氢气体化合生成氯化铵固体,放出176kJ热量,则此反应的热化学方程式为___________ 。
(2)已知3g乙烷(C2H6)气体完全燃烧生成CO2气体与液态水时放出的热量为156kJ,则乙烷燃烧热的热化学方程式为___________ 。
(3)温度在150℃以上时,H2O2便迅速分解为H2O和O2,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:a.H2(g)+O2(g)=H2O2(l) ΔH1=-134.3kJ·mol-1
b.H2O(l)=H2(g)+ O2(g) ΔH2=+286kJ·mol-1
O2(g) ΔH2=+286kJ·mol-1
则反应H2O2(l)=H2O(l)+ O2(g)的ΔH=
O2(g)的ΔH=___________ 。
Ⅱ.在一定体积的密闭容器中,进行化学反应CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表:
(4)该反应为___________ (填“吸热或放热”)反应
(5)若830℃时,向容器中充入1molCO,5molH2O,反应达到平衡后,其化学平衡常数K___________ (填大于、小于或等于)1.0。
(6)若830℃时,容器中的反应达到化学平衡,在其它条件不变的情况下扩大容器的体积,平衡___________ (填“向正反应方向”“向逆反应方向”或“不”)移动。
(7)若1200℃时,在某时刻平衡体系中CO2(g)、H2(g)、CO(g)、H2O(g)的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时平衡___________ (填“向正反应方向”“向逆反应方向”或“不”)移动,此时上述反应的速率v(正)___________ v(逆)(填大于、小于或等于)
(1)1mol氨气和1mol氯化氢气体化合生成氯化铵固体,放出176kJ热量,则此反应的热化学方程式为
(2)已知3g乙烷(C2H6)气体完全燃烧生成CO2气体与液态水时放出的热量为156kJ,则乙烷燃烧热的热化学方程式为
(3)温度在150℃以上时,H2O2便迅速分解为H2O和O2,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:a.H2(g)+O2(g)=H2O2(l) ΔH1=-134.3kJ·mol-1
b.H2O(l)=H2(g)+
 O2(g) ΔH2=+286kJ·mol-1
O2(g) ΔH2=+286kJ·mol-1则反应H2O2(l)=H2O(l)+
 O2(g)的ΔH=
O2(g)的ΔH=Ⅱ.在一定体积的密闭容器中,进行化学反应CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(5)若830℃时,向容器中充入1molCO,5molH2O,反应达到平衡后,其化学平衡常数K
(6)若830℃时,容器中的反应达到化学平衡,在其它条件不变的情况下扩大容器的体积,平衡
(7)若1200℃时,在某时刻平衡体系中CO2(g)、H2(g)、CO(g)、H2O(g)的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时平衡
更新时间:2023-12-04 07:27:39
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】氮氧化物( )、
)、 和
和 等气体会造成环境问题。对燃煤废气进行化学方法处理,可实现绿色环保、节能减排、废物利用等目的。
等气体会造成环境问题。对燃煤废气进行化学方法处理,可实现绿色环保、节能减排、废物利用等目的。
(1)利用甲烷催化还原 。
。
已知:

则甲烷将 还原为
还原为 并生成气态水时的热化学方程式为
并生成气态水时的热化学方程式为___________ 。
(2)利用 生成甲醇燃料。
生成甲醇燃料。

已知: ,将
,将 和
和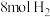 充入容积为2L的密闭容器中,恒温下,
充入容积为2L的密闭容器中,恒温下, 的物质的量随时间的变化曲线如图1实线所示,则:
的物质的量随时间的变化曲线如图1实线所示,则:
①该反应在0~8 内
内 的平均反应速率为
的平均反应速率为___________ 。
②仅改变某一条件再进行实验,测得 的物质的量随时间的变化曲线如图1虚线所示。与实线相比,虚线改变的条件可能是
的物质的量随时间的变化曲线如图1虚线所示。与实线相比,虚线改变的条件可能是___________ 。
(3)工业上利用 与
与 反应合成甲醇。
反应合成甲醇。
已知: ,在一恒容密闭容器中,按照
,在一恒容密闭容器中,按照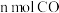 和
和 投料,测得
投料,测得 在不同温度下的平衡转化率与压强的关系如图2所示,则下列说法正确的是
在不同温度下的平衡转化率与压强的关系如图2所示,则下列说法正确的是___________ (填字母)。

A.温度:
B.正反应速率: 、
、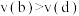
C.平衡常数: 、
、
D.平均摩尔质量: 、
、
(4)利用如图3所示装置(电极均为惰性电极)可吸收 ,阳极的电极反应式为
,阳极的电极反应式为___________ 。

(5)常温下,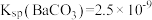 ,
,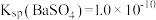 ,控制条件可实现如下沉淀转换:
,控制条件可实现如下沉淀转换: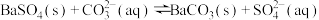 。
。
欲用 溶液将
溶液将 全部转化为
全部转化为 ,此时溶液中
,此时溶液中 为
为___________ 。
 )、
)、 和
和 等气体会造成环境问题。对燃煤废气进行化学方法处理,可实现绿色环保、节能减排、废物利用等目的。
等气体会造成环境问题。对燃煤废气进行化学方法处理,可实现绿色环保、节能减排、废物利用等目的。(1)利用甲烷催化还原
 。
。已知:


则甲烷将
 还原为
还原为 并生成气态水时的热化学方程式为
并生成气态水时的热化学方程式为(2)利用
 生成甲醇燃料。
生成甲醇燃料。
已知:
 ,将
,将 和
和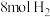 充入容积为2L的密闭容器中,恒温下,
充入容积为2L的密闭容器中,恒温下, 的物质的量随时间的变化曲线如图1实线所示,则:
的物质的量随时间的变化曲线如图1实线所示,则:①该反应在0~8
 内
内 的平均反应速率为
的平均反应速率为②仅改变某一条件再进行实验,测得
 的物质的量随时间的变化曲线如图1虚线所示。与实线相比,虚线改变的条件可能是
的物质的量随时间的变化曲线如图1虚线所示。与实线相比,虚线改变的条件可能是(3)工业上利用
 与
与 反应合成甲醇。
反应合成甲醇。已知:
 ,在一恒容密闭容器中,按照
,在一恒容密闭容器中,按照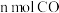 和
和 投料,测得
投料,测得 在不同温度下的平衡转化率与压强的关系如图2所示,则下列说法正确的是
在不同温度下的平衡转化率与压强的关系如图2所示,则下列说法正确的是
A.温度:

B.正反应速率:
 、
、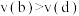
C.平衡常数:
 、
、
D.平均摩尔质量:
 、
、
(4)利用如图3所示装置(电极均为惰性电极)可吸收
 ,阳极的电极反应式为
,阳极的电极反应式为
(5)常温下,
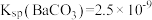 ,
,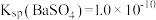 ,控制条件可实现如下沉淀转换:
,控制条件可实现如下沉淀转换: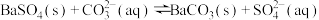 。
。欲用
 溶液将
溶液将 全部转化为
全部转化为 ,此时溶液中
,此时溶液中 为
为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ. 催化重整是减少温室气体排放的重要途径。
催化重整是减少温室气体排放的重要途径。
已知以下的热化学反应方程式:
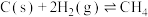
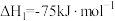
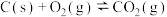
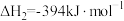
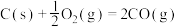
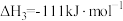
(1)写出催化重整反应 和
和 生成
生成 和
和 的热化学方程式:
的热化学方程式:_______ 。
Ⅱ.CO是煤气的主要成分,可与水蒸气反应生成氢气: 。查阅资料得出相关数据如下:
。查阅资料得出相关数据如下:
(2)通过表格中的数值可以推断:反应
_______ 0(填“>”或“<”)。该反应升高到一定温度时,反应将不能正向进行,由此判断该反应的
_______ 0(填“>”或“<”)。
(3)在容积为10L的密闭容器中通入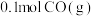 和
和 发生反应,在400℃时反应达到平衡,此时
发生反应,在400℃时反应达到平衡,此时 的转化率为
的转化率为_______ 。
(4)在绝热恒容条件下,反应物物质的量均为1mol发生反应,下列不能说明反应达到平衡状态的有_______ (填字母)。
a.体系的温度不再发生变化 b.混合气体的密度不变
c.混合气体的平均相对分子质量不变 d.各组分的物质的量浓度不再改变
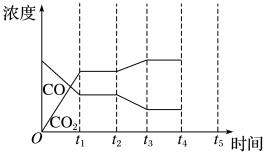
(5)如下图是反应在 时刻达到平衡,在
时刻达到平衡,在 时刻因改变某个条件而发生变化的情况:则
时刻因改变某个条件而发生变化的情况:则 时刻改变的条件可能是
时刻改变的条件可能是_______ (写出1种即可)。若 时刻通过改变容积的方法将压强增大为原来的2倍,在图中
时刻通过改变容积的方法将压强增大为原来的2倍,在图中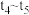 区间内画出CO、
区间内画出CO、 浓度变化曲线,并标明物质化学式(假设各物质状态均保持不变)。
浓度变化曲线,并标明物质化学式(假设各物质状态均保持不变)。_______
 催化重整是减少温室气体排放的重要途径。
催化重整是减少温室气体排放的重要途径。已知以下的热化学反应方程式:
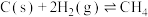
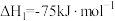
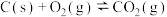
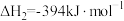
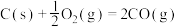
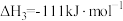
(1)写出催化重整反应
 和
和 生成
生成 和
和 的热化学方程式:
的热化学方程式:Ⅱ.CO是煤气的主要成分,可与水蒸气反应生成氢气:
 。查阅资料得出相关数据如下:
。查阅资料得出相关数据如下:| 温度/℃ | 400 | 500 |
| 平衡常数K | 9 | 5.3 |


(3)在容积为10L的密闭容器中通入
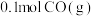 和
和 发生反应,在400℃时反应达到平衡,此时
发生反应,在400℃时反应达到平衡,此时 的转化率为
的转化率为(4)在绝热恒容条件下,反应物物质的量均为1mol发生反应,下列不能说明反应达到平衡状态的有
a.体系的温度不再发生变化 b.混合气体的密度不变
c.混合气体的平均相对分子质量不变 d.各组分的物质的量浓度不再改变
(5)如下图是反应在
 时刻达到平衡,在
时刻达到平衡,在 时刻因改变某个条件而发生变化的情况:则
时刻因改变某个条件而发生变化的情况:则 时刻改变的条件可能是
时刻改变的条件可能是 时刻通过改变容积的方法将压强增大为原来的2倍,在图中
时刻通过改变容积的方法将压强增大为原来的2倍,在图中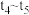 区间内画出CO、
区间内画出CO、 浓度变化曲线,并标明物质化学式(假设各物质状态均保持不变)。
浓度变化曲线,并标明物质化学式(假设各物质状态均保持不变)。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】回答下列问题:
(1)工业上制备水煤气的反应如下:
①
②
则
___________  ,该反应在
,该反应在_____ 条件下自发进行。(填“高温”、“低温”或“任何温度”)
(2)体积为 的密闭容器中,进行如下化学反应:
的密闭容器中,进行如下化学反应: ,化学平衡常数
,化学平衡常数 与温度
与温度 的关系如下表:
的关系如下表:
回答下列问题:
①若某温度下,平衡浓度符合下列关系: ,此时的温度为
,此时的温度为___________ ;在此温度下,若该容器中含有 、
、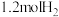 、
、 、
、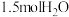 ,则此时反应所处的状态为
,则此时反应所处的状态为___________ (填“向正反应方向进行中”“向逆反应方向进行中”或“平衡状态”)。
②下列情况能说明该反应一定达到化学平衡的是___________
a.容器中混合气体的密度不变 b.正反应和逆反应的速率相等
c. 的含量保持不变 d.
的含量保持不变 d. 、
、 、
、 、
、 物质的量相等
物质的量相等
(3)①已知 时,
时,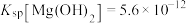 ,
,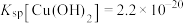 。在
。在 下,向浓度均为
下,向浓度均为 的
的 和
和 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成___________ 沉淀(填化学式),生成该沉淀的离子方程式为___________ 。
②已知 时,
时, ,则将
,则将 加入蒸馏水中形成饱和溶液,溶液中的
加入蒸馏水中形成饱和溶液,溶液中的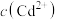 约为
约为___________  。
。
(1)工业上制备水煤气的反应如下:
①

②

则

 ,该反应在
,该反应在(2)体积为
 的密闭容器中,进行如下化学反应:
的密闭容器中,进行如下化学反应: ,化学平衡常数
,化学平衡常数 与温度
与温度 的关系如下表:
的关系如下表:| T/℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①若某温度下,平衡浓度符合下列关系:
 ,此时的温度为
,此时的温度为 、
、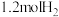 、
、 、
、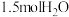 ,则此时反应所处的状态为
,则此时反应所处的状态为②下列情况能说明该反应一定达到化学平衡的是
a.容器中混合气体的密度不变 b.正反应和逆反应的速率相等
c.
 的含量保持不变 d.
的含量保持不变 d. 、
、 、
、 、
、 物质的量相等
物质的量相等(3)①已知
 时,
时,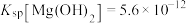 ,
,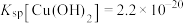 。在
。在 下,向浓度均为
下,向浓度均为 的
的 和
和 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成②已知
 时,
时, ,则将
,则将 加入蒸馏水中形成饱和溶液,溶液中的
加入蒸馏水中形成饱和溶液,溶液中的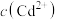 约为
约为 。
。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,16.0gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ(25℃时),写出表示N2H4燃烧热的热化学方程式 。
(2)甲烷----氧气燃料电池以20%~30%的KOH溶液为电解质溶液。
正极的电极反应式是 。
负极的电极反应式是 。
(3)右图是一个电化学过程示意图。
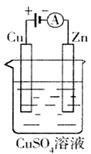
①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)
(2)甲烷----氧气燃料电池以20%~30%的KOH溶液为电解质溶液。
正极的电极反应式是 。
负极的电极反应式是 。
(3)右图是一个电化学过程示意图。

①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】为减小和消除过量 和
和 对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对
对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对 和
和 创新利用的研究。
创新利用的研究。
(1)25℃、101KPa条件下充分燃烧一定量的丁烷气体放出热量为 ,经测定,将生成的
,经测定,将生成的 通入足量澄清石灰水中产生40g白色沉淀,写出表示丁烷燃烧热的热化学方程式
通入足量澄清石灰水中产生40g白色沉淀,写出表示丁烷燃烧热的热化学方程式_______ 。
(2)用 催化还原
催化还原 还可以消除氮氧化物的污染。例如:
还可以消除氮氧化物的污染。例如:
 ;
;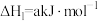
 ;
;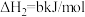
若用1mol 还原
还原 至
至 ,则该反应过程中的反应热
,则该反应过程中的反应热
___ 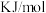 (用含a、b的式子表示)
(用含a、b的式子表示)
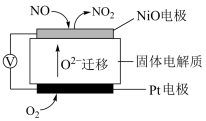
(3)通过 传感器可监测
传感器可监测 的含量,其工作原理示意图为:
的含量,其工作原理示意图为: 电极上发生的是
电极上发生的是_______ (填“氧化”或“还原”)反应。写出 电极的电极反应式
电极的电极反应式_______ 。
 和
和 对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对
对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对 和
和 创新利用的研究。
创新利用的研究。(1)25℃、101KPa条件下充分燃烧一定量的丁烷气体放出热量为
 ,经测定,将生成的
,经测定,将生成的 通入足量澄清石灰水中产生40g白色沉淀,写出表示丁烷燃烧热的热化学方程式
通入足量澄清石灰水中产生40g白色沉淀,写出表示丁烷燃烧热的热化学方程式(2)用
 催化还原
催化还原 还可以消除氮氧化物的污染。例如:
还可以消除氮氧化物的污染。例如: ;
;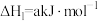
 ;
;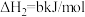
若用1mol
 还原
还原 至
至 ,则该反应过程中的反应热
,则该反应过程中的反应热
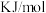 (用含a、b的式子表示)
(用含a、b的式子表示)(3)通过
 传感器可监测
传感器可监测 的含量,其工作原理示意图为:
的含量,其工作原理示意图为: 电极上发生的是
电极上发生的是 电极的电极反应式
电极的电极反应式
您最近一年使用:0次
【推荐3】Ⅰ.用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
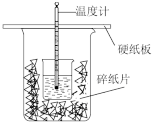
(1)从实验装置上看,图中尚缺少的一种玻璃用品是___________ ;由图可知此装置除了两烧杯没有填满碎泡沫塑料外,还有何不妥之处,应如何改正?___________ ;
(2)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会___________ (填“偏大”、“偏小”、“无影响”)。
Ⅱ.回答下列问题
(3)已知:①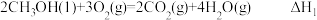 ,
,
②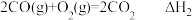 ,
,
③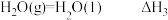 。
。
则反应 的
的 =
=___________ (用含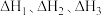 的式子表示)。
的式子表示)。
(4)某些化学键的键能如表所示:
试回答下列问题:
已知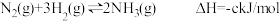 ,则N-H键的键能是
,则N-H键的键能是___________ kJ/mol (用含有a、b、c的式子表示)。
(5)1molNO2气体和1molCO气体反应生成CO2气体和NO气体过程中的能量变化如图所示,请写出NO2与CO反应的热化学方程式:___________ 。

(6)家用液化气的主要成分之一是丁烷(C4H10)。常温常压条件下,1g丁烷气体完全氧化生成CO2气体和液态水时放出热量50kJ,则表示丁烷燃烧热 的热化学方程式为___________ 。

(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
Ⅱ.回答下列问题
(3)已知:①
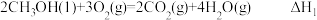 ,
,②
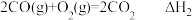 ,
,③
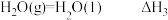 。
。则反应
 的
的 =
=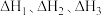 的式子表示)。
的式子表示)。(4)某些化学键的键能如表所示:
| 化学键 | H-H |  |
| 键能/(kJ/mol) | a | b |
已知
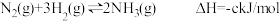 ,则N-H键的键能是
,则N-H键的键能是(5)1molNO2气体和1molCO气体反应生成CO2气体和NO气体过程中的能量变化如图所示,请写出NO2与CO反应的热化学方程式:

(6)家用液化气的主要成分之一是丁烷(C4H10)。常温常压条件下,1g丁烷气体完全氧化生成CO2气体和液态水时放出热量50kJ,则表示丁烷
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】某温度时,在一个容积为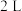 的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为___________ 。
(2)反应开始至 ,气体Y的平均反应速率为
,气体Y的平均反应速率为___________ 。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的___________ 倍;
②若此时将容器的体积缩小为原来的一半,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为___________ 反应(填“放热”或“吸热”)。
(4)若上述反应在 后的
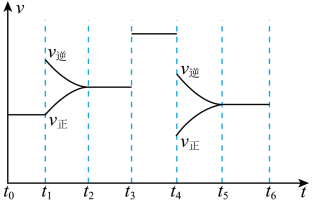
后的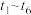 内反应速率与反应时间图象如下,在每一时刻均改变一个影响反应速率的因素,则______。
内反应速率与反应时间图象如下,在每一时刻均改变一个影响反应速率的因素,则______。
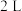 的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为
(2)反应开始至
 ,气体Y的平均反应速率为
,气体Y的平均反应速率为(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的
②若此时将容器的体积缩小为原来的一半,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
(4)若上述反应在
 后的
后的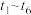 内反应速率与反应时间图象如下,在每一时刻均改变一个影响反应速率的因素,则______。
内反应速率与反应时间图象如下,在每一时刻均改变一个影响反应速率的因素,则______。
A.在 时增大了压强 时增大了压强 | B.在 时加入了催化剂 时加入了催化剂 |
C.在 时降低了温度 时降低了温度 | D. 时X的转化率最高 时X的转化率最高 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
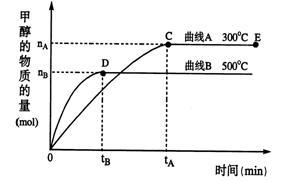
【推荐2】一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
根据题意完成下列各小题:
(1)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=____________ 。
(用上图中出现的字母表示)
(2)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是____________________ 。
a.氢气的浓度减小 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(3)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:___________ (用化学方程式表示)。
(4)能源问题是人类社会面临的重大课题,甲醇是未来的重要的能源物质。常温下,1g甲醇完全燃烧生成液态水时放出22. 7kJ的能量,写出甲醇燃烧热的热化学方程式___________ 。
 CH3OH(g)
CH3OH(g)根据题意完成下列各小题:
(1)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(用上图中出现的字母表示)

(2)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a.氢气的浓度减小 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(3)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:
(4)能源问题是人类社会面临的重大课题,甲醇是未来的重要的能源物质。常温下,1g甲醇完全燃烧生成液态水时放出22. 7kJ的能量,写出甲醇燃烧热的热化学方程式
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】1,6−己二醇是一种重要的化工原料,与乙二醇相比,用1,6−己二醇为原料制备的聚酯具有更为优异的柔韧性和抗腐蚀性。工业上利用己二酸二甲酯加氢制备1,6−己二醇,该反应的化学方程式如图:
 (g)+4H2(g)→
(g)+4H2(g)→ (g)+2CH3OH(g) ΔH。
(g)+2CH3OH(g) ΔH。
(1)已知:
计算上述反应的△H=___ ;此反应自发进行的条件是____ (填“高温易自发”“低温易自发”或“任何温度都能自发”)。
(2)将组成(物质的量分数)为4n%H2(g)、n% (g)的气体通入刚性密闭反应器中,在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时
(g)的气体通入刚性密闭反应器中,在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时 (g)的转化率为=
(g)的转化率为=____ (用p、q的代数式表示,下同),平衡常数Kp=____ (以分压表示,分压=总压×物质的量分数)。
(3)科研小组在高压反应釜中进行催化加氢反应,对己二酸二甲酯制备1,6−己二醇的工艺条件进行了研究。图甲和图乙为此反应在相同时间时,反应压力、反应温度与反应物的转化率和1,6−己二醇选择性的变化关系。

已知,选择性= ×100%。
×100%。
①由图可知,在压强为27MPa时,己二酸二甲酯制备1,6−己二醇应选择的合适温度为____ ;选择此温度的理由是____ ;当260℃时,转化率随着压强增大而不断增大的原因是____ 。
②图丙为反应时间与加氢反应时反应物的转化率和选择性的关系。

综合考虑,反应时间控制在5h左右较为合适。此时1,6−己二醇的产率为____ 。
 (g)+4H2(g)→
(g)+4H2(g)→ (g)+2CH3OH(g) ΔH。
(g)+2CH3OH(g) ΔH。(1)已知:
化学键 | C=O | C−O | C−H | C−C | O−H | H−H |
| 键能/ kJ∙mol−1 | 745 | 358 | 413 | 347 | 467 | 436 |
(2)将组成(物质的量分数)为4n%H2(g)、n%
 (g)的气体通入刚性密闭反应器中,在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时
(g)的气体通入刚性密闭反应器中,在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时 (g)的转化率为=
(g)的转化率为=(3)科研小组在高压反应釜中进行催化加氢反应,对己二酸二甲酯制备1,6−己二醇的工艺条件进行了研究。图甲和图乙为此反应在相同时间时,反应压力、反应温度与反应物的转化率和1,6−己二醇选择性的变化关系。

已知,选择性=
 ×100%。
×100%。①由图可知,在压强为27MPa时,己二酸二甲酯制备1,6−己二醇应选择的合适温度为
②图丙为反应时间与加氢反应时反应物的转化率和选择性的关系。

综合考虑,反应时间控制在5h左右较为合适。此时1,6−己二醇的产率为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】CO可用于合成甲醇,下图是反应CO(g)+2H2(g)⇌CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。

①该反应的焓变ΔH_______ 0(填“>”“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1_______ K2(填“>”、“<”或“=”)。
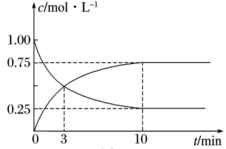
③在T1温度下,往体积为1 L的密闭容器中,充入1 mol CO和2 mol H2 ,经测得CO和CH3OH(g)的浓度随时间变化如下图所示。则该反应的平衡常数为_______ 。
④若容器容积不变,下列措施可增加CO转化率的是_______ (填字母)。
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大

①该反应的焓变ΔH
②T1和T2温度下的平衡常数大小关系是K1
③在T1温度下,往体积为1 L的密闭容器中,充入1 mol CO和2 mol H2 ,经测得CO和CH3OH(g)的浓度随时间变化如下图所示。则该反应的平衡常数为

④若容器容积不变,下列措施可增加CO转化率的是
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为________________________________ 。
(2)20s时,N2O4的的浓度为__________ mol·L-1,0~20s内N2O4的平均反应速率为_____________ 。
(3)该反应的平衡常数表达式K=____________ ,80℃反应K值为___________ 保留2位小数)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时______________ 。
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
(5)要增大该反应的K值,可采取的措施_________
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂 D.升高温度
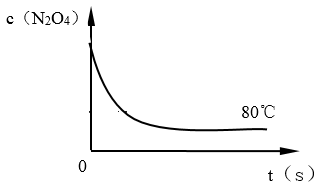
(6)下图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线_______ 。
 时间(s) 时间(s)c(mol·L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.10 | C | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)该反应的化学方程式为
(2)20s时,N2O4的的浓度为
(3)该反应的平衡常数表达式K=
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
(5)要增大该反应的K值,可采取的措施
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂 D.升高温度
(6)下图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】甲烷和氯气都是重要的化工原料。
I.CH4在光照条件下与C12反应,可得到各种氯代甲烷。
(1)CH4氯代的机理为自由基(带有单电子的原子或原子团,如C1·、·CH3)反应,包括以下几步:
写出由CH3Cl生成CH2Cl2过程中链传递的方程式:_______ ,_______ 。
(2)丙烷氯代反应中链传递的一步反应能量变化如下。

推知−CH3中C−H键能比-CH2-中C−H键能_______ (填“大”或“小”)。
II.甲烷重整制合成气,主要反应如下:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH2
各反应平衡常数与温度的关系如图。
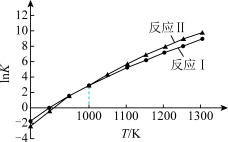
(3)①假设ΔH、ΔS不随温度变化,平衡常数与温度间存在的关系为:lnK1−lnK2= (
( −
− ),R为正常数。则ΔH1
),R为正常数。则ΔH1_______ 0(填“>”或“<”);ΔH1_______ ΔH2(填“>”或“<”)。
②通过调整投料比可调控平衡时合成气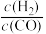 的值。1000K,平衡时
的值。1000K,平衡时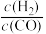 =2,则
=2,则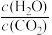 =
=_______ ,应控制投料比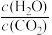 =
=_______ 。
III.氯碱工业是化工产业的重要基础,其装置示意图如图。

(4)X为_______ ,Y为_______ 。(写化学式)
(5)淡盐水中含少量的HClO,阴极区生成NaOH的物质的量小于氢气的两倍,下列关于造成NaOH的物质的量小于氢气的两倍的原因中合理的是_______ (填序号)。
a.Cl-在电极上放电,产生HClO
b.有H+穿过阳离子交换膜
c.阳离子交换膜破损导致OH-向阳极区迁移
d.O2在阴极放电
I.CH4在光照条件下与C12反应,可得到各种氯代甲烷。
(1)CH4氯代的机理为自由基(带有单电子的原子或原子团,如C1·、·CH3)反应,包括以下几步:
| I.链引发 | II.链传递 | III.链终止 |
Cl2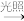 2Cl∙ 2Cl∙ | Cl∙+CH4→∙CH3+HCl ∙CH3+Cl2→CH3Cl+Cl∙ …… | 2Cl∙→Cl2 Cl∙+∙CH3→CH3Cl …… |
写出由CH3Cl生成CH2Cl2过程中链传递的方程式:
(2)丙烷氯代反应中链传递的一步反应能量变化如下。

推知−CH3中C−H键能比-CH2-中C−H键能
II.甲烷重整制合成气,主要反应如下:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH2
各反应平衡常数与温度的关系如图。

(3)①假设ΔH、ΔS不随温度变化,平衡常数与温度间存在的关系为:lnK1−lnK2=
 (
( −
− ),R为正常数。则ΔH1
),R为正常数。则ΔH1②通过调整投料比可调控平衡时合成气
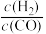 的值。1000K,平衡时
的值。1000K,平衡时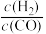 =2,则
=2,则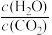 =
=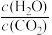 =
=III.氯碱工业是化工产业的重要基础,其装置示意图如图。

(4)X为
(5)淡盐水中含少量的HClO,阴极区生成NaOH的物质的量小于氢气的两倍,下列关于造成NaOH的物质的量小于氢气的两倍的原因中合理的是
a.Cl-在电极上放电,产生HClO
b.有H+穿过阳离子交换膜
c.阳离子交换膜破损导致OH-向阳极区迁移
d.O2在阴极放电
您最近一年使用:0次



