甲烷不仅是一种燃料,还可以作化工原料用来生产氢气、乙炔、碳黑等物质。回答下列问题:
(1)向一恒容密闭容器中加入 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
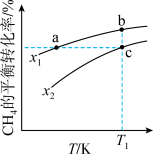
的平衡转化率按不同投料比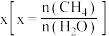 随温度的变化曲线如下图所示。
随温度的变化曲线如下图所示。
①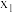
_______ 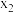 (填“>”、“<”“=”,下同)。
(填“>”、“<”“=”,下同)。
②点a、b、c对应的平衡常数 三者之间的关系是
三者之间的关系是_______ 。
③比较b、c两点的正反应速率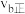 与
与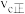 的大小并说明理由:
的大小并说明理由:_______ 。
(2)一定条件下,甲烷和水蒸气催化制氢主要有如下两个反应:
Ⅰ.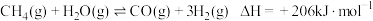
Ⅱ.
恒定压强为 时,将
时,将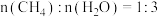 的混合气体投入反应器中,发生以上两反应,平衡时各组分的物质的量分数与温度的关系如下图所示。
的混合气体投入反应器中,发生以上两反应,平衡时各组分的物质的量分数与温度的关系如下图所示。
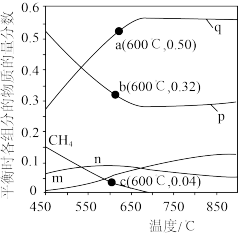
①分析图中各曲线所代表的物质,其中 的物质的量分数与温度的变化曲线是
的物质的量分数与温度的变化曲线是_______ (填图中字母标号)。
②已知投料比为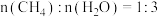 的混合气体,
的混合气体,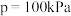 ,
, 时,
时, 的平衡转化率为
的平衡转化率为_______ (保留2位有效数字)。
(1)向一恒容密闭容器中加入
 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比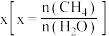 随温度的变化曲线如下图所示。
随温度的变化曲线如下图所示。
①
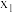
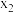 (填“>”、“<”“=”,下同)。
(填“>”、“<”“=”,下同)。②点a、b、c对应的平衡常数
 三者之间的关系是
三者之间的关系是③比较b、c两点的正反应速率
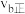 与
与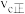 的大小并说明理由:
的大小并说明理由:(2)一定条件下,甲烷和水蒸气催化制氢主要有如下两个反应:
Ⅰ.
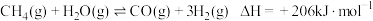
Ⅱ.

恒定压强为
 时,将
时,将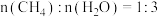 的混合气体投入反应器中,发生以上两反应,平衡时各组分的物质的量分数与温度的关系如下图所示。
的混合气体投入反应器中,发生以上两反应,平衡时各组分的物质的量分数与温度的关系如下图所示。
①分析图中各曲线所代表的物质,其中
 的物质的量分数与温度的变化曲线是
的物质的量分数与温度的变化曲线是②已知投料比为
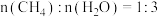 的混合气体,
的混合气体,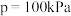 ,
, 时,
时, 的平衡转化率为
的平衡转化率为
更新时间:2023-12-26 21:35:29
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】利用合成气(主要成分为CO、CO2、 H2) 一定条件下合成甲醇(CH3OH),发生的主要反应如下:
Ⅰ. CO(g) + 2H2(g)=CH3OH(g) △H。
Ⅱ. CO(g) + H2O(g)=CO2(g) +H2(g) ∆H2=-41.2 kJ/mol
回答下列问题:
(1)已知反应①中的相关化学键键能数据如下:
写出由二氧化碳、氢气制备甲醇的热化学方程式_______ 反应I在_______ (填“高温”、“低温”或“任意温度”)条件下自发进行。
(2)在T℃时,向5L恒容密闭容器中加入0.6 mol CO和0.45 molH2,发生反应Ⅰ。CO和CH3OH的浓度在不同时刻的变化状况如图所示:
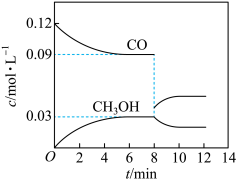
①下列能够说明反应在第6min时达到平衡状态的是______
A.混合气体的平均摩尔质量不再改变
B. CH3OH 的浓度不变
C. v(CO)正 : v(H2)逆= 2:1
D. P(CO):P( H2)= 1:2
第8 min时改变的条件是_______
②在第12 min时升高温度,重新达到平衡时,化学平衡常数将_______ (填 “增大”“不变”或“减小”),理由是_______
(3)某科研小组研究了反应CO(g) + 2H2(g)= CH3OH(g)的动力学,获得其速率方程v=k[c(H2)]1/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
CO的反应级数m=_______ , 当实验2进行到某时刻,测得c(H3)= 0.010 mol·L-1,则此时的反应速率v_______ mol·L-1·s-1(已知: ≈0.3)。
≈0.3)。
(4)利用CH4重整CO2的催化转化如图所示,CH4与CO2重整反应的方程式为_______ 。有关转化过程,下列说法正确的是_______ (填序号)。
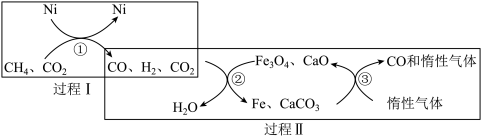
a. 过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d. 转化③中Fe与CaCO3,反应的物质的量之比为4:3
Ⅰ. CO(g) + 2H2(g)=CH3OH(g) △H。
Ⅱ. CO(g) + H2O(g)=CO2(g) +H2(g) ∆H2=-41.2 kJ/mol
回答下列问题:
(1)已知反应①中的相关化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
(2)在T℃时,向5L恒容密闭容器中加入0.6 mol CO和0.45 molH2,发生反应Ⅰ。CO和CH3OH的浓度在不同时刻的变化状况如图所示:

①下列能够说明反应在第6min时达到平衡状态的是
A.混合气体的平均摩尔质量不再改变
B. CH3OH 的浓度不变
C. v(CO)正 : v(H2)逆= 2:1
D. P(CO):P( H2)= 1:2
第8 min时改变的条件是
②在第12 min时升高温度,重新达到平衡时,化学平衡常数将
(3)某科研小组研究了反应CO(g) + 2H2(g)= CH3OH(g)的动力学,获得其速率方程v=k[c(H2)]1/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
| 实验序号 | c(H2)/mol/L | c(CO)/mol/L | v/mol/L |
| 1 | 0.100 | 0.100 | 1.2×10-2 |
| 2 | 0.050 | 0.100 | 8.4×10-3 |
| 3 | 0.100 | 0.200 | 2.4×10-2 |
 ≈0.3)。
≈0.3)。(4)利用CH4重整CO2的催化转化如图所示,CH4与CO2重整反应的方程式为

a. 过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d. 转化③中Fe与CaCO3,反应的物质的量之比为4:3
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】如何降低大气中CO2的含量及有效地开发利用CO2是当前科学家研究的重要课题。
(1)科学家用H2和CO2生产甲醇燃料。为探究该反应原理,进行如下实验:某温度下,在容积为2 L的密闭容器中充入1 mol CO2和3.25 mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
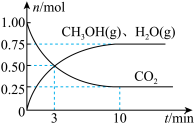
①从反应开始到3 min时,氢气的平均反应速率v(H2)=__________________ 。
②下列措施中一定能使CO2的转化率增大的是______________ 。
A.在原容器中再充入1 mol CO2 B.在原容器中再充入1 mol H2
C.在原容器中充入1 mol He D.使用更有效的催化剂
E.缩小容器的容积 F.将水蒸气从体系中分离出
(2)科学家还利用氢气在一定条件下与二氧化碳反应生成乙醇燃料,其热化学反应方程式为2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,在一定压强下,测得该反应的CO2转化率/ (%)与温度、
CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,在一定压强下,测得该反应的CO2转化率/ (%)与温度、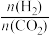 实验数据如表所示。请根据表中数据回答下列问题。
实验数据如表所示。请根据表中数据回答下列问题。
①上述反应的a________ 0(填“大于”或“小于”)。
②恒温下,向反应体系中加入固体催化剂,则反应产生的热量___________ (填“增大”、“减小”或“不变”)。
③增大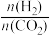 的值,则生成乙醇的物质的量
的值,则生成乙醇的物质的量______________________ (填“增大”、“减小”、“不变”或“不能确定”)。
(1)科学家用H2和CO2生产甲醇燃料。为探究该反应原理,进行如下实验:某温度下,在容积为2 L的密闭容器中充入1 mol CO2和3.25 mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。

①从反应开始到3 min时,氢气的平均反应速率v(H2)=
②下列措施中一定能使CO2的转化率增大的是
A.在原容器中再充入1 mol CO2 B.在原容器中再充入1 mol H2
C.在原容器中充入1 mol He D.使用更有效的催化剂
E.缩小容器的容积 F.将水蒸气从体系中分离出
(2)科学家还利用氢气在一定条件下与二氧化碳反应生成乙醇燃料,其热化学反应方程式为2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,在一定压强下,测得该反应的CO2转化率/ (%)与温度、
CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,在一定压强下,测得该反应的CO2转化率/ (%)与温度、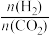 实验数据如表所示。请根据表中数据回答下列问题。
实验数据如表所示。请根据表中数据回答下列问题。温度(K) 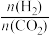 | 500 | 600 | 700 | 800 |
1.5 | 45 | 33 | 20 | 12 |
2 | 60 | 43 | 28 | 15 |
3 | 83 | 62 | 37 | 22 |
①上述反应的a
②恒温下,向反应体系中加入固体催化剂,则反应产生的热量
③增大
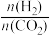 的值,则生成乙醇的物质的量
的值,则生成乙醇的物质的量
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.工业上以乙苯催化脱氢制取苯乙烯的反应如下:
 (g)
(g)
 (g)+H2(g) ΔH
(g)+H2(g) ΔH
现将 乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强
乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强 恒定。在某催化剂作用下,乙苯的平衡转化率随温度变化如图所示。
恒定。在某催化剂作用下,乙苯的平衡转化率随温度变化如图所示。

已知:气体分压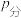 =气体总压(
=气体总压( )×体积分数。
)×体积分数。
 (g)、
(g)、 (g)、
(g)、 (g)的燃烧热
(g)的燃烧热 分别为
分别为 、
、 、
、 。
。
(1)上述反应中,
_______  (用含a、b、c的代数式表示)。
(用含a、b、c的代数式表示)。
(2)500℃时,10分钟建立平衡,用单位时间内物质的量的改变表示平均反应速率,则10分钟内v( )=
)=_______ 。
(3)a、b点的平衡常数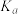
_______ 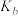 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是_______ 。
(4)550℃时,用平衡分压代替平衡浓度表示的化学平衡常数
_______ 。
 (g)
(g)
 (g)+H2(g) ΔH
(g)+H2(g) ΔH现将
 乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强
乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强 恒定。在某催化剂作用下,乙苯的平衡转化率随温度变化如图所示。
恒定。在某催化剂作用下,乙苯的平衡转化率随温度变化如图所示。
已知:气体分压
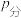 =气体总压(
=气体总压( )×体积分数。
)×体积分数。 (g)、
(g)、 (g)、
(g)、 (g)的燃烧热
(g)的燃烧热 分别为
分别为 、
、 、
、 。
。(1)上述反应中,

 (用含a、b、c的代数式表示)。
(用含a、b、c的代数式表示)。(2)500℃时,10分钟建立平衡,用单位时间内物质的量的改变表示平均反应速率,则10分钟内v(
 )=
)=(3)a、b点的平衡常数
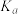
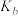 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是(4)550℃时,用平衡分压代替平衡浓度表示的化学平衡常数

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】N2O和CO是常见的环境污染气体。
(1)对于反应N2O(g)+CO(g) CO2(g)+N2(g),“Fe+”可作为该反应的催化剂。其总反应分两步进行:第一步为Fe++N2O
CO2(g)+N2(g),“Fe+”可作为该反应的催化剂。其总反应分两步进行:第一步为Fe++N2O FeO++N2;则第二步为
FeO++N2;则第二步为___________ (写离子方程式)。
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g) 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示:
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示:

①该反应的ΔH___________ 0(填“>”或“<”)。
②若容器Ⅰ的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器I中用O2表示的反应速率为___________ 。B点对应的平衡常数K=___________ (保留两位有效数字)。
③图中A、C、D三点容器内气体密度由大到小的顺序是___________ 。
(1)对于反应N2O(g)+CO(g)
 CO2(g)+N2(g),“Fe+”可作为该反应的催化剂。其总反应分两步进行:第一步为Fe++N2O
CO2(g)+N2(g),“Fe+”可作为该反应的催化剂。其总反应分两步进行:第一步为Fe++N2O FeO++N2;则第二步为
FeO++N2;则第二步为(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g)
 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示:
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示:
①该反应的ΔH
②若容器Ⅰ的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器I中用O2表示的反应速率为
③图中A、C、D三点容器内气体密度由大到小的顺序是
您最近一年使用:0次
【推荐2】含氮化合物是化工、能源、环保等领域的研究热点。
(1)工业上常用NH3和CO2合成尿素[CO(NH2)2],利用该反应可以在一定程度上减缓温室效应。该反应可分两步进行,其能量变化和反应历程如图所示___________ ;
②合成尿素总反应自发进行的条件是___________ (填“高温”或“低温”)。
(2)一定温度下,将NH3和CO2按2:1的物质的量之比充入一容积恒为10L的密闭容器中发生总反应。15min时达到平衡,各物质的浓度变化曲线如图所示。___________ g min﹣1。
min﹣1。
②下列叙述中能说明该反应达到平衡状态的是___________ (填选项字母)。
A.体系压强不再变化
B.NH3和CO2的浓度之比为2:1
C.气体平均摩尔质量不再变化
D.NH3的消耗速率和CO2的消耗速率之比为2:1
③25min时再向容器中充入2mol的NH3、1molCO2和2molH2O,则此时平衡___________ (填“正向移动”或“逆向移动”),再次平衡时总反应的平衡常数为 ___________ 。
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量NO。中国科学家在以H2为还原剂清除NO的研究方面取得了显著成果,其化学方程式为2NO(g)+2H2(g)⇌N2(g)+2H2O(g) ΔH<0。当固定比例的NO(g)和H2(g)的混合气体,以相同流速分别通过填充有两种催化剂的反应器,测得NO的转化率与温度的关系如图所示。___________ 。
②M、N、P、Q四点中一定未达到平衡状态的是___________ (填字母)。
(1)工业上常用NH3和CO2合成尿素[CO(NH2)2],利用该反应可以在一定程度上减缓温室效应。该反应可分两步进行,其能量变化和反应历程如图所示

②合成尿素总反应自发进行的条件是
(2)一定温度下,将NH3和CO2按2:1的物质的量之比充入一容积恒为10L的密闭容器中发生总反应。15min时达到平衡,各物质的浓度变化曲线如图所示。

 min﹣1。
min﹣1。②下列叙述中能说明该反应达到平衡状态的是
A.体系压强不再变化
B.NH3和CO2的浓度之比为2:1
C.气体平均摩尔质量不再变化
D.NH3的消耗速率和CO2的消耗速率之比为2:1
③25min时再向容器中充入2mol的NH3、1molCO2和2molH2O,则此时平衡
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量NO。中国科学家在以H2为还原剂清除NO的研究方面取得了显著成果,其化学方程式为2NO(g)+2H2(g)⇌N2(g)+2H2O(g) ΔH<0。当固定比例的NO(g)和H2(g)的混合气体,以相同流速分别通过填充有两种催化剂的反应器,测得NO的转化率与温度的关系如图所示。
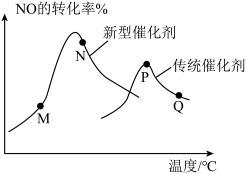
②M、N、P、Q四点中一定未达到平衡状态的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
I.温室气体让地球发烧,倡导低碳生活,是一种可持续发展的环保责任,将CO2应用于生产中实现其综合利用是目前的研究热点。
(1)在催化作用下由CO2和CH4转化为CH3COOH的反应历程示意图如图。

在合成CH3COOH的反应历程中,下列有关说法正确的是___________ (填字母序号)。
a.该催化剂使反应的平衡常数增大
b.CH4→CH3COOH过程中,有C—H键断裂和C—C键形成
c.生成乙酸的反应原子利用率100%
d.ΔH=E2-E1
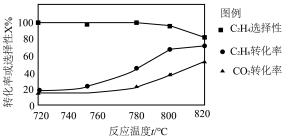
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应:CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示:工业生产中主反应应选择的温度是
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示:工业生产中主反应应选择的温度是___________ 。
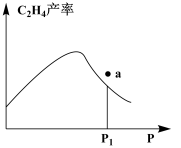
(3)在一定温度下的密闭容器中充入一定量的CO2和C2H6,发生主反应:CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1,固定时间测定不同压强下C2H4的产率如图所示,P1压强下a点反应速率v(正)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1,固定时间测定不同压强下C2H4的产率如图所示,P1压强下a点反应速率v(正)___________ v(逆)。
(4)某温度下,在0.1MPa恒压密闭容器中充入等物质的量的CO2和C2H6,只发生主反应:CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应),达到平衡时C2H4的物质的量分数为20%,该温度下反应的平衡常数Kp=
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应),达到平衡时C2H4的物质的量分数为20%,该温度下反应的平衡常数Kp=___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅱ.以氨气作还原剂,可除去烟气中的氮氧化物。其中除去NO的反应原理为:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH=−1980kJ/mol
5N2(g)+6H2O(g) ΔH=−1980kJ/mol
(5)反应速率与浓度之间存在如下关系:v正=k正c4(NH3)·c6(NO),v逆=k逆c5(N2)·c6(H2O)。k正、k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9molNH3(g)和1.2molNO(g)发生反应,保持温度不变,平衡时NO的转化率为50%,则此温度下 =
=___________ ;当温度升高时,k正增大m倍,k逆增大n倍,则m___________ n(填“>”、“<”或“=”)。
(6)保持温度不变,在恒容密闭容器中按一定比充入NH3(g)和NO(g)发生反应,达到平衡时H2O(g)的体积分数φ(H2O)随 的变化如图所示,当
的变化如图所示,当 时,达到平衡时φ(H2O)可能是A、B、C三点中的
时,达到平衡时φ(H2O)可能是A、B、C三点中的___________ (填“A”、“B”或“C”)。

I.温室气体让地球发烧,倡导低碳生活,是一种可持续发展的环保责任,将CO2应用于生产中实现其综合利用是目前的研究热点。
(1)在催化作用下由CO2和CH4转化为CH3COOH的反应历程示意图如图。

在合成CH3COOH的反应历程中,下列有关说法正确的是
a.该催化剂使反应的平衡常数增大
b.CH4→CH3COOH过程中,有C—H键断裂和C—C键形成
c.生成乙酸的反应原子利用率100%
d.ΔH=E2-E1
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应:CO2(g)+C2H6(g)
 C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示:工业生产中主反应应选择的温度是
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示:工业生产中主反应应选择的温度是
(3)在一定温度下的密闭容器中充入一定量的CO2和C2H6,发生主反应:CO2(g)+C2H6(g)
 C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1,固定时间测定不同压强下C2H4的产率如图所示,P1压强下a点反应速率v(正)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1,固定时间测定不同压强下C2H4的产率如图所示,P1压强下a点反应速率v(正)
(4)某温度下,在0.1MPa恒压密闭容器中充入等物质的量的CO2和C2H6,只发生主反应:CO2(g)+C2H6(g)
 C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应),达到平衡时C2H4的物质的量分数为20%,该温度下反应的平衡常数Kp=
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应),达到平衡时C2H4的物质的量分数为20%,该温度下反应的平衡常数Kp=Ⅱ.以氨气作还原剂,可除去烟气中的氮氧化物。其中除去NO的反应原理为:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) ΔH=−1980kJ/mol
5N2(g)+6H2O(g) ΔH=−1980kJ/mol(5)反应速率与浓度之间存在如下关系:v正=k正c4(NH3)·c6(NO),v逆=k逆c5(N2)·c6(H2O)。k正、k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9molNH3(g)和1.2molNO(g)发生反应,保持温度不变,平衡时NO的转化率为50%,则此温度下
 =
=(6)保持温度不变,在恒容密闭容器中按一定比充入NH3(g)和NO(g)发生反应,达到平衡时H2O(g)的体积分数φ(H2O)随
 的变化如图所示,当
的变化如图所示,当 时,达到平衡时φ(H2O)可能是A、B、C三点中的
时,达到平衡时φ(H2O)可能是A、B、C三点中的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】将烟气和空气中的 通过催化方式直接还原为甲烷等燃料的过程具有非常重要的意义。
通过催化方式直接还原为甲烷等燃料的过程具有非常重要的意义。
Ⅰ.光催化还原
(1)华中科技大学某团队通过卟啉聚合物在空心 纳米粒子表面交联,构建了一种性能优异的复合结构光催化剂,其催化原理如图所示,其中
纳米粒子表面交联,构建了一种性能优异的复合结构光催化剂,其催化原理如图所示,其中 的转化率约为12%,
的转化率约为12%, 的选择性约为70%。图中
的选择性约为70%。图中 和
和 转化为
转化为 和
和 的化学方程式为
的化学方程式为___________ 。

Ⅱ.热催化还原——萨巴蒂尔反应: ,
, 时,在一恒容密闭容器中通入
时,在一恒容密闭容器中通入 、
、 ,至其分压分别为
,至其分压分别为 ,再加入催化剂并加热使其发生萨巴蒂尔反应。
,再加入催化剂并加热使其发生萨巴蒂尔反应。
(2)为使固体催化剂与反应物充分接触,应采取的措施是___________ 。
(3)研究表明 的反应速率
的反应速率 ,某时刻测得
,某时刻测得 的分压为
的分压为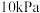 ,则该时刻
,则该时刻
___________  。
。
(4) ,平衡时,
,平衡时, 的分压为
的分压为 ,该反应的平衡常数
,该反应的平衡常数 为
为___________  (平衡常数可以用反应体系中气体物质的分压表示)。
(平衡常数可以用反应体系中气体物质的分压表示)。
(5)相同时间内,不同催化剂(Ⅰ、Ⅱ、Ⅲ)下,测得 的转化率如图所示。在
的转化率如图所示。在 时,不同催化剂下,
时,不同催化剂下, 的转化率相同的原因是
的转化率相同的原因是___________ 。温度高于 时,
时, 的转化率降低的原因是
的转化率降低的原因是___________ 。

(6) 光催化还原和热催化还原法中更好的是
光催化还原和热催化还原法中更好的是___________ ,简述理由:___________ (答一条即可)
 通过催化方式直接还原为甲烷等燃料的过程具有非常重要的意义。
通过催化方式直接还原为甲烷等燃料的过程具有非常重要的意义。Ⅰ.光催化还原
(1)华中科技大学某团队通过卟啉聚合物在空心
 纳米粒子表面交联,构建了一种性能优异的复合结构光催化剂,其催化原理如图所示,其中
纳米粒子表面交联,构建了一种性能优异的复合结构光催化剂,其催化原理如图所示,其中 的转化率约为12%,
的转化率约为12%, 的选择性约为70%。图中
的选择性约为70%。图中 和
和 转化为
转化为 和
和 的化学方程式为
的化学方程式为
Ⅱ.热催化还原——萨巴蒂尔反应:
 ,
, 时,在一恒容密闭容器中通入
时,在一恒容密闭容器中通入 、
、 ,至其分压分别为
,至其分压分别为 ,再加入催化剂并加热使其发生萨巴蒂尔反应。
,再加入催化剂并加热使其发生萨巴蒂尔反应。(2)为使固体催化剂与反应物充分接触,应采取的措施是
(3)研究表明
 的反应速率
的反应速率 ,某时刻测得
,某时刻测得 的分压为
的分压为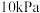 ,则该时刻
,则该时刻
 。
。(4)
 ,平衡时,
,平衡时, 的分压为
的分压为 ,该反应的平衡常数
,该反应的平衡常数 为
为 (平衡常数可以用反应体系中气体物质的分压表示)。
(平衡常数可以用反应体系中气体物质的分压表示)。(5)相同时间内,不同催化剂(Ⅰ、Ⅱ、Ⅲ)下,测得
 的转化率如图所示。在
的转化率如图所示。在 时,不同催化剂下,
时,不同催化剂下, 的转化率相同的原因是
的转化率相同的原因是 时,
时, 的转化率降低的原因是
的转化率降低的原因是
(6)
 光催化还原和热催化还原法中更好的是
光催化还原和热催化还原法中更好的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】双温–双催化剂(Fe–TiO2–xHy)法可提升合成氨反应中NH3的产率。将一定比例N2、H2混合气体,匀速通过装有不同催化剂的反应器中发生反应:N2(g) + 3H2(g) 2NH3(g) ΔH =-92.4 kJ·mol−1,NH3的平衡浓度随体系温度的变化如图所示。
2NH3(g) ΔH =-92.4 kJ·mol−1,NH3的平衡浓度随体系温度的变化如图所示。
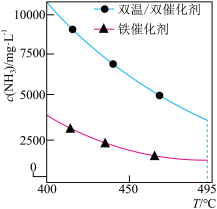
(1)体系温度为495℃,光照条件下,双催化剂(Fe–TiO2–xHy)会产生温差。分别使用双温–双催化剂以及铁催化剂催化合成氨反应,可能的机理如图所示。
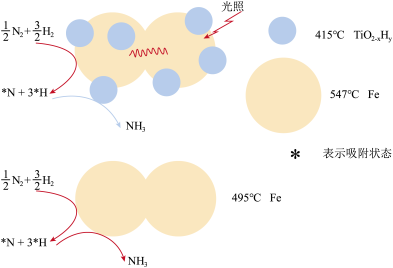
双温–双催化剂法的反应过程可描述为___________ 。从化学反应速率和化学平衡的角度出发,双温–双催化剂法的优点是___________ 。合成氨过程中需要不断分离出氨,原因是___________ 。
(2)利用NH3可消除氮氧化物对环境的污染。NH3和NO在Ag2O催化剂表面反应时,相同时间下,NO生成N2的转化率随温度的变化如图所示。
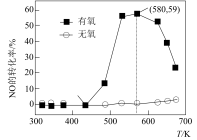
NH3与NO反应生成N2的化学方程式为___________ ,当生成1 mol N2时,转移的电子数为___________ mol。在500~580 K之间,有氧气存在的条件下NO生成N2的转化率明显高于无氧条件,可能的原因是___________ 。
 2NH3(g) ΔH =-92.4 kJ·mol−1,NH3的平衡浓度随体系温度的变化如图所示。
2NH3(g) ΔH =-92.4 kJ·mol−1,NH3的平衡浓度随体系温度的变化如图所示。
(1)体系温度为495℃,光照条件下,双催化剂(Fe–TiO2–xHy)会产生温差。分别使用双温–双催化剂以及铁催化剂催化合成氨反应,可能的机理如图所示。

双温–双催化剂法的反应过程可描述为
(2)利用NH3可消除氮氧化物对环境的污染。NH3和NO在Ag2O催化剂表面反应时,相同时间下,NO生成N2的转化率随温度的变化如图所示。

NH3与NO反应生成N2的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】含氮化合物在农业、工业、国防等领域都有着广泛的应用。氮元素部分常见物质间的相互转化如图所示。
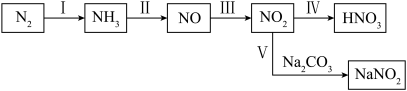
回答相关问题。
Ⅰ.
(1)图示中标示出了以氨为原料制备硝酸的全过程,写出过程Ⅱ的化学方程式:_____ ;过程Ⅳ不断通入空气,理论上能使 最终完全吸收,则1.7吨
最终完全吸收,则1.7吨 理论上可以得到
理论上可以得到_____ 吨质量分数为63%的硝酸。
(2)某温度下,在容积恒定为 的密闭容器中充入
的密闭容器中充入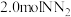 和
和 ,一段时间后反应达平衡状态,实验数据如下表所示
,一段时间后反应达平衡状态,实验数据如下表所示
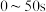 内的平均反应速率
内的平均反应速率
_____ ,250s时, 的转化率为
的转化率为_____ 。
Ⅱ.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是 )和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
)和水分子通过。其工作原理的示意图如图所示,请回答下列问题:

(3)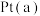 电极是电池的
电极是电池的_____ (填“正”或“负”)极。
(4)电解质溶液中的 向
向_____ (填“a”或“b”)极移动。
(5)该电池的负极反应式为_____

回答相关问题。
Ⅰ.
(1)图示中标示出了以氨为原料制备硝酸的全过程,写出过程Ⅱ的化学方程式:
 最终完全吸收,则1.7吨
最终完全吸收,则1.7吨 理论上可以得到
理论上可以得到(2)某温度下,在容积恒定为
 的密闭容器中充入
的密闭容器中充入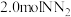 和
和 ,一段时间后反应达平衡状态,实验数据如下表所示
,一段时间后反应达平衡状态,实验数据如下表所示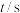 | 0 | 50 | 150 | 250 | 350 |
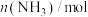 | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
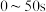 内的平均反应速率
内的平均反应速率
 的转化率为
的转化率为Ⅱ.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是
 )和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
)和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
(3)
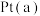 电极是电池的
电极是电池的(4)电解质溶液中的
 向
向(5)该电池的负极反应式为
您最近一年使用:0次



