下列事实能用勒夏特列原理解释的是
| A.液氯用干燥的钢瓶储存 |
| B.把食品存放在冰箱里可延长保质期 |
| C.合成氨工业中使用铁触媒作催化剂 |
| D.配置FeCl3溶液,常将FeCl3晶体溶于较浓的盐酸中 |
更新时间:2023-12-26 22:11:40
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】关于某反应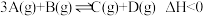 ,下列说法正确的是
,下列说法正确的是
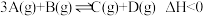 ,下列说法正确的是
,下列说法正确的是| A.增大压强,平衡正向移动,该反应的平衡常数K增大 |
| B.升高温度可使该反应的正反应速率增大,逆反应速率减小 |
| C.温度越低越有利于该反应的进行,从而提高甲醇的生产效率 |
| D.使用高效催化剂,能增大活化分子百分数,提高反应速率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在锌与某浓度的盐酸反应的实验中,得到如下结果:
下列说法中,正确的是
①t1<t2 ②t1>150 ③实验1和实验2比较,单位时间内消耗的锌的质量前者小于后者
| 实验序号 | 锌的质量/g | 锌的形状 | 温度/℃ | 锌完全溶解于酸的时间/s |
1 | 2 | 薄片 | 15 | 150 |
2 | 2 | 薄片 | 35 | t1 |
3 | 2 | 粉末 | 35 | t2 |
①t1<t2 ②t1>150 ③实验1和实验2比较,单位时间内消耗的锌的质量前者小于后者
| A.只有① | B.①② | C.只有③ | D.②③ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO: 该反应在恒容的密闭容器中进行,下列有关说法正确的是
该反应在恒容的密闭容器中进行,下列有关说法正确的是
 该反应在恒容的密闭容器中进行,下列有关说法正确的是
该反应在恒容的密闭容器中进行,下列有关说法正确的是
A.当生成速率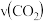 : :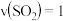 :1时反应达到平衡 :1时反应达到平衡 |
| B.平衡后保持其他条件不变,分离出部分MgO,平衡向正反应方向移动 |
C.平衡后保持其他条件不变,通入CO再次平衡时CO与 的物质的量之比减小 的物质的量之比减小 |
| D.平衡后保持其他条件不变,升高温度CO的转化率及该反应的化学平衡常数均增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】生物大分子血红蛋白分子链的部分结构及载氧示意如图, 与周围的6个原子均以配位键结合。
与周围的6个原子均以配位键结合。 也可与血红蛋白配位,使人体中毒。二者与血红蛋白
也可与血红蛋白配位,使人体中毒。二者与血红蛋白 结合的反应可表示为:①
结合的反应可表示为:①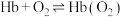 ;②
;②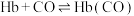 。下列说法错误的是
。下列说法错误的是
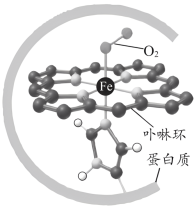
 与周围的6个原子均以配位键结合。
与周围的6个原子均以配位键结合。 也可与血红蛋白配位,使人体中毒。二者与血红蛋白
也可与血红蛋白配位,使人体中毒。二者与血红蛋白 结合的反应可表示为:①
结合的反应可表示为:①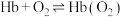 ;②
;②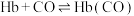 。下列说法错误的是
。下列说法错误的是
| A.构成血红蛋白分子链的多肽链之间存在氢键 |
B.电负性:C>O,故 中与 中与 配位的是C 配位的是C |
C. 与血红素中 与血红素中 结合能力强于 结合能力强于 |
D. 中毒患者进入高压氧舱治疗,平衡①、②移动的方向相反 中毒患者进入高压氧舱治疗,平衡①、②移动的方向相反 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实,不能用勒夏特列原理解释的是
| A.氨水中加酸,NH4+ 的浓度增大 |
| B.装有NO2和N2O4平衡的混合气体的玻璃球在冷水中气体颜色变浅 |
| C.实验室中常用排饱和食盐水的方法收集Cl2 |
| D.H2、I2、HI的体系平衡后,加压混合气体颜色变深 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.在恒温的密闭容器中发生可逆反应2NO2⇌N2O4,在一定条件下达到平衡后,在平衡后的某一时刻迅速增大压强,混合气体的颜色先变深后变浅,最后比原来深 |
| B.在一定条件下,可逆反应C(s)+CO2(g)⇌2CO(g) △H>0达到平衡状态,升高温度,正反应速率增大,逆反应速率减小,平衡正向移动 |
| C.在FeCl3和KSCN反应后的溶液里加入少量KCl固体,血红色变浅 |
| D.反应中加入催化剂,可以降低反应所需要的活化能,增加了单位体积内活化分子数,但活化分子百分数不变 |
您最近半年使用:0次

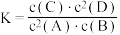 。恒容时,若降低温度,D的浓度增大。下列说法错误的是
。恒容时,若降低温度,D的浓度增大。下列说法错误的是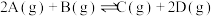
 不变
不变 ,反应速率加快
,反应速率加快

