湿法炼锌净化钴渣中含有Zn、Co、Cu和Fe的单质及Zn(OH)2,可利用过硫酸钠氧化水解法实现钴的富集,同时分别回收锌、铜和铁元素,工艺流程如下:
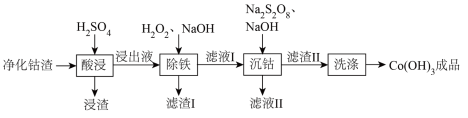
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
回答下列问题:
(1)净化钴渣研细的目的是___________ 。
(2)浸渣的主要成分为________ (填名称),其对应元素原子的价电子排布式为_________ 。
(3)钴属于铁系元素,性质与铁相似。根据流程可知:Co2+的还原性___________ (填“强于”、“弱于”)Fe2+。
(4)利用上述表格数据,计算Co(OH)2的Ksp=___________ ;如果滤液I中Co2+浓度为0.1mol·L−1,则“除铁”应控制的pH范围是___________ 。
(5)氨水可代替沉钴工序中的NaOH,此时发生的主要反应的离子方程式为___________ 。
(6)上述流程中___________(填标号)可返回湿法炼锌系统,提高锌的利用率。
(7)Co(OH)3可与浓盐酸反应产生黄绿色气体,其化学方程式为___________ 。

该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
| 金属离子 | Fe3+ | Fe2+ | Co2+ |
| 开始沉淀(c=0.01mol/L)的pH | 1.9 | 7.5 | 7.7 |
| 沉淀完全(c=1.0×10-5mol/L)的pH | 3.2 | 9.0 | 9.2 |
(1)净化钴渣研细的目的是
(2)浸渣的主要成分为
(3)钴属于铁系元素,性质与铁相似。根据流程可知:Co2+的还原性
(4)利用上述表格数据,计算Co(OH)2的Ksp=
(5)氨水可代替沉钴工序中的NaOH,此时发生的主要反应的离子方程式为
(6)上述流程中___________(填标号)可返回湿法炼锌系统,提高锌的利用率。
| A.浸渣 | B.滤渣I | C.滤液Ⅱ | D.滤渣Ⅱ |
更新时间:2024-01-05 20:18:28
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】硫氰化钾( )俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示。已知:
)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示。已知: ,该反应比较缓慢且
,该反应比较缓慢且 在高于170℃易分解。
在高于170℃易分解。

回答下列问题:
(1)装置C的作用是观察气泡流速,以便控制加热温度,则C中所选用的最佳试剂是______ 。
(2)装置D中三颈烧瓶的左侧导气管口必须插入下层 液体中,其目的是
液体中,其目的是______ 。
(3)制备 溶液:熄灭A处的酒精灯,关闭
溶液:熄灭A处的酒精灯,关闭 ,保持三颈烧瓶内液温105℃一段时间,其目的是
,保持三颈烧瓶内液温105℃一段时间,其目的是______ ,然后打开 ,继续保持液温105℃,缓缓滴入适量的
,继续保持液温105℃,缓缓滴入适量的 溶液,写出装置D中生成
溶液,写出装置D中生成 的化学方程式:
的化学方程式:______ 。
(4)装置E的作用为吸收尾气,防止污染环境,写出吸收 时的离子方程式
时的离子方程式______ 。
(5)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再在减压条件下______ 、过滤、洗涤、干燥,得到硫氰化钾晶体。
(6)测定晶体中 的含量:称取
的含量:称取 样品。配成
样品。配成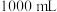 溶液量取
溶液量取 于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用
于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用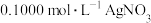 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液
标准溶液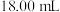 。已知:滴定时发生的反应:
。已知:滴定时发生的反应: (白色)。
(白色)。
①滴定过程的指示剂a为______ 。
②晶体中 的质量分数为
的质量分数为______ 。
 )俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示。已知:
)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示。已知: ,该反应比较缓慢且
,该反应比较缓慢且 在高于170℃易分解。
在高于170℃易分解。
回答下列问题:
(1)装置C的作用是观察气泡流速,以便控制加热温度,则C中所选用的最佳试剂是
(2)装置D中三颈烧瓶的左侧导气管口必须插入下层
 液体中,其目的是
液体中,其目的是(3)制备
 溶液:熄灭A处的酒精灯,关闭
溶液:熄灭A处的酒精灯,关闭 ,保持三颈烧瓶内液温105℃一段时间,其目的是
,保持三颈烧瓶内液温105℃一段时间,其目的是 ,继续保持液温105℃,缓缓滴入适量的
,继续保持液温105℃,缓缓滴入适量的 溶液,写出装置D中生成
溶液,写出装置D中生成 的化学方程式:
的化学方程式:(4)装置E的作用为吸收尾气,防止污染环境,写出吸收
 时的离子方程式
时的离子方程式(5)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再在减压条件下
(6)测定晶体中
 的含量:称取
的含量:称取 样品。配成
样品。配成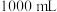 溶液量取
溶液量取 于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用
于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用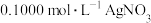 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液
标准溶液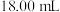 。已知:滴定时发生的反应:
。已知:滴定时发生的反应: (白色)。
(白色)。①滴定过程的指示剂a为
②晶体中
 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】锰及其化合物用途广泛,以菱锰矿(主要成分为MnCO3,还含有铁、镍、钴的碳酸盐以及SiO2杂质)为原料生产金属锰和高品位MnCO3的工艺流程如图:

(1)“溶浸”过程中,从实际可行的工艺出发,下列措施可用于提高浸出率的有_______ (填字母)。
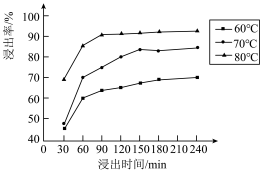
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳工艺条件为_______ 。
(3)滤渣1中残余的MnO2,可加入葡萄糖(C6H12O6)和硫酸溶液处理,反应的氧化产物为CO2,写出对应的离子方程式:________ 。
(4)“除杂”步骤所得滤渣2的主要成分除了CoS、NiS以外,还有________ (填化学式)。
(5)“沉锰”的原理为_________ (用离子方程式表示);“沉锰”的关键操作是将反应终点pH控制在7附近,原因是________ 。
(6)若以Fe作电极,MnSO4、ZnSO4溶液为电解液,经过一系列步骤制得隐形战机涂料ZnxMn(1-x)Fe2O4,则电解过程中生成ZnxMn(1-x)Fe2O4的电极反应为________ 。

(1)“溶浸”过程中,从实际可行的工艺出发,下列措施可用于提高浸出率的有
| A.适当升高溶浸温度 | B.适当加快搅拌速度 |
| C.适当缩短溶浸时间 | D.使用浓硝酸代替稀硫酸 |
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳工艺条件为

(3)滤渣1中残余的MnO2,可加入葡萄糖(C6H12O6)和硫酸溶液处理,反应的氧化产物为CO2,写出对应的离子方程式:
(4)“除杂”步骤所得滤渣2的主要成分除了CoS、NiS以外,还有
(5)“沉锰”的原理为
(6)若以Fe作电极,MnSO4、ZnSO4溶液为电解液,经过一系列步骤制得隐形战机涂料ZnxMn(1-x)Fe2O4,则电解过程中生成ZnxMn(1-x)Fe2O4的电极反应为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】ZnO是电镀、涂料、有机合成等化学工业的重要原料。某课题组设计由含锌工业废料(含Fe、Cu、Mn等杂质)生产ZnO的工艺流程如下:
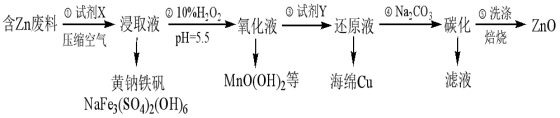
已知:黄钠铁矾在pH为1.5,温度为90℃时完全沉淀,且易于过滤。
(1)试剂X为Na2SO4和___________ 的混合液,步骤①的浸取液里除含有Cu2+、Mn2+以外,还含有的金属离子有___________ ,写出Cu溶解变为Cu2+离子方程式___________ 。
(2)步骤②可进一步氧化除铁,还氧化除去了Mn2+,试写出相应的除去Mn2+的离子方程式___________ 。
(3)步骤③加入试剂Y的目的是置换出Cu,则Y的化学式为___________ ,整个工艺流程中可以循环使用的试剂是___________ 。
(4)步骤⑤中检验沉淀是否洗涤干净的操作方法是___________ 。
(5)步骤④碳化实际得到的是一种碱式碳酸锌[ZnCO3·xZn(OH)2·yH2O],取该样品6.82g,充分灼烧后测得残留物质量为4.86g,将所得气体通入足量澄清石灰水中,得到2.00g沉淀,则此碱式碳酸锌的化学式是___________ 。

已知:黄钠铁矾在pH为1.5,温度为90℃时完全沉淀,且易于过滤。
(1)试剂X为Na2SO4和
(2)步骤②可进一步氧化除铁,还氧化除去了Mn2+,试写出相应的除去Mn2+的离子方程式
(3)步骤③加入试剂Y的目的是置换出Cu,则Y的化学式为
(4)步骤⑤中检验沉淀是否洗涤干净的操作方法是
(5)步骤④碳化实际得到的是一种碱式碳酸锌[ZnCO3·xZn(OH)2·yH2O],取该样品6.82g,充分灼烧后测得残留物质量为4.86g,将所得气体通入足量澄清石灰水中,得到2.00g沉淀,则此碱式碳酸锌的化学式是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而_____________ 。
(2) 加入NH3·H2O调节pH=8可除去____ (填离子符号),此时,溶液中该离子的浓度为______ mol·L-1。再加入NaOH调pH=12.5,溶液内剩余的阳离子中______ 完全沉淀,____ 部分沉淀 (填离子符号)。加入H2C2O4时应避免过量,原因是____ 。已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9, Ksp[Fe(OH)3] =2.6×10-39。
(3由于Na2S2O5具有毒性,因此国家对其在食品中的用量有严格的规定。某化学兴趣小组在测定某白葡萄酒中Na2S2O5的残留量时,取40mL葡萄酒样品于锥形瓶中,滴入几滴淀粉溶液,用0.02 mol·L-1碘的标准溶液滴定至终点,消耗碘标准溶液5mL,则滴定终点的现象为__________ ,Na2S2O5的含量是以SO2来计算的,则该样品中Na2S2O5的残留量以 计为
计为______  。
。
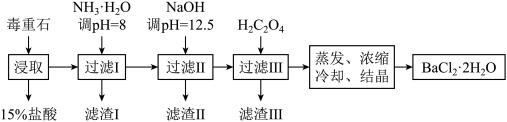
(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而
(2) 加入NH3·H2O调节pH=8可除去
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
 计为
计为 。
。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料。氯化水解法生产三氯氧磷的流程如下:
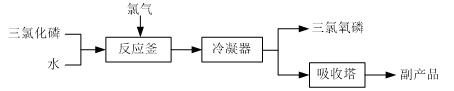
⑴氯化水解法生产三氯氧磷的化学方程式为______ 。
⑵通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取a g产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用c mol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是______ (选填字母),滴定终点的现象为______ 。
a.NH4Fe(SO4)2 b.FeCl2 c.甲基橙 d.淀粉
②实验过程中加入硝基苯的目的是_____________________ ,如无此操作所测Cl元素含量将会______ (填“偏大”、“偏小”或“不变”)
⑶氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水。在废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。
①在沉淀前先加入适量漂白粉的作用是_________________ 。
②下图是不同条件对磷的沉淀回收率的影响图象。
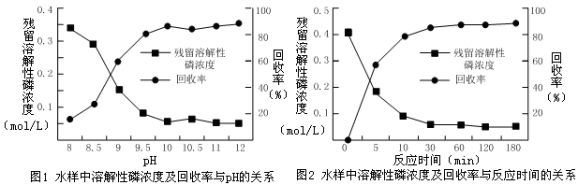
处理该厂废水最合适的工艺条件为______ (选填字母)。
a.调节pH=9 b.调节pH=10 c.反应时间30 min d.反应时间120 min
③若处理后的废水中c(PO43-)=4×10-7 mol·L-1,溶液中c(Ca2+)=__________ mol·L-1。
(已知Ksp[Ca3(PO4)2]=2×10-29)

⑴氯化水解法生产三氯氧磷的化学方程式为
⑵通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取a g产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用c mol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是
a.NH4Fe(SO4)2 b.FeCl2 c.甲基橙 d.淀粉
②实验过程中加入硝基苯的目的是
⑶氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水。在废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。
①在沉淀前先加入适量漂白粉的作用是
②下图是不同条件对磷的沉淀回收率的影响图象。

处理该厂废水最合适的工艺条件为
a.调节pH=9 b.调节pH=10 c.反应时间30 min d.反应时间120 min
③若处理后的废水中c(PO43-)=4×10-7 mol·L-1,溶液中c(Ca2+)=
(已知Ksp[Ca3(PO4)2]=2×10-29)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】纳米铁在废水处理、材料研发等领域有重要应用。以某钛白粉厂副产品(主要含 ,还含有
,还含有 、
、 、
、 等杂质)为原料制备纳米铁的流程如下:
等杂质)为原料制备纳米铁的流程如下:

已知: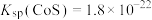 ,
, ,
,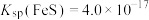 ,
,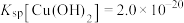 。当溶液中离子浓度小于
。当溶液中离子浓度小于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。 在溶液中以
在溶液中以 和
和 形式存在。
形式存在。
(1) 中阴离子的空间结构为
中阴离子的空间结构为___________ 。
(2)结合离子方程式解释“除钛”时加入铁粉的作用:___________ 。
(3)“除钴镍”完全后,溶液中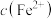 的最大值为
的最大值为___________  。
。
(4)“还原”时 与
与 以物质的量之比
以物质的量之比 反应,写出该反应的化学方程式
反应,写出该反应的化学方程式___________ 。
(5)用纳米铁去除废水中的 。常温下,选择
。常温下,选择 初始浓度为
初始浓度为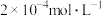 的废水,控制纳米铁用量相同,测得
的废水,控制纳米铁用量相同,测得 去除率随初始
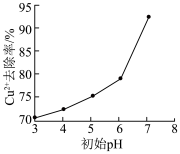
去除率随初始 的变化如图所示。写出初始
的变化如图所示。写出初始 在
在 内
内 去除率随初始
去除率随初始 增大缓慢上升而初始
增大缓慢上升而初始 在
在 内
内 去除率随初始
去除率随初始 增大快速上升的原因:
增大快速上升的原因:___________ 。
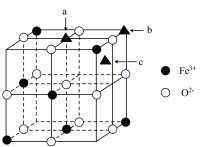
(6)利用该纳米铁制成的改性 是一种优良的磁性材料,该
是一种优良的磁性材料,该 晶胞的
晶胞的 的结构如图所示,研究发现结构中的
的结构如图所示,研究发现结构中的 只可能出现在图中某一“▲”所示位置上,请确定
只可能出现在图中某一“▲”所示位置上,请确定 所在晶胞的位置
所在晶胞的位置___________ (填a或b或c)。
 ,还含有
,还含有 、
、 、
、 等杂质)为原料制备纳米铁的流程如下:
等杂质)为原料制备纳米铁的流程如下:
已知:
 ,
, ,
,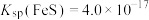 ,
,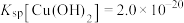 。当溶液中离子浓度小于
。当溶液中离子浓度小于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。 在溶液中以
在溶液中以 和
和 形式存在。
形式存在。(1)
 中阴离子的空间结构为
中阴离子的空间结构为(2)结合离子方程式解释“除钛”时加入铁粉的作用:
(3)“除钴镍”完全后,溶液中
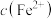 的最大值为
的最大值为 。
。(4)“还原”时
 与
与 以物质的量之比
以物质的量之比 反应,写出该反应的化学方程式
反应,写出该反应的化学方程式(5)用纳米铁去除废水中的
 。常温下,选择
。常温下,选择 初始浓度为
初始浓度为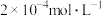 的废水,控制纳米铁用量相同,测得
的废水,控制纳米铁用量相同,测得 去除率随初始
去除率随初始 的变化如图所示。写出初始
的变化如图所示。写出初始 在
在 内
内 去除率随初始
去除率随初始 增大缓慢上升而初始
增大缓慢上升而初始 在
在 内
内 去除率随初始
去除率随初始 增大快速上升的原因:
增大快速上升的原因:
(6)利用该纳米铁制成的改性
 是一种优良的磁性材料,该
是一种优良的磁性材料,该 晶胞的
晶胞的 的结构如图所示,研究发现结构中的
的结构如图所示,研究发现结构中的 只可能出现在图中某一“▲”所示位置上,请确定
只可能出现在图中某一“▲”所示位置上,请确定 所在晶胞的位置
所在晶胞的位置
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】X、Y、Z、M、Q、R是元素周期表中前四周期元素,且原子序数依次增大,其相关信息如表所示:
回答下列问题。
(1)X与Q的电负性大小顺序为___________ (用元素符号表示)。
(2)Y元素基态原子的简化电子排布式为___________ ;R元素基态原子的价层电子轨道表示式为___________ 。
(3)R元素可形成 和
和 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(4)Y、Z的电负性较大的是___________ (填元素符号)。
(5)与M元素成对角线规则关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物对应的水化物反应的离子方程式:___________ 。
| 元素 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 原子半径在同周期主族元素中最大 |
| M | 逐级电离能(单位: )依次为578、1817、2745、11575、14830、18376、23293 )依次为578、1817、2745、11575、14830、18376、23293 |
| Q | 基态原子的核外电子占据5个能级,且最外层p轨道上有2个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子3d能级上有6个电子 |
(1)X与Q的电负性大小顺序为
(2)Y元素基态原子的简化电子排布式为
(3)R元素可形成
 和
和 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(4)Y、Z的电负性较大的是
(5)与M元素成对角线规则关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】氮化硼(BN)被称为一种“宇宙时代的材料”,具有很大的硬度。
(1)基态硼原子有__________ 个未成对电子,氮离子的电子排布式为__________ 。
(2)部分硼的化合物有以下转化: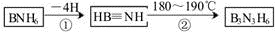
则下列叙述正确的是__________ (填序号);
A.B3N3H6俗称无机苯,但不是平面分子
B.BNH6与乙烷是等电子体
C.HB≡NH中的硼原子、氮原子的杂化类型相同
D.硼、氮、氧三元素的第一电离能比较:B<N<O
(3)下图的晶体结构中,黑球白球分别代表不同的原子、离子或分子,则图1的晶胞中含有的粒子总数为__________ ;图2中的白球的配位数是__________ 。
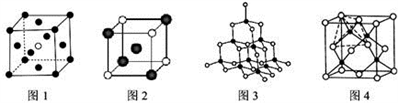
(4)已知图3、4均表示BN晶体的结构,制备氮化硼的原理为:BCl3+2NH3=BN+2HCl+NH4Cl,当该反应中有1mol BN生成时,则反应中可形成__________ mol配位键,比较氮化硼晶体与晶体硅的沸点高低并解释原因________________________
(1)基态硼原子有
(2)部分硼的化合物有以下转化:

则下列叙述正确的是
A.B3N3H6俗称无机苯,但不是平面分子
B.BNH6与乙烷是等电子体
C.HB≡NH中的硼原子、氮原子的杂化类型相同
D.硼、氮、氧三元素的第一电离能比较:B<N<O
(3)下图的晶体结构中,黑球白球分别代表不同的原子、离子或分子,则图1的晶胞中含有的粒子总数为

(4)已知图3、4均表示BN晶体的结构,制备氮化硼的原理为:BCl3+2NH3=BN+2HCl+NH4Cl,当该反应中有1mol BN生成时,则反应中可形成
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】铜及其化合物在生产生活中有广泛的应用。
(1)基态Cu+离子的核外电子排布式为_______ ;Cu2O和Cu2S都是离子晶体,二者熔点较高的是_______ 。
(2)Cu2+与4-甲基咪唑(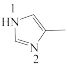 )形成的配合物可用于反向ATRP(原子转移自由基聚合)的新型催化剂。4-甲基咪唑中1号N原子的孤电子对可参与形成大π键,使电子云密度降低,分子具有一定的稳定性。则能与Cu2+形成配位键的是
)形成的配合物可用于反向ATRP(原子转移自由基聚合)的新型催化剂。4-甲基咪唑中1号N原子的孤电子对可参与形成大π键,使电子云密度降低,分子具有一定的稳定性。则能与Cu2+形成配位键的是_______ (填“1”或“2”)号N原子。
(3)Cu2+可形成[Cu (en)2NH3](BF4)2,其巾en代表H2N- CH2-CH2- NH2,[Cu(en)2NH3](BF4)2中VSEPR模型为四面体的非金属原子共有_______ 个 。
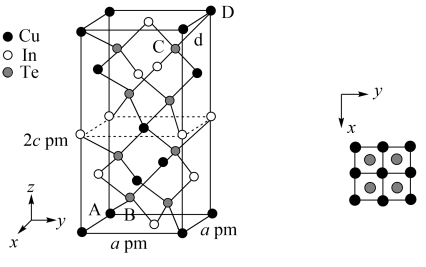
(4)一种铜合金由Cu、In、Te组成,可做热电材料。其晶胞及晶胞中各原子的投影位置如图所示,晶胞棱边夹角均为90° ,该晶体的化学式为_______ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点、B点原子的分数坐标分别为(0,0,0)、( ,
, ,
, )。则C点原子的分数坐标为
)。则C点原子的分数坐标为_______ ;晶胞 中C、D原子间距离d=_______ pm。
(1)基态Cu+离子的核外电子排布式为
(2)Cu2+与4-甲基咪唑(
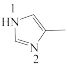 )形成的配合物可用于反向ATRP(原子转移自由基聚合)的新型催化剂。4-甲基咪唑中1号N原子的孤电子对可参与形成大π键,使电子云密度降低,分子具有一定的稳定性。则能与Cu2+形成配位键的是
)形成的配合物可用于反向ATRP(原子转移自由基聚合)的新型催化剂。4-甲基咪唑中1号N原子的孤电子对可参与形成大π键,使电子云密度降低,分子具有一定的稳定性。则能与Cu2+形成配位键的是(3)Cu2+可形成[Cu (en)2NH3](BF4)2,其巾en代表H2N- CH2-CH2- NH2,[Cu(en)2NH3](BF4)2中VSEPR模型为四面体的非金属原子共有
(4)一种铜合金由Cu、In、Te组成,可做热电材料。其晶胞及晶胞中各原子的投影位置如图所示,晶胞棱边夹角均为90° ,该晶体的化学式为
 ,
, ,
, )。则C点原子的分数坐标为
)。则C点原子的分数坐标为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】硫酸镍广泛应用于电镀、电池、催化剂等工业。某科研小组以粗硫酸镍(含Cu2+、Fe3+、Ca2+、 Mg2+、Zn2+等)为原料,经下图一系列除杂过程模拟精制硫酸镍工艺,回答下列问题。
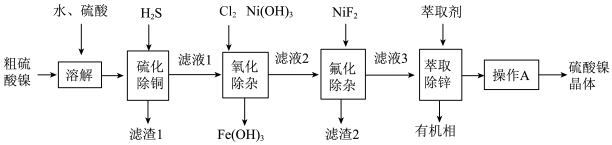
(1)①“硫化除铜”过程中除Cu2+发生的反应外,另一离子反应方程式为___________ 。
②“硫化除铜”后滤液1中主要金属阳离子为Ca2+、Mg2+、Zn2+、___________ 。
(2)“氧化除杂” 时加入Cl2和Ni (OH)2的主要作用分别是__________ 、_______ 。
(3)“氟化除杂”后滤渣2的主要成分是___________ (写化学式)。
(4)“滤液3”中加入有机萃取剂后,Zn2+与有机萃取剂形成易溶于萃取剂的络合物。该过程选用的萃取剂一般为P204[ (二(2-乙基)己基)磷酸酯],其萃取原理为: 2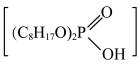 +Zn2+
+Zn2+ +2H+,反萃取是用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。取“萃取除锌”过程中的有机相,加入反萃取剂可回收ZnSO4,具体过程如图,其中反萃取剂可以选择下列哪种物质
+2H+,反萃取是用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。取“萃取除锌”过程中的有机相,加入反萃取剂可回收ZnSO4,具体过程如图,其中反萃取剂可以选择下列哪种物质________ (填选项)。

A.NaOH溶液 B. H2SO4溶液 C.ZnSO4溶液
(5)“萃取除锌”后的溶液经操作A可得硫酸镍晶体,称取1.000g硫酸镍晶体(NiSO4·6H2O )样品溶解,定容至250mL。取25.00mL试液,滴入几滴紫脲酸胺指示剂,用0.01mol·L-1的EDTA (Na2H2Y)标准溶液滴定至终点,重复操作2-3次,平均消耗EDTA标准溶液体积为23.50mL。
已知:反应为Ni2++H2Y2-=NiY2- +2H+;紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
①滴定终点的操作和现象是________ 。
②计算样品纯度为___________ 。(保留三位有 效数字,不考虑杂质反应)

(1)①“硫化除铜”过程中除Cu2+发生的反应外,另一离子反应方程式为
②“硫化除铜”后滤液1中主要金属阳离子为Ca2+、Mg2+、Zn2+、
(2)“氧化除杂” 时加入Cl2和Ni (OH)2的主要作用分别是
(3)“氟化除杂”后滤渣2的主要成分是
(4)“滤液3”中加入有机萃取剂后,Zn2+与有机萃取剂形成易溶于萃取剂的络合物。该过程选用的萃取剂一般为P204[ (二(2-乙基)己基)磷酸酯],其萃取原理为: 2
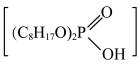 +Zn2+
+Zn2+ +2H+,反萃取是用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。取“萃取除锌”过程中的有机相,加入反萃取剂可回收ZnSO4,具体过程如图,其中反萃取剂可以选择下列哪种物质
+2H+,反萃取是用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。取“萃取除锌”过程中的有机相,加入反萃取剂可回收ZnSO4,具体过程如图,其中反萃取剂可以选择下列哪种物质
A.NaOH溶液 B. H2SO4溶液 C.ZnSO4溶液
(5)“萃取除锌”后的溶液经操作A可得硫酸镍晶体,称取1.000g硫酸镍晶体(NiSO4·6H2O )样品溶解,定容至250mL。取25.00mL试液,滴入几滴紫脲酸胺指示剂,用0.01mol·L-1的EDTA (Na2H2Y)标准溶液滴定至终点,重复操作2-3次,平均消耗EDTA标准溶液体积为23.50mL。
已知:反应为Ni2++H2Y2-=NiY2- +2H+;紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
①滴定终点的操作和现象是
②计算样品纯度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】Mg(OH)2可用作塑料的阻燃剂。现以某矿石(主要成分为 3MgO·2SiO2·2H2O,还有少量 Fe2O3、FeO、CaO 和Al2O3)为原料生产 Mg(OH)2,其工艺流程如图:
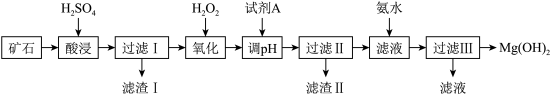
已知:生成氢氧化物沉淀的 pH
回答下列问题:
(1)酸浸时,为提高矿石的浸出率可采取的措施为_______ (任写一条)。该过程H2SO4适当过量的目的除了使固体充分溶解外还有_______
(2)写出氧化过程加H2O2发生反应的离子方程式_______
(3)为了提高产品纯度加入试剂A 为_______ (填化学式),为控制 Mg2+浓度为1.0mol/L,调节溶液 pH 范围为_______ ;得到滤渣 II 的成分是_______ (填化学式)
(4)实际生产中,可由 Mg(OH)2为原料制备单质镁,请写出制备过程中涉及氧化还原的方程式方法_______ 。

已知:生成氢氧化物沉淀的 pH
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的 pH | 7.6 | 1.9 | 3.4 | 9.0 |
| 完全沉淀的 pH (c=1.0×10-5 mol/L) | 9.6 | 3.2 | 4.8 | 11.1 |
(1)酸浸时,为提高矿石的浸出率可采取的措施为
(2)写出氧化过程加H2O2发生反应的离子方程式
(3)为了提高产品纯度加入试剂A 为
(4)实际生产中,可由 Mg(OH)2为原料制备单质镁,请写出制备过程中涉及氧化还原的方程式方法
您最近一年使用:0次
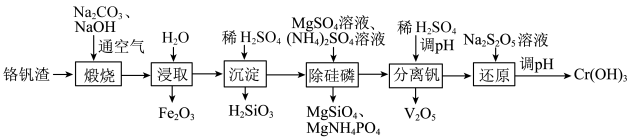
【推荐3】铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如图所示: 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。
回答下列问题:
(1)若铬钒渣中铬的含氧酸盐为 ,则“煅烧”过程中
,则“煅烧”过程中 发生反应的化学方程式为
发生反应的化学方程式为___________ 。若在实验室中进行煅烧铬钒渣,___________ (填“能”或“不能”)用陶瓷坩埚,理由是___________ 。
(2) 是
是___________ (填“酸性”、“碱性”或“两性”)氧化物,写出它在日常生活中的一种用途:___________ 。
(3)“沉淀”步骤中生成 反应的离子方程式为
反应的离子方程式为___________ 。
(4)“还原”步骤中氧化剂与还原剂的物质的量之比为___________ 。
 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。回答下列问题:
(1)若铬钒渣中铬的含氧酸盐为
 ,则“煅烧”过程中
,则“煅烧”过程中 发生反应的化学方程式为
发生反应的化学方程式为(2)
 是
是(3)“沉淀”步骤中生成
 反应的离子方程式为
反应的离子方程式为(4)“还原”步骤中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次



