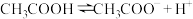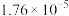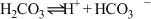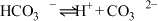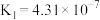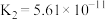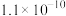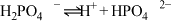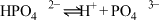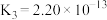在室温下,下列五种溶液:①0.1mol/LNH4Cl;②0.1mol/LCH3COONH4;③0.1mol/LNH4HSO4;④0.1mol/LNH3·H2O和0.1mol/LNH4Cl混合液;⑤0.1mol/LNH4Al(SO4)2。请根据要求填写下列空白:
(1)将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m_______ n(填“大于”、“等于”或“小于”)。
(2)①、②、③、⑤中c( )由大到小的顺序是:
)由大到小的顺序是:_______ (用①、②、③、⑤表示)。
(3)室温,溶液②的pH=7,该溶液中各离子浓度的大小关系是_______ 。
(4)若室温下,在溶液④中pH>7,则c(NH3·H2O)_______ c( )(填“大于”、“等于”或“小于”)。
)(填“大于”、“等于”或“小于”)。
(5)向③中滴加等体积等浓度NaOH溶液时,此时溶液呈_______ (填“酸性”“中性”或“碱性”),其离子浓度大小关系:c( )
)_______ c(Na+)_______ c( );c(
);c( )+c(H+)
)+c(H+)_______ c( )+c(OH-)。(以上均填“大于”、“等于”或“小于”)。
)+c(OH-)。(以上均填“大于”、“等于”或“小于”)。
(1)将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m
(2)①、②、③、⑤中c(
 )由大到小的顺序是:
)由大到小的顺序是:(3)室温,溶液②的pH=7,该溶液中各离子浓度的大小关系是
(4)若室温下,在溶液④中pH>7,则c(NH3·H2O)
 )(填“大于”、“等于”或“小于”)。
)(填“大于”、“等于”或“小于”)。(5)向③中滴加等体积等浓度NaOH溶液时,此时溶液呈
 )
) );c(
);c( )+c(H+)
)+c(H+) )+c(OH-)。(以上均填“大于”、“等于”或“小于”)。
)+c(OH-)。(以上均填“大于”、“等于”或“小于”)。
更新时间:2024-01-14 21:58:52
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)常温下,在pH=5的稀醋酸溶液中,c(CH3COO-)=____________ (列式,不必化简);下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是______ 。
a.加入少量0.10 mol·L-1的稀盐酸
b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1
d.加入少量冰醋酸
e.加入少量氯化钠固体
f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)_________ V(醋酸),反应的最初速率为:v(盐酸)_________ v(醋酸)。(填写“>”、“<”或“=”)
(3)常温下,向体积为Va mL,pH为3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:__________________ 。
(4)常温下,将0.1 mol/L盐酸和0.1 mol/L醋酸钠溶液混合,所得溶液为中性,则混合溶液中各离子的浓度按由大到小排序为_______________________________ 。
(5)已知:90℃时,水的离子积常数为Kw = 3.8×10-13,在此温度下,将pH=3的盐酸和pH = 11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=______________ (保留三位有效数字)mol/L。
 CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。(1)常温下,在pH=5的稀醋酸溶液中,c(CH3COO-)=
a.加入少量0.10 mol·L-1的稀盐酸
b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1
d.加入少量冰醋酸
e.加入少量氯化钠固体
f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)
(3)常温下,向体积为Va mL,pH为3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:
(4)常温下,将0.1 mol/L盐酸和0.1 mol/L醋酸钠溶液混合,所得溶液为中性,则混合溶液中各离子的浓度按由大到小排序为
(5)已知:90℃时,水的离子积常数为Kw = 3.8×10-13,在此温度下,将pH=3的盐酸和pH = 11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】亚磷酸 为二元酸,其酸性比磷酸稍强,可用作农药中间体以及有机磷水处理药剂的原料。回答下列问题:
为二元酸,其酸性比磷酸稍强,可用作农药中间体以及有机磷水处理药剂的原料。回答下列问题:
(1) 属于
属于___________ (填“正盐”、“酸式盐”或“无法确定”)。
(2)设计一种实验方案,证明亚磷酸不是强酸:___________ 。
(3)某温度下, 溶液的
溶液的 为2,该温度下
为2,该温度下 的电离平衡常数
的电离平衡常数 约为
约为___________ (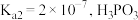 的二级电离和水的电离忽略不计)。
的二级电离和水的电离忽略不计)。
(4)向 溶液中滴加
溶液中滴加 溶液:
溶液:
①当溶液呈中性时,所得溶液中
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②若用甲基橙作指示剂,用 溶液滴定,达到滴定终点时,所得溶液中
溶液滴定,达到滴定终点时,所得溶液中
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 为二元酸,其酸性比磷酸稍强,可用作农药中间体以及有机磷水处理药剂的原料。回答下列问题:
为二元酸,其酸性比磷酸稍强,可用作农药中间体以及有机磷水处理药剂的原料。回答下列问题:(1)
 属于
属于(2)设计一种实验方案,证明亚磷酸不是强酸:
(3)某温度下,
 溶液的
溶液的 为2,该温度下
为2,该温度下 的电离平衡常数
的电离平衡常数 约为
约为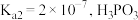 的二级电离和水的电离忽略不计)。
的二级电离和水的电离忽略不计)。(4)向
 溶液中滴加
溶液中滴加 溶液:
溶液:①当溶液呈中性时,所得溶液中

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②若用甲基橙作指示剂,用
 溶液滴定,达到滴定终点时,所得溶液中
溶液滴定,达到滴定终点时,所得溶液中
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.食醋常用于食品调味,其主要成分为醋酸。请回答:
(1)写出醋酸的电离方程式________________
(2)0.1mol/L醋酸溶液中加入少量盐酸,电离平衡向___ 反应方向移动(填“正”或“逆”)。
(3)在0.1mol/L醋酸溶液中加入少量醋酸钠晶体,晶体溶解后,醋酸溶液的pH____ (选填“增大”“减小”或“不变”)。
(4)0.1mol/L醋酸溶液的pH____ (选填“>”“=”或“<”)0.1mol/L盐酸溶液的pH。
(5)在0.1mol/L醋酸溶液中加入等体积等浓度的氢氧化钠溶液,反应后溶液显____ 性。
II.某同学想用实验确定CH3COOH是弱电解质。其方案是:
①称取一定质量的CH3COOH配制0.1mol•L-1的溶液100mL;
②用pH试纸测出该溶液的pH,即可证明HCOOH是弱电解质。
(1)方案的第①步中,要用到的玻璃定量仪器是______ 。
(2)该方案中,说明CH3COOH是弱电解质的理由是测得溶液的pH______ 1(选填>、<、=)。
(3)结合你所学的知识,试再提出一个简单易操作的可行方案证明CH3COOH是弱电解质(药品可任取)。_______________
(1)写出醋酸的电离方程式
(2)0.1mol/L醋酸溶液中加入少量盐酸,电离平衡向
(3)在0.1mol/L醋酸溶液中加入少量醋酸钠晶体,晶体溶解后,醋酸溶液的pH
(4)0.1mol/L醋酸溶液的pH
(5)在0.1mol/L醋酸溶液中加入等体积等浓度的氢氧化钠溶液,反应后溶液显
II.某同学想用实验确定CH3COOH是弱电解质。其方案是:
①称取一定质量的CH3COOH配制0.1mol•L-1的溶液100mL;
②用pH试纸测出该溶液的pH,即可证明HCOOH是弱电解质。
(1)方案的第①步中,要用到的玻璃定量仪器是
(2)该方案中,说明CH3COOH是弱电解质的理由是测得溶液的pH
(3)结合你所学的知识,试再提出一个简单易操作的可行方案证明CH3COOH是弱电解质(药品可任取)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有常温下的4种溶液:①0.01 mol·L-1CH3COOH溶液;②0.01 mol·L-1HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。
回答下列问题:
(1)4种溶液中水的电离程度最大的是________ (填序号)。
(2)将4种溶液同等程度稀释10倍后,溶液pH由大到小的顺序是_______ 。
(3)若将①④混合后所得溶液中的c(CH3COO-)>c(H+),则下列说法正确的是______ (填序号)。
A.溶液一定呈酸性 B.溶液一定呈碱性
C.溶液一定呈中性 D.溶液可能呈酸性、中性或碱性
(4)若将②③混合后所得溶液的pH=7,则消耗溶液的体积:②_____ ③ (填“>”“<”或“=”)。
(5)若将②④混合后所得溶液的pH=10,则消耗②和④溶液的体积比: =
=_____ 。
回答下列问题:
(1)4种溶液中水的电离程度最大的是
(2)将4种溶液同等程度稀释10倍后,溶液pH由大到小的顺序是
(3)若将①④混合后所得溶液中的c(CH3COO-)>c(H+),则下列说法正确的是
A.溶液一定呈酸性 B.溶液一定呈碱性
C.溶液一定呈中性 D.溶液可能呈酸性、中性或碱性
(4)若将②③混合后所得溶液的pH=7,则消耗溶液的体积:②
(5)若将②④混合后所得溶液的pH=10,则消耗②和④溶液的体积比:
 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据中学化学常见的①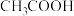 、②
、②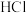 、③
、③ 三种溶液,请用A~H
三种溶液,请用A~H
A.①<②<③ B.①=②=③ C.①>②>③
D.①<②=③ E.①=③>② F.①>②=③
G.①=②>③ H.①=②<③
(1)当它们 相同时,其物质的量浓度关系是
相同时,其物质的量浓度关系是______ 。
(2)当它们的物质的量浓度相同时,其 的关系是
的关系是______ 。
(3)中和等体积、等物质的量浓度的烧碱溶液,需同物质的量浓度的三种醋溶液的体积关系为______ 。
(4)当它们 相同、体积相同时,同时加入锌,则开始时反应速率
相同、体积相同时,同时加入锌,则开始时反应速率______ ,若产生相同体积的气体(相同状况),所需时间______ 。
(5)将 相同的三种酸均稀释10倍后,
相同的三种酸均稀释10倍后, 关系为
关系为______ 。
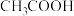 、②
、②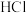 、③
、③ 三种溶液,请用A~H
三种溶液,请用A~HA.①<②<③ B.①=②=③ C.①>②>③
D.①<②=③ E.①=③>② F.①>②=③
G.①=②>③ H.①=②<③
(1)当它们
 相同时,其物质的量浓度关系是
相同时,其物质的量浓度关系是(2)当它们的物质的量浓度相同时,其
 的关系是
的关系是(3)中和等体积、等物质的量浓度的烧碱溶液,需同物质的量浓度的三种醋溶液的体积关系为
(4)当它们
 相同、体积相同时,同时加入锌,则开始时反应速率
相同、体积相同时,同时加入锌,则开始时反应速率(5)将
 相同的三种酸均稀释10倍后,
相同的三种酸均稀释10倍后, 关系为
关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求回答问题:
(1)写出醋酸的电离平衡常数表达式:______ 。
(2)取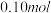
 (冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示。比较a、b点的相关性质(填“>”“<”或“=”):
(冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示。比较a、b点的相关性质(填“>”“<”或“=”):
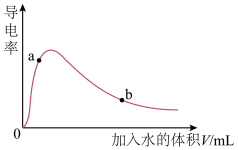
①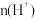 :a
:a______ b;
② :a
:a______ b;
(3) 浓度相同等体积的两份溶液A(盐酸)和B(
浓度相同等体积的两份溶液A(盐酸)和B( )分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是
)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是______ (填写序号)
①反应所需要的时间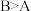 ②开始反应时的速率
②开始反应时的速率
③参加反应的锌的物质的量 ④A中有锌剩余
④A中有锌剩余
(4)某温度( )时,
)时, 的氢氧化钠溶液中,由水电离出的
的氢氧化钠溶液中,由水电离出的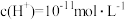 ,请回答下列问题:
,请回答下列问题:
①此温度下水的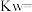
______ ;
②在相同温度下, 氢氧化钠溶液的
氢氧化钠溶液的 应为
应为______ 。
(1)写出醋酸的电离平衡常数表达式:
(2)取
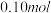
 (冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示。比较a、b点的相关性质(填“>”“<”或“=”):
(冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示。比较a、b点的相关性质(填“>”“<”或“=”):
①
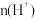 :a
:a②
 :a
:a(3)
 浓度相同等体积的两份溶液A(盐酸)和B(
浓度相同等体积的两份溶液A(盐酸)和B( )分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是
)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是①反应所需要的时间
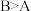 ②开始反应时的速率
②开始反应时的速率
③参加反应的锌的物质的量
 ④A中有锌剩余
④A中有锌剩余(4)某温度(
 )时,
)时, 的氢氧化钠溶液中,由水电离出的
的氢氧化钠溶液中,由水电离出的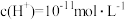 ,请回答下列问题:
,请回答下列问题:①此温度下水的
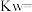
②在相同温度下,
 氢氧化钠溶液的
氢氧化钠溶液的 应为
应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】平衡常数的计算:
下表是几种弱电解质的电离平衡常数(25℃)
回答下列问题:
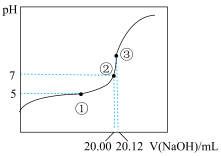
(1)用 溶液滴定20.00mL某未知浓度的一元酸HX溶液,如图所示。其中①点所示溶液中
溶液滴定20.00mL某未知浓度的一元酸HX溶液,如图所示。其中①点所示溶液中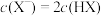 ,③点所示溶液中存在
,③点所示溶液中存在 ,则HX的电离平衡常数
,则HX的电离平衡常数
___________ 。
(2)水解反应是典型的可逆反应。请写出Na2CO3水解反应的离子方程式:___________ 。
(3)水解反应的化学平衡常数称为水解常数(用 表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:
表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:
___________ 。根据上表数据计算,25℃该常数的数值为___________ (保留2位小数)。
下表是几种弱电解质的电离平衡常数(25℃)
电解质 | 电离方程式 | 平衡常数K |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)用
 溶液滴定20.00mL某未知浓度的一元酸HX溶液,如图所示。其中①点所示溶液中
溶液滴定20.00mL某未知浓度的一元酸HX溶液,如图所示。其中①点所示溶液中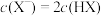 ,③点所示溶液中存在
,③点所示溶液中存在 ,则HX的电离平衡常数
,则HX的电离平衡常数

(2)水解反应是典型的可逆反应。请写出Na2CO3水解反应的离子方程式:
(3)水解反应的化学平衡常数称为水解常数(用
 表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:
表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.食醋(主要成分CH3COOH)、纯碱(Na2CO3)和小苏打(NaHCO3)均为家庭厨房中常用的物质。已知:
请回答下列问题:
(1)25℃时,0.10mol·L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)_______ ;
(2)常温下,将20mL0.10mol·L-1CH3COOH溶液和 20mL0.10mol·L-1HNO2溶液分别与 20mL 0.10mol·L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计)。
①反应开始时,v (CH3COOH )_______ v (HNO2)(填“>”、“<”或“=”)。
②充分反应后。两溶液中c(CH3COO-)_______ c(NO2-)(填“>”、“<”或“=”)。
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的PH=6,则混合
液中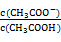 =
=_________ ;
(4)常温下,下列方法可以使0.1mol • L-1CH3COOH的电离程度增大的是_____________ 。
Ⅱ.常温时向一定体积pH= 12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的ph=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积之比是____________________ 。
| 弱酸 | CH3COOH | H2CO3 | HNO2 |
| 电离常数 | K=1.8×10-5 | K=4.3×10-7 K=5.6×10-11 | K=5.0×10-4 |
请回答下列问题:
(1)25℃时,0.10mol·L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)
(2)常温下,将20mL0.10mol·L-1CH3COOH溶液和 20mL0.10mol·L-1HNO2溶液分别与 20mL 0.10mol·L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计)。
①反应开始时,v (CH3COOH )
②充分反应后。两溶液中c(CH3COO-)
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的PH=6,则混合
液中
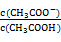 =
=(4)常温下,下列方法可以使0.1mol • L-1CH3COOH的电离程度增大的是
a.加入少量的稀盐酸 b.加热溶液 c.加水稀释 d.加入少量冰醋酸
Ⅱ.常温时向一定体积pH= 12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的ph=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】25 ℃时部分弱酸的电离平衡常数如下表:
(1)在温度相同时,各弱酸的Ka值与酸性的相对强弱的关系为_______ 。
(2)室温下①0.1 mol·L-1HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,
④0.1 mol·L-1NaHCO3,溶液的pH由大到小的关系为_______ 。
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中, 、
、 、
、 、
、 浓度由大到小的顺序为
浓度由大到小的顺序为_______ 。
(4)下列离子方程式书写正确的是_______ (填字母)。
a.2ClO-+H2O+CO2=2HClO+
b.2HCOOH+ =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-=2HCOOH+
d.Cl2+H2O+2 =2
=2 +Cl-+ClO-
+Cl-+ClO-
(5)在25 ℃时,将a mol·L-1 的NaCN溶液与0.01 mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,则a_______ (填“>”“<”或“=”)0.01。
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数 | Ka=1.8×10-4 | Ka=4.7×10-8 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(1)在温度相同时,各弱酸的Ka值与酸性的相对强弱的关系为
(2)室温下①0.1 mol·L-1HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,
④0.1 mol·L-1NaHCO3,溶液的pH由大到小的关系为
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,
 、
、 、
、 、
、 浓度由大到小的顺序为
浓度由大到小的顺序为(4)下列离子方程式书写正确的是
a.2ClO-+H2O+CO2=2HClO+

b.2HCOOH+
 =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑c.H2SO3+2HCOO-=2HCOOH+

d.Cl2+H2O+2
 =2
=2 +Cl-+ClO-
+Cl-+ClO-(5)在25 ℃时,将a mol·L-1 的NaCN溶液与0.01 mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,则a
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.已知水在25℃和95℃时的电离平衡曲线如图所示:

(1)25℃时水的电离平衡曲线应为_____ (填“A”或“B”)。
(2)95℃时,将 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为_____ 。
(3)25℃时,等体积的 的NaOH溶液和氨水分别与
的NaOH溶液和氨水分别与 的盐酸发生中和反应,恰好完全反应时消耗盐酸的体积
的盐酸发生中和反应,恰好完全反应时消耗盐酸的体积_____ (填“前者多”“后者多”或“一样多”)。
Ⅱ.NaOH溶液可用于多种气体的处理。
(4) 是温室气体,可用NaOH溶液吸收得到
是温室气体,可用NaOH溶液吸收得到 或
或 ,已知25℃时,
,已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数 ,当溶液中
,当溶液中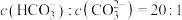 时,溶液的
时,溶液的
_____ 。
(5)已知金属与浓硝酸反应产生的 可用NaOH溶液吸收,反应的化学方程式为:
可用NaOH溶液吸收,反应的化学方程式为: 。含0.2molNaOH的水溶液与
。含0.2molNaOH的水溶液与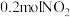 恰好完全反应得1L溶液A,溶液B为
恰好完全反应得1L溶液A,溶液B为 溶液,则两份溶液中
溶液,则两份溶液中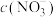 、
、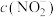 和
和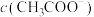 由大到小的顺序为
由大到小的顺序为_____ (已知 的电离常数
的电离常数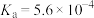 ,
, 的电离常数
的电离常数 )。可使溶液A和溶液B的pH相等的方法是
)。可使溶液A和溶液B的pH相等的方法是_____ (填字母)。
A.向溶液A中加适量NaOH B.向溶液A中加适量水
C.向溶液B中加适量NaOH D.向溶液B中加适量水

(1)25℃时水的电离平衡曲线应为
(2)95℃时,将
 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为(3)25℃时,等体积的
 的NaOH溶液和氨水分别与
的NaOH溶液和氨水分别与 的盐酸发生中和反应,恰好完全反应时消耗盐酸的体积
的盐酸发生中和反应,恰好完全反应时消耗盐酸的体积Ⅱ.NaOH溶液可用于多种气体的处理。
(4)
 是温室气体,可用NaOH溶液吸收得到
是温室气体,可用NaOH溶液吸收得到 或
或 ,已知25℃时,
,已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数 ,当溶液中
,当溶液中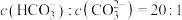 时,溶液的
时,溶液的
(5)已知金属与浓硝酸反应产生的
 可用NaOH溶液吸收,反应的化学方程式为:
可用NaOH溶液吸收,反应的化学方程式为: 。含0.2molNaOH的水溶液与
。含0.2molNaOH的水溶液与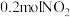 恰好完全反应得1L溶液A,溶液B为
恰好完全反应得1L溶液A,溶液B为 溶液,则两份溶液中
溶液,则两份溶液中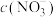 、
、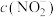 和
和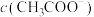 由大到小的顺序为
由大到小的顺序为 的电离常数
的电离常数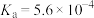 ,
, 的电离常数
的电离常数 )。可使溶液A和溶液B的pH相等的方法是
)。可使溶液A和溶液B的pH相等的方法是A.向溶液A中加适量NaOH B.向溶液A中加适量水
C.向溶液B中加适量NaOH D.向溶液B中加适量水
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】雪碧是常见的碳酸型饮料。其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
(1)上表中三种酸的酸性由强到弱的顺序为________ 。
(2)水存在电离平衡,下列能促进水的电离,且溶液显碱性的是________(填标号)。
(3)25℃时,求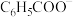 的水解平衡常数)Kh=
的水解平衡常数)Kh=________ (填数值,保留三位有效数字)(提示: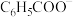 的水解平衡常数
的水解平衡常数 );该温度下,等物质的量浓度的苯甲酸(C6H5COOH)和苯甲酸钠(C6H5COONa)的混合溶液的pH
);该温度下,等物质的量浓度的苯甲酸(C6H5COOH)和苯甲酸钠(C6H5COONa)的混合溶液的pH________ (填“>”“<”或“=”)7,溶液中离子浓度由大到小的顺序是________ 。
(4)柠檬酸的结构简式为 ,所含官能团名称为
,所含官能团名称为________ 、________ ,柠檬酸与足量NaOH反应所得到的盐的结构简式为________ 。
(5)25℃时,等浓度的Na2CO3、NaHCO3两种盐溶液中,碱性较强的是________ (填化学式)。
(6)25℃时,pH=4的柠檬酸溶液中由水电离出的 与pH=4的NH4Cl溶液中由水电离出的
与pH=4的NH4Cl溶液中由水电离出的 之比是
之比是________ 。
| 化学式 | 苯甲酸(C6H5COOH) | 碳酸(H2CO3) | 柠檬酸(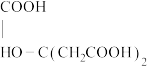 ) ) |
| 电离常数 | Ka=6.3×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=7.4×10-4 Ka2=1.7×10-5 Ka3=4.0×10-7 |
(2)水存在电离平衡,下列能促进水的电离,且溶液显碱性的是________(填标号)。
| A.通入氯气 | B.加入AlCl3固体 |
| C.加入苯甲酸钠(C6H5COONa)固体 | D.加热至90℃ |
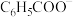 的水解平衡常数)Kh=
的水解平衡常数)Kh=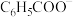 的水解平衡常数
的水解平衡常数 );该温度下,等物质的量浓度的苯甲酸(C6H5COOH)和苯甲酸钠(C6H5COONa)的混合溶液的pH
);该温度下,等物质的量浓度的苯甲酸(C6H5COOH)和苯甲酸钠(C6H5COONa)的混合溶液的pH(4)柠檬酸的结构简式为
 ,所含官能团名称为
,所含官能团名称为(5)25℃时,等浓度的Na2CO3、NaHCO3两种盐溶液中,碱性较强的是
(6)25℃时,pH=4的柠檬酸溶液中由水电离出的
 与pH=4的NH4Cl溶液中由水电离出的
与pH=4的NH4Cl溶液中由水电离出的 之比是
之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学土肥外加少量酸、碱,而pH基本不变的溶液,称为缓冲溶液,现有25℃时,浓度均为0.10mol/L的CH3COOH和CH3COONa的缓冲溶液,pH=4.76,回答下列问题:
[Ka(CH3COOH)=1.75×10-5,Kb为盐的水解常数]
(1)CH3COOH的电离方程式为__ 。
(2)该缓冲溶液中离子浓度由大到小的顺序是___ 。
(3)25℃时,Ka(CH3COOH)___ Kb(CH3COO-)(填“>”“<”或“=”)。
(4)用1.0L上述缓冲溶液中滴加几滴NaOH稀溶液(忽略溶液体积的变化),反应后溶液中c(H+)__ mol/L。
(5)人体血液存在H2CO3(CO2)与NaHCO3的缓冲体系,能有效除掉人体正常代谢产生的酸、碱,保持pH的稳定,有关机理说法正确的是__ (填写选项字母)。
a.代谢产生的 被HCO3-结合形成H2CO3
被HCO3-结合形成H2CO3
b.血液中的缓冲体系可抵抗大量酸、碱的影响
c.代谢产生的碱被H+中和,H+又由H2CO3电离补充
[Ka(CH3COOH)=1.75×10-5,Kb为盐的水解常数]
(1)CH3COOH的电离方程式为
(2)该缓冲溶液中离子浓度由大到小的顺序是
(3)25℃时,Ka(CH3COOH)
(4)用1.0L上述缓冲溶液中滴加几滴NaOH稀溶液(忽略溶液体积的变化),反应后溶液中c(H+)
(5)人体血液存在H2CO3(CO2)与NaHCO3的缓冲体系,能有效除掉人体正常代谢产生的酸、碱,保持pH的稳定,有关机理说法正确的是
a.代谢产生的
 被HCO3-结合形成H2CO3
被HCO3-结合形成H2CO3b.血液中的缓冲体系可抵抗大量酸、碱的影响
c.代谢产生的碱被H+中和,H+又由H2CO3电离补充
您最近一年使用:0次