近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长,因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题。
(1)氯化氢的直接氧化法为 。下图为刚性容器中,进料浓度比
。下图为刚性容器中,进料浓度比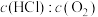 分别等于1:1、4:1、7:1时HCl平衡转化率随温度变化的关系:
分别等于1:1、4:1、7:1时HCl平衡转化率随温度变化的关系:
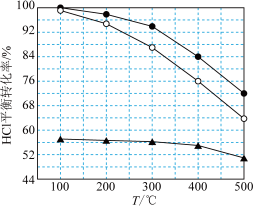
可知反应平衡常数K(200℃)______ K(300℃)(填“>”或“<”)。设HCl初始浓度为c,根据进料浓度比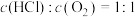 的数据计算K(400℃)=
的数据计算K(400℃)=______ (列出计算式)。按化学计量数之比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比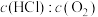 过低、过高的不利影响分别是
过低、过高的不利影响分别是_______ 、_______ 。
(2)直接氧化法可按下列催化过程进行:




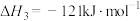
则 的
的
_______  。
。
(3)在一定温度的条件下,进一步提高HCl的转化率的方法是________ (写出2种)。
(1)氯化氢的直接氧化法为
 。下图为刚性容器中,进料浓度比
。下图为刚性容器中,进料浓度比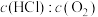 分别等于1:1、4:1、7:1时HCl平衡转化率随温度变化的关系:
分别等于1:1、4:1、7:1时HCl平衡转化率随温度变化的关系:
可知反应平衡常数K(200℃)
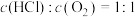 的数据计算K(400℃)=
的数据计算K(400℃)=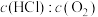 过低、过高的不利影响分别是
过低、过高的不利影响分别是(2)直接氧化法可按下列催化过程进行:





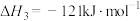
则
 的
的
 。
。(3)在一定温度的条件下,进一步提高HCl的转化率的方法是
更新时间:2024-01-16 13:23:34
|
相似题推荐
【推荐1】为保护环境,汽车尾气中SO2和NOX的脱除已经引起了人们的广泛关注。
(1)SO2易溶于水,其水溶液被称为“亚硫酸”溶液。在“亚硫酸”溶液中存在下列平衡:SO2 + xH2O SO2·xH2O K1、SO2·xH2O
SO2·xH2O K1、SO2·xH2O H++ HSO3-+(x﹣1)H2O K2
H++ HSO3-+(x﹣1)H2O K2
温度升高时,平衡常数增大的是______________ (填“K1”或“ K2”)。
(2)汽车尾气中的NO2和SO2直接反应可生成SO3。已知:
N2(g)+O2(g)=2NO (g) ΔH =+180.5 kJ·mol﹣1
2NO(g)+ O2(g)=2NO2(g) ΔH =-113.0 kJ·mol﹣1
2SO2(g)+ O2(g)=2SO3(g) ΔH =-196.6 kJ·mol﹣1
写出NO2与SO2反应生成SO3(g)和N2的热化学方程式______________ 。
(3)液相吸收法去除汽车尾气中SO2、NOX。
①SO2、NOX在自来水、纯水及氨水中的吸收率如下。
ⅰ.自来水中SO2吸收率比纯水的高,可能的原因是_________________ 。
ⅱ.氨水吸收SO2的化学方程式为______________ 。
ⅲ.三种吸收剂中NOX的吸收率均较低,可能原因是______________ (填标号)。
a. NO难溶于水 b. NO2难溶于水 c. NO、NO2均不与氨水反应
②吸收液中加Fe2(SO4)3,将NO转化为NO2-,提高脱硝率。写出该反应离子方程式________________________ 。
(4)电化学膜技术去除汽车尾气中的SO2。尾气中的SO2 预氧化生成SO3并伴随O2一同到达多孔阴极板。
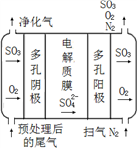
①写出多孔阴极的电极反应式_____________________ 。
②该电解池除尾气脱硫外,还有的作用是_____________ 。
(1)SO2易溶于水,其水溶液被称为“亚硫酸”溶液。在“亚硫酸”溶液中存在下列平衡:SO2 + xH2O
 SO2·xH2O K1、SO2·xH2O
SO2·xH2O K1、SO2·xH2O H++ HSO3-+(x﹣1)H2O K2
H++ HSO3-+(x﹣1)H2O K2温度升高时,平衡常数增大的是
(2)汽车尾气中的NO2和SO2直接反应可生成SO3。已知:
N2(g)+O2(g)=2NO (g) ΔH =+180.5 kJ·mol﹣1
2NO(g)+ O2(g)=2NO2(g) ΔH =-113.0 kJ·mol﹣1
2SO2(g)+ O2(g)=2SO3(g) ΔH =-196.6 kJ·mol﹣1
写出NO2与SO2反应生成SO3(g)和N2的热化学方程式
(3)液相吸收法去除汽车尾气中SO2、NOX。
①SO2、NOX在自来水、纯水及氨水中的吸收率如下。
| 吸收剂 | 自来水 | 纯水 | 氨水 |
| SO2吸收率 | 51.4% | 41.4% | 85.5% |
| NOx吸收率 | 5% | 5% | 5% |
ⅰ.自来水中SO2吸收率比纯水的高,可能的原因是
ⅱ.氨水吸收SO2的化学方程式为
ⅲ.三种吸收剂中NOX的吸收率均较低,可能原因是
a. NO难溶于水 b. NO2难溶于水 c. NO、NO2均不与氨水反应
②吸收液中加Fe2(SO4)3,将NO转化为NO2-,提高脱硝率。写出该反应离子方程式
(4)电化学膜技术去除汽车尾气中的SO2。尾气中的SO2 预氧化生成SO3并伴随O2一同到达多孔阴极板。

①写出多孔阴极的电极反应式
②该电解池除尾气脱硫外,还有的作用是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】反应 Fe(s)+CO2(g)⇌FeO(s)+CO(g) △H1,平衡常数为 K1,反应 Fe(s)+H2O(g)⇌FeO(s)+H2(g) △H2,平衡常数为 K2;在不同温度时 K1、K2 的值如表:
(1) 反应 CO2(g)+H2(g)⇌CO(g)+H2O(g)的反应热为△H ,平衡常数为 K,则△H=____________ (用△H1 和△H2 表 示), K= _______________ (用 K1 和 K2 表示),且由上述计算可知,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)是______________________________ 反应(填“吸热”或“放热”)。
(2) 现有反应:mA(g)+nB(g) ⇌ pC(g)达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
①该反应的逆反应为反应___________ (填“吸热”或“放热”,且 m+n___ p(填“>"“=或“<”)
②减压使容器容积增大时,A的质量分数____________ (填“增大”“减小”或“不变”,下同)。
③若容积不变加入B,则A的转化率_______________ , B的转化率 ______________
④ 若加入催化剂,平衡时气体混合物的总物质的量____________
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
(1) 反应 CO2(g)+H2(g)⇌CO(g)+H2O(g)的反应热为△H ,平衡常数为 K,则△H=
(2) 现有反应:mA(g)+nB(g) ⇌ pC(g)达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
①该反应的逆反应为反应
②减压使容器容积增大时,A的质量分数
③若容积不变加入B,则A的转化率
④ 若加入催化剂,平衡时气体混合物的总物质的量
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】近年来,我国大力加强温室气体 氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。
氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。
(1)已知:①


②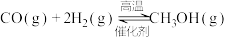


则反应③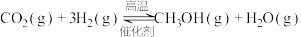

_______  。
。
(2)若将物质的量之比为1∶3的 (g)和
(g)和 (g)充入容积为1.0 L的恒容密闭容器中发生反应③,不同压强下
(g)充入容积为1.0 L的恒容密闭容器中发生反应③,不同压强下 转化率随温度的变化关系如图所示。
转化率随温度的变化关系如图所示。
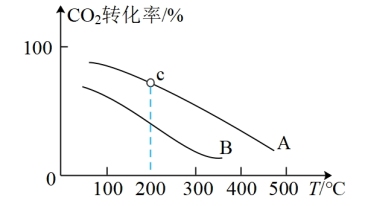
a.A、B两条曲线的压强分别为 、
、 ,则
,则
_______ (填“>”、“<”或“=”) ;
;
b.在曲线A的条件下,起始充入 (g)和
(g)和 (g)的物质的量分别为1 mol、3 mol,且c点时K=300,则c点对应
(g)的物质的量分别为1 mol、3 mol,且c点时K=300,则c点对应 转化率为
转化率为_______ 。
(3)在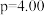 MPa、原料气
MPa、原料气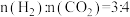 、合适催化剂的条件下发生反应,温度对
、合适催化剂的条件下发生反应,温度对 转化率、
转化率、 产率、
产率、 选择性的影响如图所示。已知:
选择性的影响如图所示。已知: 选择性
选择性 。
。

a. 转化率随温度升高而增大的原因可能是
转化率随温度升高而增大的原因可能是_______ ;
b. 选择性随温度升高而减小的原因可能是
选择性随温度升高而减小的原因可能是_______ ;
c.写出240℃时反应①的平衡常数的表达式:_______ 。
(4)除调控合适的温度外,使 选择性增大的方法有
选择性增大的方法有_______ 。
 氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。
氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。(1)已知:①



②
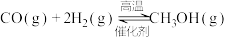


则反应③
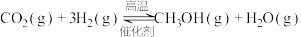

 。
。(2)若将物质的量之比为1∶3的
 (g)和
(g)和 (g)充入容积为1.0 L的恒容密闭容器中发生反应③,不同压强下
(g)充入容积为1.0 L的恒容密闭容器中发生反应③,不同压强下 转化率随温度的变化关系如图所示。
转化率随温度的变化关系如图所示。
a.A、B两条曲线的压强分别为
 、
、 ,则
,则
 ;
;b.在曲线A的条件下,起始充入
 (g)和
(g)和 (g)的物质的量分别为1 mol、3 mol,且c点时K=300,则c点对应
(g)的物质的量分别为1 mol、3 mol,且c点时K=300,则c点对应 转化率为
转化率为(3)在
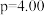 MPa、原料气
MPa、原料气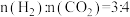 、合适催化剂的条件下发生反应,温度对
、合适催化剂的条件下发生反应,温度对 转化率、
转化率、 产率、
产率、 选择性的影响如图所示。已知:
选择性的影响如图所示。已知: 选择性
选择性 。
。
a.
 转化率随温度升高而增大的原因可能是
转化率随温度升高而增大的原因可能是b.
 选择性随温度升高而减小的原因可能是
选择性随温度升高而减小的原因可能是c.写出240℃时反应①的平衡常数的表达式:
(4)除调控合适的温度外,使
 选择性增大的方法有
选择性增大的方法有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知难溶性化合物 的化学式为
的化学式为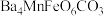 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。
(1) 高温下在
高温下在 气流中的反应
气流中的反应________ 氧化还原反应(填“属于”或“不属于”), 中钡元素的化合价为
中钡元素的化合价为________ 。
(2)步骤Ⅳ可以进行的原因除了生成 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因________ 。
(3)下列说法正确的是________。
(4)固体 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式________ 。
(5)设计实验检验混合气体A(除 外)的成份
外)的成份________ 。
 的化学式为
的化学式为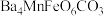 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。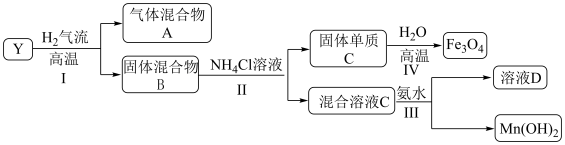
 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。(1)
 高温下在
高温下在 气流中的反应
气流中的反应 中钡元素的化合价为
中钡元素的化合价为(2)步骤Ⅳ可以进行的原因除了生成
 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因(3)下列说法正确的是________。
A.溶液D中阳离子只有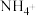 |
| B.若磁铁能吸引反应Ⅳ的剩余固体,则证明铁有剩余 |
| C.步骤Ⅱ中的氯化铵溶液也可以用盐酸代替 |
D.依据步骤Ⅲ可知碱性强弱 |
(4)固体
 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式(5)设计实验检验混合气体A(除
 外)的成份
外)的成份
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】完成下列填空
(1)通过甲烷制备 :
:
 。常温下,在2L的密闭容器中通入
。常温下,在2L的密闭容器中通入
 气体和
气体和
 气体发生反应,5min后达到平衡,测得
气体发生反应,5min后达到平衡,测得 气体的浓度为
气体的浓度为 。
。
①平衡时,该反应的平均反应速率
_______ 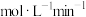 。
。
②在不改变反应混合物用量的前提下,为了提高 气体的转化率,可采取的措施是
气体的转化率,可采取的措施是_______ 。
(2)25℃时,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液
溶液混合,若所得混合溶液 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为_______ 。
(3)25℃时, 和
和 组成的混合溶液,若其
组成的混合溶液,若其 ,则该溶液中
,则该溶液中
_______  ;若
;若 ,则该溶液中
,则该溶液中
_______  。(填“>”、“<”、“=”)。
。(填“>”、“<”、“=”)。
(4)含有 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含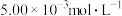 的
的 。为使废水能达标排放,做如下处理
。为使废水能达标排放,做如下处理 、
、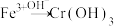 、
、 。若处理后的废水中残留的
。若处理后的废水中残留的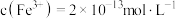 ,则残留的
,则残留的 的浓度为
的浓度为_______  (已知:
(已知: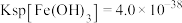 ,
,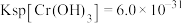 )。
)。
(1)通过甲烷制备
 :
:
 。常温下,在2L的密闭容器中通入
。常温下,在2L的密闭容器中通入
 气体和
气体和
 气体发生反应,5min后达到平衡,测得
气体发生反应,5min后达到平衡,测得 气体的浓度为
气体的浓度为 。
。①平衡时,该反应的平均反应速率

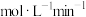 。
。②在不改变反应混合物用量的前提下,为了提高
 气体的转化率,可采取的措施是
气体的转化率,可采取的措施是(2)25℃时,将
 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液
溶液混合,若所得混合溶液 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为(3)25℃时,
 和
和 组成的混合溶液,若其
组成的混合溶液,若其 ,则该溶液中
,则该溶液中
 ;若
;若 ,则该溶液中
,则该溶液中
 。(填“>”、“<”、“=”)。
。(填“>”、“<”、“=”)。(4)含有
 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含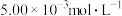 的
的 。为使废水能达标排放,做如下处理
。为使废水能达标排放,做如下处理 、
、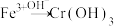 、
、 。若处理后的废水中残留的
。若处理后的废水中残留的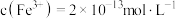 ,则残留的
,则残留的 的浓度为
的浓度为 (已知:
(已知: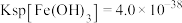 ,
,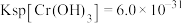 )。
)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯化亚铜(CuCl)晶体呈白色,见光分解,露置于潮湿空气中易被氧化。某研究小组设计如下两种方案在实验室制备氯化亚铜。
方案一:铜粉还原CuSO4溶液

已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+2Cl- [CuCl3]2-(无色溶液)。
[CuCl3]2-(无色溶液)。
(1)步骤①中发生反应的离子方程式为________________ 。
(2)步骤②中,加入大量水的作用是_____________ 。
(3)如图流程中用95%乙醇洗涤和真空干燥是为了防止________________ 。
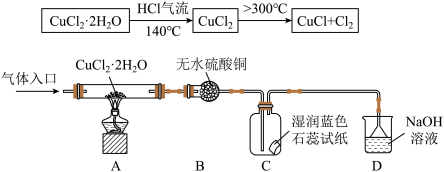
方案二:在氯化氢气流中加热CuCl2•2H2O晶体制备,其流程和实验装置(夹持仪器略)如下:
请回答下列问题:
(4)实验操作的先后顺序是a→_____ →______ →_______ →e (填操作的编号)
a.检查装置的气密性后加入药品b.点燃酒精灯,加热
c.在“气体入口”处通入干燥HCl d.熄灭酒精灯,冷却
e.停止通入HCl,然后通入N2
(5)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是______ 。
(6)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2杂质,请分析产生CuCl2杂质的原因________________________ 。
(7)准确称取0. 2500 g氯化亚铜样品置于一定量的0.5 mol/L FeCl3溶液中,待样品完全溶解后,加水20 mL,用0. 1000 mol/L的Ce(SO4)2溶液滴定到终点,消耗24. 60 mLCe(SO4)2溶液。有关化学反应为Fe3++CuCl=Fe2++Cu2++Cl-、Ce4++Fe2+=Fe3++Ce3+,计算上述样品中CuCl的质量分数是_____________ %(答案保留4位有效数字)。
方案一:铜粉还原CuSO4溶液

已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+2Cl-
 [CuCl3]2-(无色溶液)。
[CuCl3]2-(无色溶液)。(1)步骤①中发生反应的离子方程式为
(2)步骤②中,加入大量水的作用是
(3)如图流程中用95%乙醇洗涤和真空干燥是为了防止
方案二:在氯化氢气流中加热CuCl2•2H2O晶体制备,其流程和实验装置(夹持仪器略)如下:

请回答下列问题:
(4)实验操作的先后顺序是a→
a.检查装置的气密性后加入药品b.点燃酒精灯,加热
c.在“气体入口”处通入干燥HCl d.熄灭酒精灯,冷却
e.停止通入HCl,然后通入N2
(5)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是
(6)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2杂质,请分析产生CuCl2杂质的原因
(7)准确称取0. 2500 g氯化亚铜样品置于一定量的0.5 mol/L FeCl3溶液中,待样品完全溶解后,加水20 mL,用0. 1000 mol/L的Ce(SO4)2溶液滴定到终点,消耗24. 60 mLCe(SO4)2溶液。有关化学反应为Fe3++CuCl=Fe2++Cu2++Cl-、Ce4++Fe2+=Fe3++Ce3+,计算上述样品中CuCl的质量分数是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)Ⅰ.T℃时,0.01mol/LNaOH溶液的pH为11。该温度下,将1LpH=12的NaOH溶液与9L pH=2的H2SO4溶液混合后(溶液体积变化忽略不计),混合溶液的pH=___________ 。
(2)25 ℃时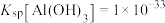 ,
,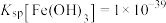 ,pH=7.1时Mn(OH)2开始沉淀。室温下欲除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于
,pH=7.1时Mn(OH)2开始沉淀。室温下欲除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于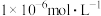 ),需调节溶液的pH范围为
),需调节溶液的pH范围为___________ 。
Ⅱ.已知反应Ⅰ:2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ/mol
反应Ⅱ:NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ/mol
反应Ⅲ:H2O(l)=H2O(g) ΔH=+44.0kJ/mol
工业上以CO2、NH3为原料合成尿素CO(NH2)2和液态水的热化学方程式为___________ ,该反应在___________ 条件下可以自发进行(填“高温”、“低温”或“任何温度”)。
Ⅲ.升高温度绝大多数的化学反应速率增大,但是ΔH<0的速率却随温度的升高而减小。某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
①2NO(g) N2O2(g)(快)v1正=k1正c2(NO) v1逆=k1逆c(N2O2) ΔH1<0
N2O2(g)(快)v1正=k1正c2(NO) v1逆=k1逆c(N2O2) ΔH1<0
②N2O2(g)+O2(g) 2NO2(g)(慢)v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2) ΔH2<0
2NO2(g)(慢)v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2) ΔH2<0
(3)一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=___________ 。根据速率方程分析,升高温度该反应速率减小的原因是___________ (填字母)。
a.k2正增大,c(N2O2)增大 b.k2正减小,c(N2O2)减小
c.k2正增大,c(N2O2)减小 d.k2正减小,c(N2O2)增大
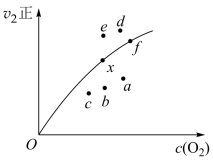
(4)由实验数据得到v2正~c(O2)的关系可用如图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点可能为___________ (填字母)。
(1)Ⅰ.T℃时,0.01mol/LNaOH溶液的pH为11。该温度下,将1LpH=12的NaOH溶液与9L pH=2的H2SO4溶液混合后(溶液体积变化忽略不计),混合溶液的pH=
(2)25 ℃时
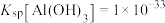 ,
,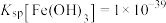 ,pH=7.1时Mn(OH)2开始沉淀。室温下欲除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于
,pH=7.1时Mn(OH)2开始沉淀。室温下欲除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于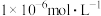 ),需调节溶液的pH范围为
),需调节溶液的pH范围为Ⅱ.已知反应Ⅰ:2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ/mol
反应Ⅱ:NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ/mol
反应Ⅲ:H2O(l)=H2O(g) ΔH=+44.0kJ/mol
工业上以CO2、NH3为原料合成尿素CO(NH2)2和液态水的热化学方程式为
Ⅲ.升高温度绝大多数的化学反应速率增大,但是ΔH<0的速率却随温度的升高而减小。某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g)
 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:①2NO(g)
 N2O2(g)(快)v1正=k1正c2(NO) v1逆=k1逆c(N2O2) ΔH1<0
N2O2(g)(快)v1正=k1正c2(NO) v1逆=k1逆c(N2O2) ΔH1<0②N2O2(g)+O2(g)
 2NO2(g)(慢)v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2) ΔH2<0
2NO2(g)(慢)v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2) ΔH2<0(3)一定温度下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=a.k2正增大,c(N2O2)增大 b.k2正减小,c(N2O2)减小
c.k2正增大,c(N2O2)减小 d.k2正减小,c(N2O2)增大
(4)由实验数据得到v2正~c(O2)的关系可用如图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点可能为

您最近一年使用:0次
【推荐2】【化学—选修2化学与技术】煤是重要的能源,也是生产化工产品的重要原料。
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为____ 和____ 。
(2)煤制油是一项新兴的、科技含量较高的煤化工技术,发展煤制油对我国而言具有重大意义。下列是煤制汽油和丙烯的主要工艺流程图。

①为了提高原料利用率,上述工艺中应控制合成气中V(CO):V(H2)=_____ 。
②采用MTG法生产的汽油中,均四甲苯(1,2,4,5-四甲基苯)质量分数约占4 %~7%,均四甲苯的结构简式为:__________________ 。
(3)利用煤的气化技术可获得合成氨的原料氢气,在制取原料气的过程中常混有一些杂质,其中某些杂质会使催化剂__________ ,必须除去。
①写出除去H2S杂质的反应方程式___________________________ 。
②欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H2O(g) CO2(g)+H2(g),已知850℃时该反应的平衡常数K=1,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于
CO2(g)+H2(g),已知850℃时该反应的平衡常数K=1,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于_____ 。
(4)煤做能源在燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
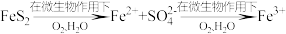
这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为____ ,第二步反应的离子方程式为________ 。
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为
(2)煤制油是一项新兴的、科技含量较高的煤化工技术,发展煤制油对我国而言具有重大意义。下列是煤制汽油和丙烯的主要工艺流程图。

①为了提高原料利用率,上述工艺中应控制合成气中V(CO):V(H2)=
②采用MTG法生产的汽油中,均四甲苯(1,2,4,5-四甲基苯)质量分数约占4 %~7%,均四甲苯的结构简式为:
(3)利用煤的气化技术可获得合成氨的原料氢气,在制取原料气的过程中常混有一些杂质,其中某些杂质会使催化剂
①写出除去H2S杂质的反应方程式
②欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H2O(g)
 CO2(g)+H2(g),已知850℃时该反应的平衡常数K=1,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于
CO2(g)+H2(g),已知850℃时该反应的平衡常数K=1,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于(4)煤做能源在燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
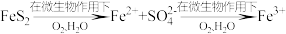
这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
您最近一年使用:0次
【推荐3】甲醇是重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4mol 发生反应,
发生反应, 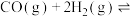
 ΔH<0,CO的平衡转化率与温度,压强的关系如图所示。
ΔH<0,CO的平衡转化率与温度,压强的关系如图所示。

①A、B两点对应的压强大小关系是
___________  (填“>、<、=”)。
(填“>、<、=”)。
②A、B、C三点的平衡常数 ,
, ,
, 的大小关系是
的大小关系是___________ 。
(2)下列叙述能说明上述反应能达到化学平衡状态的是___________(填代号)。
(3)在 压强、
压强、 ℃时,该反应的平衡常数K=
℃时,该反应的平衡常数K=___________ ,再加入1.0molCO后重新到达平衡,则CO的转化率___________ (填“增大,不变或减小”)。 ℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、
℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、 :0.2mol、
:0.2mol、 :0.2mol,此时v(正)
:0.2mol,此时v(正)___________ v(逆)(填“>、<或=”)。
(4)已知:在 ℃时,向体积为2L的密闭容器中充入物质的量之和为3mol的CO和
℃时,向体积为2L的密闭容器中充入物质的量之和为3mol的CO和 ,n(CO)的反应达到平衡时
,n(CO)的反应达到平衡时 (g)的体积分数(
(g)的体积分数( )与
)与 的关系如图所示。
的关系如图所示。
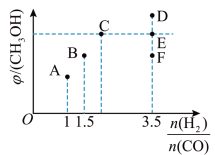
①B、C两点CO的平衡转化率α(B)___________ α(C)(填“>、<或=”)
②当 =3.5时,
=3.5时, 的平衡体积分数可能是图像中的
的平衡体积分数可能是图像中的___________ (填“D”、“E”或“F”)点。
③理论上合成甲醇的适宜条件___________ 。
A.低温、高压 B.高温、低压
C.起始投料比: =2 D.起始投料比:
=2 D.起始投料比: =3.5
=3.5
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4mol
 发生反应,
发生反应, 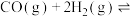
 ΔH<0,CO的平衡转化率与温度,压强的关系如图所示。
ΔH<0,CO的平衡转化率与温度,压强的关系如图所示。
①A、B两点对应的压强大小关系是

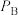 (填“>、<、=”)。
(填“>、<、=”)。②A、B、C三点的平衡常数
 ,
, ,
, 的大小关系是
的大小关系是(2)下列叙述能说明上述反应能达到化学平衡状态的是___________(填代号)。
A. 的消耗速率是 的消耗速率是 生成速率的2倍 生成速率的2倍 |
B. 的体积分数不再改变 的体积分数不再改变 |
| C.恒容条件下混合气体的密度不再改变 |
D.CO和 的物质的量之和保持不变 的物质的量之和保持不变 |
 压强、
压强、 ℃时,该反应的平衡常数K=
℃时,该反应的平衡常数K= ℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、
℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、 :0.2mol、
:0.2mol、 :0.2mol,此时v(正)
:0.2mol,此时v(正)(4)已知:在
 ℃时,向体积为2L的密闭容器中充入物质的量之和为3mol的CO和
℃时,向体积为2L的密闭容器中充入物质的量之和为3mol的CO和 ,n(CO)的反应达到平衡时
,n(CO)的反应达到平衡时 (g)的体积分数(
(g)的体积分数( )与
)与 的关系如图所示。
的关系如图所示。
①B、C两点CO的平衡转化率α(B)
②当
 =3.5时,
=3.5时, 的平衡体积分数可能是图像中的
的平衡体积分数可能是图像中的③理论上合成甲醇的适宜条件
A.低温、高压 B.高温、低压
C.起始投料比:
 =2 D.起始投料比:
=2 D.起始投料比: =3.5
=3.5
您最近一年使用:0次



