对反应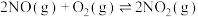 ,
,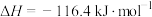 。下列说法正确的是
。下列说法正确的是
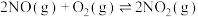 ,
,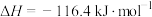 。下列说法正确的是
。下列说法正确的是A.该反应能够自发的原因 |
B.工业上使用合适的催化剂可提高 的生产效率 的生产效率 |
C.升高温度,该反应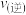 减小, 减小, 增大,平衡向逆反应方向移动 增大,平衡向逆反应方向移动 |
D.2 mol  和1 mol 和1 mol  中所含化学键能总和比2 mol 中所含化学键能总和比2 mol 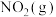 中大116.4 中大116.4  |
更新时间:2024-01-12 18:10:08
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】肼(H2N—NH2)是一种高能燃料,共价键的键能与热化学方程式信息如表:
则关于反应N2H4(g)+O2(g)=N2(g)+2H2O(g)说法正确的是
| 共价键 | N—H | N—N | O=O | N≡N | O—H |
| 键能/(kJ•mol-1) | 391 | 161 | 498 | 946 | 463 |
| A.该反应是吸热反应 | B.N2H4(l)比N2H4(g)能量高 |
| C.反应物总键能小于生成物总键能 | D.H2O空间结构是直线型 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】甲烷与氧气反应过程中的能量变化如图所示。下列有关说法中正确的是( )
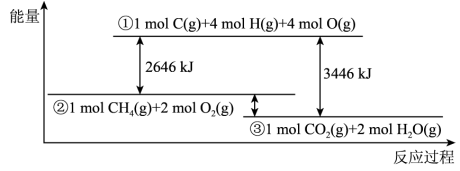

| A.CH4(g)的能量大于CO2(g)和H2O(g)的能量总和 |
| B.反应CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H=-800kJ•mol-1 |
| C.若破坏1molO2(g)中的化学键需吸收热量493kJ,则破坏1molC-H键需吸收热量415kJ |
| D.在反应CH4(g)+2O2(g)═CO2(g)+2H2O(g)中,放出热量400kJ,有1molO-H键生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度时,N2与H2反应过程中的能量变化如图所示。下列叙述正确的是( )
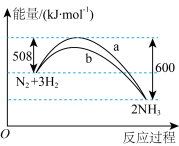

| A.正反应的活化能等于逆反应的活化能 |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.1moN2与3moH2充分反应放出的热量小于92kJ |
| D.增大压强,可以提高反应物活化分子百分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。如图,我国学者发现T℃时,甲醇(CH3OH)在铜基催化剂上的反应机理如下(该反应为可逆反应):
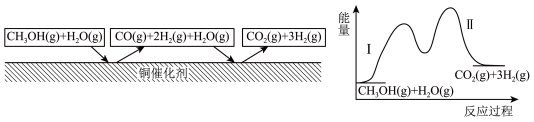
下列有关说法正确的是

下列有关说法正确的是
| A.反应I和反应Ⅱ相比,反应I更容易发生 |
| B.反应I为CH3OH(g)=CO(g)+2H2(g) ∆H<0 |
| C.通过控制催化剂的用量可以控制反应的速率和反应进行的程度 |
| D.CH3OH(g)与H2O(g)在高温条件下更容易反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】CO2催化加氢制CH4的反应为: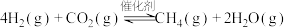 。催化剂上反应过程示意如图1所示。其他条件不变时,CO2的转化率和CH4的选择性(CO2转化为甲烷的量/ CO2转化的总量)随温度变化如图2所示。下列说法不正确的是
。催化剂上反应过程示意如图1所示。其他条件不变时,CO2的转化率和CH4的选择性(CO2转化为甲烷的量/ CO2转化的总量)随温度变化如图2所示。下列说法不正确的是
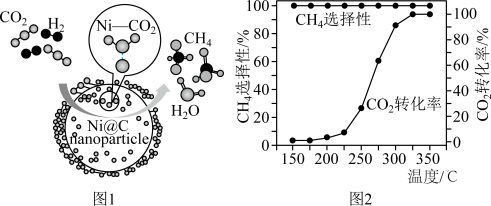
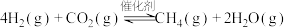 。催化剂上反应过程示意如图1所示。其他条件不变时,CO2的转化率和CH4的选择性(CO2转化为甲烷的量/ CO2转化的总量)随温度变化如图2所示。下列说法不正确的是
。催化剂上反应过程示意如图1所示。其他条件不变时,CO2的转化率和CH4的选择性(CO2转化为甲烷的量/ CO2转化的总量)随温度变化如图2所示。下列说法不正确的是
A.催化剂改变了 中O—C—O键的键角 中O—C—O键的键角 |
| B.150℃到350℃时,基本没有发生副反应 |
C. 催化加氢制 催化加氢制 是一个吸热反应 是一个吸热反应 |
D.结合下列热化学方程式,可以通过盖斯定律计算 加氢制 加氢制 的反应热 的反应热 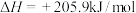 、 、  |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在2L恒容密闭容器中充入2mol X和1mol Y发生反应: ,反应过程持续升高温度,测得混合体系中Z的体积分数与温度的关系如图所示,下列推断正确的是
,反应过程持续升高温度,测得混合体系中Z的体积分数与温度的关系如图所示,下列推断正确的是
 ,反应过程持续升高温度,测得混合体系中Z的体积分数与温度的关系如图所示,下列推断正确的是
,反应过程持续升高温度,测得混合体系中Z的体积分数与温度的关系如图所示,下列推断正确的是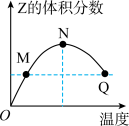
| A.该反应为吸热反应 |
B.平衡常数: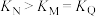 |
| C.升高温度,平衡左移,正反应速率减小,逆反应速率增大 |
| D.达平衡后将容器的体积扩大到4升,Z的体积分数不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知298K时,反应Ag2O(s)→2Ag(s)+ O2(g)的∆S=66.7J·mol-1·K-1,∆H(Ag2O,s)=+31.1kJ·mol-1,则Ag2O的最低分解温度约为。
O2(g)的∆S=66.7J·mol-1·K-1,∆H(Ag2O,s)=+31.1kJ·mol-1,则Ag2O的最低分解温度约为。
 O2(g)的∆S=66.7J·mol-1·K-1,∆H(Ag2O,s)=+31.1kJ·mol-1,则Ag2O的最低分解温度约为。
O2(g)的∆S=66.7J·mol-1·K-1,∆H(Ag2O,s)=+31.1kJ·mol-1,则Ag2O的最低分解温度约为。| A.740K | B.466K | C.233K | D.194K |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】基元反应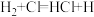 的能量变化如图所示。下列说法不正确的是
的能量变化如图所示。下列说法不正确的是

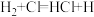 的能量变化如图所示。下列说法不正确的是
的能量变化如图所示。下列说法不正确的是
A.该基元反应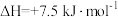 | B.过渡态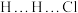 能量高,不稳定 能量高,不稳定 |
C.加入催化剂,则 小于 小于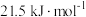 | D.若 ,则该反应在任何温度下都能自发进行 ,则该反应在任何温度下都能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】一定条件下,分别向容积固定的密闭容器中充入A和足量B,发生反应:2A(g)+B(s)  2D(g) ΔH<0,测得相关数据如下,分析可知下列说法不正确的是
2D(g) ΔH<0,测得相关数据如下,分析可知下列说法不正确的是
 2D(g) ΔH<0,测得相关数据如下,分析可知下列说法不正确的是
2D(g) ΔH<0,测得相关数据如下,分析可知下列说法不正确的是| 实验 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应温度/℃ | 800 | 800 | 850 |
| c(A)始/mol·L-1 | 1 | 2 | 1 |
| c(A)平/mol·L-1 | 0.5 | 1 | 0.85 |
| 放出的热量/kJ | a | b | c |
| A.实验Ⅲ的化学平衡常数:K<1 |
| B.放出的热量关系为b kJ>2a kJ |
| C.实验Ⅲ在30 min时达到平衡,则30 min内A的平均反应速率v(A)为0.005 mol·L-1·min-1 |
| D.当容器内气体密度不随时间变化时,表明上述反应已达平衡 |
您最近一年使用:0次

 2NH3
2NH3 、
、 、
、 分别表示N2、H2、NH3,下列说法
分别表示N2、H2、NH3,下列说法


