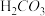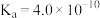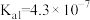HA是有机合成中常用的一元酸。
(1)向20.00mL HA溶液中,滴加VmL 0.1000 mol·L-1NaOH溶液,滴定过程中溶液pH随NaOH溶液体积的变化如下图所示。
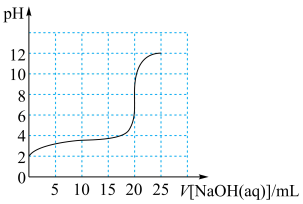
①HA是_____ 酸(填“强”或“弱”)。
②从滴定曲线可得出此HA溶液的浓度为__________ 。
③由此可以计算出HA的电离常数的数量级接近______ 。
A.10-1 B.10-3 C.10-5 D.10-7
④V(NaOH)=10mL时,粒子浓度(不包含水分子)由大到小是________ 。
(2)已知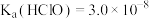
①常温下稀释相同pH的HA和HClO溶液图像如下图,则稀释HA溶液的图像为________ (填“a”或“b”)。
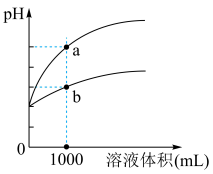
②0.1 mol·L-1HA溶液加水稀释过程中,下列表达式的数据变大的是_____ (填序号)
A. c(H+) B. C.
C. 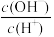 D.
D. 
③常温下浓度均为0.01mol·L-1的NaClO和NaA的溶液的pH较大的是__________________ 。
(1)向20.00mL HA溶液中,滴加VmL 0.1000 mol·L-1NaOH溶液,滴定过程中溶液pH随NaOH溶液体积的变化如下图所示。

①HA是
②从滴定曲线可得出此HA溶液的浓度为
③由此可以计算出HA的电离常数的数量级接近
A.10-1 B.10-3 C.10-5 D.10-7
④V(NaOH)=10mL时,粒子浓度(不包含水分子)由大到小是
(2)已知
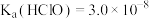
①常温下稀释相同pH的HA和HClO溶液图像如下图,则稀释HA溶液的图像为

②0.1 mol·L-1HA溶液加水稀释过程中,下列表达式的数据变大的是
A. c(H+) B.
 C.
C. 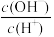 D.
D. 
③常温下浓度均为0.01mol·L-1的NaClO和NaA的溶液的pH较大的是
更新时间:2024-01-24 06:48:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】常温下,将某一元酸HA 和NaOH 溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH 如下表:
请回答下列问题:
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸___________________________ 。
(2)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2______ (填“是”或“否”)。混合溶液中离子浓度c(A-)与c(Na+)的大小关系是_______ 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是______________ 酸(填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是 ___________________________ 。
(4)丁组实验所得混合溶液中由水电离出的c(H+)=________ mol/L。写出该混合溶液中下列算式的精确结果(不能做近似计算)。 c(N+)-c(A-)=__________ mol/L 。
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | cl | 0.2 | pH=7 |
| 丙 | 0.1 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
请回答下列问题:
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸
(2)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是
(4)丁组实验所得混合溶液中由水电离出的c(H+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫代硫酸钠(Na2S2O3)应用广泛,可用作定影液、含砷废水去除剂、定量分析还原剂等。
(1)Na2S2O3可用作定影液熔解未曝光的溴化银(AgBr),通过如图1所示转化可实现定影液再生,也可达到回收银的目的。
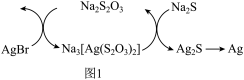
AgBr溶于Na2S2O3溶液反应的离子方程式为________ 。
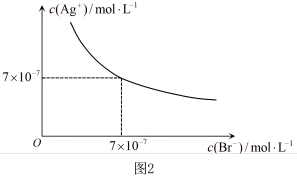
(2)在t℃时,AgBr在水中的沉淀溶解平衡曲线如图2所示。已知t℃时,Ksp(AgCl)=4.9×10-10,在t℃时,反应AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数K=
AgBr(s)+Cl-(aq)的平衡常数K=_______ 。
(3)Na2S2O3去除酸性废水中H3AsO3的反应机理如图3所示(图中“HS”为自由基,“•”表示孤单电子)。
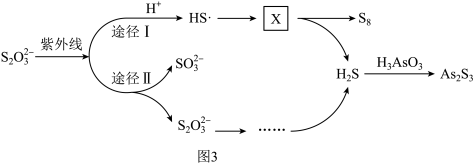
方框中X的化学式为_______ 。
(4)Na2S2O3可测定含Cr2O 废水中Cr元素的含量。量取废水20.00mL,硫酸酸化后加入过量KI溶液,发生反应:6I-+14H++Cr2O
废水中Cr元素的含量。量取废水20.00mL,硫酸酸化后加入过量KI溶液,发生反应:6I-+14H++Cr2O =3I2+2Cr3++7H2O。加入少量淀粉作为指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,发生反应:I2+2S2O
=3I2+2Cr3++7H2O。加入少量淀粉作为指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,发生反应:I2+2S2O =2I-+S4O
=2I-+S4O 平行滴定3次,平均消耗标准Na2S2O3溶液24.00mL。
平行滴定3次,平均消耗标准Na2S2O3溶液24.00mL。
①滴定终点的现象为_______ 。
②废水中Cr元素的量为_______ 。
(1)Na2S2O3可用作定影液熔解未曝光的溴化银(AgBr),通过如图1所示转化可实现定影液再生,也可达到回收银的目的。
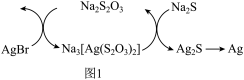
AgBr溶于Na2S2O3溶液反应的离子方程式为
(2)在t℃时,AgBr在水中的沉淀溶解平衡曲线如图2所示。已知t℃时,Ksp(AgCl)=4.9×10-10,在t℃时,反应AgCl(s)+Br-(aq)
 AgBr(s)+Cl-(aq)的平衡常数K=
AgBr(s)+Cl-(aq)的平衡常数K=
(3)Na2S2O3去除酸性废水中H3AsO3的反应机理如图3所示(图中“HS”为自由基,“•”表示孤单电子)。

方框中X的化学式为
(4)Na2S2O3可测定含Cr2O
 废水中Cr元素的含量。量取废水20.00mL,硫酸酸化后加入过量KI溶液,发生反应:6I-+14H++Cr2O
废水中Cr元素的含量。量取废水20.00mL,硫酸酸化后加入过量KI溶液,发生反应:6I-+14H++Cr2O =3I2+2Cr3++7H2O。加入少量淀粉作为指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,发生反应:I2+2S2O
=3I2+2Cr3++7H2O。加入少量淀粉作为指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,发生反应:I2+2S2O =2I-+S4O
=2I-+S4O 平行滴定3次,平均消耗标准Na2S2O3溶液24.00mL。
平行滴定3次,平均消耗标准Na2S2O3溶液24.00mL。①滴定终点的现象为
②废水中Cr元素的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下检测方法:将v L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化成NO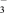 ,加水稀释至100.00 mL。量取20.00 mL该溶液,加入v1 mL c1 mol·L-1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。回答下列问题:
,加水稀释至100.00 mL。量取20.00 mL该溶液,加入v1 mL c1 mol·L-1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。回答下列问题:
(1)NO被H2O2氧化为NO 的离子方程式为
的离子方程式为_________________________________________________ 。
(2)滴定过程中发生下列反应:
3Fe2++NO +4H+===NO↑+3Fe3++2H2O
+4H+===NO↑+3Fe3++2H2O
Cr2O +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
则气样中NOx折合成NO2的含量为________________ mg·m-3。
(3)若FeSO4标准溶液部分变质,会使测定结果___________________________________________ (填“偏高”“偏低”或“无影响”)
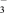 ,加水稀释至100.00 mL。量取20.00 mL该溶液,加入v1 mL c1 mol·L-1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。回答下列问题:
,加水稀释至100.00 mL。量取20.00 mL该溶液,加入v1 mL c1 mol·L-1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。回答下列问题:(1)NO被H2O2氧化为NO
 的离子方程式为
的离子方程式为(2)滴定过程中发生下列反应:
3Fe2++NO
 +4H+===NO↑+3Fe3++2H2O
+4H+===NO↑+3Fe3++2H2OCr2O
 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O则气样中NOx折合成NO2的含量为
(3)若FeSO4标准溶液部分变质,会使测定结果
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.已知:在相同条件下醋酸与氨水电离程度相同,现有浓度均为0.1mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是 填序号
填序号
____ 。
(2)若④、⑤、⑥、⑦、⑧五种溶液中NH 浓度相等,则五种溶液的物质的量浓度由大到小的顺序是
浓度相等,则五种溶液的物质的量浓度由大到小的顺序是 填序号
填序号
___ 。
Ⅱ 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(3)pH相等的下列溶液,它们的物质的量浓度由大到小排列的顺序是____ (用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:____ 。
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=____ (填准确数值 。
。
(6)25℃时,将amol•L-1的醋酸与bmol•L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为____ 。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是
 填序号
填序号
(2)若④、⑤、⑥、⑦、⑧五种溶液中NH
 浓度相等,则五种溶液的物质的量浓度由大到小的顺序是
浓度相等,则五种溶液的物质的量浓度由大到小的顺序是 填序号
填序号
Ⅱ
 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4,.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=
 。
。(6)25℃时,将amol•L-1的醋酸与bmol•L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】今有a.盐酸 b.硫酸 c.醋酸三种酸,物质的量浓度为0.1 mol/L的三种酸溶液的pH由大到小的顺序是___________ ;如果取等体积的0.1 mol/L的三种酸溶液,用0.1 mol/L的NaOH溶液中和,当恰好完全反应时,消耗NaOH溶液的体积由大到小的顺序是__________ 。(用a、b、c表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】运用相关原理,回答下列各小题:
(1)某 溶液的浓度是
溶液的浓度是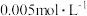 :
:
①此溶液的 为
为_______ ;
②用水稀释到原来体积的100倍, 为
为_______ ;
③再继续稀释 倍,
倍, 为
为_______ 。
(2)室温下、某水溶液中存在的离子有 、
、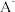 、
、 、
、 。根据题意,回答下列问题:
。根据题意,回答下列问题:
①若由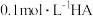 溶液与
溶液与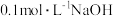 溶液等体积混合而得,则溶液的
溶液等体积混合而得,则溶液的
_______ 7(填大小关系)。
②若溶液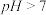 ,则
,则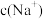
_______ 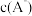 ,理由是
,理由是_______
③若溶液由 的HA溶液
的HA溶液 与
与 的
的 溶液
溶液 混合而得,则下列说法中正确的是
混合而得,则下列说法中正确的是_______ (填选项代号)。
A.若反应后溶液呈中性,则
B.若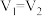 反应后溶液的
反应后溶液的 一定等于7
一定等于7
C.若反应后溶液呈酸性,则 一定大于
一定大于
D.若反应后溶液呈碱性,则 一定小于
一定小于
(1)某
 溶液的浓度是
溶液的浓度是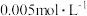 :
:①此溶液的
 为
为②用水稀释到原来体积的100倍,
 为
为③再继续稀释
 倍,
倍, 为
为(2)室温下、某水溶液中存在的离子有
 、
、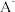 、
、 、
、 。根据题意,回答下列问题:
。根据题意,回答下列问题:①若由
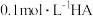 溶液与
溶液与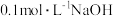 溶液等体积混合而得,则溶液的
溶液等体积混合而得,则溶液的
②若溶液
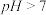 ,则
,则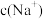
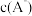 ,理由是
,理由是③若溶液由
 的HA溶液
的HA溶液 与
与 的
的 溶液
溶液 混合而得,则下列说法中正确的是
混合而得,则下列说法中正确的是A.若反应后溶液呈中性,则

B.若
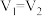 反应后溶液的
反应后溶液的 一定等于7
一定等于7C.若反应后溶液呈酸性,则
 一定大于
一定大于
D.若反应后溶液呈碱性,则
 一定小于
一定小于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)25℃时,FeCl3溶液的pH_______ 7(填“>”、“<”或“=”),原因是(用离子方程式表示)____ 。把FeCl3溶液蒸干灼烧得到的主要产物是_______ 。
(2)某温度下纯水中的c(H+)=2×10-7 mol/L,则此时溶液中的c(OH-)=_______ ;若温度不变,滴入稀盐酸,使c(H+)=5×10-4 mol/L,则此时溶液中由水电离产生的c(H+)=_______ 。
(3)常温下,0.1 mol/L HA溶液中 =108,现取0.1 mol/L HA溶液与pH=13的NaOH溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:
=108,现取0.1 mol/L HA溶液与pH=13的NaOH溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:
①混合溶液呈_______ (填“酸”“中”或“碱”)性,理由是_______ (用离子方程式表示)。
②混合溶液中由水电离出的c(H+)_______ (填“大于”“小于”或“等于”)0.1 mol/L NaOH溶液中由水电离出的c(H+)。
(1)25℃时,FeCl3溶液的pH
(2)某温度下纯水中的c(H+)=2×10-7 mol/L,则此时溶液中的c(OH-)=
(3)常温下,0.1 mol/L HA溶液中
 =108,现取0.1 mol/L HA溶液与pH=13的NaOH溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:
=108,现取0.1 mol/L HA溶液与pH=13的NaOH溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:①混合溶液呈
②混合溶液中由水电离出的c(H+)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】物质在水中可能存在电离平衡、盐的水解平衡等,它们都可看作化学平衡。请根据所学的知识回答:
(1)A为0.1mol•L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为___________ 。
(2)B为0.1 mol•L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(分别用离子方程式表示):___________ ;实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因:___________ 。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入______ ,目的是___________ ;将B和C溶液混合后,反应的离子方程式为___________ 。
(1)A为0.1mol•L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为
(2)B为0.1 mol•L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(分别用离子方程式表示):
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)25℃时,将pH=12的NaOH溶液aL与pH=l的HCl溶液bL混合,若所得混合液为中性,则a:b=____ 。
(2)25℃时,将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液pH>7,则溶液中c(Na+)____ c(CH3COO-)(填“>”、“<”或“=”)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液显____ 性(填“酸”、“中”或“碱”)。
(4)已知T℃时:CH3COOH CH3COO-+H+Ka=m
CH3COO-+H+Ka=m
H2O=H++OH-Kw=n
则: =
=____ 。
(5)电离常数(25℃):CH3COOH:Ka=1.8 10-5H2SO3:Ka1=1.3
10-5H2SO3:Ka1=1.3 10-2、Ka2=6.0
10-2、Ka2=6.0 10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:____ 。
(1)25℃时,将pH=12的NaOH溶液aL与pH=l的HCl溶液bL混合,若所得混合液为中性,则a:b=
(2)25℃时,将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液pH>7,则溶液中c(Na+)
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液显
(4)已知T℃时:CH3COOH
 CH3COO-+H+Ka=m
CH3COO-+H+Ka=mH2O=H++OH-Kw=n
则:
 =
=(5)电离常数(25℃):CH3COOH:Ka=1.8
 10-5H2SO3:Ka1=1.3
10-5H2SO3:Ka1=1.3 10-2、Ka2=6.0
10-2、Ka2=6.0 10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】常温下,部分酸的电离平衡常数如下:
(1) 相同的三种酸,则
相同的三种酸,则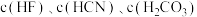 的浓度从大到小为
的浓度从大到小为___________ 。
(2)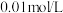 的
的 溶液中,
溶液中, 为
为_____  ,使此溶液中
,使此溶液中 的电离程度增大且
的电离程度增大且 也增大的方法是
也增大的方法是_______ 。
(3)中和等量的 ,消耗等
,消耗等 的氢氟酸和硫酸的体积分别为
的氢氟酸和硫酸的体积分别为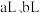 ,则a
,则a______ b(填“大于”、“小于”或“等于”,下同)。中和等浓度、等体积的氢氟酸和硫酸需要 的物质的量为
的物质的量为 ,则
,则
___________  。
。
(4)向 中通入少量的
中通入少量的 ,发生的离子方程式为
,发生的离子方程式为___________ 。
(5)设计实验证明氢氟酸比盐酸的酸性弱___________ 。
化学式 |
|
|
|
电离常数 |
|
|
|
 相同的三种酸,则
相同的三种酸,则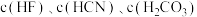 的浓度从大到小为
的浓度从大到小为(2)
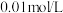 的
的 溶液中,
溶液中, 为
为 ,使此溶液中
,使此溶液中 的电离程度增大且
的电离程度增大且 也增大的方法是
也增大的方法是(3)中和等量的
 ,消耗等
,消耗等 的氢氟酸和硫酸的体积分别为
的氢氟酸和硫酸的体积分别为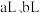 ,则a
,则a 的物质的量为
的物质的量为 ,则
,则
 。
。(4)向
 中通入少量的
中通入少量的 ,发生的离子方程式为
,发生的离子方程式为(5)设计实验证明氢氟酸比盐酸的酸性弱
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知,常温下几种物质的电离常数如下:
(1)(NH4)2CO3溶液的pH_______ (填“大于”或“小于”)7
(2)物质的量浓度均为0.1mol·L-1的4种溶液:① 、②
、② 、③
、③ 、④
、④ ,按要求从大到小排序。
,按要求从大到小排序。 :
:_______ ; :
:_______ 。(用序号填空)
①少量 通入到过量的
通入到过量的 溶液中:
溶液中:_______ 。
②少量 通入到过量的NaClO溶液中:
通入到过量的NaClO溶液中:_______ 。
(3)25℃时,若氨水的浓度为2.0mol·L-1,溶液中的c(OH−)=_______ mol·L−1。将SO2通入该氨水中,当c(OH−)降至1.0×10−7mol·L−1时,溶液中的 =
=_______ 。SO2可用足量小苏打溶液吸收,反应的离子方程式是_______ 。
| 化学式 | H2CO3 | CH3COOH | NH3·H2O | H2SO3 | HClO |
| 电离平衡常数 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=1.8×10-5 | Kb=1.8×10-5 | Ka1=1.4×10-2 Ka2=6.0×10-8 | 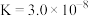 |
(2)物质的量浓度均为0.1mol·L-1的4种溶液:①
 、②
、② 、③
、③ 、④
、④ ,按要求从大到小排序。
,按要求从大到小排序。 :
: :
:①少量
 通入到过量的
通入到过量的 溶液中:
溶液中:②少量
 通入到过量的NaClO溶液中:
通入到过量的NaClO溶液中:(3)25℃时,若氨水的浓度为2.0mol·L-1,溶液中的c(OH−)=
 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知:25℃时,①亚硫酸的电离平衡常数为K1=1.6×10-2,K2=1.0×10-7;②次氯酸的电离平衡常数为K1=4.0×10-8;③碳酸的电离平衡常数为K1=4.0×10-7,K1=4.0×10-11。回答下列问题:
(1)上述三种酸由强到弱的顺序为(填分子式)_______ 。
(2)写出碳酸的电离方程式_______
(3)向H2SO3溶液中加入NaOH溶液时,溶液中c(H+)_______ (填“增大”、“减小”或“不变”,下同),c(SO )
)_______ 。
(4)将次氯酸溶液升高温度,则电离度_______ (填“增大”、“减小”或“不变”,下同),导电能力_______ ,c(H+)与c(HClO)的比值_______
(1)上述三种酸由强到弱的顺序为(填分子式)
(2)写出碳酸的电离方程式
(3)向H2SO3溶液中加入NaOH溶液时,溶液中c(H+)
 )
)(4)将次氯酸溶液升高温度,则电离度
您最近一年使用:0次