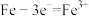化学在生活和化工生产中起着重要的作用。有关下列叙述正确的是
A.用食醋清洗水壶里的水垢,是因为 的酸性比 的酸性比 强 强 |
| B.合成氨工业中,升高温度或增大压强都是为了提高氨的平衡产量 |
| C.在钢铁船体上装一块锌板防止腐蚀是运用了勒夏特列原理 |
| D.煅烧硫铁矿制硫酸时,将矿石粉碎是为了减慢反应速率 |
更新时间:2024-01-22 21:53:32
|
相似题推荐
【推荐1】中国科学家研究在Pd/SVG催化剂上H2还原NO生成N2和NH3的路径,各基元反应及活化能Ea(kJ/mol)如图所示,下列说法错误的是
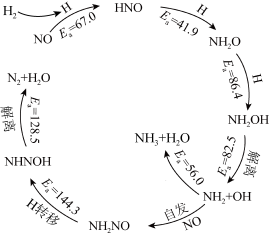

| A.生成NH3的各基元反应中,N元素均被还原 |
B.生成NH3的总反应方程式为5H2+2NO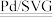 2H2O+2NH3 2H2O+2NH3 |
| C.决定NO生成NH3速率的基元反应为NH2O+H→NH2OH |
| D.在Pd/SVG催化剂上,NO更容易被H2还原为N2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验中,对应的实验以及结论都正确且二者具有因果关系的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向盛有氨水的烧杯中插入两个石墨电极,接通电源,电流表指针发生较大偏转 | 氨水是电解质 |
| B | 取2支都装有5mL 10%的H2O2溶液的试管,向其中一支加入少量MnO2,观察实验现象。 | 催化剂能加快反应速率 |
| C | 分别取装有等体积的0.1 mol·L-1和0.2 mol·L-1 KI溶液的试管放入20 ℃和30 ℃ 的水中,再向其中加入0.1 mol·L-1的硫酸和淀粉溶液,发生反应4H++O2+4I-=2I2+2H2O观察实验现象 | 反应物温度越高,反应速率越快 |
| D | 探究浓度对反应速率的影响,向2支盛有5 mL不同浓度NaHSO3溶液的试管中同时加入2 mL 5% H2O2溶液,观察实验现象 | 反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】N2O5是一种新型硝化剂,在一定温度下可发生如下反应: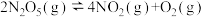 △H>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表,下列说法不正确的是
△H>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表,下列说法不正确的是
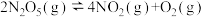 △H>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表,下列说法不正确的是
△H>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表,下列说法不正确的是| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/(mol/L) | 5.00 | 3.50 | 2.50 | 2.50 |
| A.反应在1000 s时处于平衡状态 | B.升高温度,既能加快反应速率,也能增大NO2的产率 |
| C.增大压强,能提高N2O5的平衡转化率 | D.0~500 s内,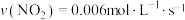 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验能达到预期目的是
| 编号 | 实验内容 | 实验目的 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快 | 证明HX酸性比HY强 |
| B | 室温下,用pH试纸测定浓度为0.1mo/LNaClO和0.1mol/LCH3COONa溶液的pH | 比较HClO和CHCOOH酸性强弱 |
| C | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| D | 向10mL0.2mo/LNaOH溶液中滴2滴0.1mol/LMgCl2溶液,产生白色沉淀后再滴加2滴0.1mol/LFeCl3又生成红褐色沉淀 | 证明相同温度下Ksp:Mg(OH)2>Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作能达到目的的是
| 选项 | 目的 | 操作 |
| A | 验证微蓝色透明的硫的酒精溶液属于胶体 | 激光笔照射 |
| B | 除去氯化铵溶液中的氯化铁 | 加NaOH溶液调节pH |
| C | 证明氧化性: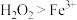 | 将用稀硫酸酸化后的 溶液滴入 溶液滴入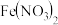 溶液中 溶液中 |
| D | 验证铁的析氢腐蚀 | 将铁钉放在试管中,用NaCl溶液浸没 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于电化学的叙述正确的是( )
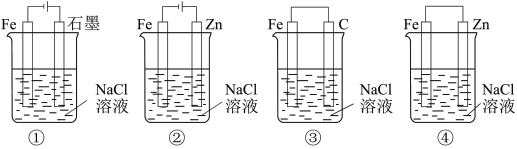
| A.图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红 |
| B.图②装置中Fe电极参与反应发生腐蚀 |
| C.图③可以模拟钢铁的吸氧腐蚀,碳棒一极的电极反应式:O2+2H2O+4e-=4OH- |
| D.上述4个装置中,图①、②中Fe腐蚀速率较快,图③中Fe腐蚀速率较慢 |
您最近一年使用:0次

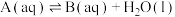 (快)
(快) (慢)
(慢) 的浓度为wmol/L。下列说法错误的是
的浓度为wmol/L。下列说法错误的是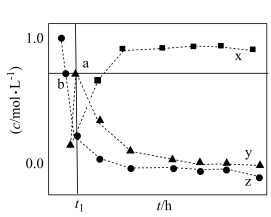
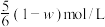
 pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法正确的是
pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法正确的是