在一定条件下,下列叙述与图像对应正确的是
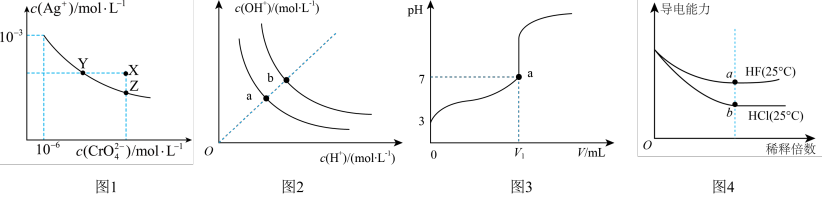

A.图1表示 T℃时, 在水溶液中的沉淀溶解平衡曲线,x点对应该温度下的不饱和溶液 在水溶液中的沉淀溶解平衡曲线,x点对应该温度下的不饱和溶液 |
B.图2表示不同温度下水中  和 和  的浓度变化曲线,图中 a点对应温度高于 b点 的浓度变化曲线,图中 a点对应温度高于 b点 |
C.图3表示某温度下向  溶液中逐滴加入 溶液中逐滴加入  溶液,滴定过程宜选用甲基橙作指示剂 溶液,滴定过程宜选用甲基橙作指示剂 |
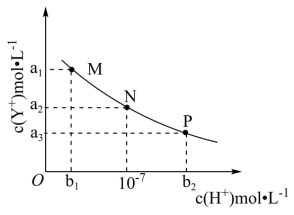
D.图 4表示氢氟酸为弱酸,且 a点对应  比 b点对应 比 b点对应  小 小 |
更新时间:2024-02-01 21:13:09
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常温下,纯水中存在电离平衡:H2O H++OH-,若要使水的电离平衡向正反应方向移动,并使溶液中的c(H+)减小,应加入的适当物质是
H++OH-,若要使水的电离平衡向正反应方向移动,并使溶液中的c(H+)减小,应加入的适当物质是
 H++OH-,若要使水的电离平衡向正反应方向移动,并使溶液中的c(H+)减小,应加入的适当物质是
H++OH-,若要使水的电离平衡向正反应方向移动,并使溶液中的c(H+)减小,应加入的适当物质是| A.NaHSO4 | B.AlCl3 | C.NaOH | D.NaHCO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】室温下,下列各组离子在指定溶液中一定能大量共存的是
A.在澄清透明的溶液中: 、 、 、 、 、 、 |
B.中性溶液中: 、 、 、 、 、 、 |
C.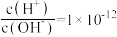 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.水电离出的 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,用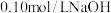 溶液分别滴定
溶液分别滴定 浓度均为
浓度均为 的
的 溶液
溶液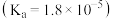 和
和 溶液
溶液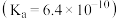 所得滴定曲线如图,下列说法正确的是
所得滴定曲线如图,下列说法正确的是

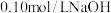 溶液分别滴定
溶液分别滴定 浓度均为
浓度均为 的
的 溶液
溶液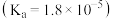 和
和 溶液
溶液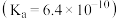 所得滴定曲线如图,下列说法正确的是
所得滴定曲线如图,下列说法正确的是
| A.溶液中水的电离程度②<③<④ |
| B.滴定过程可使用甲基橙做指示剂 |
C.点①和点②所示溶液中: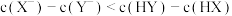 |
D.曲线 是滴定 是滴定 溶液的 溶液的 变化曲线 变化曲线 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图是用0.1 mol·L-1 NaOH溶液分别滴定20 mL浓度均为0.1 mol·L-1的不同一元酸的滴定曲线(图中曲线由上向下依次是氢氰酸、醋酸、氢氟酸、盐酸),下列说法错误的是
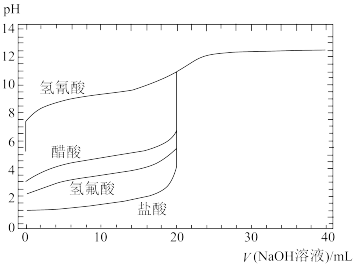

| A.酸性:HF>CH3COOH>HCN |
| B.当加入10 mL NaOH溶液时,c(CN-)>c(CH3COO-) |
| C.用NaOH溶液滴定醋酸时,应用酚酞作指示剂不能使用甲基橙 |
| D.随NaOH溶液滴入,CH3COOH溶液中水的电离程度先变大后变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,下列说法中错误的是
A. 的 的 和 和 混合溶液中: 混合溶液中: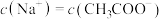 |
B. 溶液中, 溶液中,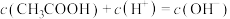 |
C. 的氨水,稀释10倍后,其 的氨水,稀释10倍后,其 ,则 ,则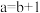 |
D.pH相同的① 、② 、② 、③ 、③ 三种溶液的 三种溶液的 :①>②>③ :①>②>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】调节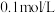 的二元弱酸
的二元弱酸 溶液的pH,溶液中各种微粒的分布分数
溶液的pH,溶液中各种微粒的分布分数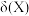 与溶液的pH的关系如下图所示(已知
与溶液的pH的关系如下图所示(已知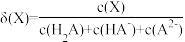 ),下列叙述错误的是
),下列叙述错误的是

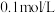 的二元弱酸
的二元弱酸 溶液的pH,溶液中各种微粒的分布分数
溶液的pH,溶液中各种微粒的分布分数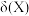 与溶液的pH的关系如下图所示(已知
与溶液的pH的关系如下图所示(已知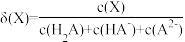 ),下列叙述错误的是
),下列叙述错误的是
A.溶液pH从1变到接近3的过程中发生的反应主要是 |
B.由图象中的数据可以求出 的两级电离常数分别为 的两级电离常数分别为 、 、 |
C.当溶液中的 时, 时, |
D.当溶液 时, 时, |
您最近一年使用:0次
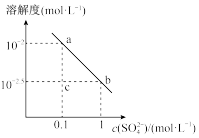
【推荐1】已知溶解度也可用物质的量浓度表示,25℃时, 在不同浓度
在不同浓度 溶液中的溶解度如图所示。下列说法正确的是
溶液中的溶解度如图所示。下列说法正确的是
 在不同浓度
在不同浓度 溶液中的溶解度如图所示。下列说法正确的是
溶液中的溶解度如图所示。下列说法正确的是
A.图中a、b两点 相同 相同 |
| B.把a点的溶液加热蒸发掉一部分水,恢复到室温,可得到b点的溶液 |
C.该温度下, 溶度积的数量级为 溶度积的数量级为 |
D.在c点的溶液中加入少量 固体,溶液可变为b点 固体,溶液可变为b点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,Ksp[Mg(OH)2]=10-12,Ksp(MgF2)=10-10。下列说法正确的是
| A.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4F固体,c(Mg2+)减小 |
| B.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| C.25℃时,向浓度均为0.1mol•L-1的NaOH和NaF的混合溶液中逐滴滴加MgCl2溶液,先生成Mg(OH)2沉淀 |
| D.25℃时,Mg(OH)2固体在20mL 0.01 mol•L-1氨水中的Ksp比在20mL 0.01 mol•L-1NH4F溶液中的Ksp小 |
您最近一年使用:0次


 悬浊液中存在如下平衡:
悬浊液中存在如下平衡:


 ,已知
,已知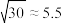



 固体,
固体, 减小,
减小, 增大
增大

