25℃时,在 溶液中滴入等浓度盐酸标准液,溶液pH与所加盐酸的体积关系如图.下列说法错误的是
溶液中滴入等浓度盐酸标准液,溶液pH与所加盐酸的体积关系如图.下列说法错误的是
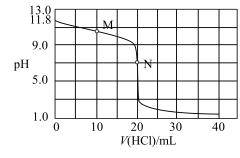
 溶液中滴入等浓度盐酸标准液,溶液pH与所加盐酸的体积关系如图.下列说法错误的是
溶液中滴入等浓度盐酸标准液,溶液pH与所加盐酸的体积关系如图.下列说法错误的是
| A.该滴定过程可选择甲基橙作为指示剂 |
B. 的数量级为 的数量级为 |
C.M点处有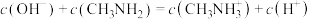 |
D.N点处 的电离程度与 的电离程度与 水解程度相同 水解程度相同 |
更新时间:2024-02-17 10:45:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】室温下,用0.100 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 mol·L-1的盐酸和醋酸,滴定曲线如图所示。下列说法不正确的是
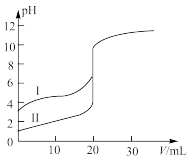

| A.II表示的是滴定盐酸的曲线 |
| B.pH=7时,滴定醋酸消耗的V(NaOH)等于20.00 mL |
| C.初始时盐酸的浓度为0.10mol/L |
| D.滴定醋酸溶液、盐酸时,均可选择酚酞溶液做指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某学生以酚酞为指示剂用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,三次实验分别记录有关数据如下表:
下列说法正确的是
| 滴定次数 | 待测氢氧化钠溶液的体积/mL |  盐酸的体积/mL 盐酸的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 27.45 |
| 第二次 | 25.00 | 0.00 | 30.30 |
| 第三次 | 25.00 | 0.00 | 27.55 |
| A.当溶液从红色刚好变成无色时,则达到滴定终点 |
B.该氢氧化钠溶液中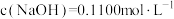 |
| C.滴定达终点时,滴定管尖嘴有悬液,则测定结果偏低 |
| D.实验中锥形瓶应用待测氢氧化钠溶液润洗 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】298 K时,向20 mL 0.1 mol·L1 HR溶液中滴加0.1 mol·L1 NaOH溶液,混合溶液的pH与所加NaOH溶液体积的关系如图所示。下列说法正确的是
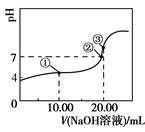

| A.①点对应溶液中:c(Na)>c(R)>c(H)>c(OH) |
| B.加少量蒸馏水稀释②对应的溶液,稀释后溶液pH>7 |
| C.③点对应的溶液中:c(Na)=c(OH)+c(HR) |
D.若②点坐标为(x,7),则HR的电离常数Ka=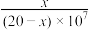 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下表数据(均在同温、同压下测定)
可得出弱电解质强弱顺序正确的是
| 酸 | HX | HY | HZ |
| 物质的量浓度/mol·L−1 | 0.1 | 0.2 | 0.3 |
| 电离平衡常数 | 7.2×10−4 | 1.8×10−4 | 1.8×10−5 |
| A.HX>HY>HZ | B.HZ>HY>HX |
| C.HY>HZ>HX | D.HZ>HX>HY |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列有关说法正确的是
| A.4CuO(s)=2Cu2O(s)+O2(g)在室温下不能自发进行,说明该反应△H>0 |
| B.向稀醋酸中加入醋酸钠固体,溶液pH升高的主要原因是醋酸钠水解呈碱性 |
| C.室温下K(HCN)<K(CH3COOH),说明CH3COOH的电离度一定比HCN大 |
D.H2S(g)+FeO(s) FeS(s)+H2O(g),其他条件不变时增大压强,反应速率V正(H2S)和H2S的平衡转化率均增大 FeS(s)+H2O(g),其他条件不变时增大压强,反应速率V正(H2S)和H2S的平衡转化率均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.等物质的量的 和 和 中所含阴离子数均为 中所含阴离子数均为 |
B.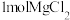 中 中 键个数为 键个数为 |
C.标准状况下, 中一定含有 中一定含有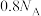 个 个 键 键 |
D.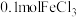 水解制得的 水解制得的 胶体中胶粒数小于 胶体中胶粒数小于 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
A.已知KHC2O4溶液中c(HC2O )>c(C2O )>c(C2O )>c(H2C2O4),则c(H+)>c(OH-) )>c(H2C2O4),则c(H+)>c(OH-) |
| B.常温下,体积相等、pH相等的盐酸和氯化铵两溶液,导电能力相同 |
C.向NaHCO3溶液中加入CH3COONa固体,则c(HCO )变大 )变大 |
D.Ca2+、Al3+、S2-、OH-、ClO-、NO 几种离子中,对水的电离平衡无影响的有2种 几种离子中,对水的电离平衡无影响的有2种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】室温下,通过下列实验探究NaHSO3、Na2SO3溶液的性质。
实验1:向酸性KMnO4溶液中滴加0.1 mol· L-1Na2SO3溶液,溶液褪色
实验2:向0.1 mol· L-1 Na2SO3溶液中通入少量SO2,溶液的pH从10下降到8
实验3:用pH试纸测定0.1mol·L-1NaHSO3溶液的pH,测得pH约为4
实验4:向0.1 mol·L-1NaHSO3溶液中滴加NaClO溶液,观察不到实验现象
下列说法正确的是
实验1:向酸性KMnO4溶液中滴加0.1 mol· L-1Na2SO3溶液,溶液褪色
实验2:向0.1 mol· L-1 Na2SO3溶液中通入少量SO2,溶液的pH从10下降到8
实验3:用pH试纸测定0.1mol·L-1NaHSO3溶液的pH,测得pH约为4
实验4:向0.1 mol·L-1NaHSO3溶液中滴加NaClO溶液,观察不到实验现象
下列说法正确的是
| A.实验1中溶液褪色,说明Na2SO3有氧化性 |
B.实验2得到的溶液中有c(OH- )> c(H+ )+ c(HSO )+ 2c(H2SO3) )+ 2c(H2SO3) |
C.实验3可以得出: c(H+ )+ c(SO )>c(OH- )+c(H2SO3) )>c(OH- )+c(H2SO3) |
D.实验4中反应的离子方程式: HSO + ClO-=SO + ClO-=SO + HClO + HClO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知:H2A为二元弱酸,25℃时,在0.1mol/L50mL的H2A溶液中,H2A、 、
、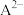 的物质的量浓度随溶液pH变化的关系如图所示(注:溶液的pH用NaOH固体调节,体积变化忽略不计)。下列说法不正确的是
的物质的量浓度随溶液pH变化的关系如图所示(注:溶液的pH用NaOH固体调节,体积变化忽略不计)。下列说法不正确的是
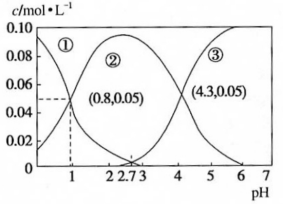
 、
、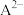 的物质的量浓度随溶液pH变化的关系如图所示(注:溶液的pH用NaOH固体调节,体积变化忽略不计)。下列说法不正确的是
的物质的量浓度随溶液pH变化的关系如图所示(注:溶液的pH用NaOH固体调节,体积变化忽略不计)。下列说法不正确的是
A.在pH=2.7时,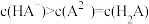 |
B.pH在2.7, |
C.在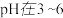 的过程中,主要发生反应 的过程中,主要发生反应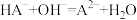 |
D.在pH=4.3时,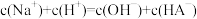 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,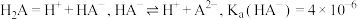 ,向
,向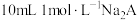 溶液中滴加
溶液中滴加 盐酸,下列有关说法正确的是
盐酸,下列有关说法正确的是

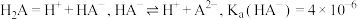 ,向
,向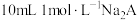 溶液中滴加
溶液中滴加 盐酸,下列有关说法正确的是
盐酸,下列有关说法正确的是
A.滴定前, |
B.V(盐酸)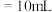 时,溶液 时,溶液 |
C.当滴定至溶液呈中性时,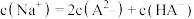 |
D.滴定过程中 变化曲线如图 变化曲线如图 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】室温下,将两种溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
| A.0.1mol·L-1HF(Ka=6.8×10-4)溶液和0.1mol·L-1NaOH溶液混合:c(Na+)>c(OH-)>c(F-)>c(H+) |
B.0.1mol·L-1NaHCO3溶液和0.1mol·L-1Na2CO3溶液混合:3c(Na+)=2c(CO )+2c(HCO )+2c(HCO )+2c(H2CO3) )+2c(H2CO3) |
C.0.1mol·L-1NaOH溶液和0.1mol·L-1H2C2O4(Ka1=5.4×10−2,Ka2=5.4×10-5)溶液混合:c(Na+)>c(HC2O )>c(C2O )>c(C2O )>c(H2C2O4) )>c(H2C2O4) |
| D.0.1mol·L-1CH3COONa和0.1mol·L-1HCl溶液混合:c(Na+)+c(CH3COO-)=c(Cl-)+c(H+) |
您最近一年使用:0次

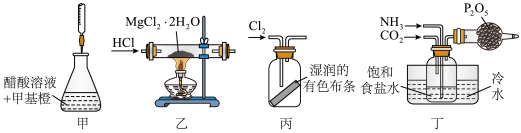
 溶液滴定未知浓度的醋酸
溶液滴定未知浓度的醋酸

