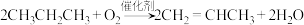一定条件下, 水溶液在密封石英管中的分解反应如下:
水溶液在密封石英管中的分解反应如下:
I.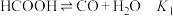
II.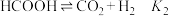
已知: 仅对反应I有催化作用。一定温度下,在密封石英管内完全充满
仅对反应I有催化作用。一定温度下,在密封石英管内完全充满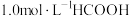 水溶液,使
水溶液,使 分解,分解产物均完全溶于水。(忽略水的电离,其浓度视为常数)
分解,分解产物均完全溶于水。(忽略水的电离,其浓度视为常数)
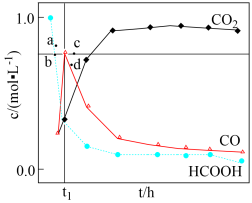
含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列说法正确的是
 水溶液在密封石英管中的分解反应如下:
水溶液在密封石英管中的分解反应如下:I.
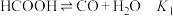
II.
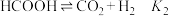
已知:
 仅对反应I有催化作用。一定温度下,在密封石英管内完全充满
仅对反应I有催化作用。一定温度下,在密封石英管内完全充满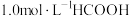 水溶液,使
水溶液,使 分解,分解产物均完全溶于水。(忽略水的电离,其浓度视为常数)
分解,分解产物均完全溶于水。(忽略水的电离,其浓度视为常数)含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列说法正确的是

| A.反应的活化能:反应I>反应II |
B.反应达平衡后,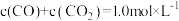 |
C.反应的平衡常数: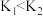 |
D.若起始时向体系中加入盐酸,则 新的浓度峰值点可能是b点 新的浓度峰值点可能是b点 |
更新时间:2024/03/04 10:00:09
|
相似题推荐
单选题
|
较难
(0.4)
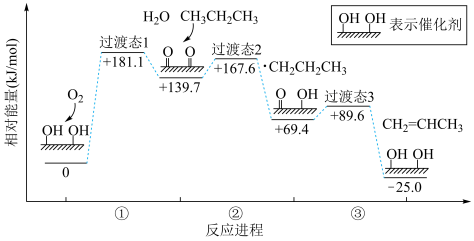
【推荐1】标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知 和
和 的相对能量为0],下列说法
的相对能量为0],下列说法不正确 的是
 和
和 的相对能量为0],下列说法
的相对能量为0],下列说法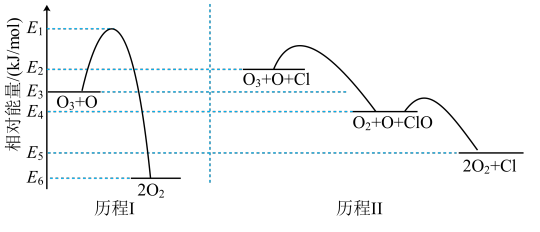
A. |
B.可计算 键能为 键能为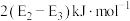 |
C.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ 的平衡转化率:历程Ⅱ>历程Ⅰ |
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为: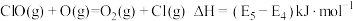 |
您最近一年使用:0次
单选题-单题
|
较难
(0.4)
名校
解题方法
【推荐2】 的转化一直是世界范围内的研究热点。利用两种金属催化剂,在水溶液体系中将
的转化一直是世界范围内的研究热点。利用两种金属催化剂,在水溶液体系中将 分别转化为
分别转化为 和
和 的反应过程示意图如下。下列说法正确的是
的反应过程示意图如下。下列说法正确的是
 的转化一直是世界范围内的研究热点。利用两种金属催化剂,在水溶液体系中将
的转化一直是世界范围内的研究热点。利用两种金属催化剂,在水溶液体系中将 分别转化为
分别转化为 和
和 的反应过程示意图如下。下列说法正确的是
的反应过程示意图如下。下列说法正确的是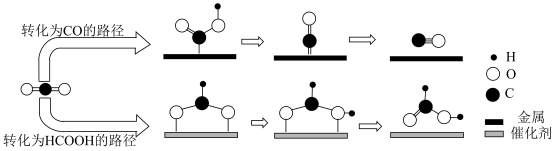
A.在转化为 的路径中,只涉及碳氧键的断裂和氧氢键的形成 的路径中,只涉及碳氧键的断裂和氧氢键的形成 |
B.在转化为两种产物的路径中, 都是作还原剂而被氧化 都是作还原剂而被氧化 |
C.在转化为 的过程中碳、氧原子的利用率为100% 的过程中碳、氧原子的利用率为100% |
| D.两个转化路径中所有元素的化合价都发生了变化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】利用 和
和 反应生成
反应生成 的过程中主要涉及的反应如下:
的过程中主要涉及的反应如下:
反应Ⅰ
反应Ⅱ
向密闭容器中充入一定量 和
和 发生上述反应,保持温度和容器体积一定,平衡时
发生上述反应,保持温度和容器体积一定,平衡时 和
和 的转化率、
的转化率、 和
和 的产率及随起始
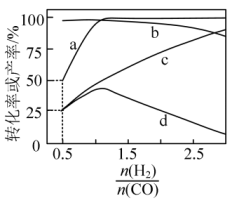
的产率及随起始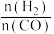 的变化情况如下图所示。
的变化情况如下图所示。
[ 的产率
的产率 的选择性
的选择性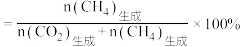 ]。
]。
下列说法不正确 的是
 和
和 反应生成
反应生成 的过程中主要涉及的反应如下:
的过程中主要涉及的反应如下:反应Ⅰ

反应Ⅱ

向密闭容器中充入一定量
 和
和 发生上述反应,保持温度和容器体积一定,平衡时
发生上述反应,保持温度和容器体积一定,平衡时 和
和 的转化率、
的转化率、 和
和 的产率及随起始
的产率及随起始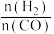 的变化情况如下图所示。
的变化情况如下图所示。[
 的产率
的产率 的选择性
的选择性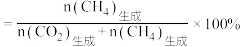 ]。
]。下列说法
| A.当容器内气体总压强保持不变时,反应Ⅰ、Ⅱ均达到平衡状态 |
B.曲线 表示 表示 的产率随 的产率随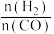 的变化 的变化 |
C.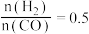 ,反应达平衡时, ,反应达平衡时, 的选择性为 的选择性为 |
D.随着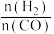 增大, 增大, 的选择性先增大后减小 的选择性先增大后减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】使用合适的催化剂进行乙酸直接加氢可制备乙醇,反应原理如下:
主反应:

副反应:
 (热效应小可忽略)
(热效应小可忽略)
在密闭容器中控制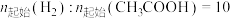 。
。 下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为
下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为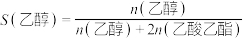 。下列说法正确的是
。下列说法正确的是
主反应:


副反应:

 (热效应小可忽略)
(热效应小可忽略)在密闭容器中控制
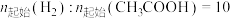 。
。 下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为
下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为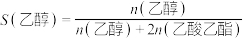 。下列说法正确的是
。下列说法正确的是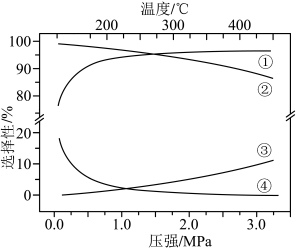
A.反应  |
| B.曲线②变化的原因是随温度升高,副反应正向进行的程度减小 |
| C.图中曲线③表示250℃,乙醇选择性随压强变化的曲线 |
D.300℃、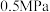 下,反应足够长时间,S(乙醇) 下,反应足够长时间,S(乙醇)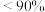 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体,一定条件下发生反应,各物质浓度随时间变化如甲图所示(t0~t1阶段的c(B)变化未画出),乙图为t时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件(浓度、温度、压强、催化剂)且互不相同,t3~t4阶段为使用催化剂。下列说法中不正确的是
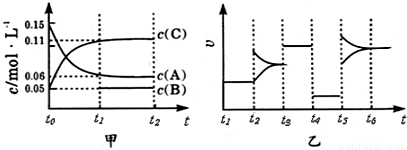

| A.若t1=15 s,则用C的浓度变化表示的t0~t1段的平均反应速率为0.004mol•L-1•s-1 |
| B.t4~t5阶段改变的条件一定为减小压强 |
| C.该容器的容积为2 L,B的起始物质的量为0.02 mol |
D.该化学反应方程式为3A(g) B(g)+2C(g) B(g)+2C(g) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】向温度为300℃的2 L密闭容器中充入2 mol SO2和1 mol O2,发生反应2SO2 (g)+ O2 (g)  2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
 2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是| A.该温度下,反应的平衡常数K =1620 |
| B.SO2和O2的平衡转化率相等 |
| C.平衡后保持温度和容器体积不变,再充入SO3(g),平衡常数不变 |
| D.若不再向容器中加入任何物质,仅改变条件不可能使SO2的浓度达到1 mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:
①v1<v2 ②v1<v3 ③c2<2c1 ④c2>2c3 ⑤p2>2p3 ⑥p2<2p1 ⑦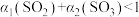 ⑧
⑧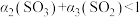 ⑨
⑨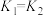 ⑩
⑩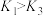
以上说法正确的有
 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2mol 、1mol 、1mol | 4mol | 2mol 、1mol 、1mol |
平衡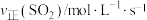 | v1 | v2 | v3 |
平衡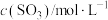 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的平衡转化率 | 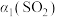 | 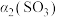 | 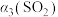 |
| 平衡常数K | 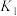 | 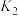 |  |
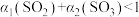 ⑧
⑧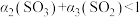 ⑨
⑨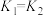 ⑩
⑩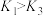
以上说法正确的有
| A.6 | B.7 | C.8 | D.9 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知碳酸钙的分解为可逆反应,一定温度下,在容积为2L的恒容密闭容器甲中盛有10.0g纯净碳酸钙固体,反应达到平衡后,剩余固体8.9g;相同温度下,另有一真空密闭容器乙(活塞的质量与摩擦均不计,侧面足够长)中同样盛有10.0g纯净碳酸钙固体,在恒压下反应达到平衡后体积恰好为1L(不考虑固体体积)。下列说法正确的是
| A.平衡后再向乙容器中充入0.02molCO2气体,至容器体积不再变化时,c(CO2)=0.0125mol/L |
| B.平衡后再向乙容器中充入0.02molAr,至容器体积不再变化时,c(CO2)=0.0125mol/L |
| C.达到平衡后,容器乙中剩余固体质量小于容器甲中剩余固体质量 |
| D.甲、乙两容器的情况下,反应的平衡常数K都为0.025mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】实验室测定反应 的平衡常数K的过程为:
的平衡常数K的过程为:
①一定温度下,将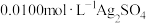 溶液与
溶液与 溶液
溶液 等体积混合,产生灰黑色沉淀;
等体积混合,产生灰黑色沉淀;
②待步骤①中反应达到平衡时,取v mL上层清液,用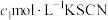 标准溶液滴定
标准溶液滴定 ,至出现稳定的浅红色时消耗KSCN标准溶液
,至出现稳定的浅红色时消耗KSCN标准溶液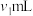 。
。
资料: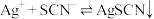 (白色)
(白色) 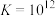 ,
,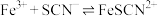 (红色)
(红色) 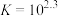
下列说法正确的是
 的平衡常数K的过程为:
的平衡常数K的过程为:①一定温度下,将
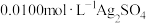 溶液与
溶液与 溶液
溶液 等体积混合,产生灰黑色沉淀;
等体积混合,产生灰黑色沉淀;②待步骤①中反应达到平衡时,取v mL上层清液,用
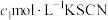 标准溶液滴定
标准溶液滴定 ,至出现稳定的浅红色时消耗KSCN标准溶液
,至出现稳定的浅红色时消耗KSCN标准溶液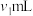 。
。资料:
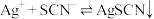 (白色)
(白色) 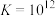 ,
,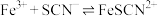 (红色)
(红色) 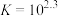
下列说法正确的是
A. 溶液可替换为 溶液可替换为 溶液 溶液 |
| B.过程①中产生的灰黑色沉淀为Fe或Ag元素的氧化物 |
C.可用KCl标准溶液代替KSCN的标准溶液滴定 |
D.步骤②中不待溶液澄清,直接用浊液做滴定实验测定 ,则所测K值偏小 ,则所测K值偏小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定温度下,在三个容积均为1 L的恒容密闭容器中按不同方式投入反应物,发生反应:2SO2(g) + O2(g) 2SO3(g) ΔH<0,测得反应的相关数据如下:
2SO3(g) ΔH<0,测得反应的相关数据如下:
下列说法错误的是
 2SO3(g) ΔH<0,测得反应的相关数据如下:
2SO3(g) ΔH<0,测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | T1 | T1 | T2(T2>T1) |
| 反应物投入量 | 2 mol SO2、1 mol O2 | 4 mol SO3 | 2 mol SO2、1 mol O2 |
| 平衡c(SO3)/mol·L-1 | 1 mol·L-1 | c2 | c3 |
| 物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(SO2) |
| A.c2 > 2 mol·L-1 |
| B.α2(SO3) + α3(SO2) =1 |
C.T1时,若SO2、O2、SO3的浓度分别为1.2 mol·L-1、0.6 mol·L-1、1.2 mol·L-1,则此时 (正)> (正)> (逆) (逆) |
| D.若在恒压条件下,c2 = 1 mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】某温度下,在甲、乙、丙、丁四个恒容密闭容器中投入H2和I2,发生反应H2(g) + I2(g) 2HI(g),反应体系中各物质浓度的有关数据如下。
2HI(g),反应体系中各物质浓度的有关数据如下。
下列判断正确的是
 2HI(g),反应体系中各物质浓度的有关数据如下。
2HI(g),反应体系中各物质浓度的有关数据如下。| 容器 | 起始浓度 | 平衡浓度 | |
| c(H2)/mol·L-1 | c(I2)/mol·L-1 | c(HI)/mol·L-1 | |
| 甲 | 0.01 | 0.01 | 0.004 |
| 乙 | 0.01 | 0.02 | a |
| 丙 | 0.02 | 0.01 | b |
| 丁 | 0.02 | 0.02 | ___________ |
| A.HI的平衡浓度:a=b>0.004 |
| B.平衡时,H2的转化率: 丙> 甲 |
| C.平衡时,乙中I2的转化率等于10% |
D.丙中条件下,该反应的平衡常数K > |
您最近一年使用:0次