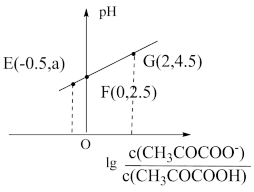
在 下用KOH溶液分别滴定HA、
下用KOH溶液分别滴定HA、 、
、 三种溶液,pM[
三种溶液,pM[ ,M表示
,M表示 、
、 、
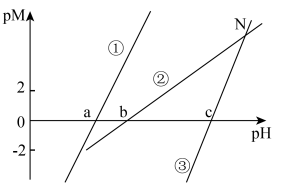
、 ]随pH变化有①②③三条曲线,已知图像中
]随pH变化有①②③三条曲线,已知图像中 ,
,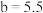 ,
, ,且
,且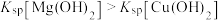 ,下列说法错误的是
,下列说法错误的是
 下用KOH溶液分别滴定HA、
下用KOH溶液分别滴定HA、 、
、 三种溶液,pM[
三种溶液,pM[ ,M表示
,M表示 、
、 、
、 ]随pH变化有①②③三条曲线,已知图像中
]随pH变化有①②③三条曲线,已知图像中 ,
,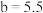 ,
, ,且
,且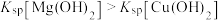 ,下列说法错误的是
,下列说法错误的是
A.HA的电离常数 |
B.当 刚好完全沉淀时,溶液 刚好完全沉淀时,溶液 |
C.在 下 下 易溶于HA溶液中 易溶于HA溶液中 |
D.②③两条曲线交点N的横坐标 |
更新时间:2024-03-08 09:39:59
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】下列事实中,不能比较次氯酸与醋酸的酸性强弱的是
| A.0.10 mol·L-1的次氯酸和醋酸的pH分别为4.8和3.1 |
| B.次氯酸的导电能力低于相同浓度的醋酸 |
| C.醋酸的稳定性强于次氯酸 |
| D.次氯酸不能与碳酸氢钠溶液反应,而醋酸可以 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】25℃时,某二元碱 水溶液中相关组分的物质的量分数
水溶液中相关组分的物质的量分数 随溶液
随溶液 变化的曲线如图所示,下列说法错误的是
变化的曲线如图所示,下列说法错误的是
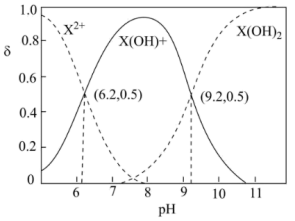
 水溶液中相关组分的物质的量分数
水溶液中相关组分的物质的量分数 随溶液
随溶液 变化的曲线如图所示,下列说法错误的是
变化的曲线如图所示,下列说法错误的是
A.由图可得 一级、二级电离平衡常数 一级、二级电离平衡常数 |
B.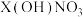 水溶液显酸性 水溶液显酸性 |
C.等物质的量的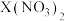 和 和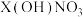 混合溶液中, 混合溶液中,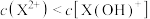 |
D.在 的水溶液中, 的水溶液中,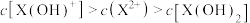 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,保持某含少量 浊液的水体中
浊液的水体中 与空气中
与空气中 的平衡,调节水体pH,水体中
的平衡,调节水体pH,水体中 与pH的关系如图所示(其中X为
与pH的关系如图所示(其中X为 、
、 、
、 或
或 )。下列说法错误的是
)。下列说法错误的是

 浊液的水体中
浊液的水体中 与空气中
与空气中 的平衡,调节水体pH,水体中
的平衡,调节水体pH,水体中 与pH的关系如图所示(其中X为
与pH的关系如图所示(其中X为 、
、 、
、 或
或 )。下列说法错误的是
)。下列说法错误的是
A.曲线Ⅱ表示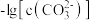 与pH的关系 与pH的关系 |
B.该温度下, 的电离常数 的电离常数 的数量级为 的数量级为 |
C.向水体中加入适量 固体,可使溶液由b点变到c点 固体,可使溶液由b点变到c点 |
D.a点的水体中: |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】以 固体为原料制备纯
固体为原料制备纯 ,其部分实验过程如下:
,其部分实验过程如下:

已知:① ;
;
② ,
, 有两性,
有两性, ;
;
③ 。
。
下列说法错误的是
 固体为原料制备纯
固体为原料制备纯 ,其部分实验过程如下:
,其部分实验过程如下:
已知:①
 ;
;②
 ,
, 有两性,
有两性, ;
;③
 。
。下列说法错误的是
| A.“酸溶”后再“氧化”可提高氧化速率 |
B.“氧化”过程中可能有 生成 生成 |
C. 既能溶于NaOH溶液又能溶于氨水 既能溶于NaOH溶液又能溶于氨水 |
D.“氧化”不充分,“沉钯”时所得 的产率无影响 的产率无影响 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,分别向体积均为10mL、浓度均为0.1mol/L的FeCl2和MnCl2溶液中滴加0.1mol/L的K2S溶液,滴加过程中溶液-1gc(Fe2+)和-1gc(Mn2+)与滴入K2S溶液体积(V)的关系如图所示。[已知:Ksp(MnS)>Ksp(FeS),lg3≈0.5,忽略溶液混合时温度和体积的变化],下列说法正确的是
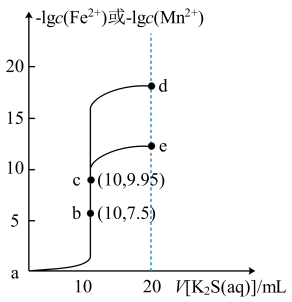

| A.a-b-e为MnCl2溶液的滴定曲线 |
| B.加入过量难溶的FeS可除去FeCl2溶液中混有的Mn2+ |
| C.e点纵坐标约为12.5 |
| D.溶液的pH:c>d>a |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】一定温度下,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),形成沉淀所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示。下列说法不正确的是
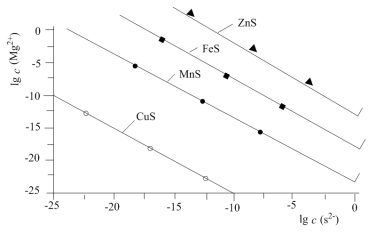

| A.若向沉淀剂Na2S溶液通入HCl气体至中性,存在关系: c(HS-)+2c(H2S)=c(Cl-) |
| B.该温度下,Ksp(MnS)大于1.0×10-35 |
| C.若将MnS、FeS的饱和溶液等体积混合,再加入足量的浓 Na2S溶液,发生的反应为MnS沉淀少于FeS |
| D.向l00mL浓度均为10-5mol·L-1Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol·L-1Na2S溶液,ZnS先沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】利用平衡移动原理,分析一定温度下 在不同pH的
在不同pH的 (起始浓度为
(起始浓度为 )体系中的可能产物。
)体系中的可能产物。
已知:
ⅰ.图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。
ⅱ.图2表示不同pH下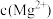 的变化。
的变化。
 在不同pH的
在不同pH的 (起始浓度为
(起始浓度为 )体系中的可能产物。
)体系中的可能产物。已知:
ⅰ.图1中曲线表示
 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。ⅱ.图2表示不同pH下
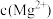 的变化。
的变化。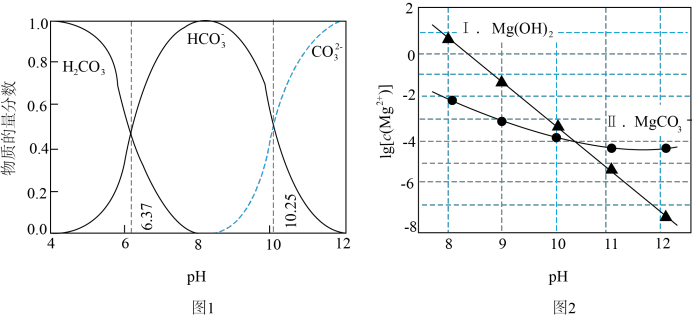
A.由图1,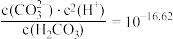 |
B.在 时,一定存在 时,一定存在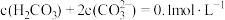 |
C.由图2,初始状态 、 、 ,无沉淀生成 ,无沉淀生成 |
D.由图1和图2,初始状态 、 、 ,主要发生反应: ,主要发生反应: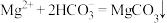  |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
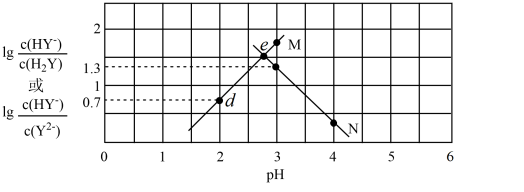
【推荐2】常温下,向二元弱酸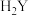 溶液中滴加
溶液中滴加 溶液,所得混合溶液的
溶液,所得混合溶液的 与离子浓度变化的关系如图所示。下列有关说法正确的是
与离子浓度变化的关系如图所示。下列有关说法正确的是
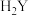 溶液中滴加
溶液中滴加 溶液,所得混合溶液的
溶液,所得混合溶液的 与离子浓度变化的关系如图所示。下列有关说法正确的是
与离子浓度变化的关系如图所示。下列有关说法正确的是
A.曲线 表示 表示 与 与 的变化关系 的变化关系 |
B. 的数量级为 的数量级为 |
C. 点溶液中: 点溶液中: |
D.交点 的溶液中: 的溶液中: |
您最近一年使用:0次

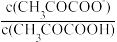 与pH的关系曲线如图所示。下列说法错误的是
与pH的关系曲线如图所示。下列说法错误的是