随着科学的发展,氟及其化合物的用途日益广泛。
Ⅰ.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如下图。
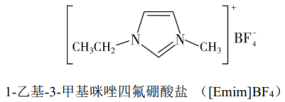
(1)基态N原子的价层电子轨道表示式为_______ 。
(2)①N、F、P三种元素的电负性由大到小的顺序为_______ 。
②根据VSEPR模型, 的中心原子上的价层电子对数为
的中心原子上的价层电子对数为_______ ,空间结构为_______ 形。
(3) 是制备此离子液体的原料。
是制备此离子液体的原料。
①微粒中F—B—F键角:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
② 可以与NaF反应生成
可以与NaF反应生成 的原因是
的原因是_______ 。
(4)以 和
和 的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为
的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为_______ ,电解质溶液中 向
向_______ (填“阴”或“阳”)极移动。
Ⅱ.NaF等氟化物可以做光导纤维材料,一定条件下,某NaF的晶胞结构示意图如下图所示,晶胞的边长为apm 。
。

(5)与 距离最近且相等的
距离最近且相等的 有
有_______ 个。
(6)已知NaF的摩尔质量是Mg/mol,阿伏伽德罗常数为 。该晶体的密度为
。该晶体的密度为_______  。
。
Ⅰ.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如下图。

(1)基态N原子的价层电子轨道表示式为
(2)①N、F、P三种元素的电负性由大到小的顺序为
②根据VSEPR模型,
 的中心原子上的价层电子对数为
的中心原子上的价层电子对数为(3)
 是制备此离子液体的原料。
是制备此离子液体的原料。①微粒中F—B—F键角:

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②
 可以与NaF反应生成
可以与NaF反应生成 的原因是
的原因是(4)以
 和
和 的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为
的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为 向
向Ⅱ.NaF等氟化物可以做光导纤维材料,一定条件下,某NaF的晶胞结构示意图如下图所示,晶胞的边长为apm
 。
。
(5)与
 距离最近且相等的
距离最近且相等的 有
有(6)已知NaF的摩尔质量是Mg/mol,阿伏伽德罗常数为
 。该晶体的密度为
。该晶体的密度为 。
。
更新时间:2024-02-28 20:27:18
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:
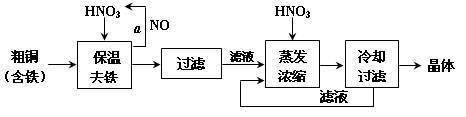
(1)在步骤a中,还需要通入氧气和水,发生反应的化学方程式是_____________ 。
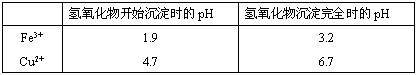
(2)在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在______________ 范围。若调节溶液的pH=4,此时,溶液中c (Fe3+) =________ 。[已知该条件下,Fe(OH)3的KSP= 4.0×10-36 ]
(3)不用加水的方法调节溶液pH的原因是_______________ 。
(4)进行蒸发浓缩时,要加适量的硝酸以保持溶液一定的c(H+),其目的是(结合离子方程式简要说明)_________________________ 。
(5)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是_____________ 。

(1)在步骤a中,还需要通入氧气和水,发生反应的化学方程式是
(2)在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在

(3)不用加水的方法调节溶液pH的原因是
(4)进行蒸发浓缩时,要加适量的硝酸以保持溶液一定的c(H+),其目的是(结合离子方程式简要说明)
(5)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分为ZnO,还含有Fe2O3、CuO、SiO2等杂成) 制备ZnSO4·7H2O的流程如下。

相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)如下表:
(1)“滤渣1”的主要成分为_________ (填化学式)。“酸浸”过程中,提高锌元素浸出率的措施有:适当提高酸的浓度、______________ (填一种)。
(2)“置换”过程中,加入适量的锌粉,除与溶液中的Fe3+,H+反应外,另一主要反应的化学方程式为__________________________ 。
(3)“氧化”一步中,发生氧化还原反应的离子方程式为_______________________ 。溶液pH控制在[3.2,6.4)之间的目的是_______________________________ 。
(4)“母液”中含有的盐类物质有_________ (填化学式)。
(5)ZnSO4·7H2O可用于配制铁件上镀锌电镀池的电解液,下列说法不正确的是_______
A.配制一定物质的量浓度ZnSO4溶液时必需的玻璃仪器为容量瓶、烧杯、玻璃棒
B.电镀池的阳极为铁件
C.阴极质量增加65g时,理论上导线中通过2mol电子
D.电镀过程中电解质溶液的浓度不变

相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)如下表:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 6.4 | 8.0 |
(2)“置换”过程中,加入适量的锌粉,除与溶液中的Fe3+,H+反应外,另一主要反应的化学方程式为
(3)“氧化”一步中,发生氧化还原反应的离子方程式为
(4)“母液”中含有的盐类物质有
(5)ZnSO4·7H2O可用于配制铁件上镀锌电镀池的电解液,下列说法不正确的是
A.配制一定物质的量浓度ZnSO4溶液时必需的玻璃仪器为容量瓶、烧杯、玻璃棒
B.电镀池的阳极为铁件
C.阴极质量增加65g时,理论上导线中通过2mol电子
D.电镀过程中电解质溶液的浓度不变
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】CuSO4溶液是一种较重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(1)下图是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池:

该原电池的正极为___________ (填“Zn”或“Cu”),电解质溶液甲是___________ (填“ZnSO4”或“CuSO4”)溶液;若盐桥中的成分是KNO3溶液,则盐桥中K+向___________ (填“甲”或“乙”)烧杯中移动。
(2)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是___________ (填字母)。
a.溶液中Cu2+向阳极移动 b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小 d.利用阳极泥可回收Ag、Pt、Au等金属
(3)利用反应2Cu+O2+2H2SO4=2CuSO4 + 2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应为___________ 。
(4)下图中,Ⅰ 是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。

①该同学想在Ⅱ中实现铁上镀铜,b处通入的是___________ (填“CH4”或“O2”),a处电极上发生的电极反应式是___________ 。
②Ⅱ中电解前CuSO4溶液的浓度为2mol/L,当线路中有0.2 mol电子通过时,则此时电解液CuSO4溶液的浓度为___________ ,阴极增重___________ g。
(1)下图是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池:

该原电池的正极为
(2)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.溶液中Cu2+向阳极移动 b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小 d.利用阳极泥可回收Ag、Pt、Au等金属
(3)利用反应2Cu+O2+2H2SO4=2CuSO4 + 2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应为
(4)下图中,Ⅰ 是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。

①该同学想在Ⅱ中实现铁上镀铜,b处通入的是
②Ⅱ中电解前CuSO4溶液的浓度为2mol/L,当线路中有0.2 mol电子通过时,则此时电解液CuSO4溶液的浓度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】I.新型储氢材料是开发利用氢能的重要研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
(1)基态Cl原子有_______ 种运动状态的电子,属于_______ 区(填“s”或“p”或“d”或“f”);
(2)LiBH4由Li+和 构成,
构成, 的立体结构是
的立体结构是_______ ,与 互为等电子体的分子为
互为等电子体的分子为_______ ,Li、Be、B元素的第一电离能由大到小排列顺序为_______ ;
(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_______ (填元素符号)。
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为:N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和 。试回答下列问题:
。试回答下列问题:
(4)下列有关说法正确的是_______(填序号);
(5)叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,在该配合物中钴显_______ 价;根据价层电子对互斥理论判断 的空间构型为
的空间构型为_______ ;
(6)与 互为等电子体的分子有
互为等电子体的分子有_______ (写两种即可)。
(1)基态Cl原子有
(2)LiBH4由Li+和
 构成,
构成, 的立体结构是
的立体结构是 互为等电子体的分子为
互为等电子体的分子为(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为:N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和
 。试回答下列问题:
。试回答下列问题:(4)下列有关说法正确的是_______(填序号);
| A.HN3中含有5个σ键 |
| B.HN3中的三个氮原子均采用sp2杂化 |
| C.HN3、HNO2、H2O、N2H4都是极性分子 |
| D.N2H4沸点高达113.5℃,说明肼分子间可形成氢键 |
 的空间构型为
的空间构型为(6)与
 互为等电子体的分子有
互为等电子体的分子有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】焦亚硫酸钠( )在医药、橡胶、印染、食品等方面应用广泛。利用烟道气中的
)在医药、橡胶、印染、食品等方面应用广泛。利用烟道气中的 生产
生产 的工艺流程如图所示。
的工艺流程如图所示。

回答下列问题:
(1) 的VSEPR模型名称是
的VSEPR模型名称是______ , 的中心原子的杂化方式为
的中心原子的杂化方式为____________ 。
(2)发生反应Ⅰ后的溶液中的溶质仅含 (此时溶液的
(此时溶液的 ),Ⅰ中发生反应的离子方程式为
),Ⅰ中发生反应的离子方程式为____________ 。
(3)在反应Ⅰ中:
① 的俗名为
的俗名为______ ,其用途有____________ (填一种即可)。
② 、
、 、
、 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为____________ 。
(4)在反应Ⅱ中,通入 的目的是得到
的目的是得到 过饱和溶液,“一系列操作”是
过饱和溶液,“一系列操作”是____________ 。
(5)写出Ⅳ 的第2)步反应的化学方程式:
的第2)步反应的化学方程式:____________ 。
(6) 可用作食品的抗氧化剂。在测定葡萄酒中
可用作食品的抗氧化剂。在测定葡萄酒中 的残留量时,取80.00 mL葡萄酒样品,往葡萄酒样品中滴入
的残留量时,取80.00 mL葡萄酒样品,往葡萄酒样品中滴入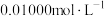 的碘标准液,反应完全后,共消耗12.00 mL碘标准液。则该样品中
的碘标准液,反应完全后,共消耗12.00 mL碘标准液。则该样品中 的残留量为
的残留量为____________  (以
(以 计)。
计)。
 )在医药、橡胶、印染、食品等方面应用广泛。利用烟道气中的
)在医药、橡胶、印染、食品等方面应用广泛。利用烟道气中的 生产
生产 的工艺流程如图所示。
的工艺流程如图所示。
回答下列问题:
(1)
 的VSEPR模型名称是
的VSEPR模型名称是 的中心原子的杂化方式为
的中心原子的杂化方式为(2)发生反应Ⅰ后的溶液中的溶质仅含
 (此时溶液的
(此时溶液的 ),Ⅰ中发生反应的离子方程式为
),Ⅰ中发生反应的离子方程式为(3)在反应Ⅰ中:
①
 的俗名为
的俗名为②
 、
、 、
、 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为(4)在反应Ⅱ中,通入
 的目的是得到
的目的是得到 过饱和溶液,“一系列操作”是
过饱和溶液,“一系列操作”是(5)写出Ⅳ
 的第2)步反应的化学方程式:
的第2)步反应的化学方程式:(6)
 可用作食品的抗氧化剂。在测定葡萄酒中
可用作食品的抗氧化剂。在测定葡萄酒中 的残留量时,取80.00 mL葡萄酒样品,往葡萄酒样品中滴入
的残留量时,取80.00 mL葡萄酒样品,往葡萄酒样品中滴入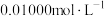 的碘标准液,反应完全后,共消耗12.00 mL碘标准液。则该样品中
的碘标准液,反应完全后,共消耗12.00 mL碘标准液。则该样品中 的残留量为
的残留量为 (以
(以 计)。
计)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】按要求完成下列问题:
(1)写出CCl4中心原子成键时采取的杂化轨道类型及分子中共价键的键角:___________ 、___________ 。
(2)气态 分子的空间构型为
分子的空间构型为___________ , 离子的空间构型为
离子的空间构型为___________ ;
(3)写出基态铁原子的简化电子排布式和Mg2+的核外电子排布式:___________ 、___________ 。
(4) 的沸点比
的沸点比 高的原因是
高的原因是___________ 。
(1)写出CCl4中心原子成键时采取的杂化轨道类型及分子中共价键的键角:
(2)气态
 分子的空间构型为
分子的空间构型为 离子的空间构型为
离子的空间构型为(3)写出基态铁原子的简化电子排布式和Mg2+的核外电子排布式:
(4)
 的沸点比
的沸点比 高的原因是
高的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶胞结构如图所示。

(1)该晶体中Xn+中n=_______ 。
(2)元素X的原子序数是_______ 。
(3)X的价层电子排布式为:_______
(4)晶体中每个N3-被_______ 个等距离的Xn+包围。
(5)该化合物的相对分子质量为M,NA为阿伏加德罗常数。若该晶胞的边长为apm,则该晶体的密度是_______ g·cm-3。(1pm=10-12m)

(1)该晶体中Xn+中n=
(2)元素X的原子序数是
(3)X的价层电子排布式为:
(4)晶体中每个N3-被
(5)该化合物的相对分子质量为M,NA为阿伏加德罗常数。若该晶胞的边长为apm,则该晶体的密度是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】深井岩盐的主要配料为:精制盐、碘酸钾(KIO3)、亚铁氰化钾[K4Fe(CN)6·3H2O]。其中亚铁氰化钾的无水盐在高温下会发生分解:3K4[Fe(CN)6] 2(CN)2↑+12KCN+N2↑+Fe3C+C。请回答下列问题:
2(CN)2↑+12KCN+N2↑+Fe3C+C。请回答下列问题:
(1)①基态Fe原子价电子排布图(轨道表示式)为_________________________
②C、N和O三种元素的第一电离能的大小顺序为_____________ ,原因是__________ 。
③IO3-的中心原子的杂化方式为______ 。一种与CN-互为等电子体的分子的电子式为_______ 。
④1molFe(CN)63−中含有σ键的数目为____ mol。
(2)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___ 。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于__________ (填晶体类型)。
(3)如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体,该立方体中三价铁离子处于氧离子围成的________ (填空间结构)空隙。
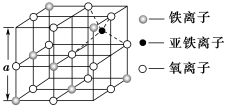
(4)Fe能形成多种氧化物,其中FeO晶胞结构为NaCl型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1),若测得某FexO晶体密度为5.71g•cm﹣3,晶胞边长为4.28×10﹣10 m,则FexO中x=____ 。(用代数式表示,不要求算出具体结果)。
 2(CN)2↑+12KCN+N2↑+Fe3C+C。请回答下列问题:
2(CN)2↑+12KCN+N2↑+Fe3C+C。请回答下列问题:(1)①基态Fe原子价电子排布图(轨道表示式)为
②C、N和O三种元素的第一电离能的大小顺序为
③IO3-的中心原子的杂化方式为
④1molFe(CN)63−中含有σ键的数目为
(2)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(3)如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体,该立方体中三价铁离子处于氧离子围成的

(4)Fe能形成多种氧化物,其中FeO晶胞结构为NaCl型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1),若测得某FexO晶体密度为5.71g•cm﹣3,晶胞边长为4.28×10﹣10 m,则FexO中x=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硼和氮的单质及一些化合物在工农业生产等领域有重要应用。回答下列问题:
(1)N原子核外有__________ 种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的电子排布式为:__________
(2)经测定发现N2O5固体由NO2+和NO3-两种离子组成,该固体中N 原子杂化类型分别为__________ ;与NO2+互为等电子体的微粒有_______________ (写出一种)。
(3)铵盐大多不稳定。NH4F、NH4I中,较易分解的是___________ ,原因是_____________________
(4)第二周期中,第一电离能介于B元素和N元素间的元素有__________ 种。
(5)氮化镓是第三代半导体材料,其晶体结构和单晶硅相似,晶胞结构如图所示:

①原子坐标参数是表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0 );B为(1/2,1/2,0) ;C为(1,0,1)。则D原子的坐标参数为____________________ 。
②已知氮化镓晶胞的边长为anm,其密度为dg/cm3。则阿伏伽德罗常数NA=__________ ( 用a、d表示)
(1)N原子核外有
(2)经测定发现N2O5固体由NO2+和NO3-两种离子组成,该固体中N 原子杂化类型分别为
(3)铵盐大多不稳定。NH4F、NH4I中,较易分解的是
(4)第二周期中,第一电离能介于B元素和N元素间的元素有
(5)氮化镓是第三代半导体材料,其晶体结构和单晶硅相似,晶胞结构如图所示:

①原子坐标参数是表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0 );B为(1/2,1/2,0) ;C为(1,0,1)。则D原子的坐标参数为
②已知氮化镓晶胞的边长为anm,其密度为dg/cm3。则阿伏伽德罗常数NA=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有七种元素,其中 、
、 、
、 、
、 、
、 为短周期主族元素,
为短周期主族元素, 、
、 为第四周期元素,它们的原子序数依次增大。
为第四周期元素,它们的原子序数依次增大。 元素原子核外电子数和电子层数相同;
元素原子核外电子数和电子层数相同; 的价电子层中未成对电子有
的价电子层中未成对电子有 个;
个; 元素为最活泼非金属元素;
元素为最活泼非金属元素; 的最高价氧化物对应的水化物既能与酸又能与强碱反应;
的最高价氧化物对应的水化物既能与酸又能与强碱反应; 元素正三价离子的
元素正三价离子的 轨道上填充了
轨道上填充了 个电子;
个电子; 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层只有
层只有 个电子。
个电子。
(1) 元素在元素周期表中的位置是
元素在元素周期表中的位置是___________ , 元素基态原子中填有电子的能量最高的能级符号是
元素基态原子中填有电子的能量最高的能级符号是___________ 。
(2) 元素基态原子的价电子排布式为
元素基态原子的价电子排布式为___________ , 为离子化合物,写出其阴离子的电子式
为离子化合物,写出其阴离子的电子式___________ (用化学符号表示)。
(3) 元素的第一电高能
元素的第一电高能___________  元素的第一电离能(填“
元素的第一电离能(填“ ”“
”“ ”或“
”或“ ”),
”), 、
、 、
、 三种元素的电负性由大到小的顺序是
三种元素的电负性由大到小的顺序是___________ (用化学符号表示), 、
、 、
、 元素形成的简单离子中半径最大的是
元素形成的简单离子中半径最大的是___________ (用化学符号表示)。
(4) 元素正三价离子比正二价离子稳定的原因是
元素正三价离子比正二价离子稳定的原因是___________ 。
(5)向盛有 的硫酸盐溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解并得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。蓝色沉淀溶解时发生反应的离子方程式是
的硫酸盐溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解并得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。蓝色沉淀溶解时发生反应的离子方程式是___________ ,深蓝色晶体中不存在的化学键有___________ (填字母序号)。
a.离子键 b.极性键 c.非极性键 d.配位键
 、
、 、
、 、
、 、
、 为短周期主族元素,
为短周期主族元素, 、
、 为第四周期元素,它们的原子序数依次增大。
为第四周期元素,它们的原子序数依次增大。 元素原子核外电子数和电子层数相同;
元素原子核外电子数和电子层数相同; 的价电子层中未成对电子有
的价电子层中未成对电子有 个;
个; 元素为最活泼非金属元素;
元素为最活泼非金属元素; 的最高价氧化物对应的水化物既能与酸又能与强碱反应;
的最高价氧化物对应的水化物既能与酸又能与强碱反应; 元素正三价离子的
元素正三价离子的 轨道上填充了
轨道上填充了 个电子;
个电子; 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层只有
层只有 个电子。
个电子。(1)
 元素在元素周期表中的位置是
元素在元素周期表中的位置是 元素基态原子中填有电子的能量最高的能级符号是
元素基态原子中填有电子的能量最高的能级符号是(2)
 元素基态原子的价电子排布式为
元素基态原子的价电子排布式为 为离子化合物,写出其阴离子的电子式
为离子化合物,写出其阴离子的电子式(3)
 元素的第一电高能
元素的第一电高能 元素的第一电离能(填“
元素的第一电离能(填“ ”“
”“ ”或“
”或“ ”),
”), 、
、 、
、 三种元素的电负性由大到小的顺序是
三种元素的电负性由大到小的顺序是 、
、 、
、 元素形成的简单离子中半径最大的是
元素形成的简单离子中半径最大的是(4)
 元素正三价离子比正二价离子稳定的原因是
元素正三价离子比正二价离子稳定的原因是(5)向盛有
 的硫酸盐溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解并得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。蓝色沉淀溶解时发生反应的离子方程式是
的硫酸盐溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解并得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。蓝色沉淀溶解时发生反应的离子方程式是a.离子键 b.极性键 c.非极性键 d.配位键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】元素及其化合物的应用研究是目前科学研究的前沿之一。试回答下列问题:
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出A 在基态时的外围电子排布式为______________ 。
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。水分子中心原子价层电子对数为_______ ,苯分子中碳原子的杂化类型为________ 。
(3)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+ 等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。该盐中铑离子的配位数为____ 。
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出A 在基态时的外围电子排布式为
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。水分子中心原子价层电子对数为
(3)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+ 等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。该盐中铑离子的配位数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】铁的硫化物被认为是有前景的锂电池材料,但导电性较差,放电时易膨胀。
(1)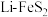 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。
①水热法合成 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为___________ 。
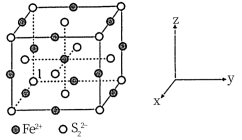
② 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为___________ (任写一个),每个 周围距离最近且相等的
周围距离最近且相等的 有
有___________ 个。
(2)①将 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且___________ 。多孔碳/ 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和___________ 。
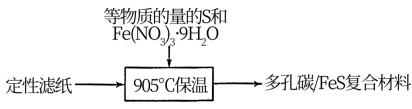
②分别取多孔碳、多孔碳/ 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。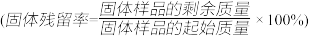
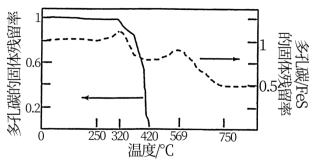
420℃~569℃时,多孔碳/ 固体残留率增大的原因是
固体残留率增大的原因是___________ 。
③ 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: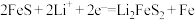
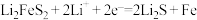
该多孔碳/ 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子___________  。(写出计算过程)
。(写出计算过程)
(1)
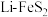 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。①水热法合成
 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为②
 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为 周围距离最近且相等的
周围距离最近且相等的 有
有
(2)①将
 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和
②分别取多孔碳、多孔碳/
 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。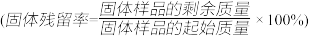

420℃~569℃时,多孔碳/
 固体残留率增大的原因是
固体残留率增大的原因是③
 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: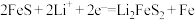
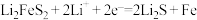
该多孔碳/
 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子 。(写出计算过程)
。(写出计算过程)
您最近一年使用:0次



