在体积不变的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)⇌Ni(CO)4(g),已知该反应的平衡常数与温度的关系如表所示;下列说法不正确的是
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A.上述生成Ni(CO4)(g)的反应为放热反应 |
| B.25℃时反应Ni(CO)4(g)⇌Ni(s)+4CO(g)的平衡常数为:2×10-5(mol·L-1)3 |
| C.80℃达到平衡时,测得c(CO)=0.3mol/L,则Ni(CO)4的平衡浓度为0.6mol/L-1 |
| D.在80℃时,测得某时刻,Ni(CO)4、CO的浓度均为0.5mol·L-1,则此时v(正)<v(逆) |
更新时间:2024-03-14 09:08:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于化学反应与能量的说法中,不正确 的是
| A.化学反应必然伴随发生能量变化 |
| B.Ba(OH)2·8H2O与NH4Cl的反应属于放热反应 |
| C.放热反应中反应物的总能量高于生成物的总能量 |
| D.化学变化中的能量变化主要是由化学键变化引起的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①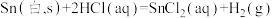

②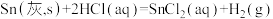

③
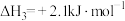
下列说法错误的是
①
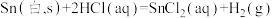

②
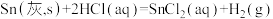

③

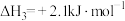
下列说法错误的是
A.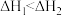 |
| B.锡在常温下以灰锡状态存在 |
| C.灰锡转化为白锡的反应是吸热反应 |
| D.锡制器皿长期处在低于13.2℃的环境中,会自行毁坏 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知:键能通常是指在101.3kPa、298K下,断开气态分子中1mol化学键变成气态原子时所吸收的能量;N≡N键的键能是946.2kJ·mol-1,N-H键的键能是391.1kJ·mol-1;合成氨反应为N2(g)+3H2(g) 2NH3,当生成2molNH3时体系放出92.4kJ能量。下列说法正确的是
2NH3,当生成2molNH3时体系放出92.4kJ能量。下列说法正确的是
 2NH3,当生成2molNH3时体系放出92.4kJ能量。下列说法正确的是
2NH3,当生成2molNH3时体系放出92.4kJ能量。下列说法正确的是| A.当3v(NH3)逆=2v(H2)正时,该反应达到化学平衡状态 |
| B.合成氨反应中,断开化学键放出的总能量大于形成化学键吸收的总能量 |
| C.H-H键的键能是416.0kJ·mol-1 |
| D.其它条件不变,升高反应温度,正反应速率加快,逆反应速率减慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在体积均为 的甲、乙两恒容密闭容器中加入足量相同的碳粉,再分别加入
的甲、乙两恒容密闭容器中加入足量相同的碳粉,再分别加入
 和
和
 ,发生反应
,发生反应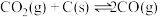 达到平衡。
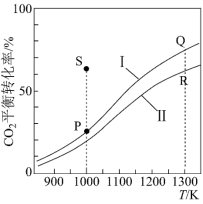
达到平衡。 的平衡转化率随温度的变化如图所示。下列说法正确的是
的平衡转化率随温度的变化如图所示。下列说法正确的是
 的甲、乙两恒容密闭容器中加入足量相同的碳粉,再分别加入
的甲、乙两恒容密闭容器中加入足量相同的碳粉,再分别加入
 和
和
 ,发生反应
,发生反应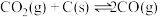 达到平衡。
达到平衡。 的平衡转化率随温度的变化如图所示。下列说法正确的是
的平衡转化率随温度的变化如图所示。下列说法正确的是 
A.反应 的 的 |
B.曲线II表示容器甲中 的平衡转化率 的平衡转化率 |
C.达平衡后,两容器中c(CO):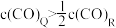 |
D.其他条件不变时,在曲线I对应容器中加入合适的催化剂,可使 的平衡转化率由P点达到S点I 的平衡转化率由P点达到S点I |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】CO2催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程主要发生下列反应:
反应①:CO2(g)+3H2(g)= CH3OH(g)+H2O(g); ΔH= - 49.5 kJ·mol-1
反应②:CO2(g)+H2(g)=CO(g)+H2O(g);ΔH=41.2 kJ·mol-1
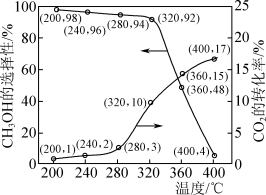
在0.5 MPa条件下,将n(CO2):n(H2)为1:3的混合气体以一定流速通过装有催化剂的反应器,实验测得CO2的转化率、CH3OH的选择性[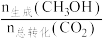 ×100%]与温度的关系如图所示。下列有关说法不正确的是
×100%]与温度的关系如图所示。下列有关说法不正确的是
反应①:CO2(g)+3H2(g)= CH3OH(g)+H2O(g); ΔH= - 49.5 kJ·mol-1
反应②:CO2(g)+H2(g)=CO(g)+H2O(g);ΔH=41.2 kJ·mol-1

在0.5 MPa条件下,将n(CO2):n(H2)为1:3的混合气体以一定流速通过装有催化剂的反应器,实验测得CO2的转化率、CH3OH的选择性[
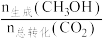 ×100%]与温度的关系如图所示。下列有关说法不正确的是
×100%]与温度的关系如图所示。下列有关说法不正确的是| A.反应②继续加氢生成甲醇的热化学方程式可表示为CO(g)+2H2(g)=CH3OH(g);ΔH=-90.7 kJ·mol -1 |
| B.其他条件不变,增大起始n(CO2):n(H2)的比值,可提高CO2的平衡转化率 |
| C.其他条件不变,在280~400°C间,产物中n(CH3OH)随温度的升高先增大后减小 |
| D.为高效生产CH3OH,需研发低温下CO2转化率高和CH3OH选择性高的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】K、Ka、Kw分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是
| A.25°C时,pH均为4的盐酸和NH4Cl溶液中Kw不相等 |
| B.在500°C时, 在5 L密闭容器中进行合成氨的反应,使用催化剂后K增大 |
C.2SO2+O2 2SO3达平衡后,改变某一条件时 K不变,SO2的转化率可能增大 2SO3达平衡后,改变某一条件时 K不变,SO2的转化率可能增大 |
| D.相同温度下Ka(HCN)< Ka(CH3COOH),说明CH3COOH的电离程度一定比HCN的大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,体积一定的密闭容器中进行反应:N2(g)+3H2(g)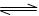 2NH3 (g) △H<0。下列分析正确的是
2NH3 (g) △H<0。下列分析正确的是
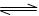 2NH3 (g) △H<0。下列分析正确的是
2NH3 (g) △H<0。下列分析正确的是 | A.平衡后加入N2,该反应的△H增大 |
| B.若平衡昏升高温度,则平衡常数K变大 |
| C.平衡后再充入NH3,达到新平衡时,NH3的百分含量变大 |
| D.若反应前充人的N2与H2物质的量相等,达平衡时N2的转化率比H2的高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】五氧化二氮(化学式: )又称硝酐,是硝酸的酸酐,在一定温度下可发生以下反应:
)又称硝酐,是硝酸的酸酐,在一定温度下可发生以下反应: 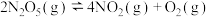
 。某温度下,向恒容密闭容器中充入
。某温度下,向恒容密闭容器中充入 ,发生上述反应,部分实验数据见下表:下列说法正确的是
,发生上述反应,部分实验数据见下表:下列说法正确的是
 )又称硝酐,是硝酸的酸酐,在一定温度下可发生以下反应:
)又称硝酐,是硝酸的酸酐,在一定温度下可发生以下反应: 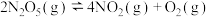
 。某温度下,向恒容密闭容器中充入
。某温度下,向恒容密闭容器中充入 ,发生上述反应,部分实验数据见下表:下列说法正确的是
,发生上述反应,部分实验数据见下表:下列说法正确的是| 时间/s | 0 | 500 | 1000 | 1500 |
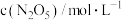 | 5.00 | 3.52 | 2.50 | 2.50 |
A.0~1000s内, |
| B.当气体密度不变时,反应达到平衡状态 |
C.该温度下反应的平衡常数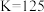 |
D.反应达到平衡后,保持其他条件不变,加入合适的催化剂, 变大 变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备,正丁烷(C4H10)催化脱氢制1-丁烯(C4H8) 的化学方程式如下:C4H10(g)=C4H8(g)+ H2(g) △H,如图是该反应平衡转化率与反应温度及压强的关系图,下列说法正确的是
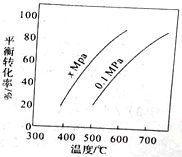

| A.x>0.1 |
| B.△H>O |
| C.500C时,压强xMPa比0.1MPa条件下的平衡常数大 |
| D.一定温度下,在一恒容密闭容器中发生该反应,C4H10的浓度越高,平衡转化率越大 |
您最近一年使用:0次

 和一定量的水蒸气,发生反应:
和一定量的水蒸气,发生反应:
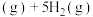 ,
, ],随温度的变化曲线如图所示。下列说法正确的是
],随温度的变化曲线如图所示。下列说法正确的是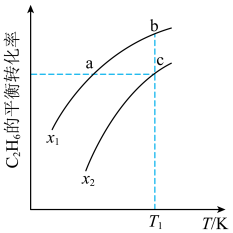
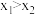

 ,当容器内气体的平均相对分子质量不再变化时,反应达到平衡状态
,当容器内气体的平均相对分子质量不再变化时,反应达到平衡状态 2HI(g),充分反应后达到平衡,测得c(H2)=0.008 mol•L-1,则该反应的平衡常数为( )
2HI(g),充分反应后达到平衡,测得c(H2)=0.008 mol•L-1,则该反应的平衡常数为( )

