铁和硒( )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
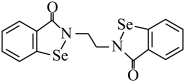
①该新药分子中有_____________ 种不同化学环境的C原子;
②比较键角大小:气态 分子
分子___________  离子(填“>”、“<”或“=”),原因是:
离子(填“>”、“<”或“=”),原因是:____________ 。
(2) 晶胞为立方体,边长为
晶胞为立方体,边长为 ,如图所示。
,如图所示。

①与 紧邻的阴离子个数为
紧邻的阴离子个数为___________ 。
②晶胞的密度为
___________  。
。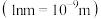
 )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①该新药分子中有
②比较键角大小:气态
 分子
分子 离子(填“>”、“<”或“=”),原因是:
离子(填“>”、“<”或“=”),原因是:(2)
 晶胞为立方体,边长为
晶胞为立方体,边长为 ,如图所示。
,如图所示。
①与
 紧邻的阴离子个数为
紧邻的阴离子个数为②晶胞的密度为

 。
。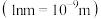
更新时间:2024-03-15 14:19:08
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】I.金属催化剂M(Co、Ni)催化硼氢化钠( )水解释放
)水解释放 机理如下图所示:
机理如下图所示:

(1)过程Ⅱ中形成化学键的类型有________(填序号)。
(2) 最终会转化为
最终会转化为 ,1个
,1个 中存在
中存在________ 个配位键。
(3) 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为________ 。
Ⅱ.过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为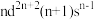 ,中子数为31,
,中子数为31,
(4)Q原子符号为________ ;基态Q原子核外成对电子数和未成对电子数之比为________ 。
Ⅲ. 、
、 是新型磁性材料的成分。依据其中有关元素回答问题:
是新型磁性材料的成分。依据其中有关元素回答问题:
(5)钕(Nd)属于镧系元素,则其在元素周期表中处于________ 区,Co元素在元素周期表中的位置________ 。
Ⅳ.分子式为 的化合物的结构如图,
的化合物的结构如图,
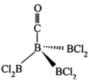
(6)其中B原子的杂化类型是________ ,B-B-B键的键角________ Cl-B-Cl的键角(填“ ”“
”“ ”或“
”或“ ”)。
”)。
 )水解释放
)水解释放 机理如下图所示:
机理如下图所示:
(1)过程Ⅱ中形成化学键的类型有________(填序号)。
| A.离子键 | B.金属键 | C.极性键 | D.非极性键 |
(2)
 最终会转化为
最终会转化为 ,1个
,1个 中存在
中存在(3)
 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为Ⅱ.过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为
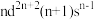 ,中子数为31,
,中子数为31,(4)Q原子符号为
Ⅲ.
 、
、 是新型磁性材料的成分。依据其中有关元素回答问题:
是新型磁性材料的成分。依据其中有关元素回答问题:(5)钕(Nd)属于镧系元素,则其在元素周期表中处于
Ⅳ.分子式为
 的化合物的结构如图,
的化合物的结构如图,
(6)其中B原子的杂化类型是
 ”“
”“ ”或“
”或“ ”)。
”)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E五种短周期元素。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上有3个未成对的电子;C元素在地壳中含量最高;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E的最外层电子数与其核外电子总数之比为3:8。
;E的最外层电子数与其核外电子总数之比为3:8。
(1)B的元素符号为_______ ,D元素在周期表中位置为_______ 。
(2)A、C形成的简单氢化物的键角顺序_______ (填化学式),并分析原因:_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)元素的非金属性C_______ (填“>”或“<”)E,并用化学原理证明(用化学方程式表示)_______ 。
 ;E的最外层电子数与其核外电子总数之比为3:8。
;E的最外层电子数与其核外电子总数之比为3:8。(1)B的元素符号为
(2)A、C形成的简单氢化物的键角顺序
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)元素的非金属性C
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氮及其化合物在生产、生活和科技等方面有着重要的应用。请回答下列问题。
(1)氮原子的原子结构示意图为______ 。
(2)氮气的电子式为______ ,在氮气分子中,氮原子之间存在着______ 个σ键和______ 个π键。
(3)磷、氮、氧是周期表中相邻的三种元素,比较:(均填“大于”“小于”或“等于”)
①氮原子的第一电离能______ 磷原子的第一电离能;
②N2分子中N—N键的键长______ 白磷分子中P—P键的键长。
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是______ 。
(1)氮原子的原子结构示意图为
(2)氮气的电子式为
(3)磷、氮、氧是周期表中相邻的三种元素,比较:(均填“大于”“小于”或“等于”)
①氮原子的第一电离能
②N2分子中N—N键的键长
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是_______ ,基态D原子价电子的轨道表达式为_______ 。
(2)DA2分子的VSEPR模型是_______ 。H2A比H2D熔沸点高得多的原因是_______ 。
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。

①C2Cl6属于_______ 晶体(填晶体类型),其中C原子的杂化轨道类型为_______ 杂化。
②[C(OH)4]-中存在的化学键有_______ 。
(4)B、C的氟化物晶格能分别是2957kJ·mol-1、5492kJ·mol-1,二者相差很大的原因是______ 。
(5)D与E所形成化合物晶体的晶胞如下图所示。
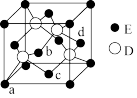
①在该晶胞中,E的配位数为_______ 。
②已知该晶胞的密度为ρg/cm3,则其中两个D原子之间的距离为_______ cm(列出计算式即可)。
(1)B、C中第一电离能较大的是
(2)DA2分子的VSEPR模型是
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。

①C2Cl6属于
②[C(OH)4]-中存在的化学键有
(4)B、C的氟化物晶格能分别是2957kJ·mol-1、5492kJ·mol-1,二者相差很大的原因是
(5)D与E所形成化合物晶体的晶胞如下图所示。

①在该晶胞中,E的配位数为
②已知该晶胞的密度为ρg/cm3,则其中两个D原子之间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态。请回答下列问题:
(1)Q+核外电子排布式为__________________ 。
(2)ZX3分子的空间构型为__________________ , ZW3-离子的立体构型是__________ 。
(3)Y、R的最高价氧化物的沸点较高的是_______ (填化学式),原因是_____________ 。
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为:______________________________________________ 。
(5)W和Na的一种离子化合物的晶胞结构如图,该离子化合物为________ (填化学式)。Na+的配位数为________ ,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为__________ 。

(1)Q+核外电子排布式为
(2)ZX3分子的空间构型为
(3)Y、R的最高价氧化物的沸点较高的是
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为:
(5)W和Na的一种离子化合物的晶胞结构如图,该离子化合物为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】镓(31Ga)是一种重要金属元素,镓及其化合物在电子工业、光电子工业、国防工业和超导材料等领域有着广泛的应用。回答下列问题:
(1)基态Ga原子占据最高能级电子的电子云轮廓图形状为__________ ,未成对电子数为________________ 。
(2)Ga(NO3)3中阴离子的立体构型是_____________ ,写出一个与该阴离子的立体构型相同的分子的化学式___________ 。
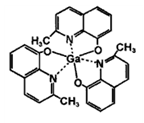
(3)2-甲基-8-羟基喹啉镓(如图)应用于分子印迹技术,2-甲基-8-羟基喹啉镓中五种元素电负性由大到小的顺序是____________________________ (填元素符号),提供孤电子对的成键原子是_____________ 。
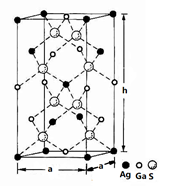
(4)一种硅镓半导体材料的晶胞结构如图所示由硫、镓、银形成的化合物的晶胞是底面为正方形的长方体,结构如下图所示,则该晶体中硫的配位数为___________ ,晶胞底面的边长a=5.75 nm,高h=10.30nm,该晶体密度为__________________ g·cm-3(列出计算式即可)。
(1)基态Ga原子占据最高能级电子的电子云轮廓图形状为
(2)Ga(NO3)3中阴离子的立体构型是
(3)2-甲基-8-羟基喹啉镓(如图)应用于分子印迹技术,2-甲基-8-羟基喹啉镓中五种元素电负性由大到小的顺序是

(4)一种硅镓半导体材料的晶胞结构如图所示由硫、镓、银形成的化合物的晶胞是底面为正方形的长方体,结构如下图所示,则该晶体中硫的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】不锈钢是由铁、铬、镍、碳及多种不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素。其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3。回答下列问题:
(1)写出基态Fe2+的电子排布式:_______ 。基态铬原子的未成对电子数为_______ 。
(2)铁和镍位于元素周期表的同一周期同一族,它们均位于第_______ 周期第_______ 族。
(3)金属铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是_______ 。
(4)某镍镧合金是优质储氢材料,其晶胞如图所示,则它的化学式为_______ 。

(5)Fe的一种晶体如图甲、乙所示。

①图甲中与铁原子等距离且最近的铁原子数为_______ 。
②若按甲中虚线(面对角线)方向切乙,得到的图像正确的是_______ (填字母)。
A. B.
B. C.
C. D.
D. 
(6)金属铬属于体心立方晶体(如图),已知其密度为7.2g/cm3,则晶体中铬原子的半径为_______ cm(阿伏加德罗常数的值为NA,列出表达式)。

(1)写出基态Fe2+的电子排布式:
(2)铁和镍位于元素周期表的同一周期同一族,它们均位于第
(3)金属铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是
(4)某镍镧合金是优质储氢材料,其晶胞如图所示,则它的化学式为

(5)Fe的一种晶体如图甲、乙所示。

①图甲中与铁原子等距离且最近的铁原子数为
②若按甲中虚线(面对角线)方向切乙,得到的图像正确的是
A.
 B.
B. C.
C. D.
D. 
(6)金属铬属于体心立方晶体(如图),已知其密度为7.2g/cm3,则晶体中铬原子的半径为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】某大学柔性电子前沿科学中心研究人员利用重力引导CVD(化学气相沉积)策略合成了一种掺杂Se的碳纳米管基FeCo双功能催化剂(FeCo/Se-CNT)。该催化剂具有出色的稳定性。含Co、Se、Fe、C等元素的化合物在生产、生活中应用广泛。回答下列问题:
(1)基态铁原子的价电子排布式为___________ 。
(2)实验室常用KSCN溶液检验Fe3+,N、O、S 的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)科学研究发现,温度在5 K时呈现超导性的晶体CoO2具有层状结构。晶体中O与Co的配位数之比为______ 。
(4)在Fe-Co催化剂的作用下,利用CO2合成甲醇的反应为CO2 +3H2 CH3OH+H2O。
CH3OH+H2O。
①写出,上述反应中由极性键构成的非极性分子的结构式:___________ 。
②CH3OH和H2O中沸点较高的是___________ 。
(5)已知:[Co(CN)6]4- 是强还原剂,与水反应能生成[Co(CN)6]3-。写出该反应的离子方程式:______ 。1 mol CN-中含有σ键的数目为___________ ,该离 子中C元素的杂化方式为___________ 。
(6)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,晶胞边长为a nm,硒化锌的相对分子质量为M。NA表示阿伏加德罗常数的值,硒化锌的密度为___________ (用含a、M、NA的代数式表示)g·cm-3。

(1)基态铁原子的价电子排布式为
(2)实验室常用KSCN溶液检验Fe3+,N、O、S 的第一电离能由大到小的顺序为
(3)科学研究发现,温度在5 K时呈现超导性的晶体CoO2具有层状结构。晶体中O与Co的配位数之比为
(4)在Fe-Co催化剂的作用下,利用CO2合成甲醇的反应为CO2 +3H2
 CH3OH+H2O。
CH3OH+H2O。①写出,上述反应中由极性键构成的非极性分子的结构式:
②CH3OH和H2O中沸点较高的是
(5)已知:[Co(CN)6]4- 是强还原剂,与水反应能生成[Co(CN)6]3-。写出该反应的离子方程式:
(6)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,晶胞边长为a nm,硒化锌的相对分子质量为M。NA表示阿伏加德罗常数的值,硒化锌的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】溴化亚氨合汞( )和甘汞(
)和甘汞(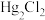 )是汞的两种重要化合物。回答下列问题:
)是汞的两种重要化合物。回答下列问题:
(1)Hg的原子序数为80,基态Hg原子的价电子排布式为___________ ,在元素周期表中的位置为___________ 。
(2) 中存在如图1所示层状结构。
中存在如图1所示层状结构。___________ ;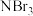 分子的空间构型为
分子的空间构型为___________ 。
②该层状结构的最简式为___________ ;层间还有 和
和 ,其个数比为
,其个数比为___________ 。
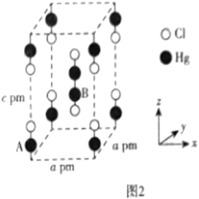
(3)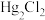 晶体属四方晶系,晶胞参数如图2所示,晶胞棱边夹角均为
晶体属四方晶系,晶胞参数如图2所示,晶胞棱边夹角均为 。已知
。已知 键长为rpm,则B点原子的分数坐标为
键长为rpm,则B点原子的分数坐标为___________ ;晶胞中A、B间距离d=___________ pm;若阿佛加德罗常数为 ,则晶胞的密度为
,则晶胞的密度为___________  。(已知
。(已知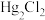 的摩尔质量为
的摩尔质量为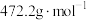 )
)
 )和甘汞(
)和甘汞(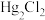 )是汞的两种重要化合物。回答下列问题:
)是汞的两种重要化合物。回答下列问题:(1)Hg的原子序数为80,基态Hg原子的价电子排布式为
(2)
 中存在如图1所示层状结构。
中存在如图1所示层状结构。
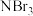 分子的空间构型为
分子的空间构型为②该层状结构的最简式为
 和
和 ,其个数比为
,其个数比为(3)
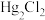 晶体属四方晶系,晶胞参数如图2所示,晶胞棱边夹角均为
晶体属四方晶系,晶胞参数如图2所示,晶胞棱边夹角均为 。已知
。已知 键长为rpm,则B点原子的分数坐标为
键长为rpm,则B点原子的分数坐标为 ,则晶胞的密度为
,则晶胞的密度为 。(已知
。(已知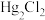 的摩尔质量为
的摩尔质量为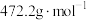 )
)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】铁的硫化物被认为是有前景的锂电池材料,但导电性较差,放电时易膨胀。
(1) 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。
①水热法合成 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为___________ 。
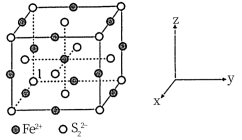
② 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为___________ (任写一个),每个 周围距离最近且相等的
周围距离最近且相等的 有
有___________ 个。
(2)①将 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
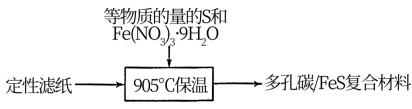
具有的优势是放电时不易膨胀且___________ 。多孔碳/ 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和___________ 。
②分别取多孔碳、多孔碳/ 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。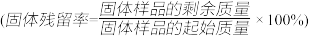
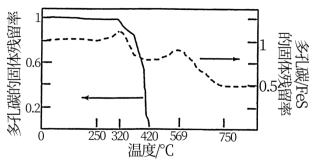
420℃~569℃时,多孔碳/ 固体残留率增大的原因是
固体残留率增大的原因是___________ 。
③ 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: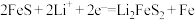
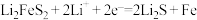
该多孔碳/ 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子___________  。(写出计算过程)
。(写出计算过程)
(1)
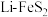 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。①水热法合成
 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为②
 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为 周围距离最近且相等的
周围距离最近且相等的 有
有
(2)①将
 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和
②分别取多孔碳、多孔碳/
 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。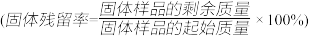

420℃~569℃时,多孔碳/
 固体残留率增大的原因是
固体残留率增大的原因是③
 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: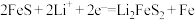
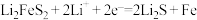
该多孔碳/
 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子 。(写出计算过程)
。(写出计算过程)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是________ ,该元素基态原子核外M层电子的自旋状态_________ (填“相同”或“相反”)。
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为________ ,其中Fe的配位数为_____________ 。
(3)苯胺 )的晶体类型是
)的晶体类型是__________ 。苯胺与甲苯(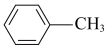 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是___________ 。
(4)NH4H2PO4中,电负性最高的元素是______ ;P的_______ 杂化轨道与O的2p轨道形成_______ 键。
(5)NH4H2PO4和LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
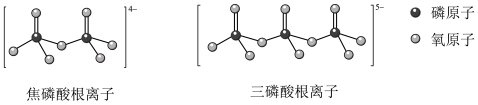
这类磷酸根离子的化学式可用通式表示为____________ (用n代表P原子数)。
(1)在周期表中,与Li的化学性质最相似的邻族元素是
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(3)苯胺
 )的晶体类型是
)的晶体类型是 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(4)NH4H2PO4中,电负性最高的元素是
(5)NH4H2PO4和LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:

这类磷酸根离子的化学式可用通式表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】实验室常利用“棕色环”现象检验NO3—离子。其方法为:取含有NO3—的溶液于试管中,加入FeSO4溶液振荡,然后沿着试管内壁加入浓H2SO4,在溶液的界面上出现“棕色环”。回答下列问题:
(1)基态Fe2+核外未成对电子个数为_____ 。
(2)形成“棕色环”主要发生如下反应:
3[Fe( H2O)6]2++ NO3-+4H+=3[Fe(H2O)6]3++ NO ↑+2H2O
[Fe( H2O)6]2++ NO=[Fe(NO) (H2O)5]2+(棕色)+ H2O
[Fe(NO)(H2O)5]2+中,配体是______ 、______ ,配位数为______ 。
(3)与NO互为等电子体的微粒是_____ (任写一例)。
(4)SO42-的空间构型是_____ ,其中S原子的杂化方式是________ 。
(5)铁原子在不同温度下排列构成不同晶体结构,在912℃以下排列构成的晶体叫做α-铁;在912℃至1394℃之间排列构成的晶体叫做γ-铁;在1394℃以上排列构成的晶体,叫做δ-铁。晶胞剖面结构如图所示:

①α-铁的原子堆积方式为_____ 。δ-铁配位数为____ 。
②已知γ-铁晶体密度为d g/cm3,则Fe原子的半径为____ nm(用含d、NA的式子表示)。
(1)基态Fe2+核外未成对电子个数为
(2)形成“棕色环”主要发生如下反应:
3[Fe( H2O)6]2++ NO3-+4H+=3[Fe(H2O)6]3++ NO ↑+2H2O
[Fe( H2O)6]2++ NO=[Fe(NO) (H2O)5]2+(棕色)+ H2O
[Fe(NO)(H2O)5]2+中,配体是
(3)与NO互为等电子体的微粒是
(4)SO42-的空间构型是
(5)铁原子在不同温度下排列构成不同晶体结构,在912℃以下排列构成的晶体叫做α-铁;在912℃至1394℃之间排列构成的晶体叫做γ-铁;在1394℃以上排列构成的晶体,叫做δ-铁。晶胞剖面结构如图所示:

①α-铁的原子堆积方式为
②已知γ-铁晶体密度为d g/cm3,则Fe原子的半径为
您最近一年使用:0次



