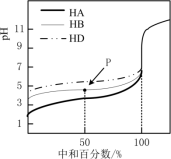
已知:H2R是二元弱酸,HY是一元弱酸。常温下,分别向20mL。0.1mol/L的Na2R、NaY溶液中滴加0.1mol/L盐酸,测得溶液pM[pM=-lgM],M=x、y、z,x= 、y=
、y=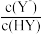 、z=
、z= 和pH关系如图所示。下列叙述正确的是
和pH关系如图所示。下列叙述正确的是
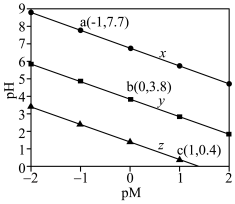
 、y=
、y=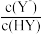 、z=
、z= 和pH关系如图所示。下列叙述正确的是
和pH关系如图所示。下列叙述正确的是
| A.NaY溶液呈中性 |
| B.直线y中b点时,c(Y-)>c(HY) |
| C.Ka1(H2R)=1×10-1.4 |
| D.a点时,溶液中c(Na+)+c(H+)=c(OH-)+c(HR-)+2c(R2-) |
更新时间:2024-03-15 18:26:08
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】我校实验小组进行下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将少量 样品溶于水,滴加足量盐酸酸化的 样品溶于水,滴加足量盐酸酸化的 溶液 溶液 | 有白色沉淀产生 | 说明 已变质 已变质 |
| B | 将稀硫酸滴入 溶液中 溶液中 | 溶液中出现凝胶 | 非金属性: |
| C | 用 试纸测定浓度均为 试纸测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 |  溶液的 溶液的 大 大 | 酸性: 比 比 强 强 |
| D | 将混合气体通入澄清石灰水 | 澄清石灰水未变浑浊 | 混合气体中不存在 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据表中数据判断,下列选项结论正确的是
| 酸 |  |  |  |
| 电离常数(25℃) | 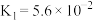  | 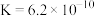 | 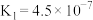  |
A.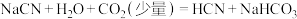 |
B. 的 的 溶液逐渐滴加到同浓度的 溶液逐渐滴加到同浓度的 溶液中,无明显现象,说明未发生反应 溶液中,无明显现象,说明未发生反应 |
C.浓度均为 的 的 、 、 、 、 、 、 溶液, 溶液, 最大的是 最大的是 |
D. 溶液中,离子浓度由大到小的顺序是 溶液中,离子浓度由大到小的顺序是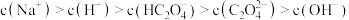 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验能达到预期目的是
| 编号 | 实验内容 | 实验目的 |
| A | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| B | 室温下,用pH试纸测定浓度为0.1mol/LNaClO溶液和0.1mol/LCH3COONa溶液的pH | 比较HClO和H3COOH的酸性强弱 |
| C | 常温下向物质的量浓度均为0.1mol·L-1的NaCl和NaI混合溶液中逐滴滴入AgNO3溶液,先出现黄色沉淀 | 证明Ksp(AgCl)<Ksp(AgI) |
| D | 向10mL 0.2mol/L NaOH溶液中滴2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下Ksp:Mg(OH)2>Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,弱酸的电离平衡常数如表所示,下列说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A.a mol·L-1HCN与b mol·L-1NaOH溶液等体积混合后c(Na+) > c(CN-),则a一定小于b |
| B.等pH的溶液物质的量浓度关系:c(CH3COONa) > c(NaHCO3) > c(NaCN) |
| C.用等pH的CH3COOH与HCN中和等物质的量的NaOH,所用CH3COOH溶液的体积小于HCN溶液的体积 |
| D.NaHCO3和Na2CO3的混合液中:c(Na+) +c(H+)=c(OH-)+ c(HCO3-)+c(CO32-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
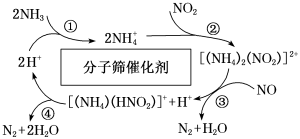
【推荐2】在化工生产中常利用某分子篮作催化剂,催化 脱除废气中的
脱除废气中的 和
和 (假定二者物质的量相等),生成两种无毒物质,其反应历程如图所示。设
(假定二者物质的量相等),生成两种无毒物质,其反应历程如图所示。设 为阿伏加德罗常数的值,下列说法中
为阿伏加德罗常数的值,下列说法中不正确 的是
 脱除废气中的
脱除废气中的 和
和 (假定二者物质的量相等),生成两种无毒物质,其反应历程如图所示。设
(假定二者物质的量相等),生成两种无毒物质,其反应历程如图所示。设 为阿伏加德罗常数的值,下列说法中
为阿伏加德罗常数的值,下列说法中
A. 溶液中含有 溶液中含有 的数目小于 的数目小于 |
B.常温下,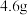 二氧化氮气体中含有的分子数为 二氧化氮气体中含有的分子数为 |
C.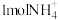 中含有 中含有 共价键的数目为 共价键的数目为 |
D.总反应中生成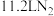 (标准状况)时转移电子数为 (标准状况)时转移电子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下向1mol/LCH3COOH溶液中逐滴加入1mol/LNaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中错误 的是
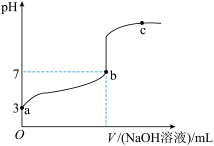

| A.a与c之间的溶液中b点水的电离程度最大 |
| B.溶液中存在c(CH3COO-)>c(Na+)>c(H+)>c(OH-)的点一定在a与b之间且靠近b |
| C.b点时,NaOH溶液与醋酸不是恰好反应,V(NaOH溶液)<V(CH3COOH溶液) |
D.a、b、c点表示的溶液中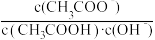 均相等 均相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,下列关于电解质溶液的说法中不正确的是
A.将 的氨水与 的氨水与 的硝酸等体积混合: 的硝酸等体积混合: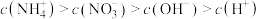 |
B.室温下,调节 溶液的 溶液的 时, 时,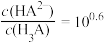 (已知:Ka1=10-2.2、Ka2=10-7.2、Ka3=10-12.4) (已知:Ka1=10-2.2、Ka2=10-7.2、Ka3=10-12.4) |
C. 时, 时, 的平衡常数 的平衡常数 [该温度下,Ksp(MS)=1.0×10-21、Ksp(RS)=4.0×10-18] [该温度下,Ksp(MS)=1.0×10-21、Ksp(RS)=4.0×10-18] |
D.加水稀释氯化铝溶液,铝离子水解程度增大, 物质的量增加,溶液酸性增强 物质的量增加,溶液酸性增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验目的对应的方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 探究SO2的漂白性 | 将SO2通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色,说明SO2具有漂白性 |
| B | 比较Ka(CH3COOH)和Ka1(H2CO3)的大小 | 向2 mL1 mol/LCH3COOH溶液中滴1 mol/LNa2CO3溶液 | 有气体生成,说明Ka(CH3COOH)>Ka1(H2CO3) |
| C | 探究淀粉水解程度 | 将稀硫酸滴入淀粉溶液中,加热一段时间,再加入新制Cu(OH)2悬浊液并加热 | 溶液中未出现砖红色沉淀,说明淀粉未水解 |
| D | 检验溶液X是否含有 | 向溶液X中滴加少量稀硝酸,然后滴入几滴Ba(NO3)2溶液 | 有白色沉淀生成,说明溶液X含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,用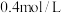 盐酸滴定
盐酸滴定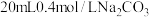 溶液,反应过程中的pH和压强变化如图所示。下列说法
溶液,反应过程中的pH和压强变化如图所示。下列说法错误 的是

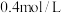 盐酸滴定
盐酸滴定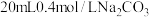 溶液,反应过程中的pH和压强变化如图所示。下列说法
溶液,反应过程中的pH和压强变化如图所示。下列说法
A.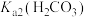 的数量级为 的数量级为 |
B.b点: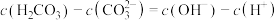 |
C.c→d段主要发生的反应为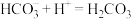 |
| D.e→f段压强增大的主要原因是盐酸的挥发 |
您最近一年使用:0次