在恒温的2L密闭容器中进行反应,气体X、Y,Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡。
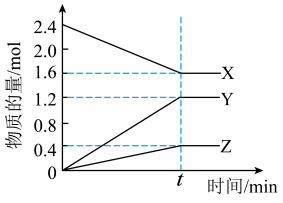
(1)上述反应_______ (填“是”或“不是”)可逆反应。
(2)该反应的化学方程式是_______ 。
(3)反应起始至t=2min时刻,Y的平均反应速率是_______ 。
(4)tmin后,体系内的压强与反应前的压强之比为:_______ 。

(1)上述反应
(2)该反应的化学方程式是
(3)反应起始至t=2min时刻,Y的平均反应速率是
(4)tmin后,体系内的压强与反应前的压强之比为:
更新时间:2024-03-17 13:11:55
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】化学反应速率与生产、生活密切相关。
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①反应速率最大的时间段是______ (填“0~1”“1~2”“2~3”“3~4”“4~5”)min,原因是:_______ 。
②反应速率最小的时间段是___________ ,原因是:___________ 。
③2~3min内该反应的反应速率υ(HCl)=_________ mol∙L−1∙min−1(设溶液体积不变)。
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列___________ (填字母)以减慢反应速率,同时不影响生成氢气的量。
A.蒸馏水 B.NaOH溶液 C.Na2CO3溶液 D.CuSO4溶液 E.NaCl溶液
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况) | 50 | 120 | 232 | 290 | 310 |
①反应速率最大的时间段是
②反应速率最小的时间段是
③2~3min内该反应的反应速率υ(HCl)=
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列
A.蒸馏水 B.NaOH溶液 C.Na2CO3溶液 D.CuSO4溶液 E.NaCl溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)恒温恒容条件下,将3molA气体和4molB气体通入体积为10L的密闭容器中发生如下反应:2A(g)+B(g) 4C(g)+2D(s),2min末达平衡,测得平衡时A为1.2mol。
4C(g)+2D(s),2min末达平衡,测得平衡时A为1.2mol。
①从开始至平衡状态,生成C的平均反应速率为___________ 。
②B的转化率为___________ 。
③该上述反应在三个容器中进行,测的反应速率如下,其中能表明反应速率最快的是___________
A.v(A)=0.2 mol·L‒1·s‒1
B.v(B)=0.5 mol·L‒1·s‒1
C.v(C)=1 mol·L‒1·s‒1
④能说明该反应已达到平衡状态的是___________ (填字母)。
a.v(A)=2v(B) b.容器内压强保持不变
c.3v逆(A)=v正(B) d.容器内混合气体的密度保持不变
(2)某温度时,在5L容器中X、Y、Z三种物质的物质的量(n)随着时间(t)变化的曲线如图所示。由图中数据分析:
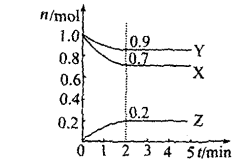
①该反应的化学方程式为___________ 。
②在密闭容器里,通入a molX(g)、b molY(g),发生上述反应,当改变下列条件时,反应速率会减小的是___________ (填序号)。
①降低温度 ②加入催化剂 ③增大容器体积
 4C(g)+2D(s),2min末达平衡,测得平衡时A为1.2mol。
4C(g)+2D(s),2min末达平衡,测得平衡时A为1.2mol。①从开始至平衡状态,生成C的平均反应速率为
②B的转化率为
③该上述反应在三个容器中进行,测的反应速率如下,其中能表明反应速率最快的是
A.v(A)=0.2 mol·L‒1·s‒1
B.v(B)=0.5 mol·L‒1·s‒1
C.v(C)=1 mol·L‒1·s‒1
④能说明该反应已达到平衡状态的是
a.v(A)=2v(B) b.容器内压强保持不变
c.3v逆(A)=v正(B) d.容器内混合气体的密度保持不变
(2)某温度时,在5L容器中X、Y、Z三种物质的物质的量(n)随着时间(t)变化的曲线如图所示。由图中数据分析:

①该反应的化学方程式为
②在密闭容器里,通入a molX(g)、b molY(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入催化剂 ③增大容器体积
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】将质量均为100g的锌片和铜片用导线与灯泡串联浸入盛有500mL 2 mol·L-1稀硫酸溶液的1.5L容器中构成如下装置。

(1)该装置中发生反应总的离子方程式为________________ ,溶液中______ (填微粒化学式)向锌极移动。
(2)若2 min后测得锌片质量减少13g,则导线中流过的电子为__________ mol,电子的流动方向____________ (用m、n表示)。若将正极生成的气体不断导入一个2L的刚性容器中,则反应开始至2min用该气体表示的反应速率为_______________ 。
(3)当反应进行到3min时灯泡亮度较弱,某同学向该装置内溶液中加入__________ (填序号)灯泡的亮度会突然增加。
a.300mL蒸馏水b.100mL 8 mol·L-1硫酸溶液
c.300mL 10 mol·L-1硫酸铜溶液d.200mL 8 mol·L-1氢氧化钠溶液

(1)该装置中发生反应总的离子方程式为
(2)若2 min后测得锌片质量减少13g,则导线中流过的电子为
(3)当反应进行到3min时灯泡亮度较弱,某同学向该装置内溶液中加入
a.300mL蒸馏水b.100mL 8 mol·L-1硫酸溶液
c.300mL 10 mol·L-1硫酸铜溶液d.200mL 8 mol·L-1氢氧化钠溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】为顺应全球应对气候变化趋势和中国国情,我国提出了碳达峰碳中和的工作战略。以CO2生产甲醇(CH3OH)是实现“碳中和”的重要途径。在体积为2L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得反应物CO2和CH3OH(g)的物质的量随时间的变化如图所示。
CH3OH(g)+H2O(g),测得反应物CO2和CH3OH(g)的物质的量随时间的变化如图所示。

(1)0~3min内,υ(CH3OH)=_______ mol∙L−1∙min−1(保留两位有效数字)
(2)A点处的正反应速率比逆反应速率_______ (填“大”或“小”或“相等”)
(3)10min后,能使该反应速率加快的措施有_______(填序号)。
(4)在相同温度、容积不变的条件下,不能 说明该反应已达平衡状态的是_______。
(5)若合成甲醇1.6t,则理论上可吸收工厂排放的CO2_______ L(标准状况下)。
 CH3OH(g)+H2O(g),测得反应物CO2和CH3OH(g)的物质的量随时间的变化如图所示。
CH3OH(g)+H2O(g),测得反应物CO2和CH3OH(g)的物质的量随时间的变化如图所示。
(1)0~3min内,υ(CH3OH)=
(2)A点处的正反应速率比逆反应速率
(3)10min后,能使该反应速率加快的措施有_______(填序号)。
| A.降低反应温度 | B.充入2molCO2 |
| C.加入高效的催化剂 | D.充入适量氦气 |
| A.CO2、H2的浓度均不再变化 |
| B.体系压强不变 |
| C.n(CH3OH)∶n(H2O)=1∶1 |
| D.H2的消耗速率与CH3OH的生成速率之比为3∶1 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】实验小组对可逆反应aX(g)+bY(g) ⇌pZ(g)进行探究。回答下列问题:
(1)T℃时,起始向 恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
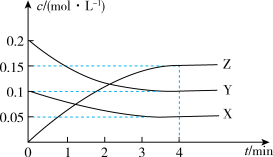
①起始充入X的物质的量为_______ 。
②a:b:p =_______ 。
③Y的平衡转化率为_______ 。
④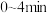 内的反应速率
内的反应速率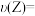
_______ 。
⑤下列事实能说明反应达到平衡状态的是_______ (填选项字母)
A.容器内气体压强不再改变 B.混合气体密度不再改变 C.X的体积分数不再改变
(2)若在不同条件下进行上述反应,测得反应速率分别为①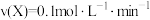 ,②
,②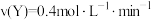 ,③
,③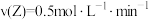 ,其中反应速率最快的是
,其中反应速率最快的是_______ (填序号)。
(1)T℃时,起始向
 恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
①起始充入X的物质的量为
②a:b:p =
③Y的平衡转化率为
④
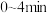 内的反应速率
内的反应速率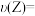
⑤下列事实能说明反应达到平衡状态的是
A.容器内气体压强不再改变 B.混合气体密度不再改变 C.X的体积分数不再改变
(2)若在不同条件下进行上述反应,测得反应速率分别为①
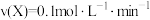 ,②
,②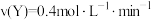 ,③
,③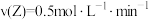 ,其中反应速率最快的是
,其中反应速率最快的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】温度为700℃的4L恒容密闭容器中,2NO(g)+O2(g) 2NO2(g)反应体系内,n(NO)随时间的变化见下表:
2NO2(g)反应体系内,n(NO)随时间的变化见下表:
(1)700℃,反应达到平衡时,NO的物质的量浓度是___________ 。
(2)用O2表示从0~2s内该反应的平均速率v=___________ (保留两位有效数字)。
(3)下图中表示NO2变化的曲线是___________ 。

(4)能说明该反应已达到平衡状态的是___________ 。
A.v(NO)=2v(O2)
B.混合气体的密度不再改变
C.气体的颜色不再改变
D.容器内压强保持不变
E.消耗2mol NO2的同时消耗1molO2
(5)下列能使化学反应速率增大的措施是___________ 。
A.适当升高温度 B.及时分离出NO2气体
C.通入O2 D.加入催化剂
 2NO2(g)反应体系内,n(NO)随时间的变化见下表:
2NO2(g)反应体系内,n(NO)随时间的变化见下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 |
| n(NO)/(mol) | 0.040 | 0.020 | 0.014 | 0.014 | 0.014 |
(1)700℃,反应达到平衡时,NO的物质的量浓度是
(2)用O2表示从0~2s内该反应的平均速率v=
(3)下图中表示NO2变化的曲线是

(4)能说明该反应已达到平衡状态的是
A.v(NO)=2v(O2)
B.混合气体的密度不再改变
C.气体的颜色不再改变
D.容器内压强保持不变
E.消耗2mol NO2的同时消耗1molO2
(5)下列能使化学反应速率增大的措施是
A.适当升高温度 B.及时分离出NO2气体
C.通入O2 D.加入催化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】将 转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人
转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 的浓度随时间变化如表所示。
的浓度随时间变化如表所示。
(1)从0min到6min,
___________  。
。
(2)能说明上述反应达到平衡状态的是___________(填标号)。
(3)上述反应10min时,混合气体中 的物质的量分数为
的物质的量分数为___________ %。(取整数)
(4)上述反应12min末时,混合气体中 和
和 的质量之比是
的质量之比是___________ 。
(5)第3min时的
___________ (填“>”、“<”、“=”或“无法比较”)第9min时的 。
。
(6)在恒温条件下,若将一定量X和Y的混合气体通入容积为2L的恒容密闭容器中,发生反应 ,X和
,X和 两种物质的浓度随时间的变化情况如表所示。
两种物质的浓度随时间的变化情况如表所示。
①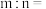
___________ 。
②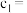
___________  。(保留两位有效数字)
。(保留两位有效数字)
③若反应在第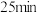 时改变某种条件,则
时改变某种条件,则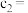
___________  。
。
 转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人
转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 的浓度随时间变化如表所示。
的浓度随时间变化如表所示。时间 | 0 | 3 | 6 | 9 | 12 |
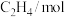 | 0 | 0.25 | 0.32 | 0.37 | 0.37 |
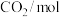 | 1 | 0.50 | 0.36 | 0.26 | 0.26 |

 。
。(2)能说明上述反应达到平衡状态的是___________(填标号)。
A.反应中 与 与 的物质的量浓度之比为 的物质的量浓度之比为 |
| B.混合气体的压强不随时间的变化而变化 |
C.单位时间内生成 ,同时生成 ,同时生成 |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
 的物质的量分数为
的物质的量分数为(4)上述反应12min末时,混合气体中
 和
和 的质量之比是
的质量之比是(5)第3min时的

 。
。(6)在恒温条件下,若将一定量X和Y的混合气体通入容积为2L的恒容密闭容器中,发生反应
 ,X和
,X和 两种物质的浓度随时间的变化情况如表所示。
两种物质的浓度随时间的变化情况如表所示。时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 |
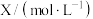 | 0.2 |  | 0.6 | 0.6 | 0.6 | 0.9 |  |  |
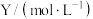 | 0.6 |  | 0.4 | 0.4 | 0.4 | 0.4 | 0.5 | 0.5 |
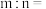
②
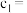
 。(保留两位有效数字)
。(保留两位有效数字)③若反应在第
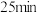 时改变某种条件,则
时改变某种条件,则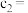
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】恒温恒容条件下,将2 mol A气体和2 mol B气体通入体积为2 L的密闭容器中发生如下反应: ,2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为
,2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为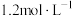 。
。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_______ 。
(2)
_______ 。2 min时A的转化率是_______ 。(用三段式写出计算过程)
(3)目前工业上有一种方法是用 生产燃料甲醇。
生产燃料甲醇。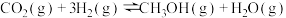 ,图1表示该反应过程中能量(单位为
,图1表示该反应过程中能量(单位为 )的变化:
)的变化:
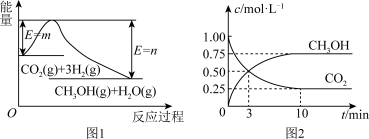
下列能说明该反应已经达到平衡状态的是_______(填字母)
 ,2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为
,2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为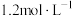 。
。(1)从开始反应至达到平衡状态,生成C的平均反应速率为
(2)

(3)目前工业上有一种方法是用
 生产燃料甲醇。
生产燃料甲醇。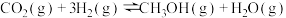 ,图1表示该反应过程中能量(单位为
,图1表示该反应过程中能量(单位为 )的变化:
)的变化:
下列能说明该反应已经达到平衡状态的是_______(填字母)
A.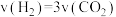 | B.容器内气体压强保持不变 |
C.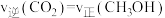 | D.容器内气体密度保持不变 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式_______ 和反应开始至2 min末Z的平均反应速率分别为_______

(2)在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
①x的值为___________ ;
②B的平衡浓度为___________ ;
③A的转化率为___________ ;
④D的体积分数为___________ ;

(2)在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则 ①x的值为
②B的平衡浓度为
③A的转化率为
④D的体积分数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在一密闭容器中发生反应N2+3H2 2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:

回答下列问题:
(1)t1、t3、t4时刻分别改变的一个条件是(填选项)。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻____ ;t3时刻____ ;t4时刻____ 。
(2)依据(2)中的结论,下列时间段中,氨的百分含量最高的是_____ (填选项)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(3)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为_____ 。
 2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
回答下列问题:
(1)t1、t3、t4时刻分别改变的一个条件是(填选项)。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻
(2)依据(2)中的结论,下列时间段中,氨的百分含量最高的是
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(3)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】一定条件下,在容积为5L的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。已知达到平衡后,降低温度,A的体积分数减小。
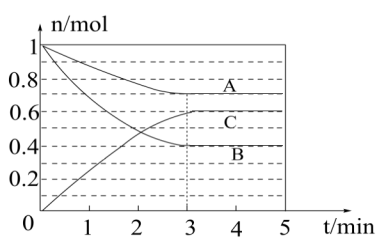
甲
(1)该反应的化学方程式___________ 。
(2)该反应的平衡常数的表达式为:___________ ,达到平衡时,A的转化率是:___________ 。
(3)若该反应ΔH <0,升高温度,K会___________ (填“增大”“减小”或“不变”)。

甲
(1)该反应的化学方程式
(2)该反应的平衡常数的表达式为:
(3)若该反应ΔH <0,升高温度,K会
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】I.某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。

请回答下列问题:
(1)该反应的化学反应方程式为_______ 。
(2)1min时,Y的正反应速率_______ Y的逆反应速率(填“>”“<”或“=”)
(3)反应从开始至2min,用X的浓度变化表示的平均反应速率为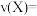
_______ 。
II.油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,通常将其回收生产硫单质(S2)。目前较为普遍的方法是克劳斯工艺和高温热分解H2S,克劳斯工艺的原理是利用以下两步反应生产单质硫:
①
②
请回答下列问题:
(4)下列措施可以加快反应②的速率的是_______。
(5)高温热分解H2S的化学反应方程式是_______ 。
(6)在1470K、100kPa反应条件下,在一容积为2L的恒容容器中充入1molH2S进行高温热分解反应,反应5分钟后达到平衡,平衡时混合气体中H2S与H2的物质的量相等,H2S平衡转化率为_______ 。

请回答下列问题:
(1)该反应的化学反应方程式为
(2)1min时,Y的正反应速率
(3)反应从开始至2min,用X的浓度变化表示的平均反应速率为
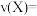
II.油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,通常将其回收生产硫单质(S2)。目前较为普遍的方法是克劳斯工艺和高温热分解H2S,克劳斯工艺的原理是利用以下两步反应生产单质硫:
①

②

请回答下列问题:
(4)下列措施可以加快反应②的速率的是_______。
| A.升高温度 | B.保持容积不变,充入N2使体系压强增大 |
| C.及时从体系中分离出S2(g) | D.加入合适的催化剂 |
(6)在1470K、100kPa反应条件下,在一容积为2L的恒容容器中充入1molH2S进行高温热分解反应,反应5分钟后达到平衡,平衡时混合气体中H2S与H2的物质的量相等,H2S平衡转化率为
您最近一年使用:0次



