黄铜矿(主要成分为CuFeS2)产生的炉渣可用于制备绿矾(FeSO4·7H2O)。工艺流程如图。

已知:焙烧时的主要反应为:① ;
;
② ;③
;③ 。
。
回答下列问题:
(1)若CuFeS2中Fe的化合价为+2,则反应①中的氧化剂为
(2)“炉渣”的主要成分为Fe2O3、FeO和少量Cu。
①Fe2O3高温下与铝粉混合发生的反应为
②“酸溶”后溶液中一定存在的金属阳离子为
③“试剂X”为
a.铁粉 b.铜粉 c.锌粉 d.30%的H2O2
④“操作”用到的玻璃仪器为
(3)“系列操作”为
更新时间:2024-03-24 18:59:49
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】根据《本草纲目》有关记载:“水银乃至阴之毒物,因火煅丹砂而出,加以盐、(明)矾而为轻粉(Hg2Cl2),加以硫磺升而为银朱(HgS)”。发生的主要化学反应方程式如下:
①HgS+O2 === Hg+SO2
② Hg+ NaCl+ KAl(SO4)2+ O2 === Hg2Cl2+ Na2SO4+ Al2O3+ K2SO4
③ Hg+S === HgS
请回答下列问题:
(1)在①的方程式中,HgS是做_______
a.氧化剂 b.还原剂 c.既做氧化剂又做还原剂 d.既不做氧化剂又不做还原剂
(2)配平②的化学方程式___________________________________________
(3)实验室制备SO2一般选用浓硫酸与Na2SO3反应。实验室制取SO2并检验其性质的装置与过程如下图:

a. 实验开始前检验气体发生装置气密 性的方法为____________________ (说明操作方法、现象和结论)
b. 分析下列装置中的现象分别为
①_________ ②__________
③_________ ④__________
c. ⑤的作用为_______________ ,所涉及的化学反应方程式为:____________________
d. 若在制备SO2时改为用稀盐酸与Na2SO3反应,则可能产生的影响为______________
①HgS+O2 === Hg+SO2
② Hg+ NaCl+ KAl(SO4)2+ O2 === Hg2Cl2+ Na2SO4+ Al2O3+ K2SO4
③ Hg+S === HgS
请回答下列问题:
(1)在①的方程式中,HgS是做
a.氧化剂 b.还原剂 c.既做氧化剂又做还原剂 d.既不做氧化剂又不做还原剂
(2)配平②的化学方程式
(3)实验室制备SO2一般选用浓硫酸与Na2SO3反应。实验室制取SO2并检验其性质的装置与过程如下图:

a. 实验开始前检验气体发生装置气密 性的方法为
b. 分析下列装置中的现象分别为
①
③
c. ⑤的作用为
d. 若在制备SO2时改为用稀盐酸与Na2SO3反应,则可能产生的影响为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】I.高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾:2Fe(OH)3+3ClO-+4OH-=2FeO +3Cl-+5H2O。
+3Cl-+5H2O。
(1)FeO 中铁元素的化合价为
中铁元素的化合价为___________ ,在该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)请用单线桥表示反应中电子转移情况:___________ 。
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:___________ (填元素符号);它在周期表中的位置为___________ 。
(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是___________ (填化学式),写出该单质与氢氧化钠反应的离子方程式___________ 。
 +3Cl-+5H2O。
+3Cl-+5H2O。(1)FeO
 中铁元素的化合价为
中铁元素的化合价为(2)请用单线桥表示反应中电子转移情况:
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
A.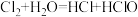 | B. |
C. | D. |
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:

(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】我国规定,食盐中加入KIO3.某厂生产碘酸钾(KIO3)的工艺流程如下:
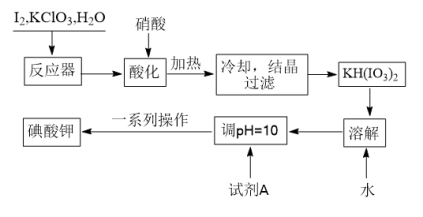
请回答下列问题:
(1)K的质子数为______ ;试剂A是______ ;流程图中“一系列操作”包括蒸发浓缩、降温结晶、过滤、洗涤、干燥。其中,“洗涤剂”是75%的酒精,而不用蒸馏水,其主要原因是______ 。
(2)工业上,还可用电解法制取KIO3。.以石墨和不锈钢为电极材料,电解KI溶液。化学方程式为 。在该反应中,氧化产物是
。在该反应中,氧化产物是___________ 。
(3)常用KI淀粉试纸检验碘盐,其操作是:取少量样品溶于蒸馏水,加几滴食醋,用KI淀粉试纸蘸取该溶液,若变蓝色,则该盐为加碘盐。写出离子方程式___________ 。
(4)测定产品纯度:取wg产品溶于蒸馏水,配制成250mL溶液。取20mL所配制溶液于锥形瓶中,加入过量的KI溶液,滴适量稀硫酸,再滴加几滴指示剂B,用c Na2S2O3溶液滴定至终点,消耗标准溶液为VmL。已知:
Na2S2O3溶液滴定至终点,消耗标准溶液为VmL。已知: 。
。
①根据上述数据,测得产品纯度为___________ (用含w、c、V表达式表示)。
②为了充分反应,滴定之前需要“振荡”锥形瓶中溶液,如果振荡时间过长,测得结果会___________ (填“偏高”、“偏低”或“无影响”)。

请回答下列问题:
(1)K的质子数为
(2)工业上,还可用电解法制取KIO3。.以石墨和不锈钢为电极材料,电解KI溶液。化学方程式为
 。在该反应中,氧化产物是
。在该反应中,氧化产物是(3)常用KI淀粉试纸检验碘盐,其操作是:取少量样品溶于蒸馏水,加几滴食醋,用KI淀粉试纸蘸取该溶液,若变蓝色,则该盐为加碘盐。写出离子方程式
(4)测定产品纯度:取wg产品溶于蒸馏水,配制成250mL溶液。取20mL所配制溶液于锥形瓶中,加入过量的KI溶液,滴适量稀硫酸,再滴加几滴指示剂B,用c
 Na2S2O3溶液滴定至终点,消耗标准溶液为VmL。已知:
Na2S2O3溶液滴定至终点,消耗标准溶液为VmL。已知: 。
。①根据上述数据,测得产品纯度为
②为了充分反应,滴定之前需要“振荡”锥形瓶中溶液,如果振荡时间过长,测得结果会
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,少量碳及二氧化硅)为原料制备的流程如下:

(1)为了提高废铁渣的浸出率,应该采用___________ (至少写一项)。
(2)“酸浸”需适宜的酸浓度、液固比、酸浸温度、氧流量等,其中酸浸温度对铁浸取率的影响如图所示:

①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为___________ 。
②酸浸时,通入O2的目的是___________ ,该反应的离子方程式为___________ 。
③当酸浸温度超过100℃时,铁浸取率反而减小,其原因是___________ 。
(3)滤渣的主要成分为___________ (填化学式)。
(4)“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+;在酸性条件下,再用K2Cr2O7标准溶液滴定Fe2+( 被还原为Cr3+),该滴定反应的离子方程式为
被还原为Cr3+),该滴定反应的离子方程式为___________ 。

(1)为了提高废铁渣的浸出率,应该采用
(2)“酸浸”需适宜的酸浓度、液固比、酸浸温度、氧流量等,其中酸浸温度对铁浸取率的影响如图所示:

①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为
②酸浸时,通入O2的目的是
③当酸浸温度超过100℃时,铁浸取率反而减小,其原因是
(3)滤渣的主要成分为
(4)“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+;在酸性条件下,再用K2Cr2O7标准溶液滴定Fe2+(
 被还原为Cr3+),该滴定反应的离子方程式为
被还原为Cr3+),该滴定反应的离子方程式为
您最近一年使用:0次
【推荐2】市政污泥含大量金属(Cu、Zn、Ni、Fe、Ag等),不经处理直接填埋会对环境造成严重的污染。市政污泥的综合利用能够使其得到科学、妥善的处置,并可以作为资源再次被我们利用,同时可以带来一定的经济价值。某科研团队利用市政污泥回收皓矾(ZnSO4·7H2O)的工艺流程如下:
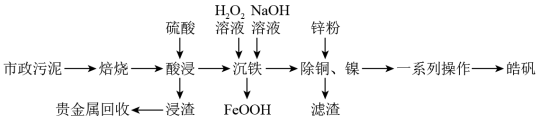
已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有___________ (任写一条)。
(2)“一系列操作”主要包括___________ 、___________ 、过滤、洗涤,干燥。
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为___________ 。
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:_______ ,则反应中氧化剂与还原剂的物质的量之比为_______ 。
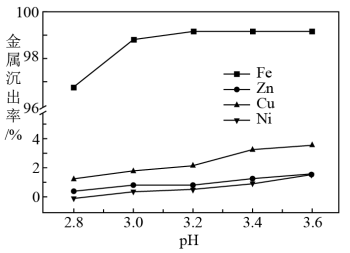
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为_______ 。pH对不同金属沉出率的影响如图所示,则“沉铁’时最合理的pH约为_______ 。在pH<6时,Zn2+、Cu2+、Ni2+在溶液中以离子形式存在,但是有铁离子存在时,pH升高,Zn、Cu、Ni损失率均升高,原因可能是_______ 。

已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有
(2)“一系列操作”主要包括
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】印刷电路产生的废腐蚀液中含有大量CuCl2、FeCl2和FeCl3, 为了减少污染并变废为宝,化学工作者计划从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液。作为腐蚀液原料循环使用。请根据以下流程图,回答下列问题:

回答下列问题:
(1)试剂a为_______ (填化学式),试剂b为 _______ (填名称),操作I、II的名称 _______ ,试剂a过量的原因为_______ 。
(2)已知试剂c为一种气体,c为_______ (填化学式) ,滤液Z和试剂c发生反应的离子方程式为_______ 。
(3)实验室制备c的化学方程式为_______ 。
(4)检验溶液W中阳离子的操作方法为_______ 。

回答下列问题:
(1)试剂a为
(2)已知试剂c为一种气体,c为
(3)实验室制备c的化学方程式为
(4)检验溶液W中阳离子的操作方法为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】炼锌厂的废渣中主要含有Zn及ZnO,还含有Fe2O3、FeO、CuO、SiO2等。对废渣进行合理处理既能减小环境污染,同时制得ZnSO4·7H2O晶体实现资源的再利用,其流程图如下。

已知:ZnSO4·7H2O易溶于水,难溶于酒精。
常温下金属离子沉淀的pH:
(1)提高废渣浸出速率可以采用的方法是(写出其中一点即可)________________________ 。
(2)滤渣2的成分是_______________ ;滤液2中含有的金属阳离子有______________ 。
(3)操作1的名称是_______________ ;加入H2O2的作用是______________________ 。
(4)加入试剂a可以是_____________ ;调pH的合适范围是________________ 。
(5)操作4依次为_______________ 、______________ 、过滤等。
(6)制得的ZnSO4·7H2O需洗涤,洗涤晶体时可选用试剂为_________________ 。

已知:ZnSO4·7H2O易溶于水,难溶于酒精。
常温下金属离子沉淀的pH:
| 金属离子 | Fe3+ | Zn2+ | Cu2+ | Fe2+ |
| 开始沉淀pH | 2.2 | 6.5 | 5.2 | 6.9 |
| 沉淀完全pH | 3.2 | 8.0 | 6.7 | 8.4 |
(2)滤渣2的成分是
(3)操作1的名称是
(4)加入试剂a可以是
(5)操作4依次为
(6)制得的ZnSO4·7H2O需洗涤,洗涤晶体时可选用试剂为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铬元素及其化合物在生产、生活中具有广泛的用途。以某铬矿石(主要成分是Cr2O3,含Fe2O3、SiO2等杂质)为原料生产Cr2O3的流程如下:

(1)Cr2O3在焙烧时生成Na2CrO4,写出第①步发生的所有方程式_________ 。
(2)沉淀2的化学式为_______ 。
(3)步骤③中CrO42-转化成Cr2O72- ,写出其离子方程式_______ ,硫酸能否换成盐酸并说明其理由______ 。
(4)滤液3中主要溶质的化学式为____________ 。
(5)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示,则B点时铬的氧化物化学式为_______ 。


(1)Cr2O3在焙烧时生成Na2CrO4,写出第①步发生的所有方程式
(2)沉淀2的化学式为
(3)步骤③中CrO42-转化成Cr2O72- ,写出其离子方程式
(4)滤液3中主要溶质的化学式为
(5)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示,则B点时铬的氧化物化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
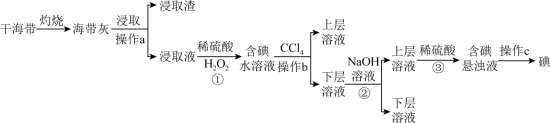
【推荐3】浩瀚的海洋里蕴藏着丰富的化学资源,从海带中提取碘单质的工艺流程如图。回答下列问题:_______ (填仪器名称)中,用酒精灯充分加热灰化。
(2)浸取液中碘主要以 存在,写出①发生反应的离子方程式
存在,写出①发生反应的离子方程式_______ ,实验步骤①后若检验溶液中碘单质的存在,具体方法是_______ 。
(3)向含有 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象
振荡静置后的实验现象_______ 。
(4)步骤②中加入浓 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为_______ ,步骤③反应中氧化剂与还原剂物质的量之比为_______ 。
(5)步骤②③是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为_______ 法。
(6)操作c的名称为_______ 。
(2)浸取液中碘主要以
 存在,写出①发生反应的离子方程式
存在,写出①发生反应的离子方程式(3)向含有
 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象
振荡静置后的实验现象(4)步骤②中加入浓
 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为(5)步骤②③是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为
(6)操作c的名称为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】认识化学反应的快慢和限度规律及影响因素,通过调控,可更好地满足工农业生产和日常生活的实际需要。回答下列问题:
Ⅰ.实验室利用下列方案探究影响化学反应速率的因素。
(1)实验时,分别量取 溶液(过量)和酸性
溶液(过量)和酸性 溶液,迅速混合并开始计时,可以通过测定
溶液,迅速混合并开始计时,可以通过测定___________ 来判断反应的快慢。
(2)探究浓度对化学反应速率的影响,应对比实验___________ (填编号);对比实验②和③是探究___________ 对化学反应速率的影响。
II.恒容密闭容器中,用 还原
还原 ,生成S的反应分两步完成(如图甲所示),在300℃反应时相关物质的物质的量浓度随时间的变化关系如图乙所示。
,生成S的反应分两步完成(如图甲所示),在300℃反应时相关物质的物质的量浓度随时间的变化关系如图乙所示。

(3)写出300℃发生反应的化学方程式:___________ 。其中一种产物X进入下一容器,在100~200℃与 反应,则每生成48gS,转移的电子的物质的量为
反应,则每生成48gS,转移的电子的物质的量为___________ mol。
(4) 时间段用
时间段用 表示的化学反应速率为
表示的化学反应速率为___________ 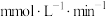 。
。
Ⅰ.实验室利用下列方案探究影响化学反应速率的因素。
| 编号 | 温度/℃ |  溶液 溶液 | 酸性 溶液 溶液 | ||
浓度 | 体积/mL | 浓度 | 体积/mL | ||
| ① | 25 | 0.10 | 2.0 | 0.010 | 4.0 |
| ② | 25 | 0.20 | 2.0 | 0.010 | 4.0 |
| ③ | 50 | 0.20 | 2.0 | 0.010 | 4.0 |
 溶液(过量)和酸性
溶液(过量)和酸性 溶液,迅速混合并开始计时,可以通过测定
溶液,迅速混合并开始计时,可以通过测定(2)探究浓度对化学反应速率的影响,应对比实验
II.恒容密闭容器中,用
 还原
还原 ,生成S的反应分两步完成(如图甲所示),在300℃反应时相关物质的物质的量浓度随时间的变化关系如图乙所示。
,生成S的反应分两步完成(如图甲所示),在300℃反应时相关物质的物质的量浓度随时间的变化关系如图乙所示。
(3)写出300℃发生反应的化学方程式:
 反应,则每生成48gS,转移的电子的物质的量为
反应,则每生成48gS,转移的电子的物质的量为(4)
 时间段用
时间段用 表示的化学反应速率为
表示的化学反应速率为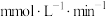 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】镍(Ni)及其化合物广泛应用于生产电池、电镀和催化剂等领域。
(1)某蓄电池反应为2NiO(OH)+Cd+2H2O Cd(OH)2+2Ni(OH)2。该蓄电池充电时,被氧化的物质是
Cd(OH)2+2Ni(OH)2。该蓄电池充电时,被氧化的物质是__ (填化学式),放电时若生成73gCd(OH)2,则外电路中转移的电子数是___ 。
(2)镍的羰化反应为:Ni(s)+4CO(g) Ni(CO)4(g) ΔH。
Ni(CO)4(g) ΔH。
①一定温度下,将一定量的粗镍和CO加入到1L的恒容密闭容器中反应,5s后测得Ni(CO)4的物质的量为1.5mol,则0~5s内平均反应速率v(CO)=__ mol·L·s-1。
②该反应的平衡常数K随温度升高而减小,则该反应的ΔH__ 0(填“>”或“<")。
(3)NiSO4·6H2O晶体是一种绿色易溶于水的晶体,广泛应用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Zn、Fe等元素)为原料制取。制取步骤如下:

①在实验室中,欲用98%的浓硫酸(密度1.84g·mL-1)配制40%的稀硫酸,需要的玻璃仪器除玻璃棒外,还有__ 。
②向滤液Ⅰ中加入Na2S的目的是_ 。(已知:Ksp[FeS]=6.3×10-18,Ksp[CuS]=1.3×10-36,Ksp[ZnS]=1.3×10-24,Ksp[NiS]=1.1×10-21)
③滤液Ⅲ中所含的阳离子主要有__ 。
④NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为__ 。
⑤在制备NiSO4·6H2O晶体时,常用无水乙醇代替蒸馏水做洗涤剂,原因是__ (写出一条即可)。
(1)某蓄电池反应为2NiO(OH)+Cd+2H2O
 Cd(OH)2+2Ni(OH)2。该蓄电池充电时,被氧化的物质是
Cd(OH)2+2Ni(OH)2。该蓄电池充电时,被氧化的物质是(2)镍的羰化反应为:Ni(s)+4CO(g)
 Ni(CO)4(g) ΔH。
Ni(CO)4(g) ΔH。①一定温度下,将一定量的粗镍和CO加入到1L的恒容密闭容器中反应,5s后测得Ni(CO)4的物质的量为1.5mol,则0~5s内平均反应速率v(CO)=
②该反应的平衡常数K随温度升高而减小,则该反应的ΔH
(3)NiSO4·6H2O晶体是一种绿色易溶于水的晶体,广泛应用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Zn、Fe等元素)为原料制取。制取步骤如下:

①在实验室中,欲用98%的浓硫酸(密度1.84g·mL-1)配制40%的稀硫酸,需要的玻璃仪器除玻璃棒外,还有
②向滤液Ⅰ中加入Na2S的目的是
③滤液Ⅲ中所含的阳离子主要有
④NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为
⑤在制备NiSO4·6H2O晶体时,常用无水乙醇代替蒸馏水做洗涤剂,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】LiNiO2是目前在锂离子电池中得到较广泛应用的一种正极材料,因其价格较为昂贵,故回收再用意义十分重大。一种以共沉淀法从废旧电池中回收并制备超细LiNiO2的工业流程如下图所示:

回答下列问题:
(1)正极材料粉碎的目的是_______ 。
(2)DMF溶液无法溶解的铝单质可以用浓NaOH溶液溶解后再回收利用,写出溶解铝反应的离子反应方程式_______ 。
(3)除C的方法可以是加入浓硝酸与过氧化氢的混合溶液,控制温度95℃,此时C与浓硝酸发生反应的化学方程式是_______ ;也可以常温加入稀硫酸与过氧化氢的混合溶液,将LiNiO2变为镍锂溶液然后通过_______ (填分离方法除去C,与前者相比,通过比较反应产物来说明后者主要优点为_______ .;试回答能否以盐酸代替硫酸并说明理由_______ (回答“能”或“不能”并简要说明原因)。
(4)高温煅烧得到1mol超细LiNiO2所转移的电子数目为_______ 。

回答下列问题:
(1)正极材料粉碎的目的是
(2)DMF溶液无法溶解的铝单质可以用浓NaOH溶液溶解后再回收利用,写出溶解铝反应的离子反应方程式
(3)除C的方法可以是加入浓硝酸与过氧化氢的混合溶液,控制温度95℃,此时C与浓硝酸发生反应的化学方程式是
(4)高温煅烧得到1mol超细LiNiO2所转移的电子数目为
您最近一年使用:0次



