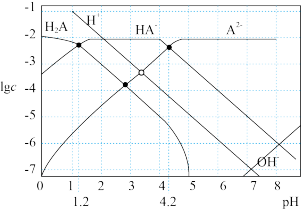
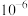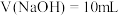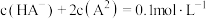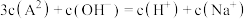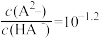已知H2A为二元弱酸,Ka1(H2A)=1.0×10 3,常温下向Na2A溶液中逐惭加入一元弱酸HB溶液,溶液离子浓度变化关系如图所示。下列说法正确的是
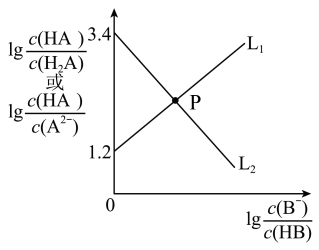
| A.K(HB)=10 2.8 |
| B.NaHA溶液呈碱性 |
| C.交点P对应溶液存在: c(H+)+c(A2-)+c(HA-)=c(B-)+c(OH-) |
| D.Na2A溶液中滴入足量HB溶液的离子方程式为A2-+HB=HA-+B- |
更新时间:2024-04-24 21:15:31
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列有关电解质溶液的说法正确的是
A.向0.1 mol·L−1CH3COOH溶液中加入少量水,溶液中 增大 增大 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向盐酸中加入氨水至中性,溶液中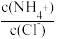 < 1 < 1 |
| D.在Na2S溶液中存在2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】25℃时,向NaHCO3溶液中滴入盐酸,混合溶液的pH与lg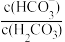 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是

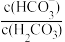 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是
| A.图中a=2.6 |
B.溶液中pH=7时,c(Na+)=2c(CO )+c(HCO )+c(HCO ) ) |
C.25℃时,HCO +H2O +H2O H2CO3+OH—的Kh=1.0×10-6.4 H2CO3+OH—的Kh=1.0×10-6.4 |
D.若图表示pH与lg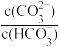 的关系,则曲线应在平行于曲线MN的下方 的关系,则曲线应在平行于曲线MN的下方 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐3】已知K2Cr2O7溶液中存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
+2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是

 +H2O
+H2O 2CrO
2CrO +2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
+2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
| A.图中T1℃>T2℃ |
B.t1后溶液中有2c(Cr2O )+c(CrO )+c(CrO )=c(K+) )=c(K+) |
| C.T2℃时,上述反应的平衡常数的数量级是10-12 |
D.T1℃下,加入一定量K2Cr2O7固体后达到新平衡时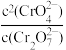 的值增大 的值增大 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,向一定浓度的 Ba(OH)2溶液中滴入某浓度的 NH4HSO4 溶液,其导电能力随滴入溶液体积的变化如图所示。下列说法正确的是


| A.b 点溶液中只存在 H2O 的电离平衡和 BaSO4的沉淀溶解平衡 |
| B.bc 段水的电离程度先增大后减小 |
| C.c 点溶液中:c(NH4+)> c(SO42-)> c(NH3·H2O)> c(H+) |
| D.bc 段之间存在某点,其溶液中:c(NH4+)=2c(SO42-) |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】40℃时,在氨-水体系中不断通入CO2,各种离子的变化趋势如下图所示,不正确 的是()
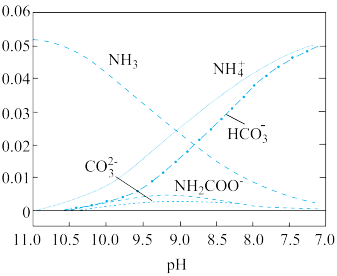

A.在pH=9.0时,c(NH )>c(HCO )>c(HCO )>c(NH2COOˉ)>c(CO )>c(NH2COOˉ)>c(CO ) ) |
B.在氨-水体系中不断通入CO2,体系中始终存在关系:c(NH )+c(H+)=2c(CO )+c(H+)=2c(CO )+c(HCO )+c(HCO )+c(OHˉ) )+c(OHˉ) |
C.随着CO2的通入, 不断减小 不断减小 |
| D.pH=7时,水的电离程度最大 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,用 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中 和
和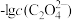 的关系如图所示,已知:
的关系如图所示,已知: 的电离平衡常数
的电离平衡常数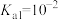 ,下列说法错误的是
,下列说法错误的是

 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中 和
和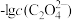 的关系如图所示,已知:
的关系如图所示,已知: 的电离平衡常数
的电离平衡常数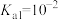 ,下列说法错误的是
,下列说法错误的是
A.常温下, 的电离平衡常数 的电离平衡常数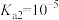 |
B. 溶液呈酸性 溶液呈酸性 |
C.滴定过程中,当 时, 时,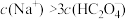 |
D.滴定过程中, 不变 不变 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25℃时,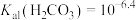 、
、 。取两份10mL
。取两份10mL 的
的 溶液,一份滴加
溶液,一份滴加 的盐酸,另一份滴加
的盐酸,另一份滴加 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法正确的是
NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法正确的是

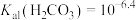 、
、 。取两份10mL
。取两份10mL 的
的 溶液,一份滴加
溶液,一份滴加 的盐酸,另一份滴加
的盐酸,另一份滴加 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法正确的是
NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法正确的是
A.由a点可知: 溶液中 溶液中 的水解程度小于电离程度 的水解程度小于电离程度 |
B.a→b→c过程中: 逐渐减小 逐渐减小 |
C.a→d→e过程中: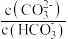 的值逐渐增大 的值逐渐增大 |
D.b、d两点对应的溶液中: |
您最近半年使用:0次

 溶液中滴加
溶液中滴加 溶液,
溶液, 的百分含量
的百分含量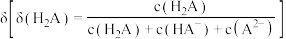 随溶液
随溶液 的变化如图所示:
的变化如图所示:
 的数量级为
的数量级为