铜是常见的、用途广泛的金属元素之一、
(1)基态Cu原子核外未成对电子所在的原子轨道是_______ 。
(2)一价铜离子某配合物的结构如图所示:_______ 。
②上述配合物中所含元素电负性由大到小的顺序为_______ (用元素符号表示)。
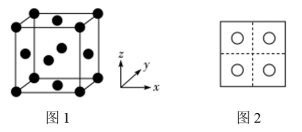
(3)常见的铜的氧化物有CuO和 两种。已知:CuO晶胞中
两种。已知:CuO晶胞中 的位置如图1所示;两种晶胞中
的位置如图1所示;两种晶胞中 和
和 的位置相同,其在晶胞侧视图中的位置相同(如图2),假设两种晶胞的参数相同,CuO晶体的密度是
的位置相同,其在晶胞侧视图中的位置相同(如图2),假设两种晶胞的参数相同,CuO晶体的密度是 。
。 、
、 、
、_______ 和_______ 。
② 晶体的密度是
晶体的密度是_______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态Cu原子核外未成对电子所在的原子轨道是
(2)一价铜离子某配合物的结构如图所示:

②上述配合物中所含元素电负性由大到小的顺序为
(3)常见的铜的氧化物有CuO和
 两种。已知:CuO晶胞中
两种。已知:CuO晶胞中 的位置如图1所示;两种晶胞中
的位置如图1所示;两种晶胞中 和
和 的位置相同,其在晶胞侧视图中的位置相同(如图2),假设两种晶胞的参数相同,CuO晶体的密度是
的位置相同,其在晶胞侧视图中的位置相同(如图2),假设两种晶胞的参数相同,CuO晶体的密度是 。
。
 、
、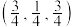 、
、②
 晶体的密度是
晶体的密度是 (用含
(用含 的代数式表示)。
的代数式表示)。
更新时间:2024-05-02 16:14:34
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】Al、Fe、Cu 是重要的材料元素,在生产生活中有着广泛的应用。回答下列问题:
1.(1)基态Fe2+的核外电子排布式为[Ar]______ ,有__ 个未成对电子。
2.(2)氯化铝熔点为194℃,而氧化铝熔点为2050℃,二者熔点相差很大的原因是_____ 。
3.(3)已知Al 的第一电离能为578kJ/mol、第二电离能为1817 kJ/mol、第三电离能为2745 kJ/mol、第四电离能为11575 kJ/mol。请解释其第二电离能增幅较大的原因________ 。
4.(4)甲醇重整制氢反应中,铜基催化剂如CuO/SiO2具有重整温度低、催化选择性高的优点。Cu、Si、O元素电负性由大到小的顺序是____ ;SiO2中Si原子采取____ 杂化。
5.(5)一种铜的溴化物晶胞结构如图所示:该晶胞中铜的配位数是___ ,与溴紧邻的溴原子数目是________ ,由图中P点和Q点的原子坐标参数可确定R点的原子坐标参数为________ ;已知晶胞参数为apm,其密度为_______ g/cm3 (列出计算式即可)。
1.(1)基态Fe2+的核外电子排布式为[Ar]
2.(2)氯化铝熔点为194℃,而氧化铝熔点为2050℃,二者熔点相差很大的原因是
3.(3)已知Al 的第一电离能为578kJ/mol、第二电离能为1817 kJ/mol、第三电离能为2745 kJ/mol、第四电离能为11575 kJ/mol。请解释其第二电离能增幅较大的原因
4.(4)甲醇重整制氢反应中,铜基催化剂如CuO/SiO2具有重整温度低、催化选择性高的优点。Cu、Si、O元素电负性由大到小的顺序是
5.(5)一种铜的溴化物晶胞结构如图所示:该晶胞中铜的配位数是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】下表为长式周期表的一部分其中的编号代表对应的元素。
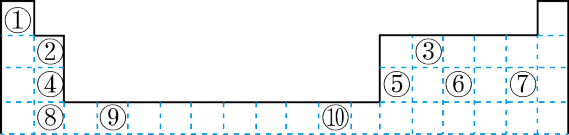
请回答下列问题:
(1)表中属于 ds 区的元素是___________ (填元素符号)它的基态原子的价电子排布式为___________ 。
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为___________ ,其中元素③的基态原子的电子排布图为_______ ;①和⑥形成的一种常见四原子分子的化学式为_______ ,该分子的立体构型为______ 。
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为___________ ;该元素与元素①形成的最简单分子 X 的电子式为___________ 。
(4)元素⑤的电负性___________ ④元素的电负性(选填>、=、<下同);元素⑥的第一电离能___________ 原子序数为 16 的元素的第一电离能。
(5)用电子式表示元素④和⑦组成的化合物的形成过程___________ 。

请回答下列问题:
(1)表中属于 ds 区的元素是
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为
(4)元素⑤的电负性
(5)用电子式表示元素④和⑦组成的化合物的形成过程
您最近一年使用:0次
【推荐3】火药是我国古代四大发明之一、黑火药爆炸时发生反应:S+2KNO3+3C=K2S+N2↑+3CO2↑,CuSO4能与K2S反应生成CuS沉淀。回答下列问题:
(1)基态Cu原子价电子排布图为___________ ,基态S原子核外电子空间运动状态有___________ 种。
(2)C、N、O的电负性从大到小的顺序为___________ ,(CN)2分子中σ键与π键的个数比为___________ 。
(3)KNO3中N原子的杂化方式为___________ ,与 互为等电子体的其中一种阴离子的化学式为
互为等电子体的其中一种阴离子的化学式为___________ 。
(4)C3N4晶体和金刚石结构类似,且金刚石的熔点比C3N4低,分析其原因:___________ 。
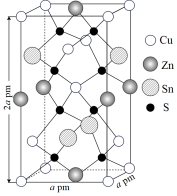
(5)已知含铜矿石一锌黄锡矿(K型)是制备薄膜太阳能电池的重要原料,其晶胞结构如图所示(晶胞参数α=β=γ= 90°)。该晶体的化学式为___________ , 晶体密度ρ=___________ g·cm-3)(用含有NA的代数式表示)。
(1)基态Cu原子价电子排布图为
(2)C、N、O的电负性从大到小的顺序为
(3)KNO3中N原子的杂化方式为
 互为等电子体的其中一种阴离子的化学式为
互为等电子体的其中一种阴离子的化学式为(4)C3N4晶体和金刚石结构类似,且金刚石的熔点比C3N4低,分析其原因:
(5)已知含铜矿石一锌黄锡矿(K型)是制备薄膜太阳能电池的重要原料,其晶胞结构如图所示(晶胞参数α=β=γ= 90°)。该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】(1)下列反应可用于检测司机是否酒后驾驶: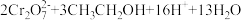
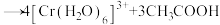 。
。
①配合物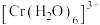 中,与
中,与 形成配位键的原子是
形成配位键的原子是__________ (填元素符号)。
② 中
中 原子的杂化轨道类型是
原子的杂化轨道类型是________ ;
 含有
含有 键的数目为
键的数目为_______ 。
(2) 分子中,
分子中, 原子的杂化轨道类型是
原子的杂化轨道类型是__________ ;写出由3个原子组成且与 具有相同空间构型的离子:
具有相同空间构型的离子:___________ (填一个即可)。
(3)石墨烯(结构如图1所示)是一种由单层碳原子构成的具有平面结构的新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(结构如图2所示)。
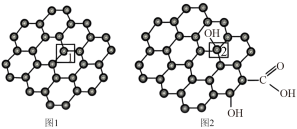
氧化石墨烯中2号 原子的杂化方式是
原子的杂化方式是_________ ,该 原子与相邻
原子与相邻 原子形成的键角
原子形成的键角______ (填“>”“<”或“=”)石墨烯中1号 与相邻
与相邻 形成的键角。
形成的键角。
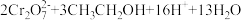
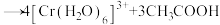 。
。①配合物
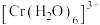 中,与
中,与 形成配位键的原子是
形成配位键的原子是②
 中
中 原子的杂化轨道类型是
原子的杂化轨道类型是
 含有
含有 键的数目为
键的数目为(2)
 分子中,
分子中, 原子的杂化轨道类型是
原子的杂化轨道类型是 具有相同空间构型的离子:
具有相同空间构型的离子:(3)石墨烯(结构如图1所示)是一种由单层碳原子构成的具有平面结构的新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(结构如图2所示)。

氧化石墨烯中2号
 原子的杂化方式是
原子的杂化方式是 原子与相邻
原子与相邻 原子形成的键角
原子形成的键角 与相邻
与相邻 形成的键角。
形成的键角。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】K4[Fe(CN)6]可用作食盐的抗结剂,高温下K4[Fe(CN)6]会分解生成(CN)2、KCN、N2、Fe3C、C等物质。
(1)基态铁原子的价电子排布式为___ ;上述物质中涉及的几种元素的第一电离能由大到小的顺序为___ ;[Fe(CN)6]4-中,铁提供的空轨道数目是___ 。
(2)(CN)2分子中存在碳碳键,则(CN)2的立体构型是__ ,分子中σ键与π键数目之比为___ ;KCN与盐酸作用可形成HCN,HCN的中心原子的杂化轨道类型为___ 。
(3)已知Fe3C的晶胞结构中碳原子的配位数为6,与碳原子紧邻的铁原子的空间构型为___ ,铁原子的配位数是___ 。
(4)碳元素可形成多种结构和性质不同的单质,其中金刚石的熔点为3550℃,C60的熔点约为280℃,导致这种差异的原因是___ 。
(5)铁、镍位于同一族,若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为___ 。一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为am,每平方米面积上分散的该晶体的质量为___ g。(用a、NA表示)
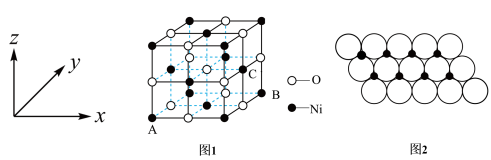
(1)基态铁原子的价电子排布式为
(2)(CN)2分子中存在碳碳键,则(CN)2的立体构型是
(3)已知Fe3C的晶胞结构中碳原子的配位数为6,与碳原子紧邻的铁原子的空间构型为
(4)碳元素可形成多种结构和性质不同的单质,其中金刚石的熔点为3550℃,C60的熔点约为280℃,导致这种差异的原因是
(5)铁、镍位于同一族,若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为

您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】化合物G可用于药用多肽的结构修饰,其人工合成路线如下:

(1)G分子中官能团名称___________ 。
(2)A→B的反应类型为___________ ,E→F过程1)的反应类型为___________
(3)D中碳原子的杂化类型有___________ 。
(4)写出C→D的化学方程式___________ 。
(5)F的分子式为C12H17NO2,其结构简式为___________ 。
(6)A的同分异构体中满足下列条件的有___________ 种。
①遇FeCl3 溶液呈紫色 ②能发生水解 ③苯环上含两个取代基,且不含其它环
写出其中核磁共振氢谱有6个峰,且峰面积之比为2:2:1:1:1:1的分子的结构简式___________ 。

(1)G分子中官能团名称
(2)A→B的反应类型为
(3)D中碳原子的杂化类型有
(4)写出C→D的化学方程式
(5)F的分子式为C12H17NO2,其结构简式为
(6)A的同分异构体中满足下列条件的有
①遇FeCl3 溶液呈紫色 ②能发生水解 ③苯环上含两个取代基,且不含其它环
写出其中核磁共振氢谱有6个峰,且峰面积之比为2:2:1:1:1:1的分子的结构简式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】某研究小组探究白色难溶盐X(含五种元素,M<200 g•mol-1)的组成,进行如图实验:
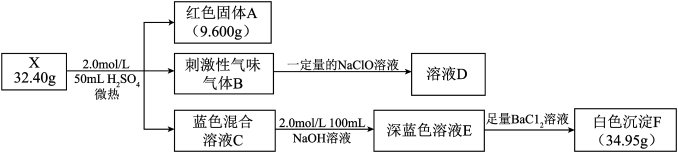
已知:固体A为常见单质:气体B能使品红褪色,实验测得气体体积为3.36L(标准状况),为防止污染环境,实验过程中用NaClO溶液吸收;溶液E中含有两种溶质,且阴离子相同。
请回答下列问题:
(1)X除含有H、O元素,还含有_________ 元素。
(2)混合溶液C中的溶质主要有_________ (填化学式)。
(3)可用气体B通入深蓝色溶液E制备X,写出相应的离子方程式________ 。
(4)设计实验方案证明吸收气体B的NaClO溶液已过量:_________ 。

已知:固体A为常见单质:气体B能使品红褪色,实验测得气体体积为3.36L(标准状况),为防止污染环境,实验过程中用NaClO溶液吸收;溶液E中含有两种溶质,且阴离子相同。
请回答下列问题:
(1)X除含有H、O元素,还含有
(2)混合溶液C中的溶质主要有
(3)可用气体B通入深蓝色溶液E制备X,写出相应的离子方程式
(4)设计实验方案证明吸收气体B的NaClO溶液已过量:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】三氯化六氨合钴(Ⅲ)是一种重要的配合物原料,实验室制备实验流程如下:
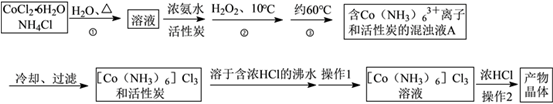
已知:[Co(NH3)6]Cl3在水中电离为[Co(NH3)6]3+和Cl-,[Co(NH3)6]Cl3的溶解度如下表:
(1)第①步需在煮沸NH4Cl溶液中加入研细的CoCl2·6H2O晶体,加热煮沸与研细的目的是__
(2)实验室制备三氯化六氨合钴(III)的化学方程式为:____________
(3)实验操作1为_________ [Co(NH3)6]Cl3溶液中加入浓盐酸的目的是_____
(4)现称取0.2675g[Co(NH3)6]Cl3(相对分子质量为267.5),在A中发生如下反应:[Co(NH3)6]Cl3+3NaOH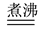 Co(OH)3↓+6NH3↑+3NaCl(装置见右下图),C中装0.5000mol·L-1的盐酸25.00mL,D中装有冰水。加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端外壁上粘附的酸液于C中,加入2-3滴甲基红指示剂,用0.5000mol·L-1的NaOH滴定。
Co(OH)3↓+6NH3↑+3NaCl(装置见右下图),C中装0.5000mol·L-1的盐酸25.00mL,D中装有冰水。加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端外壁上粘附的酸液于C中,加入2-3滴甲基红指示剂,用0.5000mol·L-1的NaOH滴定。

已知: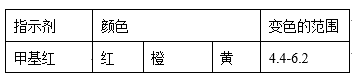
①当滴定到终点时,共需消耗NaOH溶液___ mL(准确到0.01mL)。
②当用上述原理测定某[Co(NH3)x]Cl3晶体中x值,实验过程中未用少量蒸馏水冲洗导管下端内外壁上粘附的酸液于C中,则x值将______ (填“偏大”、“偏小”或“不变”)
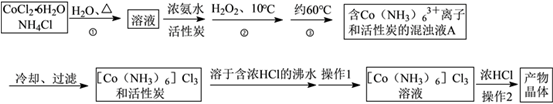
已知:[Co(NH3)6]Cl3在水中电离为[Co(NH3)6]3+和Cl-,[Co(NH3)6]Cl3的溶解度如下表:
| 温度(℃) | 0 | 20 | 47 |
| 溶解度(g) | 4.26 | 6.96 | 12.74 |
(1)第①步需在煮沸NH4Cl溶液中加入研细的CoCl2·6H2O晶体,加热煮沸与研细的目的是
(2)实验室制备三氯化六氨合钴(III)的化学方程式为:
(3)实验操作1为
(4)现称取0.2675g[Co(NH3)6]Cl3(相对分子质量为267.5),在A中发生如下反应:[Co(NH3)6]Cl3+3NaOH
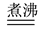 Co(OH)3↓+6NH3↑+3NaCl(装置见右下图),C中装0.5000mol·L-1的盐酸25.00mL,D中装有冰水。加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端外壁上粘附的酸液于C中,加入2-3滴甲基红指示剂,用0.5000mol·L-1的NaOH滴定。
Co(OH)3↓+6NH3↑+3NaCl(装置见右下图),C中装0.5000mol·L-1的盐酸25.00mL,D中装有冰水。加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端外壁上粘附的酸液于C中,加入2-3滴甲基红指示剂,用0.5000mol·L-1的NaOH滴定。
已知:

①当滴定到终点时,共需消耗NaOH溶液
②当用上述原理测定某[Co(NH3)x]Cl3晶体中x值,实验过程中未用少量蒸馏水冲洗导管下端内外壁上粘附的酸液于C中,则x值将
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】人体必需的元素包括常量元素与微量元素,常量元素包括碳、氢、氧、氮、钙、镁等,微量元素包括铁、铜、锌、氟、碘等,这些元素形成的化合物种类繁多,应用广泛。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出 的核外电子排布式
的核外电子排布式_______ 。
(2)1个 与2个
与2个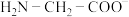 形成含两个五元环结构的内配盐(化合物),其结构简式为
形成含两个五元环结构的内配盐(化合物),其结构简式为_______ (用 标出配位键),在
标出配位键),在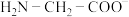 中,属于第二周期的元素的第一电离能由大到小的顺序是
中,属于第二周期的元素的第一电离能由大到小的顺序是_______ (用元素符号表示), 、
、 原子存在的相同杂化方式是
原子存在的相同杂化方式是_______ 杂化。
(3)碱酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径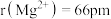 ,
,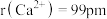 ,
, ,
,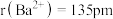 ;碳酸盐分解温度
;碳酸盐分解温度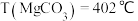 ,
,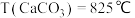 ,
,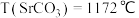 ,
,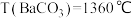 。分析数据得出的规律是
。分析数据得出的规律是_______ ,解释出现此规律的原因是_______ 。
(4)自然界的氟化钙矿物为萤石或氟石, 的晶体结构呈立方体形,其结构如下:
的晶体结构呈立方体形,其结构如下:
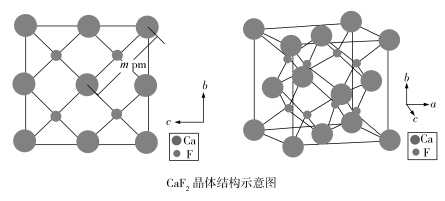
①两个最近的 之间的距离是
之间的距离是_______  (用含m的代数式表示)。
(用含m的代数式表示)。
② 晶胞的密度是
晶胞的密度是_______  (化简至带根号的最简式,
(化简至带根号的最简式, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出
 的核外电子排布式
的核外电子排布式(2)1个
 与2个
与2个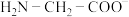 形成含两个五元环结构的内配盐(化合物),其结构简式为
形成含两个五元环结构的内配盐(化合物),其结构简式为 标出配位键),在
标出配位键),在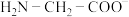 中,属于第二周期的元素的第一电离能由大到小的顺序是
中,属于第二周期的元素的第一电离能由大到小的顺序是 、
、 原子存在的相同杂化方式是
原子存在的相同杂化方式是(3)碱酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径
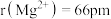 ,
,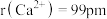 ,
, ,
,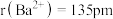 ;碳酸盐分解温度
;碳酸盐分解温度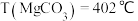 ,
,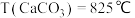 ,
,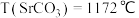 ,
,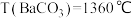 。分析数据得出的规律是
。分析数据得出的规律是(4)自然界的氟化钙矿物为萤石或氟石,
 的晶体结构呈立方体形,其结构如下:
的晶体结构呈立方体形,其结构如下:
①两个最近的
 之间的距离是
之间的距离是 (用含m的代数式表示)。
(用含m的代数式表示)。②
 晶胞的密度是
晶胞的密度是 (化简至带根号的最简式,
(化简至带根号的最简式, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的 微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。回答下列问题:
微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(2)乙二胺 是一种有机化合物,分子中氮的杂化类型分别是
是一种有机化合物,分子中氮的杂化类型分别是___________ 。乙二胺能与 等金属离子形成稳定环状离子,其原因是
等金属离子形成稳定环状离子,其原因是___________ 。
(3)一些氧化物的熔点如下表所示:
解释表中氧化物之间熔点差异的原因___________ 。
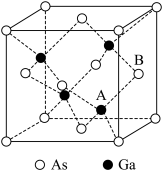
(4)原子晶体GaAs的晶胞参数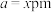 ,它的晶胞结构如图所示。该晶胞内部存在的共价键数为
,它的晶胞结构如图所示。该晶胞内部存在的共价键数为___________ ;A原子距离B原子所在六面体的侧面的最短距离为___________ (用x表示)pm;该晶胞的密度为___________  。(阿伏加德罗常数用
。(阿伏加德罗常数用 表示)。
表示)。
 微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。回答下列问题:
微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。回答下列问题:(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A.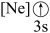 | B.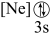 | C.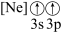 | D. |
 是一种有机化合物,分子中氮的杂化类型分别是
是一种有机化合物,分子中氮的杂化类型分别是 等金属离子形成稳定环状离子,其原因是
等金属离子形成稳定环状离子,其原因是(3)一些氧化物的熔点如下表所示:
| 氧化物 |  | MgO |  |  |
| 熔点/℃ | 1570 | 2800 | 23.8 | 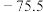 |
解释表中氧化物之间熔点差异的原因

(4)原子晶体GaAs的晶胞参数
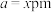 ,它的晶胞结构如图所示。该晶胞内部存在的共价键数为
,它的晶胞结构如图所示。该晶胞内部存在的共价键数为 。(阿伏加德罗常数用
。(阿伏加德罗常数用 表示)。
表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】铬是人体内微量元素之一,是重要的血糖调节剂。
(1)铬在元素周期表中的位置为___________ ,其基态原子核外电子占据的原子轨道数为___________ 。
(2)已知 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。
①该配合物中提供孤电子对形成配位键的原子是___________ 。
②配体中中心原子的杂化方式为___________ (填字母)。
a. b.
b. c.sp d.
c.sp d.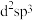
③该物质中, 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是___________ 。
(3)钛铬合金是一种高温结构材料,第二电离能
___________ (填“ ”或“
”或“ ”)
”)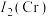 ,原因是
,原因是___________ 。
(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为 ,则B点分数坐标为
,则B点分数坐标为___________ ,已知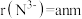 ,
,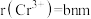 ,则AB间距离为
,则AB间距离为___________ nm。
(1)铬在元素周期表中的位置为
(2)已知
 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。①该配合物中提供孤电子对形成配位键的原子是
②配体中中心原子的杂化方式为
a.
 b.
b. c.sp d.
c.sp d.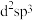
③该物质中,
 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是(3)钛铬合金是一种高温结构材料,第二电离能

 ”或“
”或“ ”)
”)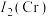 ,原因是
,原因是(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为
 ,则B点分数坐标为
,则B点分数坐标为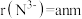 ,
,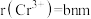 ,则AB间距离为
,则AB间距离为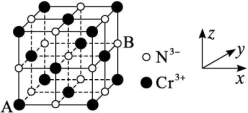
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】铜、钛、硼及其化合物有许多用途。回答下列问题:
(1)S、O、N三种元素的第一电离能由大到小的顺序为___________ , 中阴离子的空间构型为
中阴离子的空间构型为___________ 。
(2) 的熔点是
的熔点是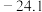 ℃,沸点是136.4℃,则固态
℃,沸点是136.4℃,则固态 属于
属于___________ 晶体。
(3)基态硼原子的核外电子排布图为___________ ,硼酸的层状结构如图甲,其中B的杂化类型是___________ 。
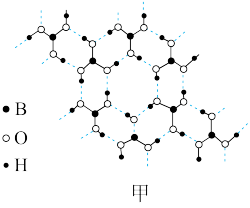
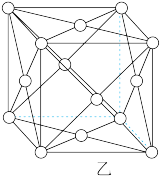
(4)铜的晶胞结构如图乙,铜原子的配位数为___________ ,若铜原子的半径为apm,则铜晶体的密度为___________  (写表达式即可)。
(写表达式即可)。
(1)S、O、N三种元素的第一电离能由大到小的顺序为
 中阴离子的空间构型为
中阴离子的空间构型为(2)
 的熔点是
的熔点是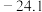 ℃,沸点是136.4℃,则固态
℃,沸点是136.4℃,则固态 属于
属于(3)基态硼原子的核外电子排布图为

(4)铜的晶胞结构如图乙,铜原子的配位数为
 (写表达式即可)。
(写表达式即可)。
您最近一年使用:0次



