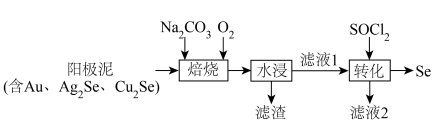
硒是一种重要的微量元素,具有生命、环境和工业应用。常从阳极泥中制备单质硒,流程图如下所示,下列说法错误的是
A.“焙烧”中产生 |
B.滤渣的主要成分 |
C.滤液1显碱性一定是因为 的水解 的水解 |
D. 水解后产生的 水解后产生的 起还原作用 起还原作用 |
更新时间:2024-05-14 20:33:53
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作和现象所得到的结论正确的是
| 实验操作和现象 | 结论 | |
| A | 相同条件下,分别测量0.1 mol·L-1和0.01 mol·L-1醋酸溶液的导电性,前者的导电性强 | 醋酸浓度越大,电离程度越大 |
| B | 向Co2O3固体中滴加浓盐酸,有黄绿色气体生成 | 氧化性:Co2O3>Cl2 |
| C | 向滴有酚酞的Na2CO3溶液中逐滴加入BaCl2溶液,溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
| D | 常温下,分别测量浓度均为0.1 mol·L-1的Na2S溶液和NaClO溶液的pH,前者的pH大 | 酸性:HClO>H2S |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25 ℃时,相同物质的量浓度的下列溶液:①NaCl 、②NaOH、③H2SO4 、④(NH4)2SO4、⑤Ba(OH)2、⑥CH3COONa、⑦NH4Cl、⑧HCl,其中pH值按由大到小顺序排列的一组是( )
| A.⑤②①⑥⑦④③⑧ | B.⑤②⑥①⑦④⑧③ |
| C.③⑧④⑦①⑥②⑤ | D.⑤②①③⑧⑦④⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,如果用0.100mol·L-1盐酸滴定10mL0.100mol·L-1Na2CO3溶液,滴定曲线如图所示。下列有关说法不正确的是( )


| A.a点:由水电离产生的c(OH-)=10-24mol·L-1 |
| B.b点:c(Na+)>c(HCO3-)>c(Cl-)>c(CO32-)>c(OH-)>c(H+) |
| C.滴定过程任何一点溶液中都符合:c(Cl-)+c(HCO3-)+2c(CO32-)+c(OH-)-c(H+)=0.2mol·L-1 |
| D.e至f点溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)<0.05mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】可用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程如下,下列说法错误是
盐卤 Mg(OH)2
Mg(OH)2 MgCl2溶液
MgCl2溶液 MgCl2•6H2O
MgCl2•6H2O MgCl2
MgCl2 Mg
Mg
盐卤
 Mg(OH)2
Mg(OH)2 MgCl2溶液
MgCl2溶液 MgCl2•6H2O
MgCl2•6H2O MgCl2
MgCl2 Mg
Mg| A.若在实验室进行操作①只需要漏斗和烧杯两种玻璃仪器 |
| B.操作①发生的反应为非氧化还原反应 |
| C.操作②是蒸发浓缩结晶 |
| D.在整个制备过程中,未发生置换反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】铝氢化钠(NaAlH4)是有机合成中的一种重要还原剂。 以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝氢化钠的一种工艺流程如图:

下列说法中不正确的是

下列说法中不正确的是
| A.为了提高“碱溶”效率,在“碱溶”前对铝土矿进行粉碎 |
| B.“反应III”为氧化还原反应 |
| C.“滤渣”的主要成分在高温下可与铝单质发生化学反应 |
| D.“滤渣”的主要成分为氧化铁 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一种制备 的改进装置如图所示,下列说法错误的是
的改进装置如图所示,下列说法错误的是

 的改进装置如图所示,下列说法错误的是
的改进装置如图所示,下列说法错误的是
A.配制 溶液时需加入硫酸 溶液时需加入硫酸 |
B.实验时先注入稀硫酸,再注入NaOH溶液和 溶液 溶液 |
| C.装置N的作用是液封,并判断装置M中的空气是否排尽 |
D.用铁粉代替 粉末,也能排尽空气 粉末,也能排尽空气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】类比推理是学习化学的重要的思维方法,下列陈述Ⅰ及类比推理陈述Ⅱ均正确的是
| 选项 | 陈述Ⅰ | 类比推理陈述Ⅱ |
| A | 单质的熔点 Br2 < I2 | 单质的熔点 Li < Na |
| B | 工业上电解熔融的 Al2O3 得到铝单质 | 工业上电解熔融的 MgO 得到镁单质 |
| C | 还原性:I->Br- | 还原性:P3->N3- |
| D | 实验室:Cl2+2KBr(aq)=2KCl(aq)+Br2 | 实验室:F2+2KBr(aq)=2KF(aq)+Br2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 、
、 、
、 )为原料制备
)为原料制备 的流程如图所示。已知水浸后溶液中主要存在的离子是
的流程如图所示。已知水浸后溶液中主要存在的离子是 、
、 、
、 、
、 。
。


 较小
较小 制取并得到纯净干燥的CO气体,合适的组合装置是
制取并得到纯净干燥的CO气体,合适的组合装置是


