题型:解答题-结构与性质
难度:0.65
引用次数:40
题号:22830554
国产大飞机C919的制造使用了较多含硼材料(如硼纤维、氮化硼等),多项技术打破了外国垄断。
(1)立方氮化硼硬度大,熔点为3000℃,其晶体类型为___________ 。
(2)耐高温材料立方BN制备流程中用到NH3、BCl3和触媒剂Ca3B2N4。
①Ca、B、N三种元素电负性从大到小的顺序为___________ 。
②BCl3中B原子的___________ 轨道与Cl原子的___________ 轨道形成 键;形成BCl3过程中,基态B原子价电子层上的电子先激发,再杂化,激发后B原子的价电子轨道表示式为
键;形成BCl3过程中,基态B原子价电子层上的电子先激发,再杂化,激发后B原子的价电子轨道表示式为___________ 。
③BCl3在四氯化碳中的溶解度远大于NH3,原因是___________ 。
(3)近年来硼氢类离子液体作为火箭推进剂燃料得到了广泛使用。该化合物(如图所示)中不存在的作用力有___________ (填字母)。 键 E.
键 E. 键 F.氢键
键 F.氢键
(4)硼化钙晶胞结构如图所示,B原子构成B6,正八面体,各个顶点通过B-B键互相连接成三维骨架,八个B6多面体围成立方体,中心为Ca。硼化钙的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。已知Ca原子的分数坐标为(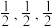 ),B6正八面体中B-B键的键长为r pm,晶胞参数为a pm,则A点原子的分数坐标为
),B6正八面体中B-B键的键长为r pm,晶胞参数为a pm,则A点原子的分数坐标为___________ 。
(1)立方氮化硼硬度大,熔点为3000℃,其晶体类型为
(2)耐高温材料立方BN制备流程中用到NH3、BCl3和触媒剂Ca3B2N4。
①Ca、B、N三种元素电负性从大到小的顺序为
②BCl3中B原子的
 键;形成BCl3过程中,基态B原子价电子层上的电子先激发,再杂化,激发后B原子的价电子轨道表示式为
键;形成BCl3过程中,基态B原子价电子层上的电子先激发,再杂化,激发后B原子的价电子轨道表示式为③BCl3在四氯化碳中的溶解度远大于NH3,原因是
(3)近年来硼氢类离子液体作为火箭推进剂燃料得到了广泛使用。该化合物(如图所示)中不存在的作用力有

 键 E.
键 E. 键 F.氢键
键 F.氢键(4)硼化钙晶胞结构如图所示,B原子构成B6,正八面体,各个顶点通过B-B键互相连接成三维骨架,八个B6多面体围成立方体,中心为Ca。硼化钙的化学式为
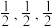 ),B6正八面体中B-B键的键长为r pm,晶胞参数为a pm,则A点原子的分数坐标为
),B6正八面体中B-B键的键长为r pm,晶胞参数为a pm,则A点原子的分数坐标为
2024·陕西榆林·三模 查看更多[1]
(已下线)2024届陕西省榆林市高三下学期第四次模拟检测(三模)理综试题-高中化学
更新时间:2024-05-16 17:07:27
|
相似题推荐
【推荐1】某市售照明材料LED晶片是一种发光二极管。材质组成为:GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、GaInN(氮化镓铟)等。请回答下列问题:
(1)砷基态原子的核外电子排布式为______________________ 。
(2)上述非金属元素氢化物的沸点从高到低的顺序为___________ 。
(3)下列说法正确的是___________
a.电负性:As<Ga b.SiC与GaAs互为等电子体 c.第一电离能:As>Se>Ga
(4)如图所示为GaAs的晶胞结构,晶体熔点为1237℃。

①晶胞中砷与镓原子间的化学键类型有___________ 。
②一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是___________ 。
③一个晶胞的组成为___________ 。
④已知晶胞棱长a=5.64×10-10m,则该晶胞密度为ρ=___________ 。
(1)砷基态原子的核外电子排布式为
(2)上述非金属元素氢化物的沸点从高到低的顺序为
(3)下列说法正确的是
a.电负性:As<Ga b.SiC与GaAs互为等电子体 c.第一电离能:As>Se>Ga
(4)如图所示为GaAs的晶胞结构,晶体熔点为1237℃。

①晶胞中砷与镓原子间的化学键类型有
②一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是
③一个晶胞的组成为
④已知晶胞棱长a=5.64×10-10m,则该晶胞密度为ρ=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W、J是元素周期表前四周期中的五种常见元素。其相关信息如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是 ______ ;
(2)元素Y位于元素周期表第______ 周期第 ______ 族;
(3)元素Z的原子最外层共有______ 种不同运动状态的电子;
(4)W的基态原子核外电子排布式是____ ,W的基态原子核外价电子排布图是 ______ ;
(5)元素Y与元素Z相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是 ______ ;
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
(6)Y、Z两元素的最高价氧化物对应的水化物的酸性较强的是______ (用化学式表示);比较下列物质的酸性强弱HZO ______ HZO3。
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
| J | J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐 |
(2)元素Y位于元素周期表第
(3)元素Z的原子最外层共有
(4)W的基态原子核外电子排布式是
(5)元素Y与元素Z相比,非金属性较强的是
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
(6)Y、Z两元素的最高价氧化物对应的水化物的酸性较强的是
您最近一年使用:0次
【推荐3】钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用,由相应的分析方法可以得到这些物质的各类数据,回答下列问题。
(1)关于下列分析方法的描述错误的是______
(2)K和Na属于同主族元素。
①写出Na原子的核外电子排布图_______ 。
②金属Na的熔点比金属K高,试解释原因_______ 。
(3)某晶体具有良好的光学性质,其晶胞结构如如图所示,该立方体晶胞的边长均为0.446nm。
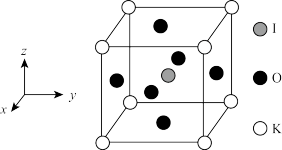
①该晶体的化学式为_______
②该晶体中与I原子紧邻的O原子个数为_______ ,I的原子坐标为_______ 。
③该晶体的密度为_______  (列出算式即可,阿伏加德罗常数用NA表示)
(列出算式即可,阿伏加德罗常数用NA表示)
(1)关于下列分析方法的描述错误的是______
| A.X射线衍射数据可分析原子在晶胞中的数目、位置 |
| B.原子发射光谱数据可以分析出化学键的键长和键角 |
| C.红外光谱属于分子光谱,可用于分析官能团的种类 |
| D.质谱法可用于分析有机物的相对分子质量 |
①写出Na原子的核外电子排布图
②金属Na的熔点比金属K高,试解释原因
(3)某晶体具有良好的光学性质,其晶胞结构如如图所示,该立方体晶胞的边长均为0.446nm。

①该晶体的化学式为
②该晶体中与I原子紧邻的O原子个数为
③该晶体的密度为
 (列出算式即可,阿伏加德罗常数用NA表示)
(列出算式即可,阿伏加德罗常数用NA表示)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】原子序数小于36的X、Y、Z、W四种元素,其中X原子核外电子只有一种运动状态,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W在周期表的位置为第四周期IB族。
回答下列问题:
(1)1molY2X4含有σ键的数目______ NA。
(2)元素X、Y、Z可形成一种一元弱酸分子,其中Y原子的杂化轨道类型为______ 。
(3)向含W2+离子的溶液中逐滴加入氨水,发生反应的现象为______ ,用离子方程式表示:______ ,继续加入氨水,会看到的现象为______ ,用离子方程式表示:______ 。
回答下列问题:
(1)1molY2X4含有σ键的数目
(2)元素X、Y、Z可形成一种一元弱酸分子,其中Y原子的杂化轨道类型为
(3)向含W2+离子的溶液中逐滴加入氨水,发生反应的现象为
您最近一年使用:0次
【推荐2】氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是______ 。在第二周期中,第一电离能介于B和N之间的有______ 种元素。
(2)NH3BH3分子中,N—B化学键称为____ 键,其电子对由____ 提供。氨硼烷在催化剂作用下水解释放氢气: 3NH3BH3+6H2O=3NH3+ +9H2,
+9H2, 的结构如图所示:;
的结构如图所示:;
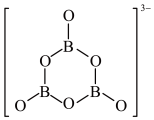
在该反应中,B原子的杂化轨道类型由______ 变为______ 。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是______ 。与NH3BH3互为等电子体的分子是_____ 。
(1)H、B、N中,原子半径最大的是
(2)NH3BH3分子中,N—B化学键称为
 +9H2,
+9H2, 的结构如图所示:;
的结构如图所示:;
在该反应中,B原子的杂化轨道类型由
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知和碳元素同主族的X元素位于元素周期表中的第一个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们形成化合物的分子式是XY4。试回答:
(1)X元素的基态原子的电子排布式:____ ,Y元素原子最外层电子的轨道表示式:____ 。
(2)若X、Y两元素电负性分别为1.8和3.0,试判断XY4中X与Y之间的化学键为____ (填“共价键”或“离子键”)。
(3)该化合物的空间结构为____ 形,中心原子的轨道杂化类型为____ ,分子为____ (填“极性分子”或“非极性分子”)。
(4)该化合物在常温下为液体,该液体微粒间的作用力是____ 。
(5)该化合物的沸点与SiCl4比较:____ (填化学式)的高,原因是____ 。
(1)X元素的基态原子的电子排布式:
(2)若X、Y两元素电负性分别为1.8和3.0,试判断XY4中X与Y之间的化学键为
(3)该化合物的空间结构为
(4)该化合物在常温下为液体,该液体微粒间的作用力是
(5)该化合物的沸点与SiCl4比较:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:

回答下列问题:
(1)基态铜原子的电子排布式为___________ ,硫、氧元素相比,第一电离能较小的元素是___________ (填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是___________ ,其立体结构是___________ 。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液 蓝色沉淀
蓝色沉淀 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式___________ ;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有___________ 。
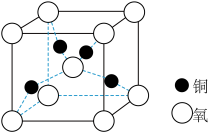
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为___________ ;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为___________ pm。(用含d和NA的式子表示)。

回答下列问题:
(1)基态铜原子的电子排布式为
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液
 蓝色沉淀
蓝色沉淀 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】锌的化合物在生产生活中有广泛的应用。
(1)L-赖氨酸锌螯合物X (结构为如图)易被人体吸收。

①X中元素(除H外)的第一电离能由小到大的顺序为_______ ,加“*”氧原子的杂化方式为_______ 。
②X的晶体中存在的微粒间作用力有._______ 。
A.离子键 B. π键 C.金属键 D.配位键 E.非极性键
③L-赖氨酸易溶于水主要原因是_______ 。
(2)某锌铁氧体[化学式为ZnxFe(III)yOz]制成的磁芯被广泛用于电子行业。
①组成微粒的原子(或离子)中存在未成对电子,该微粒具有顺磁性。指出锌铁氧体晶体中具有顺磁性的离子,并说明理由_______ 。
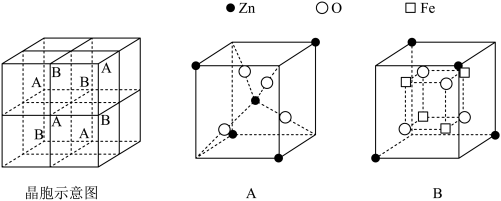
②锌铁氧体晶胞结构如图所示,该晶胞由4个A型和4个B型小立方体构成。锌铁氧体的化学式为_______ 。
(1)L-赖氨酸锌螯合物X (结构为如图)易被人体吸收。

①X中元素(除H外)的第一电离能由小到大的顺序为
②X的晶体中存在的微粒间作用力有.
A.离子键 B. π键 C.金属键 D.配位键 E.非极性键
③L-赖氨酸易溶于水主要原因是
(2)某锌铁氧体[化学式为ZnxFe(III)yOz]制成的磁芯被广泛用于电子行业。
①组成微粒的原子(或离子)中存在未成对电子,该微粒具有顺磁性。指出锌铁氧体晶体中具有顺磁性的离子,并说明理由
②锌铁氧体晶胞结构如图所示,该晶胞由4个A型和4个B型小立方体构成。锌铁氧体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硼、氮、磷、钴、镍等元素的化合物在现代农业、科技、国防中有着许多独特的用途。
(1)磷原子在成键时,能将一个 电子激发到
电子激发到 能级而参与成键,写出该激发态磷原子的核外电子排布式:
能级而参与成键,写出该激发态磷原子的核外电子排布式:___________ 。
(2)钴位于元素周期表的___________ 区,钴与 易形成正八面体形的
易形成正八面体形的 配离子,试推测
配离子,试推测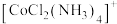 的空间构型有
的空间构型有___________ 种。
(3)制备氮化硼 的一种方法为
的一种方法为 。立方氮化硼(
。立方氮化硼( )的晶胞如图1所示,其晶体类型为
)的晶胞如图1所示,其晶体类型为___________ ,N的配位数为___________ 。试用价层电子对互斥理论解释 的键角比
的键角比 大的原因:
大的原因:___________ 。
(4)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物。 的一种螯合物的结构如图2所示,
的一种螯合物的结构如图2所示, 该配合物中通过螯合作用形成的配位键有
该配合物中通过螯合作用形成的配位键有___________  。
。

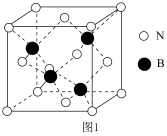
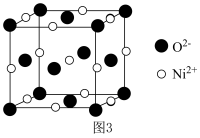
(5) 晶胞为
晶胞为 型结构(如图3)。其中
型结构(如图3)。其中 可看成填充在
可看成填充在 组成的
组成的________ 空隙中,填充率为 。将
。将 在空气中加热,部分
在空气中加热,部分 被氧化为
被氧化为 ,成为
,成为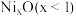 ,晶体仍保持电中性,则会出现晶体缺陷,填充率下降。现有
,晶体仍保持电中性,则会出现晶体缺陷,填充率下降。现有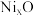 晶胞的质量为
晶胞的质量为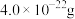 。则填充
。则填充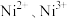 和未填充
和未填充 离子的空隙个数之比为
离子的空隙个数之比为___________ 。
(1)磷原子在成键时,能将一个
 电子激发到
电子激发到 能级而参与成键,写出该激发态磷原子的核外电子排布式:
能级而参与成键,写出该激发态磷原子的核外电子排布式:(2)钴位于元素周期表的
 易形成正八面体形的
易形成正八面体形的 配离子,试推测
配离子,试推测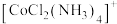 的空间构型有
的空间构型有(3)制备氮化硼
 的一种方法为
的一种方法为 。立方氮化硼(
。立方氮化硼( )的晶胞如图1所示,其晶体类型为
)的晶胞如图1所示,其晶体类型为 的键角比
的键角比 大的原因:
大的原因:
(4)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物。
 的一种螯合物的结构如图2所示,
的一种螯合物的结构如图2所示, 该配合物中通过螯合作用形成的配位键有
该配合物中通过螯合作用形成的配位键有 。
。
(5)
 晶胞为
晶胞为 型结构(如图3)。其中
型结构(如图3)。其中 可看成填充在
可看成填充在 组成的
组成的 。将
。将 在空气中加热,部分
在空气中加热,部分 被氧化为
被氧化为 ,成为
,成为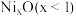 ,晶体仍保持电中性,则会出现晶体缺陷,填充率下降。现有
,晶体仍保持电中性,则会出现晶体缺陷,填充率下降。现有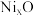 晶胞的质量为
晶胞的质量为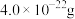 。则填充
。则填充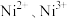 和未填充
和未填充 离子的空隙个数之比为
离子的空隙个数之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铋的化合物在电催化和光催化领域都有广泛应用。一种以氧化铋渣(主要成分是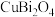 、
、 、
、 和
和 等)为原料,制取高纯
等)为原料,制取高纯 的工业流程如图所示:
的工业流程如图所示:
回答下列问题:
(1)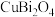 中的Cu的化合价为+2,则Bi的化合价是
中的Cu的化合价为+2,则Bi的化合价是_______ ,Bi与N同族,Bi原子处于基态时电子占据最高能级的电子云轮廓图为_______ 形。
(2)“沉铋”时加入NaOH溶液, 转化为BiOCl沉淀的离子方程式是
转化为BiOCl沉淀的离子方程式是_______ 。
(3)“洗涤”滤饼时先用水洗,再用稀硫酸洗涤(已知:BiOCl不溶于稀硫酸),用稀硫酸洗涤的目的是为了除去滤饼中的_______ (填化学式)杂质。
(4)“转化”过程中BiOCl转化为 沉淀,当溶液中
沉淀,当溶液中 浓度为
浓度为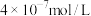 时溶液的pH为
时溶液的pH为_______ 。(该温度下,已知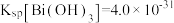 )
)
(5)硫代乙酰胺(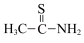 )中碳原子的杂化方式分别为
)中碳原子的杂化方式分别为_______ 。
(6)钼酸铋( )可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为
)可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为 ,晶胞棱边夹角均为90°。
,晶胞棱边夹角均为90°。 ,则原子2的分数坐标为
,则原子2的分数坐标为_______ 。
②设阿伏加德罗常数的值为 ,
, 的相对分子质量为
的相对分子质量为 ,则
,则 晶体的密度为
晶体的密度为_______  。
。
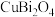 、
、 、
、 和
和 等)为原料,制取高纯
等)为原料,制取高纯 的工业流程如图所示:
的工业流程如图所示: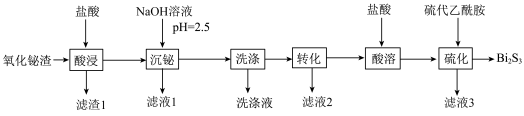
| 离子 |  |  |  |
| 开始沉淀的pH | 1.5 | 3.6 | 4.5 |
| 沉淀完全的pH | 3.2 | 4.7 | 6.7 |
(1)
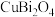 中的Cu的化合价为+2,则Bi的化合价是
中的Cu的化合价为+2,则Bi的化合价是(2)“沉铋”时加入NaOH溶液,
 转化为BiOCl沉淀的离子方程式是
转化为BiOCl沉淀的离子方程式是(3)“洗涤”滤饼时先用水洗,再用稀硫酸洗涤(已知:BiOCl不溶于稀硫酸),用稀硫酸洗涤的目的是为了除去滤饼中的
(4)“转化”过程中BiOCl转化为
 沉淀,当溶液中
沉淀,当溶液中 浓度为
浓度为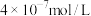 时溶液的pH为
时溶液的pH为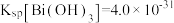 )
)(5)硫代乙酰胺(
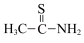 )中碳原子的杂化方式分别为
)中碳原子的杂化方式分别为(6)钼酸铋(
 )可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为
)可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为 ,晶胞棱边夹角均为90°。
,晶胞棱边夹角均为90°。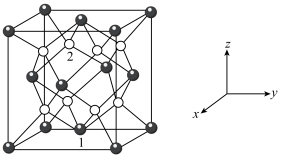
 ,则原子2的分数坐标为
,则原子2的分数坐标为②设阿伏加德罗常数的值为
 ,
, 的相对分子质量为
的相对分子质量为 ,则
,则 晶体的密度为
晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】铁、铜及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)基态Fe原子核外电子的运动状态有_______ 种;试从结构角度解释Fe2+易被氧化为Fe3+的原因 _______ 。
(2)K3[Fe(CN)6]是检验Fe2+的特征试剂,[Fe(CN)6]3-中心离子配位数是_______ ;1mol[Fe(CN)6]3-中含有 _______ molσ键,能够证明[Fe(CN)6]3-不能电离的试剂是 _______ (填化学式)。
(3)Cu2+可形成配合物[Cu(en)2](BF4)2,其中en代表H2NCH2CH2NH2分子。该配合物[Cu(en)2](BF4)2中配位离子所带电荷数为_______ ,VSEPR模型为四面体的非金属原子共有 _______ 个。
(4)一种由Cu、In,Te组成的晶体,晶胞参数如图所示,晶胞棱边夹角均为90°。

该晶体的化学式为_______ ;A点、B点原子的分数坐标分别为(0,0,0)、( ,
, ,
, ),则C点原子的分数坐标为
),则C点原子的分数坐标为 _______ ;晶胞中A、D原子间距离d=_______ pm。
(1)基态Fe原子核外电子的运动状态有
(2)K3[Fe(CN)6]是检验Fe2+的特征试剂,[Fe(CN)6]3-中心离子配位数是
(3)Cu2+可形成配合物[Cu(en)2](BF4)2,其中en代表H2NCH2CH2NH2分子。该配合物[Cu(en)2](BF4)2中配位离子所带电荷数为
(4)一种由Cu、In,Te组成的晶体,晶胞参数如图所示,晶胞棱边夹角均为90°。

该晶体的化学式为
 ,
, ,
, ),则C点原子的分数坐标为
),则C点原子的分数坐标为
您最近一年使用:0次
【推荐3】镍(Ni)、钴(Co) 、钛(Ti)是重要的金属,在材料科学等领域应用广泛。
(1)Ni在元素周期表中的位置是_______ , 其价电子层中有______ 个未成对电子。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属于______ ( 填“极性”“非极性”)分子,其立体构型为_______ 。
(3)铁、钴、镍三种元素并称铁系元素,它们的性质相似。某含镍化合物的结构如图所示,则分子内不可能含有_ (填字母)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键

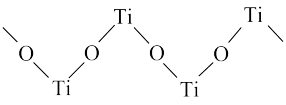
(4)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如图所示,其化学式为____ 。阴离子 中硫原子的杂化方式为
中硫原子的杂化方式为________ ,写出一种与 互为等电子体的分子:
互为等电子体的分子:_______ 。
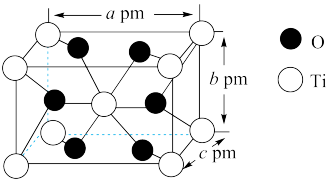
(5)自然界的钛主要以金红石(主要成分为TiO2 )的形式存在。TiO2的晶胞属于四方晶系,其长方体结构如图所示,已知TiO2的摩尔质量为Mg·mol-1,阿伏加 德罗常数的数值为NA,根据图中所示数据可知该晶体的密度ρ=______ (用NA表示阿伏加 德罗常数的数值,用含M、a、b、c、NA的代数式表示)g·cm-3。
(1)Ni在元素周期表中的位置是
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属于
(3)铁、钴、镍三种元素并称铁系元素,它们的性质相似。某含镍化合物的结构如图所示,则分子内不可能含有
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键

(4)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如图所示,其化学式为
 中硫原子的杂化方式为
中硫原子的杂化方式为 互为等电子体的分子:
互为等电子体的分子:
(5)自然界的钛主要以金红石(主要成分为TiO2 )的形式存在。TiO2的晶胞属于四方晶系,其长方体结构如图所示,已知TiO2的摩尔质量为Mg·mol-1,阿伏加 德罗常数的数值为NA,根据图中所示数据可知该晶体的密度ρ=

您最近一年使用:0次



