废 催化剂(含
催化剂(含 、
、 、
、 等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。
等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。 、
、 和
和 都能与NaOH溶液反应生成可溶性的
都能与NaOH溶液反应生成可溶性的 、
、 和不溶性的
和不溶性的 ;②
;② 易水解;③
易水解;③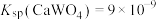 。
。
回答下列问题:
(1)基态钒原子的价层电子轨道表示式为:___________ 。
(2)碱浸步骤可以提高浸取率的操作有___________ (列举两项)。
(3)碱浸后可通过减压过滤的方式分离Ti与V、W,减压过滤的优点是___________ 。
(4)酸浸后Ti以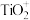 形式存在,热水解步骤的离子方程式为
形式存在,热水解步骤的离子方程式为___________ 。
(5)“沉钒”中析出 时,需要加入过量
时,需要加入过量 ,其目的是
,其目的是___________ 。
(6)向10mL0.1mol/L 的滤液中加入等体积的
的滤液中加入等体积的 溶液(忽略混合过程中的体积变化),欲使
溶液(忽略混合过程中的体积变化),欲使 浓度小于
浓度小于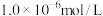 ,则
,则 溶液的最小浓度为
溶液的最小浓度为___________ mol/L。
(7)铝热法常用于冶炼高熔点金属,写出铝热法冶炼W的化学方程式___________ 。
 催化剂(含
催化剂(含 、
、 、
、 等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。
等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。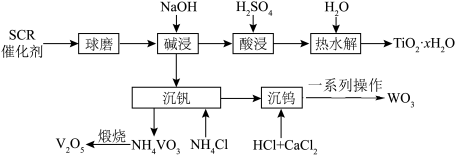
 、
、 和
和 都能与NaOH溶液反应生成可溶性的
都能与NaOH溶液反应生成可溶性的 、
、 和不溶性的
和不溶性的 ;②
;② 易水解;③
易水解;③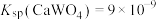 。
。回答下列问题:
(1)基态钒原子的价层电子轨道表示式为:
(2)碱浸步骤可以提高浸取率的操作有
(3)碱浸后可通过减压过滤的方式分离Ti与V、W,减压过滤的优点是
(4)酸浸后Ti以
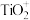 形式存在,热水解步骤的离子方程式为
形式存在,热水解步骤的离子方程式为(5)“沉钒”中析出
 时,需要加入过量
时,需要加入过量 ,其目的是
,其目的是(6)向10mL0.1mol/L
 的滤液中加入等体积的
的滤液中加入等体积的 溶液(忽略混合过程中的体积变化),欲使
溶液(忽略混合过程中的体积变化),欲使 浓度小于
浓度小于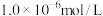 ,则
,则 溶液的最小浓度为
溶液的最小浓度为(7)铝热法常用于冶炼高熔点金属,写出铝热法冶炼W的化学方程式
更新时间:2024-05-27 12:38:04
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】中药药剂砒霜(主要成分为As2O3,微溶于水),可用于治疗急性白血病。工业上用含硫化砷(As2S3)的废渣生产砒霜的工艺流程如图1所示:

(1)硫化砷中砷元素化合价为_______ ,其难溶于水,“碱浸”过程中硫元素价态不变,发生的主要反应的离子方程式为_______ 。
(2)氧化脱硫过程中被氧化的元素是_______ 。
(3)还原过程中H3AsO4转化为H3AsO3,反应的化学方程式是_______ 。
(4)还原后加热溶液,H3AsO3分解为As2O3,结晶得到粗As2O3。As2O3在不同温度和不同浓度硫酸中的溶解度(S)曲线如图2所示。
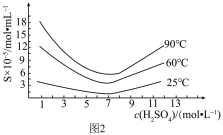
为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为_______ 。
(5)在工业生产中,最后一步所得滤液可循环使用,其目的是_______ 。
(6)砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
①砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图3写出As2O5分解为As2O3的热化学方程式_______ 。

②砷酸钠具有氧化性,298K时,在100mL烧杯中加入10mL0.1mol/LNa3AsO4溶液、20mL0.1mol/LKI溶液和20mL0.05mol/L硫酸溶液,发生下列反应:AsO (无色)+2I-+2H+
(无色)+2I-+2H+ AsO
AsO (无色)+I2(浅黄色)+H2O,测得溶液中c(I2)与时间(t)的关系如图4所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是
(无色)+I2(浅黄色)+H2O,测得溶液中c(I2)与时间(t)的关系如图4所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是_______ (填字母代号)。

a.溶液颜色保持不再变化 b.c(AsO )+c(AsO
)+c(AsO )不再变化
)不再变化
c.AsO 的生成速率等于I2的生成速率 d.
的生成速率等于I2的生成速率 d. 保持不再变化
保持不再变化

(1)硫化砷中砷元素化合价为
(2)氧化脱硫过程中被氧化的元素是
(3)还原过程中H3AsO4转化为H3AsO3,反应的化学方程式是
(4)还原后加热溶液,H3AsO3分解为As2O3,结晶得到粗As2O3。As2O3在不同温度和不同浓度硫酸中的溶解度(S)曲线如图2所示。

为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为
(5)在工业生产中,最后一步所得滤液可循环使用,其目的是
(6)砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
①砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图3写出As2O5分解为As2O3的热化学方程式

②砷酸钠具有氧化性,298K时,在100mL烧杯中加入10mL0.1mol/LNa3AsO4溶液、20mL0.1mol/LKI溶液和20mL0.05mol/L硫酸溶液,发生下列反应:AsO
 (无色)+2I-+2H+
(无色)+2I-+2H+ AsO
AsO (无色)+I2(浅黄色)+H2O,测得溶液中c(I2)与时间(t)的关系如图4所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是
(无色)+I2(浅黄色)+H2O,测得溶液中c(I2)与时间(t)的关系如图4所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是
a.溶液颜色保持不再变化 b.c(AsO
 )+c(AsO
)+c(AsO )不再变化
)不再变化c.AsO
 的生成速率等于I2的生成速率 d.
的生成速率等于I2的生成速率 d. 保持不再变化
保持不再变化
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】 在磁性材料、电化学领域应用广泛。以钴矿[主要成分是
在磁性材料、电化学领域应用广泛。以钴矿[主要成分是 、
、 、
、 ,还含
,还含 及少量
及少量 、
、 、
、 及
及 等]为原料可制取
等]为原料可制取 。步骤如下:
。步骤如下:
(1)浸取:用盐酸和 溶液浸取钴矿,浸取液中含有
溶液浸取钴矿,浸取液中含有 、
、 、
、 、
、 、
、 、
、 、
、 等离子。写出
等离子。写出 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(2)除杂:向浸取液中先加入足量 氧化
氧化 ,再加入
,再加入 调节
调节 除去
除去 、
、 、
、 。有关沉淀数据如表(“完全沉淀”时金属离子浓度
。有关沉淀数据如表(“完全沉淀”时金属离子浓度 ):
):
若浸取液中 ,则须调节溶液
,则须调节溶液 的范围是
的范围是_______ (加入 和
和 时,溶液的体积变化忽略)。
时,溶液的体积变化忽略)。
(3)萃取、反萃取:向除杂后的溶液中,加入某有机酸萃取剂 ,发生反应:
,发生反应: 。实验测得:当溶液
。实验测得:当溶液 处于
处于 范围内,
范围内, 萃取率随溶液
萃取率随溶液 的增大而增大(如图所示),其原因是
的增大而增大(如图所示),其原因是_______ 。向萃取所得有机相中加入 ,反萃取得到水相。该工艺中设计萃取、反萃取的目的是
,反萃取得到水相。该工艺中设计萃取、反萃取的目的是_______ 。

(4)沉钴、热分解:向反萃取后得到的水相中加入 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 固体,加热
固体,加热 制备
制备 。
。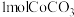 在空气中加热,反应温度对反应产物的影响如图所示,请写出
在空气中加热,反应温度对反应产物的影响如图所示,请写出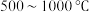 时,发生主要反应的化学方程式
时,发生主要反应的化学方程式_______ 。

(5)一种钴氧化物晶胞如图所示,该氧化物中钴离子核外电子排布式为_______ 。
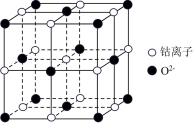
 在磁性材料、电化学领域应用广泛。以钴矿[主要成分是
在磁性材料、电化学领域应用广泛。以钴矿[主要成分是 、
、 、
、 ,还含
,还含 及少量
及少量 、
、 、
、 及
及 等]为原料可制取
等]为原料可制取 。步骤如下:
。步骤如下:(1)浸取:用盐酸和
 溶液浸取钴矿,浸取液中含有
溶液浸取钴矿,浸取液中含有 、
、 、
、 、
、 、
、 、
、 、
、 等离子。写出
等离子。写出 发生反应的离子方程式:
发生反应的离子方程式:(2)除杂:向浸取液中先加入足量
 氧化
氧化 ,再加入
,再加入 调节
调节 除去
除去 、
、 、
、 。有关沉淀数据如表(“完全沉淀”时金属离子浓度
。有关沉淀数据如表(“完全沉淀”时金属离子浓度 ):
):| 沉淀 |  |  |  |  |  |
恰好完全沉淀时的 | 5.2 | 2.8 | 9.4 | 6.7 | 10.1 |
 ,则须调节溶液
,则须调节溶液 的范围是
的范围是 和
和 时,溶液的体积变化忽略)。
时,溶液的体积变化忽略)。(3)萃取、反萃取:向除杂后的溶液中,加入某有机酸萃取剂
 ,发生反应:
,发生反应: 。实验测得:当溶液
。实验测得:当溶液 处于
处于 范围内,
范围内, 萃取率随溶液
萃取率随溶液 的增大而增大(如图所示),其原因是
的增大而增大(如图所示),其原因是 ,反萃取得到水相。该工艺中设计萃取、反萃取的目的是
,反萃取得到水相。该工艺中设计萃取、反萃取的目的是
(4)沉钴、热分解:向反萃取后得到的水相中加入
 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 固体,加热
固体,加热 制备
制备 。
。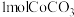 在空气中加热,反应温度对反应产物的影响如图所示,请写出
在空气中加热,反应温度对反应产物的影响如图所示,请写出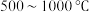 时,发生主要反应的化学方程式
时,发生主要反应的化学方程式
(5)一种钴氧化物晶胞如图所示,该氧化物中钴离子核外电子排布式为

您最近一年使用:0次
【推荐3】从报废后的锂电池(主要成分为LiCoO2,此外含铁、铝、铜、锰、镍等)中回收有关物质,回收工艺流程如下:

(1)操作②的名称为_______________ ,操作①的目的是___________________________ 。
(2)写出酸浸过程中LiCoO2发生氧化还原反应的化学方程式_______________________ 。
(3)室温下,各物质的Ksp如下表所示:(已知:lg2=0.3、1g6=0.8)
若水相中各金属离子浓度均为0.1mol/L,且离子浓度小于1.0×10-5mol/L,即认为该离子已完全除去,操作②需调节溶液pH的取值范围为_________ 。(保留1位小数)
(4)某锂离子电池正极材料含有LiNi1/3Co1/3Mn1/3O2,其中Ni、Co的化合价分别为+2、+3,则Mn的化合价为_______ 。该材料可通过回收的Ni(1-x-y)CoxMnyCO3与LiOH·H2O烧结得到,反应中不能隔绝空气,其原因是_______________________________________________________ 。

(1)操作②的名称为
(2)写出酸浸过程中LiCoO2发生氧化还原反应的化学方程式
(3)室温下,各物质的Ksp如下表所示:(已知:lg2=0.3、1g6=0.8)
| 物质 | Al(OH)3 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 |
| Ksp | 1×10-35 | 2×10-13 | 6×10-15 | 4×10-15 |
若水相中各金属离子浓度均为0.1mol/L,且离子浓度小于1.0×10-5mol/L,即认为该离子已完全除去,操作②需调节溶液pH的取值范围为
(4)某锂离子电池正极材料含有LiNi1/3Co1/3Mn1/3O2,其中Ni、Co的化合价分别为+2、+3,则Mn的化合价为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】一种利用钢铁厂烟灰(含Fe、Mn、SiO2,少量的Al2O3、CaO及MgO)制备MnCO3的工艺流程如下:

已知25℃时,下列难溶物的溶度积常数:
回答下列问题:
(1)步骤(Ⅰ)浸渣的主要成分是______________ (填化学式)。
(2)步骤(Ⅱ)加H2O2溶液时反应的离子方程式为________________ ;
加氨水调节pH沉铁铝时,步骤(Ⅲ)应调节的pH适宜范围为____________ 。(部分金属离子开始沉淀与沉淀完全的pH范围如下)
(3)步骤(Ⅳ)用KF溶液沉钙镁时,要使c(Ca2+)、c(Mg2+)均小于1×10-6mol·L-1,则应控制反应液中c(F-)>___________ mol·L-1;反应MgF2(s)+Ca2+ CaF2(s)+Mg2+的平衡常数K=
CaF2(s)+Mg2+的平衡常数K=___________ 。
(4)步骤Ⅴ沉锰时,在60℃按投料比n[(NH4)2CO3]/n(Mn2+)=2,溶液的pH对MnCO3产率的影响如图所示;pH=7,按投料比n[(NH4)2CO3]/n(Mn2+)=2,反应温度对MnCO3产率的影响如图所示。

①上图中,在pH<7.0时,pH越小产率____________ (填“越高”或“越低”;在pH>7.0时,pH越大产率越低且纯度也降低,其原因是___________________ 。

②上图中,温度高于60℃时,温度越高产率越低且纯度也越低,主要原因是______________ 。

已知25℃时,下列难溶物的溶度积常数:
| 难溶物 | CaF2 | MgF2 | MnCO3 | Mn(OH)2 |
| Ksp | 4.0×10-11 | 6.4×10-9 | 2.2×10-11 | 1.9×10-13 |
(1)步骤(Ⅰ)浸渣的主要成分是
(2)步骤(Ⅱ)加H2O2溶液时反应的离子方程式为
加氨水调节pH沉铁铝时,步骤(Ⅲ)应调节的pH适宜范围为
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 沉淀pH范围 | 7.6~9.6 | 2.7~3.7 | 3.4~5.2 | 8.3~9.3 | 9.6~11.1 |
 CaF2(s)+Mg2+的平衡常数K=
CaF2(s)+Mg2+的平衡常数K=(4)步骤Ⅴ沉锰时,在60℃按投料比n[(NH4)2CO3]/n(Mn2+)=2,溶液的pH对MnCO3产率的影响如图所示;pH=7,按投料比n[(NH4)2CO3]/n(Mn2+)=2,反应温度对MnCO3产率的影响如图所示。

①上图中,在pH<7.0时,pH越小产率

②上图中,温度高于60℃时,温度越高产率越低且纯度也越低,主要原因是
您最近一年使用:0次
【推荐2】下面是某科研小组利用废铁屑还原浸出软锰矿(主要成分为 )制备硫酸锰及电解其溶液制锰的工艺流程图:
)制备硫酸锰及电解其溶液制锰的工艺流程图:
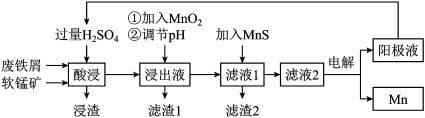
已知:①浸出液中主要含有 、
、 、
、 、
、 等杂质金属离子;
等杂质金属离子;
②生成氢氧化物的pH见下表:
③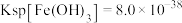 ,
,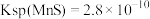 ,
,

请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是_______ 。
(2)流程图中“①加入 ”的作用是
”的作用是_______ ,其离子方程式是_______ 。
(3)流程图中“②调节pH”可以除去某种金属离子,应将溶液pH调节控制的范围是_______ 。
(4)向滤液I中加入 的作用是除去
的作用是除去 、
、 等离子,其中可以发生反应为
等离子,其中可以发生反应为 等。当该反应完全后,滤液2中的
等。当该反应完全后,滤液2中的 与
与 的物质的量浓度之比是
的物质的量浓度之比是_______ 。
(5)滤液2电解制Mn的电极方程式为_______ 。
 )制备硫酸锰及电解其溶液制锰的工艺流程图:
)制备硫酸锰及电解其溶液制锰的工艺流程图:
已知:①浸出液中主要含有
 、
、 、
、 、
、 等杂质金属离子;
等杂质金属离子;②生成氢氧化物的pH见下表:
| 物质 |  |  |  |  |
| 开始沉淀的pH | 7.5 | 7.7 | 7.6 | 8.3 |
| 完全沉淀的pH | 9.7 | 8.4 | 8.2 | 9.8 |
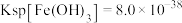 ,
, ,
,

请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是
(2)流程图中“①加入
 ”的作用是
”的作用是(3)流程图中“②调节pH”可以除去某种金属离子,应将溶液pH调节控制的范围是
(4)向滤液I中加入
 的作用是除去
的作用是除去 、
、 等离子,其中可以发生反应为
等离子,其中可以发生反应为 等。当该反应完全后,滤液2中的
等。当该反应完全后,滤液2中的 与
与 的物质的量浓度之比是
的物质的量浓度之比是(5)滤液2电解制Mn的电极方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】实验室以天青石精矿(主要含 ,还含有少量的
,还含有少量的 、
、 、
、 )为原料制取
)为原料制取 ,其实验流程如图所示:
,其实验流程如图所示:

(1)室温下,反应 达到平衡,则反应的平衡常数为(结果保留至0.1)
达到平衡,则反应的平衡常数为(结果保留至0.1)_____ 。[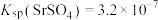 ,
, ]
]
(2)已知常温下, ,
,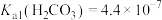 ,
,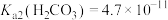 。
。
①常温下,0.1
 溶液中
溶液中
_____ (填“>”“<”或“=”) 。
。
②常温下,实测某人血液中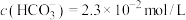 ,
, ,则人体血液呈
,则人体血液呈_____ 性。
③浸取天青石精矿时,向 溶液中加入适量浓氨水的目的是
溶液中加入适量浓氨水的目的是_____ 。
(3)“沉淀"过程中除得到 外,还得到一种可循环利用的物质,该物质为
外,还得到一种可循环利用的物质,该物质为_____ 。
(4)“浸取Ⅰ”的条件是温度在60~70℃,搅拌、反应3小时,温度过高将会导致 的转化率下降,其原因是
的转化率下降,其原因是_____ 。
(5)将 与煤粉按照一定比例混合后高温煅烧得到一种黑灰(SrS),写出其反应的化学方程式:(写出一个即可)
与煤粉按照一定比例混合后高温煅烧得到一种黑灰(SrS),写出其反应的化学方程式:(写出一个即可)_____ 。
(6)检验“沉淀”步骤中是否沉淀完全的方法:_____ 。
 ,还含有少量的
,还含有少量的 、
、 、
、 )为原料制取
)为原料制取 ,其实验流程如图所示:
,其实验流程如图所示:
(1)室温下,反应
 达到平衡,则反应的平衡常数为(结果保留至0.1)
达到平衡,则反应的平衡常数为(结果保留至0.1)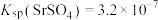 ,
, ]
](2)已知常温下,
 ,
,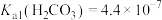 ,
,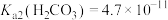 。
。①常温下,0.1

 溶液中
溶液中
 。
。②常温下,实测某人血液中
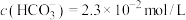 ,
, ,则人体血液呈
,则人体血液呈③浸取天青石精矿时,向
 溶液中加入适量浓氨水的目的是
溶液中加入适量浓氨水的目的是(3)“沉淀"过程中除得到
 外,还得到一种可循环利用的物质,该物质为
外,还得到一种可循环利用的物质,该物质为(4)“浸取Ⅰ”的条件是温度在60~70℃,搅拌、反应3小时,温度过高将会导致
 的转化率下降,其原因是
的转化率下降,其原因是(5)将
 与煤粉按照一定比例混合后高温煅烧得到一种黑灰(SrS),写出其反应的化学方程式:(写出一个即可)
与煤粉按照一定比例混合后高温煅烧得到一种黑灰(SrS),写出其反应的化学方程式:(写出一个即可)(6)检验“沉淀”步骤中是否沉淀完全的方法:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】以黄铜矿(主要成分为铁、铜、硫三种元素组成的化合物)为基本原料,通过一系列的冶炼可得到铜、铁、SO2、SO3、H2SO4等物质,回答下列问题:
(1)基态铁原子的价层电子排布图为____________ 。
(2)SO2、SO3、H2SO4中,硫原子的杂化轨道类型为sp3的物质是________ ,SO2的分子构型是____________ ,属于非极性分子的氧化物是___________ 。
(3)氧化铜的熔点为1326℃、沸点为1800℃;氧化亚铜的熔点为1235℃、沸点为1100℃,导致这种差异的原因是___________ 。
(4)SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸 。
。
①与SCN-互为等电子体的微粒_________ (用化学式表示,写一种即可)。
②异硫氰酸的沸点比硫氰酸沸点高的原因是_______________ 。
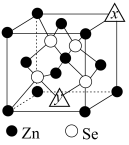
(5)硒化锌的晶胞结构如图所示,图中“△”处所堆积的原子均为________ (填元素符号);该晶胞中硒原子所处空隙类型为_________ (填“立方体”、“正四面体”或“正八面体”),该种空隙的填充率为__________ ;若该晶胞密度为 ,硒化锌的摩尔质量为M g/mol,用NA代表阿伏加德罗常数的数值,则晶胞参数a为
,硒化锌的摩尔质量为M g/mol,用NA代表阿伏加德罗常数的数值,则晶胞参数a为__________ nm。
(1)基态铁原子的价层电子排布图为
(2)SO2、SO3、H2SO4中,硫原子的杂化轨道类型为sp3的物质是
(3)氧化铜的熔点为1326℃、沸点为1800℃;氧化亚铜的熔点为1235℃、沸点为1100℃,导致这种差异的原因是
(4)SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸
 和异硫氰酸
和异硫氰酸 。
。①与SCN-互为等电子体的微粒
②异硫氰酸的沸点比硫氰酸沸点高的原因是
(5)硒化锌的晶胞结构如图所示,图中“△”处所堆积的原子均为
 ,硒化锌的摩尔质量为M g/mol,用NA代表阿伏加德罗常数的数值,则晶胞参数a为
,硒化锌的摩尔质量为M g/mol,用NA代表阿伏加德罗常数的数值,则晶胞参数a为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】A、B、C、D是四种短周期元素,E是过渡元素。A、B、C为同周期元素,C、D为同主族元素。A元素原子的结构示意图为 ,B元素原子是同周期除稀有气体元素原子外半径最大的元素原子,C元素原子的最外层有三个单电子,E元素原子的价电子排布式为3d64s2。回答下列问题:
,B元素原子是同周期除稀有气体元素原子外半径最大的元素原子,C元素原子的最外层有三个单电子,E元素原子的价电子排布式为3d64s2。回答下列问题:
(1)A为___ (填元素符号),其原子的电子排布式为___ 。
(2)B为___ (填元素符号),其原子的价电子排布式为__ 。
(3)C为___ (填元素符号),其原子的价电子排布图为___ 。
(4)D为___ (填元素符号)。
(5)E为____ (填元素符号),其原子结构示意图为__ 。
 ,B元素原子是同周期除稀有气体元素原子外半径最大的元素原子,C元素原子的最外层有三个单电子,E元素原子的价电子排布式为3d64s2。回答下列问题:
,B元素原子是同周期除稀有气体元素原子外半径最大的元素原子,C元素原子的最外层有三个单电子,E元素原子的价电子排布式为3d64s2。回答下列问题:(1)A为
(2)B为
(3)C为
(4)D为
(5)E为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】国产巨型载人飞艇AS700、歼20战机和C919国产大飞机等大国重器让世界瞩目。金属材料和复合材料在航空航天工业中具有重要的应用。回答下列问题:
(1)基态钛原子价层电子排布图为______ 。原子中运动电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的则用
表示,与之相反的则用 表示,称为电子的自旋磁量子数。对于基态钛原子,其价层电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态钛原子,其价层电子自旋磁量子数的代数和为______ 。
(2)以 为连续基体的碳陶瓷是一种复合材料,可应用于制造歼20。结构如图所示:
为连续基体的碳陶瓷是一种复合材料,可应用于制造歼20。结构如图所示:______ (填标号)。 晶体中硅原子与最近碳原子间距离为
晶体中硅原子与最近碳原子间距离为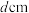 ,则硅原子与最近的硅原子间距离为
,则硅原子与最近的硅原子间距离为______  ,一个硅原子周围与其最近的硅原子的数目为
,一个硅原子周围与其最近的硅原子的数目为______ 。 晶体的密度为
晶体的密度为______  (用含有
(用含有 的式子表示)。
的式子表示)。
(1)基态钛原子价层电子排布图为
 表示,与之相反的则用
表示,与之相反的则用 表示,称为电子的自旋磁量子数。对于基态钛原子,其价层电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态钛原子,其价层电子自旋磁量子数的代数和为(2)以
 为连续基体的碳陶瓷是一种复合材料,可应用于制造歼20。结构如图所示:
为连续基体的碳陶瓷是一种复合材料,可应用于制造歼20。结构如图所示:
a.  b.
b.
c. 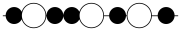 d.
d.
 晶体中硅原子与最近碳原子间距离为
晶体中硅原子与最近碳原子间距离为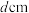 ,则硅原子与最近的硅原子间距离为
,则硅原子与最近的硅原子间距离为 ,一个硅原子周围与其最近的硅原子的数目为
,一个硅原子周围与其最近的硅原子的数目为 晶体的密度为
晶体的密度为 (用含有
(用含有 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】硫化碱法是工业制备 的方法之一,某研究小组在实验室用硫化碱法制备
的方法之一,某研究小组在实验室用硫化碱法制备 。其原理为:
。其原理为:
Ⅰ.完成下列填空:
(1)实验室制取 可选用的试剂是
可选用的试剂是_______ (选填编号)。
a.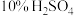 b.
b.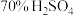 c.
c. 固体 d.
固体 d. 固体
固体
相应的制取装置可以是_______ (选填编号)。
Ⅱ.吸硫装置如图所示,通入 过程中,可观察到溶液中先析出黄色固体,其量先增多后又减小,当溶液
过程中,可观察到溶液中先析出黄色固体,其量先增多后又减小,当溶液 至7左右时,溶液接近无色,说明反应已完成。
至7左右时,溶液接近无色,说明反应已完成。

(2)实验过程中,欲检验A中 是否被充分吸收,B中试剂可以是
是否被充分吸收,B中试剂可以是_______ 。若观察到_______ ,表明A中 吸收效果好。
吸收效果好。
(3)为了使 尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是
尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是_______ (任写一条)。
(4)根据吸硫过程中的现象,可推测硫化碱法制备 的反应可以分为如下三步:
的反应可以分为如下三步:
第一步: (同时还发生
(同时还发生 )
)
第二步:_______ (用化学方程式表示);
第三步:_______ (用化学方程式表示)。
Ⅲ.反应完成后,装置A中的溶液经蒸发浓缩,冷却结晶可析出 ,其中可能含有少量
,其中可能含有少量 等杂质。
等杂质。
(5)设计实验方案,检测产品中是否存在 。
。_______
已知:① 微溶; ②
微溶; ②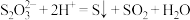
(6)提纯 晶体所用的方法是
晶体所用的方法是_______ 。
 的方法之一,某研究小组在实验室用硫化碱法制备
的方法之一,某研究小组在实验室用硫化碱法制备 。其原理为:
。其原理为:
Ⅰ.完成下列填空:
(1)实验室制取
 可选用的试剂是
可选用的试剂是a.
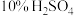 b.
b.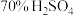 c.
c. 固体 d.
固体 d. 固体
固体相应的制取装置可以是
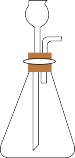 |  | 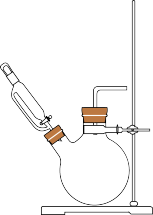 |
| a | b | c |
Ⅱ.吸硫装置如图所示,通入
 过程中,可观察到溶液中先析出黄色固体,其量先增多后又减小,当溶液
过程中,可观察到溶液中先析出黄色固体,其量先增多后又减小,当溶液 至7左右时,溶液接近无色,说明反应已完成。
至7左右时,溶液接近无色,说明反应已完成。
(2)实验过程中,欲检验A中
 是否被充分吸收,B中试剂可以是
是否被充分吸收,B中试剂可以是 吸收效果好。
吸收效果好。(3)为了使
 尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是
尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是(4)根据吸硫过程中的现象,可推测硫化碱法制备
 的反应可以分为如下三步:
的反应可以分为如下三步:第一步:
 (同时还发生
(同时还发生 )
)第二步:
第三步:
Ⅲ.反应完成后,装置A中的溶液经蒸发浓缩,冷却结晶可析出
 ,其中可能含有少量
,其中可能含有少量 等杂质。
等杂质。(5)设计实验方案,检测产品中是否存在
 。
。已知:①
 微溶; ②
微溶; ②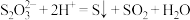
(6)提纯
 晶体所用的方法是
晶体所用的方法是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】KMnO4在生产和生活中有着广泛用途,某化学小组在实验室制备KMnO4并探究其性质。
(一) KMnO4的制备,分步骤Ⅰ、Ⅱ两步进行。
步聚Ⅰ.先利用如图所示装置制备K2MnO4。称取7.0gKOH(s)和5.0gKClO3(s)放入容器A中,加热,待混合物熔融后,加入5.0gMnO2(s),待反应物干涸后,加大火焰强热4~8min,得墨绿色的锰酸钾。
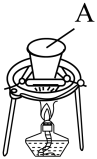
(1)A可选用_______ (填标号)。
①石英坩埚 ②瓷坩埚 ③铁坩埚
(2)实验中发生反应生成K2MnO4的化学方程式为_______ 。
Ⅱ.由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①待A处物料冷却后,用20mL4%KOH溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。
②向滤液中通入足量CO2,使K2MnO4歧化为KMnO4和MnO2,过滤出生成的MnO2。
③再将滤液进行一系列处理,得KMnO4晶体。
(3)过程②向滤液中通入足量CO2,可观察到的现象为_______ ;检验K2MnO4歧化完全的实验方法是_______ 。
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应: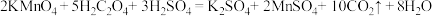 。某化学小组选用硫酸酸化的0.05mol/L高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:
。某化学小组选用硫酸酸化的0.05mol/L高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录的数据]
(4)配制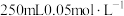 的高锰酸钾溶液肯定不需要的仪器是
的高锰酸钾溶液肯定不需要的仪器是_______ (填标号)。
a.蒸发皿 b.容量瓶 c.玻璃棒 d.烧杯 e.坩埚 f.胶头滳管
(5)为达到实验目的,H2C2O4溶液的物质的量浓度不低于_______ 。
(6)利用实验1中数据计算,0~4min内,用KMnO4的浓度变化表示的反应速率:
_______ 。
(一) KMnO4的制备,分步骤Ⅰ、Ⅱ两步进行。
步聚Ⅰ.先利用如图所示装置制备K2MnO4。称取7.0gKOH(s)和5.0gKClO3(s)放入容器A中,加热,待混合物熔融后,加入5.0gMnO2(s),待反应物干涸后,加大火焰强热4~8min,得墨绿色的锰酸钾。

(1)A可选用
①石英坩埚 ②瓷坩埚 ③铁坩埚
(2)实验中发生反应生成K2MnO4的化学方程式为
Ⅱ.由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①待A处物料冷却后,用20mL4%KOH溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。
②向滤液中通入足量CO2,使K2MnO4歧化为KMnO4和MnO2,过滤出生成的MnO2。
③再将滤液进行一系列处理,得KMnO4晶体。
(3)过程②向滤液中通入足量CO2,可观察到的现象为
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应:
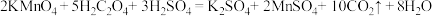 。某化学小组选用硫酸酸化的0.05mol/L高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:
。某化学小组选用硫酸酸化的0.05mol/L高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:[实验内容及记录的数据]
| 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
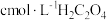 溶液 溶液 |  | 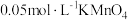 溶液 溶液 | 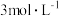 稀硫酸 稀硫酸 | ||
| 1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
| 2 | 2.0 | 2.0 | 4.0 | 2.0 | 5.2 |
| 3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
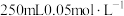 的高锰酸钾溶液肯定不需要的仪器是
的高锰酸钾溶液肯定不需要的仪器是a.蒸发皿 b.容量瓶 c.玻璃棒 d.烧杯 e.坩埚 f.胶头滳管
(5)为达到实验目的,H2C2O4溶液的物质的量浓度不低于
(6)利用实验1中数据计算,0~4min内,用KMnO4的浓度变化表示的反应速率:

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】碱式碳酸铋[( BiO)2CO3·0.5H2O]又名碳酸氧铋,高温灼烧时会分解为Bi2O3,其用途包括制备其它铋化合物、分析试剂、制备胃药等,工业生产( BiO)2CO3·0.5H2O的流程如下图所示,请回答下列相关问题。
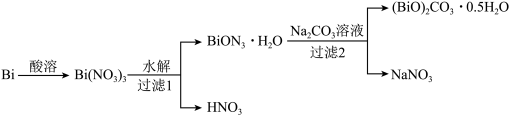
(1)(BiO)2CO3·0.5H2O中铋的化合价是___________ ,铋在周期表中的位置是___________ 。
(2)酸溶过程生成的气体是NO,该反应的离子方程式是______________________ 。工厂在生产中将NO与适量空气混合后通入水中得到稀硝酸,该操作的优点是___________ 、___________ 。
(3)水解过程中为了增大Bi(NO3)3的水解程度,可采用的措施是___________ (任写一项)。
(4)过滤得到的(BiO)2CO3·0.5H2O要在烘箱中烘干,烘干时工作人员未控制好关键条件致使产品不纯,导致纯度下降的化学方程式是______________________ 。
(5)铋的冶炼方法之一是火法炼铋,但得的铋纯度较低,粗铋可通过电解法进行精炼,其原理如下图所示,其中电极a的材料是___________ ,电极b上发生的电极反应为___________ 。

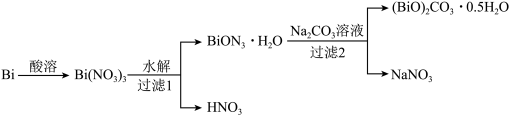
(1)(BiO)2CO3·0.5H2O中铋的化合价是
(2)酸溶过程生成的气体是NO,该反应的离子方程式是
(3)水解过程中为了增大Bi(NO3)3的水解程度,可采用的措施是
(4)过滤得到的(BiO)2CO3·0.5H2O要在烘箱中烘干,烘干时工作人员未控制好关键条件致使产品不纯,导致纯度下降的化学方程式是
(5)铋的冶炼方法之一是火法炼铋,但得的铋纯度较低,粗铋可通过电解法进行精炼,其原理如下图所示,其中电极a的材料是

您最近一年使用:0次



