2020年9月22日,国家主席习近平在第七十五届联合国大会上宣布:“中国力争在2030年前 排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是
排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是 转化为甲醇:
转化为甲醇: 。
。
1.现研究温度对于甲醇产率的影响。在210℃~290℃,保持原料气中 和
和 的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是
的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是___________ 。
2.由此判断
___________ 0(填“>”、“=”或“<”),请分别阐述你做出上述实线选择和判断 的依据
的依据___________ 。
3.该反应的自发条件是___________ 。
A.高温自发 B.低温自发 C.任何温度下都自发
4.恒温恒容条件下,有利于提高 的平衡转化率的措施有
的平衡转化率的措施有
5.向恒温恒容容器中投入2mol  和等量
和等量 ,下列能说明该反应已达平衡状态的是
,下列能说明该反应已达平衡状态的是
 除了能转化为
除了能转化为 外,还可以和
外,还可以和 反应生成CO:
反应生成CO:
其化学平衡常数和温度的关系如下表所示:
6.某温度下,平衡浓度符合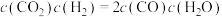 ,此时温度介于___________范围。
,此时温度介于___________范围。
7.在820℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为: 、
、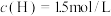 、
、 、
、 ,则下一时刻,反应向___________进行。
,则下一时刻,反应向___________进行。
 排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是
排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是 转化为甲醇:
转化为甲醇: 。
。1.现研究温度对于甲醇产率的影响。在210℃~290℃,保持原料气中
 和
和 的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是
的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是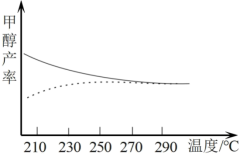
2.由此判断

 的依据
的依据3.该反应的自发条件是
A.高温自发 B.低温自发 C.任何温度下都自发
4.恒温恒容条件下,有利于提高
 的平衡转化率的措施有
的平衡转化率的措施有| A.使用催化剂 | B.加压 |
C.减小 和 和 的初始投料比 的初始投料比 | D.平衡后,同等比例的增加反应物的量 |
 和等量
和等量 ,下列能说明该反应已达平衡状态的是
,下列能说明该反应已达平衡状态的是A. 体积分数保持不变 体积分数保持不变 | B.气体的密度不再变化 |
| C.混合气体的平均摩尔质量不再变化 | D.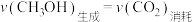 |
 除了能转化为
除了能转化为 外,还可以和
外,还可以和 反应生成CO:
反应生成CO:
其化学平衡常数和温度的关系如下表所示:
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
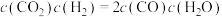 ,此时温度介于___________范围。
,此时温度介于___________范围。| A.<700℃ | B.700-800℃ | C.1000-1200℃ | D.无法判断 |
 、
、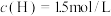 、
、 、
、 ,则下一时刻,反应向___________进行。
,则下一时刻,反应向___________进行。| A.正向 | B.逆向 | C.不移动 | D.无法判断 |
更新时间:2024-05-18 20:56:03
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.58 kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.58 kJ•mol-1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g) CH3OH(g) △H3=-90.77 kJ•mol-1
CH3OH(g) △H3=-90.77 kJ•mol-1
回答下列问题:
(1)反应Ⅱ的△H2=______________ 。
(2)反应Ⅲ自发进行的原因是___________ 。
(3)一定温度下,在一个容积为2L的密闭容器中充入4mol SO2和2mol O2,发生反应2SO2(g)+O2(g) 2SO3(g);2min后达到平衡,测得容器中SO3的浓度为0.6mol/L。
2SO3(g);2min后达到平衡,测得容器中SO3的浓度为0.6mol/L。
①下列能说明反应达到平衡状态的是____________________ 。
A.v(O2)正=2v(SO3)逆 B.气体的平均相对分子质量不变
C.气体的密度不变 D.气体的分子总数不变
②从反应开始到平衡,用SO2的浓度变化表示的反应速率为____________ 。
③该温度下,此反应的化学平衡常数为___________ 。(结果保留两位小数)
④达到平衡后,为同时提高反应速率和SO3的生成量,以下措施一定可行的是______
A.升高温度 B.缩小容器体积 C.分离出SO3 D.改变催化剂
⑤若向平衡体系中再加入4mol SO2和2mol O2,化学平衡________ 移动(填“向右”、“向左”或“不”),再次达到平衡时SO2的转化率___________ 。(填“增大”、“减小”或“不变”)。
(4)25℃时,向浓度均为0.1mol/L的NaBr和KI的混合溶液中逐滴加入AgNO3溶液,当两种沉淀共存时,c(Br-)与c(I-)的比值为______ 。(结果保留两位小数)[Ksp(AgBr)=5.4×10-13,Ksp(AgI)=8.5×10-17]
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.58 kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.58 kJ•mol-1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2反应Ⅲ:CO(g)+2H2(g)
 CH3OH(g) △H3=-90.77 kJ•mol-1
CH3OH(g) △H3=-90.77 kJ•mol-1回答下列问题:
(1)反应Ⅱ的△H2=
(2)反应Ⅲ自发进行的原因是
(3)一定温度下,在一个容积为2L的密闭容器中充入4mol SO2和2mol O2,发生反应2SO2(g)+O2(g)
 2SO3(g);2min后达到平衡,测得容器中SO3的浓度为0.6mol/L。
2SO3(g);2min后达到平衡,测得容器中SO3的浓度为0.6mol/L。①下列能说明反应达到平衡状态的是
A.v(O2)正=2v(SO3)逆 B.气体的平均相对分子质量不变
C.气体的密度不变 D.气体的分子总数不变
②从反应开始到平衡,用SO2的浓度变化表示的反应速率为
③该温度下,此反应的化学平衡常数为
④达到平衡后,为同时提高反应速率和SO3的生成量,以下措施一定可行的是
A.升高温度 B.缩小容器体积 C.分离出SO3 D.改变催化剂
⑤若向平衡体系中再加入4mol SO2和2mol O2,化学平衡
(4)25℃时,向浓度均为0.1mol/L的NaBr和KI的混合溶液中逐滴加入AgNO3溶液,当两种沉淀共存时,c(Br-)与c(I-)的比值为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】工业合成氨对人类生存贡献巨大,反应原理为:
(1)若在一容积为2L的密闭容器中加入0.2 mol的N2和0. 6 mol 的H2在一定条件下发生反应,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2 mol。则前5分钟的平均反应速率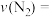
_______ 。下列各项能作为判断该反应达到化学平衡状态的依据是_______ (填序号字母)
a.容器内 、
、 、
、 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2
b.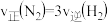
c.容器内压强保持不变
d.混合气体的密度保持不变
(2)科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中的部分微粒)。

写出步骤c的化学方程式_______ ;由图象可知合成氨反应的△H_______ 0(填“>”“<”或“=”)。
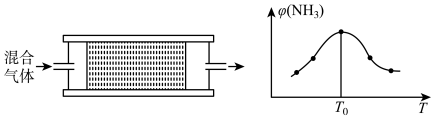
(3)将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的刚性反应器,反应器温度变化与从反应器排出气体中 的体积分数
的体积分数 关系如图。随着反应器温度升高,
关系如图。随着反应器温度升高, 的体积分数
的体积分数 先增大后减小的原因是
先增大后减小的原因是_______ 。
某温度下,混合气体在刚性容器内发生反应,起始气体总压为2×107Pa,平衡时总压为开始的90%,则H2的转化率为_______ 。用某物质的平衡分压(气体分压P分=P总×体积分数)代替物质的量浓度也可以表示化学平衡常数(记作KP),此温度下,该反应的化学平衡常数KP=_______ (分压列计算式、不化简)。
(4)合成氨的原料气H2可来自甲烷水蒸气催化重整(SMR)。我国科学家对甲烷和水蒸气催化重整反应机理也进行了广泛研究,通常认为该反应分两步进行。第一步:CH4催化裂解生成H2和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如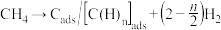 ;第二步:碳(或碳氢物种)和H2O反应生成CO2和H2,如
;第二步:碳(或碳氢物种)和H2O反应生成CO2和H2,如 。反应过程和能量变化残图如下(过程①没有加催化剂,过程②加入催化剂),过程①和②
。反应过程和能量变化残图如下(过程①没有加催化剂,过程②加入催化剂),过程①和②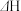 的关系为:①
的关系为:①_______ ②(填“>”“<”或“=”);控制整个过程②反应速率的是第_______ 步(填“I”或“Ⅱ”),其原因为_______ 。

(1)若在一容积为2L的密闭容器中加入0.2 mol的N2和0. 6 mol 的H2在一定条件下发生反应,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2 mol。则前5分钟的平均反应速率
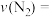
a.容器内
 、
、 、
、 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2b.
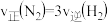
c.容器内压强保持不变
d.混合气体的密度保持不变
(2)科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中的部分微粒)。

写出步骤c的化学方程式
(3)将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的刚性反应器,反应器温度变化与从反应器排出气体中
 的体积分数
的体积分数 关系如图。随着反应器温度升高,
关系如图。随着反应器温度升高, 的体积分数
的体积分数 先增大后减小的原因是
先增大后减小的原因是
某温度下,混合气体在刚性容器内发生反应,起始气体总压为2×107Pa,平衡时总压为开始的90%,则H2的转化率为
(4)合成氨的原料气H2可来自甲烷水蒸气催化重整(SMR)。我国科学家对甲烷和水蒸气催化重整反应机理也进行了广泛研究,通常认为该反应分两步进行。第一步:CH4催化裂解生成H2和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如
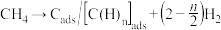 ;第二步:碳(或碳氢物种)和H2O反应生成CO2和H2,如
;第二步:碳(或碳氢物种)和H2O反应生成CO2和H2,如 。反应过程和能量变化残图如下(过程①没有加催化剂,过程②加入催化剂),过程①和②
。反应过程和能量变化残图如下(过程①没有加催化剂,过程②加入催化剂),过程①和②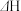 的关系为:①
的关系为:①
您最近一年使用:0次
【推荐3】在一定的温度、压强和钒催化剂存在的条件下,SO2被空气中的O2氧化为SO3。V2O5是钒催化剂的活性成分,郭汗贤等提出:V2O5在对反应I的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如图1:

图1
(1)①已知有关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
由此计算反应Ⅰ的△H=_________ kJ·mol-1。
②写出反应Ⅱ的化学方程式_________ 。
(2)不能说明反应Ⅰ达到平衡状态的是_________ 。
A.恒容密闭容器中混合气体的压强不再变化
B.恒容密闭容器中混合气体的密度不再变化
C.混合气体的总物质的量不再变化
D.混合气体的平均相对分子质量不再变化
E.n(SO2)∶n(O2)∶n(SO3)=2∶1∶2
F.SO2气体的百分含量不再变化
(3)在保持体系总压为105Pa的条件下进行反应SO2+1/2O2 SO3,原料气中SO2和O2的物质的量之比m(m=
SO3,原料气中SO2和O2的物质的量之比m(m= )不同时,SO2的平衡转化率与温度(t)的关系如下图所示:
)不同时,SO2的平衡转化率与温度(t)的关系如下图所示:

①图中m1、m2、m3的大小顺序为_________ ,理由是_________ 。
②反应I的化学平衡常数Kp表达式为_________ (用平衡分压代替平衡浓度表示)。图中A点原料气的成分是:n(SO2)=10mol,n(O2)=24.4mol,n(N2)=70mol,达平衡时SO2的分压p(SO2)为_________ Pa。(分压=总压×物质的量分数)。
③近年,有人研发出用氧气代替空气的新工艺,使SO2趋于全部转化。此工艺的优点除了能充分利用含硫的原料外,主要还有_________ 。

图1
(1)①已知有关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
| 化学键 | S=O(SO2) | O=O(O2) | S=O(SO3) |
| 能量/kJ | 535 | 496 | 472 |
由此计算反应Ⅰ的△H=
②写出反应Ⅱ的化学方程式
(2)不能说明反应Ⅰ达到平衡状态的是
A.恒容密闭容器中混合气体的压强不再变化
B.恒容密闭容器中混合气体的密度不再变化
C.混合气体的总物质的量不再变化
D.混合气体的平均相对分子质量不再变化
E.n(SO2)∶n(O2)∶n(SO3)=2∶1∶2
F.SO2气体的百分含量不再变化
(3)在保持体系总压为105Pa的条件下进行反应SO2+1/2O2
 SO3,原料气中SO2和O2的物质的量之比m(m=
SO3,原料气中SO2和O2的物质的量之比m(m= )不同时,SO2的平衡转化率与温度(t)的关系如下图所示:
)不同时,SO2的平衡转化率与温度(t)的关系如下图所示:
①图中m1、m2、m3的大小顺序为
②反应I的化学平衡常数Kp表达式为
③近年,有人研发出用氧气代替空气的新工艺,使SO2趋于全部转化。此工艺的优点除了能充分利用含硫的原料外,主要还有
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】铑基催化剂催化CO加氢合成甲醇(CH3OH)、乙醛(CH3CHO)、乙醇等碳的含氧化合物是近年来化学界比较活跃的研究课题之一。
(1)已知:(ⅰ)CO(g)+2H2(g) CH3OH(g) △H1=-90.1kJ/mol
CH3OH(g) △H1=-90.1kJ/mol
(ⅱ)2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol
CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol
(ⅲ)C2H5OH(g) CH3OCH3(g) △H3=+50.7kJ/mol
CH3OCH3(g) △H3=+50.7kJ/mol
则由CO催化加氢制备乙醇气体(另一产物为水蒸气)的热化学反应方程式为________ 。
(2)直接甲醇燃料电池(DMFC)成本低、效率高,某研究所尝试用DMFC电解处理含氰电镀废水。调节废水pHl0~12.5,电解过程中,CNˉ先被氧化成CNOˉ(两种离子中氮元素均为-3价),再进一步氧化为碳酸盐和N2。
①请写出CNOˉ被氧化的电极反应式________ 。
②欲处理1m3CNˉ含量为390mg/L的电镀废水,至少需准备________ kg甲醇。
(3)在2.0L密闭容器中放入1 molCO与2molH2,在反应温度T1时进行如下反应:
CO(g)+2H2(g)=CH3OH(g),反应时间(t)与容器内气体总物质的量(n)的数据见下表:
①在0~5min时段,反应速率v(CH3OH)为________ ;有利于提高上述反应平衡转化率的条件是________ 。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
②计算温度T1时反应的平衡常数K1________ ;T1时达平衡后,改变反应温度为T2,平衡常数增大,则T2________ T1(填“大于”“小于”),判断理由是________ 。
(1)已知:(ⅰ)CO(g)+2H2(g)
 CH3OH(g) △H1=-90.1kJ/mol
CH3OH(g) △H1=-90.1kJ/mol(ⅱ)2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol
CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol(ⅲ)C2H5OH(g)
 CH3OCH3(g) △H3=+50.7kJ/mol
CH3OCH3(g) △H3=+50.7kJ/mol则由CO催化加氢制备乙醇气体(另一产物为水蒸气)的热化学反应方程式为
(2)直接甲醇燃料电池(DMFC)成本低、效率高,某研究所尝试用DMFC电解处理含氰电镀废水。调节废水pHl0~12.5,电解过程中,CNˉ先被氧化成CNOˉ(两种离子中氮元素均为-3价),再进一步氧化为碳酸盐和N2。
①请写出CNOˉ被氧化的电极反应式
②欲处理1m3CNˉ含量为390mg/L的电镀废水,至少需准备
(3)在2.0L密闭容器中放入1 molCO与2molH2,在反应温度T1时进行如下反应:
CO(g)+2H2(g)=CH3OH(g),反应时间(t)与容器内气体总物质的量(n)的数据见下表:
| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 总物质的量n/mol | 3.0 | 2.7 | 2.5 | 2.3 | 2.1 | 2.0 | 2.0 |
①在0~5min时段,反应速率v(CH3OH)为
A.高温高压 B.低温低压 C.高温低压 D.低温高压
②计算温度T1时反应的平衡常数K1
您最近一年使用:0次
【推荐2】乙酸是生物油的主要成分之一,乙酸制氢具有重要意义:
热裂解反应:CH3COOH(g)→2CO(g)+2H2(g) △H=+213.7 kJ·mol-1
脱酸基反应 CH3COOH(g)→2CH4(g)+CO2(g) △H=-33.5 kJ·mol-1
(1)请写出CO与H2甲烷化的热化学方程式__________________________________ 。
(2)在密闭溶液中,利用乙酸制氢,选择的压强为________ (填“高压”或“常压”)。
其中温度与气体产率的关系如图:

①约650℃之前,脱酸基反应活化能低速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随着温度升高后,热裂解反应速率加快,同时_________________ 。
②保持其他条件不变,在乙酸气中掺杂一定量的水,氢气产率显著提高而CO的产率下降,请用化学方程式表示:____________________ 。
(3)若利用合适的催化剂控制其他的副反应,温度为T K时达到平衡,总压强为P kPa,热裂解反应消耗乙酸20%,脱酸基反应消耗乙酸60%,乙酸体积分数为________ (计算结果保留1位小数);脱酸基反应的平衡常数Kp分别为________________ kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
热裂解反应:CH3COOH(g)→2CO(g)+2H2(g) △H=+213.7 kJ·mol-1
脱酸基反应 CH3COOH(g)→2CH4(g)+CO2(g) △H=-33.5 kJ·mol-1
(1)请写出CO与H2甲烷化的热化学方程式
(2)在密闭溶液中,利用乙酸制氢,选择的压强为
其中温度与气体产率的关系如图:

①约650℃之前,脱酸基反应活化能低速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随着温度升高后,热裂解反应速率加快,同时
②保持其他条件不变,在乙酸气中掺杂一定量的水,氢气产率显著提高而CO的产率下降,请用化学方程式表示:
(3)若利用合适的催化剂控制其他的副反应,温度为T K时达到平衡,总压强为P kPa,热裂解反应消耗乙酸20%,脱酸基反应消耗乙酸60%,乙酸体积分数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.合成氨工业在国民生产中有重要意义。运用平衡移动原理能是合成氨工业进行的又快又好,也能为科学家寻找适合“碳中和”的反应指明方向。
(1)合成氨工业中,原料气中的杂质 需经过铜氨液处理,其反应为
需经过铜氨液处理,其反应为 ΔH<0;吸收
ΔH<0;吸收 后的溶液经过适当处理又可再生,再生的适宜条件是_______
后的溶液经过适当处理又可再生,再生的适宜条件是_______
(2)符合合成氨工业生产实际的是_______
(3)T℃,体积均为1L的甲、乙、丙容器中发生反应: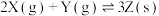
 ,
,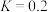 ,
, 时刻容器中X、Y与Z的物质的量如下表,下列说法正确的是_______
时刻容器中X、Y与Z的物质的量如下表,下列说法正确的是_______
Ⅱ.若在0.5L的密闭容器中,氮气和氢气进行如下反应:
 ,工业流程及化学平衡常数K与温度T的关系如下所示:
,工业流程及化学平衡常数K与温度T的关系如下所示:

(4)试比较 、
、 的大小,
的大小,
___________  (填“<”“>”或“=”);根据合成氨工业流程可知,工业上流程中循环Ⅰ的目的为
(填“<”“>”或“=”);根据合成氨工业流程可知,工业上流程中循环Ⅰ的目的为___________ 。
(5)400℃时,反应 的化学平衡常数的值为
的化学平衡常数的值为___________ 。当测得 、
、 和
和 物质的量分别为
物质的量分别为 、
、 和
和 时,则该反应的
时,则该反应的
___________  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
(6)合成氨工业中热交换器的作用为___________ 。
Ⅲ.为了达到“碳中和”的目的,科学家利用如下反应进行 的捕捉:
的捕捉:
方法一: 。
。
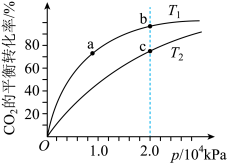
(7)相同条件下,测得 在不同温度下(
在不同温度下( )的平衡转化率与压强的关系如图所示。下列说法正确的是___________
)的平衡转化率与压强的关系如图所示。下列说法正确的是___________
在一定温度下,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ。相同时间内 的转化率随温度变化如图:
的转化率随温度变化如图:
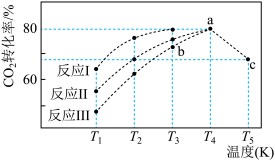
(8)催化剂效果最佳的反应是反应___________ (选填“Ⅰ”、“Ⅱ”或“Ⅲ”)。此反应的热效应为___________ (填“吸热”或“放热”),由图像说明原因:___________ 。
方法二: ①
①
 ②
②
(9)T℃,在2L的密闭容器中充入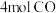 和
和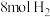 合成二甲醚,平衡时
合成二甲醚,平衡时 的转化率为0.8,且
的转化率为0.8,且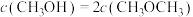 。计算反应①平衡常数的值
。计算反应①平衡常数的值___________ 。
(1)合成氨工业中,原料气中的杂质
 需经过铜氨液处理,其反应为
需经过铜氨液处理,其反应为 ΔH<0;吸收
ΔH<0;吸收 后的溶液经过适当处理又可再生,再生的适宜条件是_______
后的溶液经过适当处理又可再生,再生的适宜条件是_______| A.高温低压 | B.高温高压 | C.低温低压 | D.低温高压 |
A.增大 的浓度有利于 的浓度有利于 提高转化率 提高转化率 | B.温度选择500℃有利于平衡正移 |
| C.催化剂能提高反应物的转化率 | D.液化氨气正反应速率减慢 |
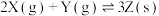
 ,
,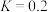 ,
, 时刻容器中X、Y与Z的物质的量如下表,下列说法正确的是_______
时刻容器中X、Y与Z的物质的量如下表,下列说法正确的是_______| X | Y | Z | |
| 甲 |  |  |  |
| 乙 |  |  |  |
| 丙 |  |  |  |
A.甲容器中 |
B.乙容器若升高温度,达到平衡时 可能为 可能为 |
| C.乙、丙容器达到平衡后,X的浓度相等 |
| D.若丙容器中X的物质的量分数不变,则该反应已达平衡 |
Ⅱ.若在0.5L的密闭容器中,氮气和氢气进行如下反应:

 ,工业流程及化学平衡常数K与温度T的关系如下所示:
,工业流程及化学平衡常数K与温度T的关系如下所示:
| T/℃ | 200 | 300 | 400 |
| K |  |  | 0.5 |
 、
、 的大小,
的大小,
 (填“<”“>”或“=”);根据合成氨工业流程可知,工业上流程中循环Ⅰ的目的为
(填“<”“>”或“=”);根据合成氨工业流程可知,工业上流程中循环Ⅰ的目的为(5)400℃时,反应
 的化学平衡常数的值为
的化学平衡常数的值为 、
、 和
和 物质的量分别为
物质的量分别为 、
、 和
和 时,则该反应的
时,则该反应的
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。(6)合成氨工业中热交换器的作用为
Ⅲ.为了达到“碳中和”的目的,科学家利用如下反应进行
 的捕捉:
的捕捉:方法一:
 。
。(7)相同条件下,测得
 在不同温度下(
在不同温度下( )的平衡转化率与压强的关系如图所示。下列说法正确的是___________
)的平衡转化率与压强的关系如图所示。下列说法正确的是___________
A. | B.反应速率: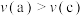 |
C.平衡常数: | D. 的体积分数: 的体积分数: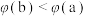 |
在一定温度下,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ。相同时间内
 的转化率随温度变化如图:
的转化率随温度变化如图:
(8)催化剂效果最佳的反应是反应
方法二:
 ①
① ②
②(9)T℃,在2L的密闭容器中充入
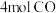 和
和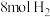 合成二甲醚,平衡时
合成二甲醚,平衡时 的转化率为0.8,且
的转化率为0.8,且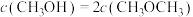 。计算反应①平衡常数的值
。计算反应①平衡常数的值
您最近一年使用:0次
【推荐1】石油化工、煤化工等行业的废气中均含有硫化氢,需要将其回收处理并利用。
(1)热分解法:
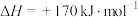 ,工业上,通常在等温、等用条件下将
,工业上,通常在等温、等用条件下将 与Ar的混合气体通入反应器,发生
与Ar的混合气体通入反应器,发生 热分解反应,达到平衡状态后,若继续向反应器中通入Ar,
热分解反应,达到平衡状态后,若继续向反应器中通入Ar, 的平衡转化率会
的平衡转化率会___________ (填“增大”、“减小”或“不变”)。
(2)氧化法: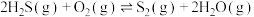
已知: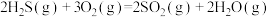
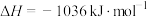
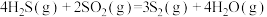
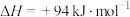
无催化剂条件下,混合加热 与
与 ,探究相同时间内
,探究相同时间内 (g)产率影响因素。
(g)产率影响因素。
①用氧化法处理 ,若生成1mol
,若生成1mol  (g),放出热量为
(g),放出热量为___________ kJ。
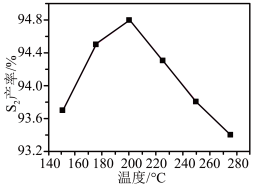
②其他条件相同时, 产率随温度的变化如图所示。随着温度升高,
产率随温度的变化如图所示。随着温度升高, (g)产率先增大后减小,原因是
(g)产率先增大后减小,原因是___________ 。
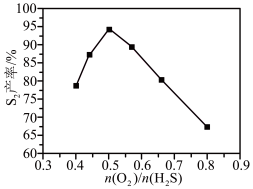
③其他条件相同时, (g)产率随
(g)产率随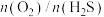 值的变化如图所示。
值的变化如图所示。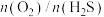 值过高不利于提高
值过高不利于提高 (g)产率,可能的原因是
(g)产率,可能的原因是___________ 。
(3)微电池法:利用电化学原理去除天然气中的 ,装置如图所示,总反应是:
,装置如图所示,总反应是: 。
。
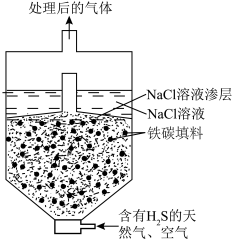
①写出负极的电极反应式___________ 。
②一段时间后,单位时间内 的去除率降低,其可能的原因是
的去除率降低,其可能的原因是___________ 。
(4)硫酸钙吸收法:如图为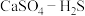 反应体系在不同温度、不同
反应体系在不同温度、不同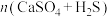 物质的量比的物相变化图。
物质的量比的物相变化图。
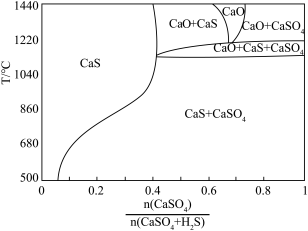
①用斜线在图中画出 可以完全转化并且有CaO生成的区域
可以完全转化并且有CaO生成的区域___________ 。
②若不通入 ,简述
,简述 随温度升高分解的规律
随温度升高分解的规律___________ 。
(1)热分解法:

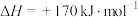 ,工业上,通常在等温、等用条件下将
,工业上,通常在等温、等用条件下将 与Ar的混合气体通入反应器,发生
与Ar的混合气体通入反应器,发生 热分解反应,达到平衡状态后,若继续向反应器中通入Ar,
热分解反应,达到平衡状态后,若继续向反应器中通入Ar, 的平衡转化率会
的平衡转化率会(2)氧化法:
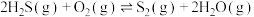
已知:
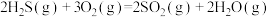
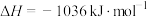
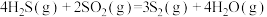
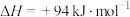
无催化剂条件下,混合加热
 与
与 ,探究相同时间内
,探究相同时间内 (g)产率影响因素。
(g)产率影响因素。①用氧化法处理
 ,若生成1mol
,若生成1mol  (g),放出热量为
(g),放出热量为②其他条件相同时,
 产率随温度的变化如图所示。随着温度升高,
产率随温度的变化如图所示。随着温度升高, (g)产率先增大后减小,原因是
(g)产率先增大后减小,原因是
③其他条件相同时,
 (g)产率随
(g)产率随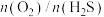 值的变化如图所示。
值的变化如图所示。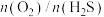 值过高不利于提高
值过高不利于提高 (g)产率,可能的原因是
(g)产率,可能的原因是
(3)微电池法:利用电化学原理去除天然气中的
 ,装置如图所示,总反应是:
,装置如图所示,总反应是: 。
。
①写出负极的电极反应式
②一段时间后,单位时间内
 的去除率降低,其可能的原因是
的去除率降低,其可能的原因是(4)硫酸钙吸收法:如图为
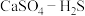 反应体系在不同温度、不同
反应体系在不同温度、不同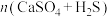 物质的量比的物相变化图。
物质的量比的物相变化图。
①用斜线在图中画出
 可以完全转化并且有CaO生成的区域
可以完全转化并且有CaO生成的区域②若不通入
 ,简述
,简述 随温度升高分解的规律
随温度升高分解的规律
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】乙酸是重要的有机化工原料之一,目前世界上一半以上的乙酸都都采用甲醇与CO反应来制备.某实验小组在一个恒压密闭容器中加入0.20molCH3OH和0.22molCO气体,发生反应CH3OH(g)+CO(g) CH3COOH(I),测得甲醇的转化率随温度的变化关系如图所示,其中曲线Ⅰ表示在5个不同温度下,均经过5min时测得的甲醇的转化率变化曲线,曲线Ⅱ表示不同温度下甲醇的平衡转化率变化曲线,已知在T2温度下,达到平衡时容器的体积刚好为2L.
CH3COOH(I),测得甲醇的转化率随温度的变化关系如图所示,其中曲线Ⅰ表示在5个不同温度下,均经过5min时测得的甲醇的转化率变化曲线,曲线Ⅱ表示不同温度下甲醇的平衡转化率变化曲线,已知在T2温度下,达到平衡时容器的体积刚好为2L.
已知:2CO(g)+O2(g)═2CO2(g) △H=﹣566kJ·mol-1
2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(I) △H=﹣1529kJ·mol-1
CH3COOH(I)+2O2(g)═2CO2(g)+2H2O(I) △H=﹣874kJ·mol-1
按要求回答下列问题:
(1)求工业制乙酸反应:CH3OH(g)+CO(g) CH3COOH(I) △H=
CH3COOH(I) △H= ______ kJ·mol-1
(2)在温度为T2时,从反应开始至5min时,用单位时间内物质的量变化表示的乙酸的平均反应速率为_________ mol·min-1.
(3)在温度为T2时,该反应的平衡常数K=_________ ;在T3温度下,C点时,ν(正) ____ ν(逆)(填“>”、“<”或“=” )。
(4)在温度为T2时,往上述已达到平衡的恒压容器中,再在瞬间通入0.12molCH3OH和0.06molCO混合气体,平衡的移动方向为__________ (填“向左”或“向右”或“不移动” )
(5)在温度为T1时,乙酸的物质的量随时间变化的趋势曲线如下图所示.当时间到达t1时,将该反应体系温度迅速上升到T3,并维持该温度。请在图中画出t1时刻后乙酸物质的量的变化总趋势曲线.
__________
 CH3COOH(I),测得甲醇的转化率随温度的变化关系如图所示,其中曲线Ⅰ表示在5个不同温度下,均经过5min时测得的甲醇的转化率变化曲线,曲线Ⅱ表示不同温度下甲醇的平衡转化率变化曲线,已知在T2温度下,达到平衡时容器的体积刚好为2L.
CH3COOH(I),测得甲醇的转化率随温度的变化关系如图所示,其中曲线Ⅰ表示在5个不同温度下,均经过5min时测得的甲醇的转化率变化曲线,曲线Ⅱ表示不同温度下甲醇的平衡转化率变化曲线,已知在T2温度下,达到平衡时容器的体积刚好为2L.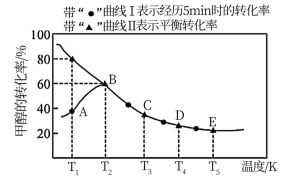
已知:2CO(g)+O2(g)═2CO2(g) △H=﹣566kJ·mol-1
2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(I) △H=﹣1529kJ·mol-1
CH3COOH(I)+2O2(g)═2CO2(g)+2H2O(I) △H=﹣874kJ·mol-1
按要求回答下列问题:
(1)求工业制乙酸反应:CH3OH(g)+CO(g)
 CH3COOH(I) △H=
CH3COOH(I) △H= (2)在温度为T2时,从反应开始至5min时,用单位时间内物质的量变化表示的乙酸的平均反应速率为
(3)在温度为T2时,该反应的平衡常数K=
(4)在温度为T2时,往上述已达到平衡的恒压容器中,再在瞬间通入0.12molCH3OH和0.06molCO混合气体,平衡的移动方向为
(5)在温度为T1时,乙酸的物质的量随时间变化的趋势曲线如下图所示.当时间到达t1时,将该反应体系温度迅速上升到T3,并维持该温度。请在图中画出t1时刻后乙酸物质的量的变化总趋势曲线.
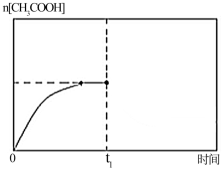
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(1)生成氢气:将水蒸气通过红热的炭即产生水煤气。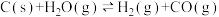 ΔH=+131.3kJ⋅mol-1,ΔS=+133.7J⋅mol-1⋅K-1,该反应在低温下
ΔH=+131.3kJ⋅mol-1,ΔS=+133.7J⋅mol-1⋅K-1,该反应在低温下_______ (“能”或“不能”)自发进行。
(2)已知在400℃时, 的
的 。相关化学键键能数据为
。相关化学键键能数据为
回答下列问题:①在400℃时,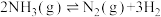 (g的K2=
(g的K2=_______ (填数值),ΔH=_______ 。
②400℃时,在1L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为4mol、2mol、4mol,则此时反应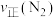
_______ 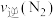 (填“>”“<”“=”或“不能确定”)。
(填“>”“<”“=”或“不能确定”)。
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡_______ (填“向左”“向右”或“不”)移动;使用催化剂_______ (填“增大”“减小”或“不改变”)反应的ΔH。
(3)氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为 ,在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(φ)如图所示。
,在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(φ)如图所示。
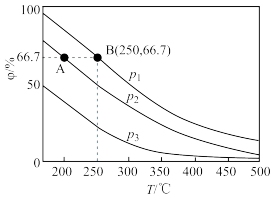
①其中,p1、p2和p3由大到小的顺序是_______
②若在250℃、p1为105Pa的条件下,反应达到平衡,此时B点N2的分压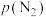 为
为_______ Pa(分压=总压×物质的量分数,保留一位小数)。
(1)生成氢气:将水蒸气通过红热的炭即产生水煤气。
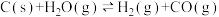 ΔH=+131.3kJ⋅mol-1,ΔS=+133.7J⋅mol-1⋅K-1,该反应在低温下
ΔH=+131.3kJ⋅mol-1,ΔS=+133.7J⋅mol-1⋅K-1,该反应在低温下(2)已知在400℃时,
 的
的 。相关化学键键能数据为
。相关化学键键能数据为| 化学键 | N≡N | H-H | N-H |
键能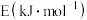 | 946 | 436 | 390.8 |
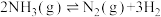 (g的K2=
(g的K2=②400℃时,在1L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为4mol、2mol、4mol,则此时反应
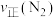
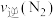 (填“>”“<”“=”或“不能确定”)。
(填“>”“<”“=”或“不能确定”)。③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡
(3)氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为
 ,在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(φ)如图所示。
,在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(φ)如图所示。
①其中,p1、p2和p3由大到小的顺序是
②若在250℃、p1为105Pa的条件下,反应达到平衡,此时B点N2的分压
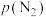 为
为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】三烯(乙烯、丙烯、丁二烯)和三苯(苯、甲苯、二甲苯)是基本的化工原料,应用广泛。回答下列问题:
(1)在三烯三苯中最重要的就是乙烯,乙烯产量甚至被作为衡量一个国家化工发展水平的指标。乙烷裂解法制取乙烯的反应机理如下:
Ⅰ.链引发
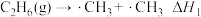
Ⅱ.链传递
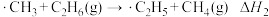
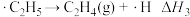

Ⅲ.链终止(略)
①乙烷裂解制乙烯的热化学方程式为_____ 。
②反应机理中生成的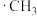 (甲基自由基)得电子变成
(甲基自由基)得电子变成 (甲基负离子),
(甲基负离子), 的VSEPR模型的名称为
的VSEPR模型的名称为_____ 。
(2)丙烯工业上常用“丙烯氨氧化法”制备丙烯腈( ),包括如下反应:
),包括如下反应:
Ⅰ.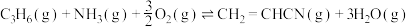
Ⅱ. (副反应)
(副反应)
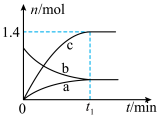
向T℃、压强为28MPa的恒压密闭容器中通入1.0mol丙烯、1.0mol氨气和4.8mol氧气发生反应Ⅰ、Ⅱ,容器内H2O(g)、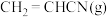 、C3H6(g)的物质的量(n)随时间(t)的变化关系如图所示。
、C3H6(g)的物质的量(n)随时间(t)的变化关系如图所示。
①图中表示H2O(g)的曲线是_____ (填“a”“b”或“c”)。
②反应Ⅰ的浓度平衡常数K的表达式为_____ 。
③平衡时,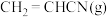 的分压
的分压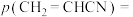
_____ MPa.
(3)国家发改委把生产尼龙-66的己二腈列为国家攻关的“卡脖子”项目,目前工业上生产己二腈主要为丙烯腈电解法。酸性条件下丙烯腈电解法制己二氰的阴极电极反应式为_____ ,其中丙烯氰中碳原子的杂化方式为_____ 。
(1)在三烯三苯中最重要的就是乙烯,乙烯产量甚至被作为衡量一个国家化工发展水平的指标。乙烷裂解法制取乙烯的反应机理如下:
Ⅰ.链引发
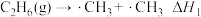
Ⅱ.链传递
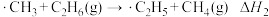
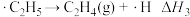

Ⅲ.链终止(略)
①乙烷裂解制乙烯的热化学方程式为
②反应机理中生成的
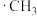 (甲基自由基)得电子变成
(甲基自由基)得电子变成 (甲基负离子),
(甲基负离子), 的VSEPR模型的名称为
的VSEPR模型的名称为(2)丙烯工业上常用“丙烯氨氧化法”制备丙烯腈(
 ),包括如下反应:
),包括如下反应:Ⅰ.
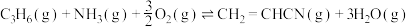
Ⅱ.
 (副反应)
(副反应)
向T℃、压强为28MPa的恒压密闭容器中通入1.0mol丙烯、1.0mol氨气和4.8mol氧气发生反应Ⅰ、Ⅱ,容器内H2O(g)、
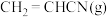 、C3H6(g)的物质的量(n)随时间(t)的变化关系如图所示。
、C3H6(g)的物质的量(n)随时间(t)的变化关系如图所示。①图中表示H2O(g)的曲线是
②反应Ⅰ的浓度平衡常数K的表达式为
③平衡时,
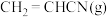 的分压
的分压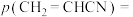
(3)国家发改委把生产尼龙-66的己二腈列为国家攻关的“卡脖子”项目,目前工业上生产己二腈主要为丙烯腈电解法。酸性条件下丙烯腈电解法制己二氰的阴极电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】乙酸是基本的有机化工原料。
I.工业上合成乙酸有多种方法。
(1)目前世界上一半以上的乙酸都采用甲醇与CO反应来制备。反应如下:
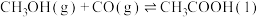
 。在恒压密闭容器中通入0.20mol的
。在恒压密闭容器中通入0.20mol的 和0.20mol的CO气体,测得甲醇的转化率随温度变化如图所示。
和0.20mol的CO气体,测得甲醇的转化率随温度变化如图所示。
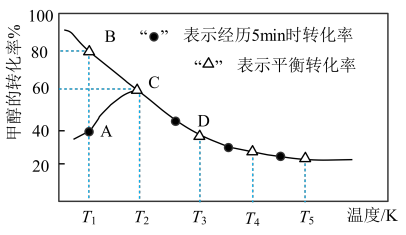
①恒容绝热条件下,不能说明上述反应达到平衡状态的是___________ 。
A.容器内温度不变 B. 的体积分数保持不变
的体积分数保持不变
C. 的物质的量浓度保持不变 D.
的物质的量浓度保持不变 D.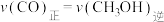
②温度为 时,5min时该反应中
时,5min时该反应中 的反应速率:
的反应速率: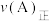
___________ 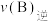 (填“>”,“=”或“<”)。
(填“>”,“=”或“<”)。
③温度为 时,上述反应达到平衡后,若此时保持容器体积、温度不变,再通入0.10mol
时,上述反应达到平衡后,若此时保持容器体积、温度不变,再通入0.10mol 和0.10molCO的混合气体,再次达到平衡,CO的转化率
和0.10molCO的混合气体,再次达到平衡,CO的转化率___________ 80%(填“>”,“=”或“<”)。
Ⅱ.乙酸制氢具有重要意义,制氢过程发生如下反应:
热裂解反应I: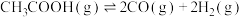
脱羧基反应II: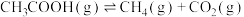
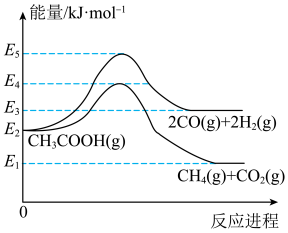
(2)已知反应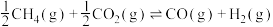
 ,由图所示,
,由图所示,
___________  (用图中有关E的代数式表示)。
(用图中有关E的代数式表示)。
(3)在容积相同的密闭容器中,加入等量乙酸蒸气制氢,在相同时间测得温度与气体产率的关系如图所示。
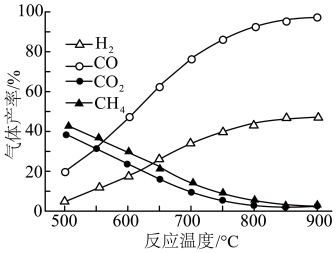
①约650℃之前,氢气产率低于甲烷的原因是___________ 。
②若保持其他条件不变,在乙酸蒸气中掺杂一定量水,氢气的产率显著提高而CO的产率下降,请用化学方程式表示可能发生的反应:___________ 。
(4)在一定温度下,利用合适的催化剂发生热裂解反应I和脱羧基反应Ⅱ,达到平衡时,总压强为p kPa,乙酸体积分数为20%;若热裂解反应消耗的乙酸占总的乙酸的20%,则脱羧基反应Ⅱ的平衡常数 为
为___________ kPa( 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
I.工业上合成乙酸有多种方法。
(1)目前世界上一半以上的乙酸都采用甲醇与CO反应来制备。反应如下:
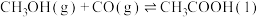
 。在恒压密闭容器中通入0.20mol的
。在恒压密闭容器中通入0.20mol的 和0.20mol的CO气体,测得甲醇的转化率随温度变化如图所示。
和0.20mol的CO气体,测得甲醇的转化率随温度变化如图所示。
①恒容绝热条件下,不能说明上述反应达到平衡状态的是
A.容器内温度不变 B.
 的体积分数保持不变
的体积分数保持不变C.
 的物质的量浓度保持不变 D.
的物质的量浓度保持不变 D.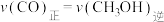
②温度为
 时,5min时该反应中
时,5min时该反应中 的反应速率:
的反应速率: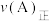
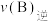 (填“>”,“=”或“<”)。
(填“>”,“=”或“<”)。③温度为
 时,上述反应达到平衡后,若此时保持容器体积、温度不变,再通入0.10mol
时,上述反应达到平衡后,若此时保持容器体积、温度不变,再通入0.10mol 和0.10molCO的混合气体,再次达到平衡,CO的转化率
和0.10molCO的混合气体,再次达到平衡,CO的转化率Ⅱ.乙酸制氢具有重要意义,制氢过程发生如下反应:
热裂解反应I:
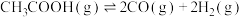
脱羧基反应II:
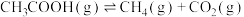
(2)已知反应
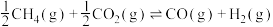
 ,由图所示,
,由图所示,
 (用图中有关E的代数式表示)。
(用图中有关E的代数式表示)。
(3)在容积相同的密闭容器中,加入等量乙酸蒸气制氢,在相同时间测得温度与气体产率的关系如图所示。

①约650℃之前,氢气产率低于甲烷的原因是
②若保持其他条件不变,在乙酸蒸气中掺杂一定量水,氢气的产率显著提高而CO的产率下降,请用化学方程式表示可能发生的反应:
(4)在一定温度下,利用合适的催化剂发生热裂解反应I和脱羧基反应Ⅱ,达到平衡时,总压强为p kPa,乙酸体积分数为20%;若热裂解反应消耗的乙酸占总的乙酸的20%,则脱羧基反应Ⅱ的平衡常数
 为
为 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】我国科学家发明了一种Zn-PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下:
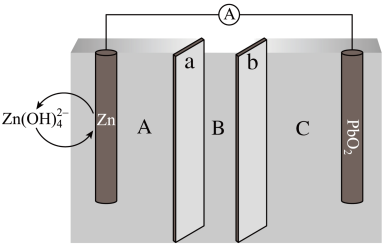
回答下列问题:
(1)电池中,Zn为_______ 极,B区域的电解质为_______ (填“K2SO4”、“H2SO4”或“KOH”)。
(2)放电时,PbO2电极的电极反应式为_______ 。
(3)充电时,Zn电极应接外电源的_______ 极,此时的电极反应式为_______ 。
(4)图中a为_______ (填“阳离子”或“阴离子”)交换膜。
(5)Zn是一种重要的金属材料,工业上一般先将ZnS氧化,再采用热还原或者电解法制备。利用H2还原ZnS也可得到Zn,其反应式如下: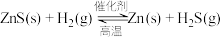 。727℃时,上述反应的平衡常数
。727℃时,上述反应的平衡常数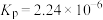 。此温度下,在盛有ZnS的刚性容器内通入压强为1.01×105Pa的H2,达平衡时H2S的分压为
。此温度下,在盛有ZnS的刚性容器内通入压强为1.01×105Pa的H2,达平衡时H2S的分压为_______ Pa(结果保留两位小数)。

回答下列问题:
(1)电池中,Zn为
(2)放电时,PbO2电极的电极反应式为
(3)充电时,Zn电极应接外电源的
(4)图中a为
(5)Zn是一种重要的金属材料,工业上一般先将ZnS氧化,再采用热还原或者电解法制备。利用H2还原ZnS也可得到Zn,其反应式如下:
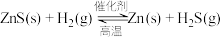 。727℃时,上述反应的平衡常数
。727℃时,上述反应的平衡常数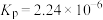 。此温度下,在盛有ZnS的刚性容器内通入压强为1.01×105Pa的H2,达平衡时H2S的分压为
。此温度下,在盛有ZnS的刚性容器内通入压强为1.01×105Pa的H2,达平衡时H2S的分压为
您最近一年使用:0次



